Abstract
A DNA extraction protocol for anopheline mosquitoes was optimized by the evaluation of various incubation times of the sample with Potassium acetate (KAc). The results showed that the highest DNA concentration and amplification frequency were obtained with the 1 h treatment, which suggests that is possible to reduce the incubation time with KAc without affecting the amount and quality of the DNA extracted.
Keywords
Introducción
Los estudios genéticos con artrópodos requieren ADN de buena calidad. En dichos estudios se deben procesar un gran número de muestras (Nodarse et al. 2004; Gutiérrez et al. 2008), por lo que es indispensable contar con un método de extracción eficiente, rápido y económico. En ocasiones se ha reportado la utilización de partes del mosquito como fuente de ADN para la amplificación por PCR, lo cual permite omitir el proceso de extracción; en dicho caso, las patas o alas son adicionadas directamente a la reacción de amplificación (Zapata et al. 2007; Cienfuegos et al. 2008); sin embargo, se ha observado que algunos marcadores, como los mitocondriales, Citocromo Oxidasa Subunidad I (COI) y NADH Deshidrogenasa Subunidad 5 (ND5), no amplifican eficientemente a partir de pata o alas (Gutierrez L, com. pers.).
Se han descrito varios métodos para la extracción del ADN a partir de mosquitos; uno de los más utilizados usa fenol cloroformo (Linton et al. 2001; Zapata et al. 2007); este método es laborioso y requiere usar solventes orgánicos, lo que representa un riesgo para la salud humana y el ambiente, principalmente por las dificultades para la eliminación de estos reactivos (Niu et al. 2008; Valter et al. 2009). Además, se ha reportado que la presencia de los residuos de fenol puede contaminar el producto de extracción e inhibir la amplificación (Rantakokko-Jalava y Jalava 2002). Otros métodos de extracción involucran el uso de aditivos como: Chelex (Angella et al. 2007), tampón Cetyl Trimethyl Ammonium Bromide - CTAB, Sarcosil (Lardeux et al. 2008) y proteinasa K (Nodarse et al. 2004), reactivos que pueden aumentar los costos del proceso (Valter et al. 2009).
Un método reportado inicialmente para la extracción de ADN de Drosophila melanogaster Meigen, 1830 (Bender et al. 1983), fue modificado y utilizado para la extracción de material genético de mosquitos Aedes albopictus Skuse, 1894 (Birungi y Munstermann 2002), siendo también de utilidad para mosquitos Anopheles spp. (Gutiérrez et al. 2008, 2009); entre sus ventajas están el no utilizar solventes orgánicos, no requerir reactivos costosos y ser sencillo de ejecutar. Un paso importante en el procedimiento es la precipitación de proteínas con acetato de potasio (AcK), el que se adiciona a la muestra a una concentración de 1M y se incuba en hielo a -20°C durante 12 horas, prolongando el tiempo del proceso. Lo anterior es una desventaja de dicho protocolo pues toma en promedio dos días de trabajo. En la literatura se han reportado protocolos que utilizan otros tiempos de incubación con el AcK: 10 min (Linton et al. 2001; Bisset et al. 2005), 15 min (Beebe et al. 2000; Nodarse et al. 2004), 30 min (Kampen et al. 2003; De Armas et al. 2005) y 60 min (Nodarse et al. 2004; Golczer y Arrivillaga 2008). Estos estudios muestran la posibilidad de modificar el tiempo de incubación con el AcK. Por esta razón, en el presente trabajo se optimizó el protocolo mediante la disminución de dicho tiempo de incubación, con el fin de agilizar la extracción, obteniendo ADN de buena calidad y cantidad, para ser empleado en diferentes estudios moleculares de anofelinos.
Materiales y Métodos
Para la extracción del ADN se utilizaron abdómenes de mosquitos Anopheles (Nyssorhynchus) albimanus Wiedemann, 1820, recolectados entre octubre y noviembre de 2006 en la localidad de Santa Rosa de Lima (Bolívar) y fueron identificados utilizando claves taxonómicas (Faran y Linthicum 1981; Suarez et al. 1988; Wilkerson 1993). Para trabajar con una muestra homogénea, se definió el tamaño de los abdómenes en 2 mm ± 0,04 DS. Con este criterio, se seleccionaron 54 abdómenes completos que se mantuvieron preservados en etanol al 95%.
Se utilizó un muestreo no probabilístico por conveniencia. Se realizó un diseño experimental de comparación de bloques completamente aleatorizados; se definieron tres bloques, cada uno conformado por 18 abdómenes de mosquitos, y estos se procesaron con una periodicidad de uno por día. Los ensayos se realizaron en días diferentes; con tres repeticiones por cada tratamiento (T), cada uno correspondiente a un tiempo de incubación con AcK 1M, así: T1=15 min, T2=30 min, T3=1 h, T4=3 h, T5=6 h y T6=12 h. El tiempo de 12 h se utilizó como control de tratamientos debido a que es el tiempo reportado en el protocolo (Birungi y Munstermann 2002). Se definió como variable independiente cada uno de los tratamientos evaluados (T1-T6) y como variables dependientes: concentración, calidad de ADN y amplificación por PCR-ITS2.
Para la extracción del ADN, los abdómenes fueron macerados y homogenizados individualmente en viales de 1,5 mL con 100 μL de tampón de lisis (NaCl 0,1 M; Sucrosa 0,1 M; Tris 0,1 M; EDTA 0,05 M; SDS 0,5%, pH 9,1) y se incubaron por 30 min a 65°C, para facilitar la ruptura de los tejidos y membranas celulares. Luego se adicionó 14,5 μL de una solución de AcK 8M para obtener una concentración final de AcK 1M y se incubaron en los diferentes tiempos: T1=15 min, T2=30 min, T3=1 h, T4=3 h, T5=6 h y T6=12 h. Posteriormente, las muestras se centrifugaron a 13.000 rpm, durante 15 min, a 4°C y el sobrenadante se transfirió a un tubo nuevo. A continuación, se realizaron tres pasos de precipitación y subsiguiente centrifugación a 13.000 rpm y 4°C, así: 100 mL etanol absoluto, centrifugando por 15 min, 100 mL etanol frío al 70% por 5 min, y nuevamente, 100 μL etanol absoluto, por 5 min. Finalmente, se dejó secar el botón por un tiempo mínimo de 30 min a temperatura ambiente y se resuspendió en 25 μL de tampón TE 1X (Tris 10 mM, EDTA 1 mM, pH 7,6). Las muestras se incubaron a 65°C por 10 min, para garantizar la resuspensión del ADN extraído y se almacenaron a 4°C.
Se prepararon tres diluciones 1:100 de cada muestra. La concentración de ADN se determinó a una densidad óptica A260; la pureza de las muestras se estimó utilizando la relación A260/280 (Clark y Christopher 2001). Se amplificó el espaciador interno transcrito 2 (ITS2) del ADN ribosomal, como una forma adicional de valorar y validar la calidad y cantidad del ADN extraído, utilizando 2 uL del producto de extracción y las condiciones de PCR descritas anteriormente (Zapata et al. 2007; Cienfuegos et al. 2008). Los productos de la PCR-ITS2 se visualizaron mediante una electroforesis en gel de agarosa al 0,8%, con tinción de bromuro de etidio (5μg/mL).
La comparación de la concentración de ADN e índice de pureza entre los diferentes tratamientos se realizó calculando promedios, desviaciones estándar (DS) y Análisis de Varianza (ANOVA) de un factor. Para identificar los tratamientos que presentaron diferencias significativas en la concentración de ADN se utilizaron las pruebas de Bonferroni y Dunnett (Díaz 1999; Molina et al. 2006). Para el análisis de las amplificaciones del marcador ITS2, se determinó el porcentaje de amplificación y se utilizó la prueba de Chi-cuadrado (X2) para establecer si existían diferencias significativas entre los porcentajes de amplificación obtenidos en los diferentes tratamientos (Halos et al. 2004). Para el análisis estadístico se utilizó el software SPSS para Windows, versión 15 (Inc. SPSS 2008).
Resultados y discusión
Se logró reducir el tiempo de procesamiento de las muestras al disminuir el tiempo de incubación con el AcK. Este logro es importante dado que en la actualidad muchos de los estudios con vectores de enfermedades involucran la extracción de ADN a partir de los especímenes; material que es utilizado para la realización de pruebas moleculares que permitan llevar a cabo diversos tipos de análisis, entre ellos: la confirmación molecular de especies anofelinas que presentan dificultades en su identificación por caracteres morfológicos (Zapata et al. 2007; Cienfuegos et al. 2008), estudios de genética poblacional (Gutiérrez et al. 2009) y filogenia (Beebe et al. 2000).
La cuantificación de los productos de extracción mostró que las concentraciones más altas correspondían al tratamiento tres, con valores entre 489 y 597 ng/uL (Tabla 1). Al aplicar la prueba t de Dunnett para comparar los tratamientos T1 a T5 con el tratamiento control (T6), no se observaron diferencias significativas (P > 0,05) en las concentraciones de ADN: T1 (P=0,116), T2 (P = 0,116), T3 (P = 0,996), T4 (P = 0,107) y T5 (P = 0,645). Sin embargo, al aplicar la prueba de Bonferroni, si se encontró una diferencia significativa entre el tratamiento T3 con respecto a los tratamientos T1 (P = 0,019), T2 (P = 0,019) y T4 (P = 0,017), lo que indicó que el tratamiento T3 o la incubación con AcK por 1 h podría utilizarse en la extracción para obtener una alta concentración de ADN.
Cuantificación por espectrofotometría del ADN extraído utilizando diferentes tiempos de incubación con el AcK.
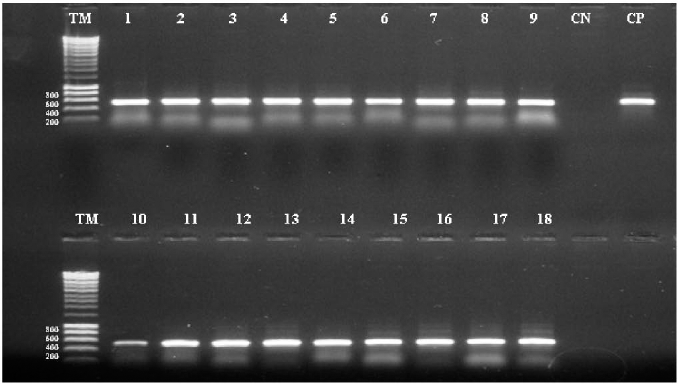
Productos de amplificación de la secuencia ITS2. Gel de agarosa 0,8%. Carriles: TM: Marcador de peso molecular 200-10000 pb. 1-18: producto de PCR obtenidos a partir de ADN extraído de A. albimanus utilizando diferentes tiempos de incubación con AcK 1M. 1-3: T1 (15 min), 4-6: T2 (30 min), 7-9: T3 (1h), 10-12: T4 (3h), 13-15: T5 (6 h), 16-18: T6 (12 h-toda la noche), CN: control negativo, CP: Control positivo: clon de ITS-2 de A. albimanus.
Los valores del índice A260/A280 se encontraron entre 1,5 y 2,0 (Tabla 1) y no mostraron diferencias significativas entre los tratamientos (F = 0,937, P = 0,466); lo que sugiere que cualquiera de los tiempos de incubación con el AcK (T1-T6), pueden ser de utilidad para obtener ADN de buena calidad. Lo anterior permite tener una mayor flexibilidad en el desarrollo de los experimentos, al poder ajustar estos tiempos según conveniencia del investigador. La calidad de ADN es una característica importante, dado que de ella depende en gran parte el éxito de los ensayos posteriores, puesto que incide en la estabilidad del ADN durante su almacenamiento por tiempo indefinido, conservando su estructura y propiedades físico-químicas (Sambrook y Russell 2001).
La amplificación de la región ITS2 fue un indicador adicional de la calidad y cantidad del ADN extraído. Se obtuvo un producto de PCR de 500 pb aproximadamente (Fig. 1), que es el tamaño esperado para este marcador en A. albimanus (Zapata et al. 2007; Cienfuegos et al. 2008). Como se observó con los resultados de concentración, el mayor porcentaje de amplificación de la región ITS2 se obtuvo con el tratamiento T3, con el cual amplificaron ocho de las nueve muestras incubadas con el AcK durante 1 h (89,9%, Tabla 2). No hubo diferencia entre los tratamientos para los valores de amplificaciones (X2, P > 0,05). Lo anterior reitera la utilidad de este tiempo de incubación con AcK para disminuir el tiempo de extracción.
Porcentaje de muestras con amplificación de la secuencia ITS2.
En general, la extracción de ADN es un procedimiento sencillo, sin embargo, en el caso de insectos como los anofelinos, el producto final puede ser poco satisfactorio por la escasa cantidad de material obtenida de un solo mosquito. Otros factores que influyen en la obtención de ADN de buena calidad y cantidad son los procedimientos de recolección, transporte y preservación de los especímenes (Rivero et al. 2007). Se han reportado diferentes temperaturas para el almacenamiento del producto de extracción como son: 4°C, -20°C y -80°C (Birungi y Munstermann 2002; Bisset et al. 2005). En ensayos preliminares de la cuantificación del ADN por espectrofotometría, se observó que se obtenían concentraciones más altas de ADN a partir de muestras almacenadas a 4°C que de aquellas a -20°C. Aunque se conoce que la congelación es ideal para almacenar muestras de ADN a largo plazo, es importante tener en cuenta que los procesos de congelación y descongelación promueven la contaminación y la degradación del ADN (Gómez y Uribe 2007); por esta razón, una buena estrategia es conservar el material extraído a 4°C y realizar los análisis posteriores en un tiempo no mayor a una semana y además, almacenar una alícuota a -20°C.
En los protocolos reportados en la literatura para la extracción de ADN a partir de anofelinos y de otros insectos de importancia médica o veterinaria, se pueden encontrar tiempos de incubación con el AcK que son menores o iguales a los evaluados en este estudio (Beebe et al. 2000; Linton et al. 2001; De Armas et al. 2005; Golczer y Arrivillaga 2008); sin embargo, las ventajas del protocolo optimizado consisten principalmente en la disminución del tiempo para el procesamiento de las muestras y el no requerir reactivos adicionales que impliquen el aumento de los costos o riesgos para la salud humana o el ambiente. Este sería de gran utilidad para laboratorios en países endémicos para enfermedades tropicales como la malaria, pues en estos generalmente se tiene mayor acceso a protocolos más sencillos, que a menudo son laboriosos o requieren reactivos nocivos. Este método posibilitaría el procesamiento más rápido de un gran número de mosquitos y podría ser estandarizado para la extracción de ADN a partir de otros artrópodos de importancia médica.
Footnotes
Agradecimientos
Este trabajo fue anidado a proyectos en ejecución del grupo de Microbiología Molecular, códigos: 8700-1416 y 8700-039, financiados por el Comité para el Desarrollo de la Investigación -CODI– Universidad de Antioquia (a MMC), y contribuyó a la formación en investigación de la Microbióloga DAR, durante sus prácticas académicas y Servicio Social Obligatorio realizado con apoyo de Estrategia para la Sostenibilidad 2007-2008, código BUPP: E01335 y Escuela de Microbiología, Universidad de Antioquia.
