Abstract
Thirty six isolates of B. bassiana were studied, these comprised 16 from coffee berry borer (CBB) in Colombia and 20 from other regions of the world. The fungal biochemical activity was evaluated using nine extracellular enzymes involved in the degradation of complex material (e.g. proteins, chitin and polysacharides). These were tested by degradation, incorporating particular substrates into modified agar growth media. The enzyme systems tested in this way were elastase, gelatinase, fatty acid degrading enzymes and fatty acid utilization or testing the spent culture fluid with specific enzyme substrates that were substituted with methylumbelliferone (n-acetylglucosaminidase, glucosidase, diacetylchitobiosidase, fucosidase, xylosidase and cellobiosidase). The relationship among the isolates was evaluated examining isoenzymes and individual proteins were separated by electrophoresis in discontinuous polyacrylamide gels. Gels were stained for catalase, acid and alkaline phosphatase and esterase (acetate and propionate) activities. DNA was amplified using the polymerase chain reaction (PCR) with four different single primers based on simple sequences. All isolates showed glucosidase, n-acetylglucosaminidase and elastase activity. No isolates displayed fucosidase activity and the different isolates showed differential results with the different physiological tests. The isolates could be split into two broad groups on the basis of these reactions, one group consisting predominantly of isolates with high protease and low chitinase activities, and one group consisting predominantly of isolates with low protease but good chitinase activity. Most isolates had very similar patterns of iso-enzyme and PCR bands although a few isolates gave unique patterns. Analysis of the major and minor pattern differences did non show any simple correlations with host, geographic origin or pathogenicity. There is apparently little genetic variability among the isolates and most of them are very closely related.
Introducción
La producción industrial y artesanal de hongos entomopatógenos que actúan como controladores biológicos de la broca del café, Hypothenemus hampei (Ferrari), requiere un mejor entendimiento de su genética, aspectos fisiológicos, enzimas y metabolitos intra y extracelulares, toxinas, factores de virulencia etc. Este conocimiento genético básico permitirá su manipulación para la obtención de cepas ambientalmente seguras y para la caracterización de la micoteca presente en el Laboratorio de Entomología de Cenicafé.
La investigación sobre los entomopatógenos Beauveria bassiana (Balsamo) Vuillemin y Metarhizium anisopliae (Metschnikoff) Sorokin se ha orientado a la entomología aplicada, a las consideraciones ecológicas relacionadas con el manejo integrado de plagas, sin embargo, recientemente se están haciendo esfuerzos para estudiar la genética y la fisiología de estos hongos.
En epidemiología, ecología y el manejo integrado de plagas es importante identificar las especies o aislamientos benéficos con exactitud. La identificación de patógenos se realiza usualmente por morfología, características culturales y análisis de isoenzimas, patrones de RFLP (Restriction Fragments Lenght Polymorphism) y otros métodos basados en el ADN. Cada uno de estos métodos tiene sus aplicaciones específicas y sus ventajas. Recientemente el uso de la técnica de la Reacción en Cadena de la Polimerasa (PCR) se ha incrementado, pues amplifica secuencias blanco de ADN, selectivamente, además menos cantidad de ADN se requiere y permite el rápido análisis de un gran número de muestras.
Por tanto, estos métodos rápidos, confiables y sensibles para la diferenciación de entomopatógenos pueden ser útiles en la implementación de medidas de control biológico apropiadas.
La cutícula está compuesta de proteínas y quitina asociada con lípidos y compuestos fenólicos que sirven como barrera a la entrada de microorganismos B. bassiana produce muchas enzimas extracelulares en medios nutritivos como lipasa, proteasa, quitinasa, además, éstas han sido evaluadas in vitro y con otros métodos (Baeth y Bridge 1989). Estas enzimas están involucradas en la penetración del integumento del hospedero y en consecuencia en la infección. La producción de lipasa es inducida por triglicéridos, más no es inhibida por ácidos grasos, aunque el efecto inhibitorio ha sido reportado por varios autores y ha sido atribuido a la presencia de ácidos grasos de cadena corta (Hegedus y Khachatourians, 1988). Bidochka y Khachatourians (1990) encontraron que el aislamiento GK2016 producía sólo una serin proteasa cuando crecía en gelatina, estas serin proteasas están ampliamente distribuidas entre los hongos y principalmente son extracelulares; se cree que la quitinasa es una enzima constitutiva y que aparece relativamente tarde en comparación con las enzimas del complejo proteolítico en el ataque al insecto (St leger et al. 1986).
Hay necesidad de métodos confiables y rápidos que sean útiles en la identificación de aislamientos de B. bassiana y que sean suficientemente sensibles para ser utilizados como sistemas de monitoreo en las etapas de producción y en el campo. Hegedus y Khachatourians (1996), utilizando la técnica PCR-SSCP (Single-Strand DNA Conformation Polymorphism analysis) hallaron que el sistema es útil para la identificación de aislamientos incluso directamente de insectos infectados.
El objetivo de este estudio fue determinar el grado de variación entre aislamientos de B. bassiana procedentes de Brasil, Colombia, Ecuador, Jamaica, Honduras, Guatemala, México, Togo, Kenia, Sri Lanka, Java e Islas Salomón. Comparando básicamente las poblaciones asociadas con la broca del café para intentar seleccionar el aislamiento más adecuado pata el control de esta plaga.
Materiales y Métodos
Todos los aislamientos utilizados se obtuvieron de la micoteca de la disciplina de Entomología del Centro Nacional de Investigaciones de Café (CENICAFE), de la colección de hongos entomopatógenos del International Mycological Institute (IMI) del Reino Unido y del Institut National de la Recherche Agronomique (INRA) de Francia y se escogieron can base en su origen biológico y geográfico. Su lista aparece en la Tabla 1 bajo su número de catálogo y código de acceso a cada una de las colecciones.
Lista de los aislamientos de B. bassiana procedentes de broca del café y su patogenicidad a este insecto 3 .
Aislamientos de INRA
Aislamientos de IMI
Datos tomados de "Patogenicidad de B. bassiana sobre la broca del café". Cenicafé. Informe interno. 1996. González, G., M. T.
El cultivo de hongos filamentosos como B. bassiana, se realiza en cultivos líquidos, pues este proceso es rápido y más práctico en comparación con el cultivo sólido para posteriormente registrar la actividad extra e intracelular, producción de proteínas, (enzimas) y para la extracción de ADN y algunas pruebas de asimilación.
Trozos de micelio de los diferentes aislamientos, procedentes de Sabouraud Dextrosa Agar (SDA) se inocularon en botellas universales (2 cm diámetro, 8 cm altura) que contenían el medio GYM (Medio Glucosa Extracto de Levadura), la tapa no se ajustó para permitir la aireación del cultivo. Después, estas botellas se incubaron en agitación orbital (200 rpm) durante 4 días a 25°C y su contenido se transfirió a matraces de 250 ml que contenían 50 ml del medio GYM, los cuales también fueron colocadas en agitación durante el mismo período de tiempo y con la misma temperatura hasta extinguir la glucosa (Paterson y Bridge 1994).
Para evaluar enzimas extracelulares se utilizaron compuestos metilumbeliferona sustitutos. El principio básico es el mismo que el de los compuestos cromóforos, excepto que el compuesto libre, metilumbeliferona, es fluorescente y se puede ver como un color azul/blanco bajo la luz UV. Los compuestos 4 metilumbeliferona se prepararon para dar una concentración madre de 50 mM en 1.6 ml de dimetilformamida, las soluciones madres se diluyeron a 0.15 ml en 9,85 ml de acetato de sodio 0,05 M, pH 5,4. En placas de titulación de fondo plano se depositaron 50µl de sustrato y luego 50µl del sobrenadante de los cultivos. Esto se hizo por duplicado y se incluyeron controles de los sobrenadantes más acetato de sodio, sustrato más acetato de sodio y acetato de sodio solamente. Las placas se incubaron a 37°C por 4 horas. Después se añadieron 50 µl de una solución saturada de bicarbonato de sodio en cada pozo, para aumentar la fluorescencia y detener la reacción (Paterson y Bridge 1994).
Los sustratos utilizados fueron:
4 metil umbeliferil β-D-xilosido (Sigma)
4 metil umbeliferil N-acetil-β-D-galactosaminido (Sigma)
4 metil umbeliferil N-acetil-β-D-glucopiranosido (Sigma)
4 metil umbeliferil β-D-celobiosido (Sigma)
4 metil umbeliferil β-D-N-N'-diacetil quitobiosido (Sigma)
4 metil umbeliferil β-D-fucopiranosido (Sigma)
Para la evaluación de metabolitos secundarios, un gran número de medios basales es utilizado, generalmente tienen ata concentración de fuentes de carbono, (sucrosa) y extractos orgánicos que proveen un amplio rango de factores de crecimiento como el Czapek Yeast Agar (CYA). Para extraer los metabolitos intracelulares, trozos de micelio procedentes de SDA, se inocularon en el medio CYA y las cajas se incubaron a 25°C durante 10-12 días. Luego, con un sacabocados, discos de agar (0,5 cm) con micelio se removieron, a los cuales les fue agregada una gota de cloroformo: metanol (2:1 v/v) e inmediatamente colocados en el origen de la lámina de Cromatografia de Capa Delgada y removidos; 5 µl de griseofulvina (Sigma), disuelta en cloroformo: metanol (2: 1 v/v), se colocó también en el origen como referencia estándar. El desarrollo de las láminas se llevó a cabo en cloroformo: acetona: 2-propanol (85:15:20 v/v/v), luego las láminas se retiraron del tanque y se dejaron secar para después ser examinadas bajo la luz visible y la luz UV (254 y 365 nm), registrando el color y la distancia Rf (Paterson y Bridge 1994).
El medio Tween 80 se utilizó como prueba presuntiva para determinar la actividad esterasa sobre ácidos grasos, este contiene Tween 80 como fuente de carbono y el púrpura de bromocresol es el indicador de pH. Se debe anotar que este no es estrictamente un ensayo para actividad lipasa. Se utilizaron trozos de micelio procedentes de SDA que fueron inoculados en el centro de la caja de petri (4.5 cm diámetro) que contenía el medio. Posterior a la inoculación, las cultivos se incubaron a 25°C durante 10 días (Paterson y Bridge 1994).
Para la determinación de la elastasa, se utilizó el método de difusión de colorante en este caso la elastin orceina. Se vertió un medio basal en pequeños viales de antibióticos, se dejaron solidificar y sobre este se virtió el medio basal mezclado con la elastin-orcina, cuando la enzima cliva el sustrato la orceina es liberada y esta se precipita al medio basal permitiendo la visualización de la reacción. 2,5 ml del medio Agar Lynch B se dispensaron en los viales, sometidas a autoclave a 10 psi por 10 minutos (medio basal), entre tanto, 1 g de elastin orceina se disolvió en 33 ml de agua destilada y sometido a autoclave, luego se mezcló con el medio Lynch B con un pH final de 5,4. Con la ayuda de una pipeta estéril, 5 ml de esta mezcla se vertieron sobre el medio basal. Trozos de micelio procedentes de SDA se inocularon en la capa superior y las botellas se incubaron a 25°C por 7 días (Paterson y Bridge 1994).
El medio de gelatina puede ser usado como una prueba general presuntiva para la actividad proteasa. En este caso, el medio de cultivo es solidificado con gelatina. Se debe recordar que la gelatina es normalmente líquida en algunas temperaturas de incubación que se utilizan; además, el ácido producido par el microorganismo puede afectar el punto de fusión de la gelatina a temperatura ambiente, por tanto, los cultivos se deben enfriar (0-4°C, 2 horas) después del período de incubación para evaluar la prueba. El medio se preparó y calentó hasta 50-60°C, vertido en la gelatina en pequeñas cantidades hasta que ésta se disolvió, El medio caliente se dispensó en botellas universales y se esterilizó por autoclave a 10 psi por 10 minutos. Cuando estaba frío, trozos de micelio procedentes de SDA, se inocularon en el medio por punción e incubaron por más de 10 días a 25°C (Paterson y Bridge 1994).
El micelio procedente del medio GYM, se cosechó por filtración al vacío, luego, se liofilizó, para posteriormente molerlo en un mortero con pistilo; de este macerado se obtuvieron dos fracciones, una se utilizó para extraer las enzimas intracelulares y la otra destinada para extraer el ADN.
Para la extracción de proteínas totales, la mitad del tubo eppendorf (1,5 ml) se llenó con el micelio molido y a éste se le agregaron 700 µl de solución amortiguadora Tris glicina, se centrifugó durante 45 minutos a 13000 g a 4°C, obteniéndose el sobrenadante. Los extractos intracelulares preparados can este método se dividieron en un número de alícuotas antes de congelar, para usar una muestra fresca cada vez. La concentración de proteínas en las muestras se determinó con el método de Lowry et al. (1951). Los geles de una concentración aproximada de 10% de paliacrilamida siempre se prepararon de soluciones madres de acrilamida, solución amortiguadora y N, N, N, N tetrametileno diamina (TMED) y cada vez las soluciones de persulfato de amonio se prepararon frescas. Para teñir los geles para actividad esterasa (acetato y propionato) y catalasa, los geles se dejaron en oscuridad durante 90 minutos; para la actividad fosfatasa (ácida y alcalina) el gel fue incubado a 37°C.
Para el análisis del ADN con la técnica RAPD's-PCR, éste fue extraído del micelio con la solución amortiguadora bromuro de cetil-timetil amonio (CTAB), purificado por extracción con cloroformo, tratado con ribonucleasa y precipitado con propanol, el CTAB se removió del ADN final utilizando soluciones amortiguadoras de acetato de amonio y las muestras se diluyeron y usaron en las reacciones de PCR. Para la amplificación del ADN, el blanco fueron los loci hipervariables también conocidos como Minisatélites, el análisis de tales secuencias repetidas adyacentes en número variable (Variable Number Tandem Repeats - VNTR) ha sido útil para el análisis de leves variaciones en las secuencias pertenecientes a individuos cercanamente relacionados, ya que ellas se heredan en una forma mendeliana y se pueden identificar individuos particulares y así determinar relaciones de familiaridad (Bridge et al. 1996).
Los iniciadores utilizados para este experimento fueron:
GF 5'(TCC)35
RY 5'(CAG)35
MR 5'(GAGGGTGGCGGTTCT)3'
71 5'(CGGCTTGGGT)³
El iniciador MR es la secuencia universal en tandem del fago M13, esta secuencia tiene un uso general para estudios de relaciones biológicas y puede ser aplicada a diferentes grupos taxonómicos incluyendo animales (vertebrados e invertebrados), plantas y microorganismos (Ryskov et al. 1988).
Después de estandarizar los diferentes parámetros de la PCR, las reacciones de amplificación se realizaron en un volumen total de 50µl, conteniendo 10mM tris HCI (pH 8,3); 50mM KCI; 1,5mM MgCl₂, 50µM de dATP, dCTP, dGTP, dTTP, 15pmol de los iniciadores, aproximadamente 25ng de ADN genómico y 1U de polimerasa Tth (Thermus termophilus). Controles negativos, en los cuales la plantilla de ADN se reemplazó por agua y otro control donde no se colocó la enzima fueron utilizados en todos los experimentos. La amplificación se realizó con un termociclador (PTC-100 MJ Research USA) programado como sigue: un ciclo por un minuto a 94°C (denaturación inicial), seguido por 45 ciclos de un minuto a 94°C (denaturación), un minuto a 35°C (alineamiento) y un minuto a 72°C (extensión). Un ciclo de 5 minutos a 72°C se utilizó como extensión final después de los 45 ciclos de amplificación. Todas las amplificaciones se condujeron al menos cuatro veces. 20µl del producto de la amplificación se separaron por electroforesis en gel de agarosa al 1,5% (Nusieve 3:1, FMC Products, USA) teñidos con bromuro de etidio y fotografiados bajo la luz UV.
La tinción para las isoenzimas y los iniciadores utilizados se seleccionó con base en aquellos que han dado resultados en el ámbito de poblaciones subespecíficas en otros estudios con hongos patógenos de insectos (Mugnai et al. 1989, Bridge et al. 1990).
Análisis de los datos
Los resultados de las pruebas bioquímicas se codificaron usando 0 para negativos, 5 para positivos de alta actividad, 3 para positivos de mediana actividad y 1 para leves o perdidos. Las comparaciones de cada perfil para cada iniciador se hizo con base en la presencia versus ausencia (1/0) de los productos de la PCR del mismo tamaño. Bandas del mismo tamaño se registraron como idénticas. Las similitudes se calcularon utilizando el coeficiente de similaridad de Gower, descontando resultados apareados negativos y se agruparon utilizando el algoritmo UPGMA (Unweighted Pair Group Mathematical Average-Promedio no ponderado para grupos pares) (Sneath y Sokal 1993).
Resultados
Los resultados para la actividad enzimática determinada con las técnicas 4-metilumbeliferona e incorporación de sustratos a medios sólidos modificados de los diferentes aislamientos se presentan en la tabla 2. Los diferentes aislamientos mostraron resultados diferenciales con las distintas pruebas fisiológicas.
Actividad enzimática extracelular y metabolitos secundarios de los aislamientos de B. bassiana evaluados
- No actividad 1 actividad baja 3 actividad media 5 actividad alta
Los datos de la actividad 4 Mufucosidasa fueron negativos.
Con la técnica 4-metilumbeliferona se encontró que la actividad N-acetil-B-glucosaminidasa se observó en todos los aislamientos evaluados con diferentes grados de intensidad en la fluorescencia de la 4-metilumbeliferona. Para el sustrato glucosa, la actividad fue variable y algunos aislamientos no mostraron dicha actividad (Bb9212). Para el diacetilquitobiosido (dimero de glucosamina), no todos los aislamientos mostraron actividad, incluso, la mayoría de aislamientos mostraron una media, baja o ninguna actividad. Las enzimas xilosidasa y celobiosidasa también fueron variables entre los aislamientos, aunque muy pocos mostraron dicha actividad. En contraste, la actividad fucosidasa no fue hallada en ninguno de los aislamientos. Los anteriores resultados están de acuerdo con los hallados por Mugnai et al. (1989) y Barth y Bridge (1989), que al evaluar diferentes aislamientos de B. bassiana con algunas de las técnicas señaladas y con el sistema API ZYM encontraron que aquellos muestran diferente actividad enzimática para cada uno de los sustratos evaluados.
Pocos metabolitos secundarios fueron detectados en el sistema usado, las pocas manchas vistas en las placas de CCD fueron verdes bajo la luz UV y similares para la mayoría de aislamientos.
La hidrólisis de la gelatina (proteasa) fue variable, no todos los aislamientos presentaron esta actividad, confirmando que ellos fueron deficientes en la producción de proteasa extracelular; estos resultados están de acuerdo con los hallados por Bidochka y Khachatourians (1990). En cuanto a la actividad esterasa (degradación del Tween 80), la mayoría de las aislamientos mostraron una fuerte actividad con sólo dos aislamientos negativos (327908-335829). Para la hidrólisis de la elastin-orceina (elastasa), todos los aislamientos mostraron actividad sobre este sustrato; estos resultados coinciden con los hallados por Mugnai et al. (1989).
En general, los aislamientos se pueden dividir en dos grandes grupos con base en estas reacciones, un grupo consistentemente predominante de aislamientos con actividad proteasa alta y baja actividad quitinasa y otro grupo consistentemente predominante de aislamientos de baja actividad proteasa pero buena actividad quitinasa; creemos que es una estrategia de adaptación, ya que la cutícula de los insectos es un sistema quitina-proteína (Rudal y Kenchington 1973; St. Leger et al. 1986), por tanto, el entomopatógeno podría atacar alguno de los dos compuestos para la penetración de la cutícula. Una estrategia en la escogencia de un aislamiento altamente virulento para utilizarlo en el manejo integrado, sería aquel que tuviera una alta actividad quitinasa y proteasa y que mostrara una alta patogenicidad en los bioensayos como lo son los aislamientos Bb9002, Bb9202 y Bb9203, teniendo en cuenta que al introducir un nuevo aislamiento se podría alterar la población de entomopatógenos establecida.
El análisis isoenzimático con acetil y propionil esterasas mostró un alto nivel de uniformidad entre los aislamientos. La mayoría tienen patrones muy similares de bandas de isoenzimas, aunque muy pocos aislamientos dieron patrones únicos como (Bb9213 y 327909). El análisis de las diferencias entre los patrones mayores y menores no señaló ninguna correlación simple con el hospedero, origen geográfico o patogenicidad. Las otras enzimas analizadas no indicaron ninguna actividad, creemos que la actividad catalasa no fue exhibida por ninguno de los aislamientos debido a la aireación de los cultivos líquidos.
Los productos de amplificación con el iniciador GF resultó en la amplificación de una sola banda con un tamaño aproximado de 3000 pb, mientras que con los otros iniciadores se generaron fragmentos desde 2600 hasta 5000 pb para RY, desde 1600 hasta 6000 pb para MR y desde 1600 hasta 4000 pb para 71. Los tres últimos iniciadores revelaron un polimorfismo útil para clasificar los aislamientos. Los patrones de cada iniciador fueron divididos en bandas (4-10) individuales y los resultados para todos los aislamientos fueron registrados en una base de datos para la comparación numérica.
Los patrones de amplificación del iniciador RY para los aislamientos Bb9213, 327909 у 329067 fueron muy distintos de los patrones de los otros aislamientos, para MR los patrones de Bb9213, 327909 y 341525 y para 71 los patrones de Bb9213 y 327909.
Los aislamientos que fueron bastante diferentes de los otros por las técnicas de PCR, también fueron consistentemente distintos por los análisis isoenzimáticos (Bb9213 у 327909) у el aislamiento 462 fue variado para dos de los cuatro iniciadores utilizados.
Los resultados de las bandas de la PCR fueron combinados con los resultados de las pruebas bioquímicas y moleculares y sus similitudes fueron calculadas para producir un dendograma (Fig. 1).
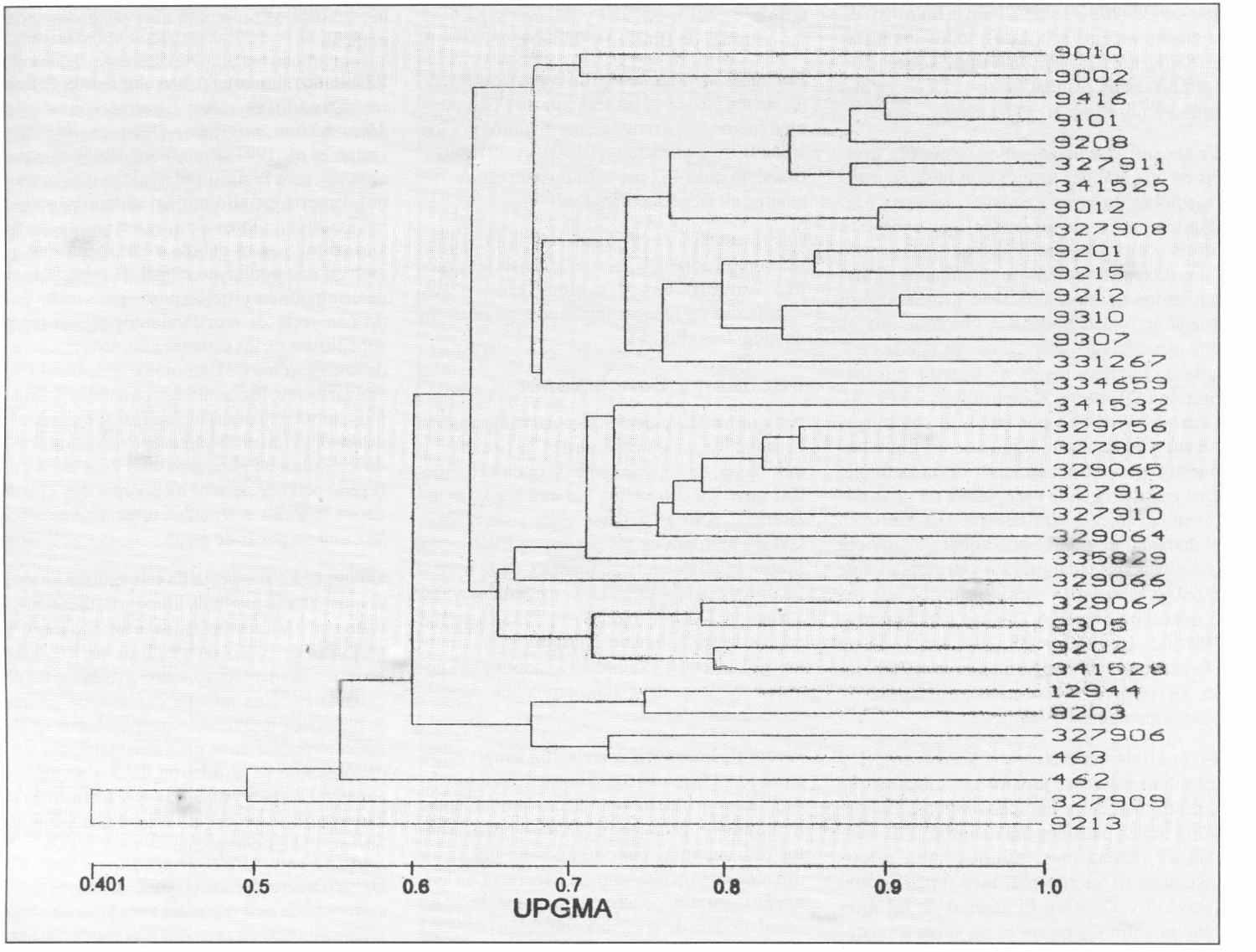
Dendograma de los datos fisiológicos y moleculares de los aislamientos de B. bassiana.
Discusión y Conclusiones
Aunque los aislamientos se pueden agrupar en la base de sus actividades proteasas y quitinasas, hay aparentemente poca variabilidad genética entre ellos Sin embargo, las diferencias podrían hallarse entre aislamientos con los patrones de las bandas de PCR; estas fueron relativamente pequeñas y en la mayoría de los casos podrían ser consideradas como variaciones de un sólo patrón. Esta situación parecería ser aplicable a la gran mayoría de los aislamientos examinados, aunque un pequeño número de aislamientos fue consistentemente diferente.
Parece no haber una correlación simple entre antecedentes genéticos y hospedero o localidad, aunque hay un número de asociaciones interesantes. Primero, hay una tendencia en los dendogramas para algunos de los aislamientos del mismo año en asociarse en pequeños grupos, posiblemente representando reaislamiento de la misma población (Bb9002 y Bb9010, Bb9212 y Bb9215, Bb9307 y Bb9310). Segundo, los aislamientos del IMI y del INRA, empleados como ejemplos de variación geográfica, tienden a agruparse juntos, más bien que con los otros aislamientos estudiados; hubo una o dos excepciones a lo anterior, las más notables fueron aislamientos de México y Guatemala, esto puede indicar que aunque los aislamientos de distribución mundial están agrupados, puede ser que el grupo está formándose porque ellos son similares en que ellos son diferentes a los aislamientos estudiados. El nivel de diferencia es generalmente leve por las características usadas aquí.
Las características y técnicas empleadas en este estudio han sido previamente halladas sensibles para diferenciar poblaciones basadas en hospedero y localidad en otros patógenos de plantas y entomopatógenos incluyendo B. bassiana procedentes de Cosmopolites sordidus (Germ.), Ostrinia nubilalis (Hb.) y Phyllophaga sp; por tanto, parece probable que estas técnicas son precisas para representar la variabilidad genética entre los aislamientos y que en este estudio los analizados presentan muy poca variación entre sí.
Resultados similares se han obtenido por otros investigadores con poblaciones de Metarhizium anisopliae (Riba et al. 1987; Fegan et al. 1993; Pipe et al. 1995), aunque en esos casos la similitud total fue mucho menor. En este estudio ningún aislamiento tuvo resultados similares a otro y es posible que la variación vista es debida a una menor variación en una población clonal. Este podría ser determinado en pruebas posteriores incluyendo una serie de reaislamientos conocidos y subcultivos de los aislamientos de la micoteca de la Disciplina de Entomología de Cenicafé; similarmente, los resultados obtenidos podrían indicar que ellos serían una forma de proceso de selección en el aislamiento y mantenimiento de los cultivos; para examinar esto, sería necesario obtener cultivos monoespóricos a partir de los insectos infectados directamente y seleccionar a partir de éstos.
Un importante aspecto de este estudio ha sido el inusual alto grado de homogeneidad observado entre los aislamientos. Con esto surge la pregunta de cómo tal grado de uniformidad genética es mantenido sobre un amplio rango geográfico. Una posible explicación es que poblaciones individuales de patógenos se establecieron por unos pocos aislamientos fundadores que se originaron de una población ancestral común y aquellos únicamente llevaban una fracción de la variabilidad genética que existía en la especie.
De acuerdo a Ferré (1988), la mayoría de cultivares de café que crecen en América, Asia y Oceanía fueron introducidas desde Yemen. Si la diseminación de B. bassiana fue efectuada a través de la dispersión de la broca del café, muchos aislamientos alrededor del mundo procedentes de este insecto podrían haber sido originados a partir de una pequeña población común ancestral.
Aunque el efecto fundador puede explicar la invariabilidad genética dentro de una región, es inadecuado explicar la uniformidad del fenotipo enzimático sobre una amplio rango geográfico. Incluso, dentro de una población fundadora, la población subsecuente crece y la heterogeneidad ambiental podría establecer más variabilidad con el tiempo (Mayr 1970). Las tazas de mutación para los loci enzimáticos basado en diferentes especies como cebada (Khaler et al. 1984), Drosophila (Mukai y Cockerham 1977) y en el hombre (Neel et al. 1980) ha sido estimada en el rango de 106 por locus por generación, si esta mutación es aplicada al loci de las enzimas en B. bassiana y dado el alto potencial de reproductividad del hongo sobre la broca del café (5 x 106 conidias/broca, González et al. 1993), podría esperarse considerable variabilidad. El hecho que se observa poca variabilidad enzimática entre los aislamientos sugiere que la mayoría de variantes electroforéticas son deletéreas o que un grupo de loci enzimáticos coadaptados en B. bassiana ha sido seleccionado bajo la influencia del hospedero.
Resumiendo, los resultados indican un alto nivel de similitud entre los aislamientos estudiados con sólo pequeñas variaciones en los marcadores moleculares. Esto es contrastante con la significativa variación fenotípica en patogenicidad y producción de enzimas extracelulares. La variabilidad de los diferentes resultados con las pruebas enzimáticas evaluadas muestra el amplio rango de hospederos del hongo B. bassiana y su poca clara especificidad.
