Abstract
Epidermal growth factor receptor-tyrosine kinase inhibitors (EGFR-TKIs) are established therapies for previously untreated advanced/metastatic non-small cell lung cancer (NSCLC) EGFR-mutated patients. Osimertinib, a third-generation TKI, has recently received the same first-line indication. This study aims at investigating management costs and potential productivity losses in Italy in this patient setting, given all the available therapeutic options. Two analyses were performed. The first evaluates first-line yearly management costs and potential productivity losses per patient, for each first-line treatment. The second, performed nationally and regionally, models all lines of treatments and costs over a five-year period, through different market-share scenarios – considering osimertinib adoption as new therapy in 60% of patients as the most probable one – and line-switch/mortality probabilities. Using this model, patients’ total months of treatment and development/progression of brain metastases were also analyzed. The first analysis shows that first-line management costs and potential productivity losses are minimized by osimertinib (first-line yearly expenditure of €25.942, 8%-12% less than TKIs). The second analysis, based on a five-year horizon and on all therapy lines, shows that total management costs and potential productivity losses decrease by increasing the adoption of osimertinib as a first-line therapy (€7.4m cumulative lower cost with osimertinib at 60% compared to 0%). Considering the average month of therapy, where results are not affected by the length of the therapy, with osimertinib at 60% on naïve patients, monthly management costs and productivity losses are 10% lower than in the non-osimertinib scenario. In advanced, metastatic EGFR-mutated NSCLC, the use of osimertinib as the first-line treatment could reduce patient management costs and potential productivity losses.
Keywords
Introduzione
Il tumore al polmone è il terzo tipo di tumore più frequentemente diagnosticato in Italia, con 41.800 nuovi casi nel 2017.
1
La forma clinica maggiormente prevalente è quella non a piccole cellule (
La prognosi è generalmente sfavorevole, essendo il tumore al polmone la prima causa di morte per tumore negli uomini e la terza nelle donne, con una sopravvivenza a cinque anni di 15,8%.
1
Tuttavia, le terapie target specifiche per il profilo molecolare del NSCLC sviluppate negli ultimi anni permettono una predizione migliore dei tassi di risposta e un aumento della sopravvivenza mediana dei pazienti.1,3 In particolare, l’utilizzo degli inibitori della tirosina chinasi (
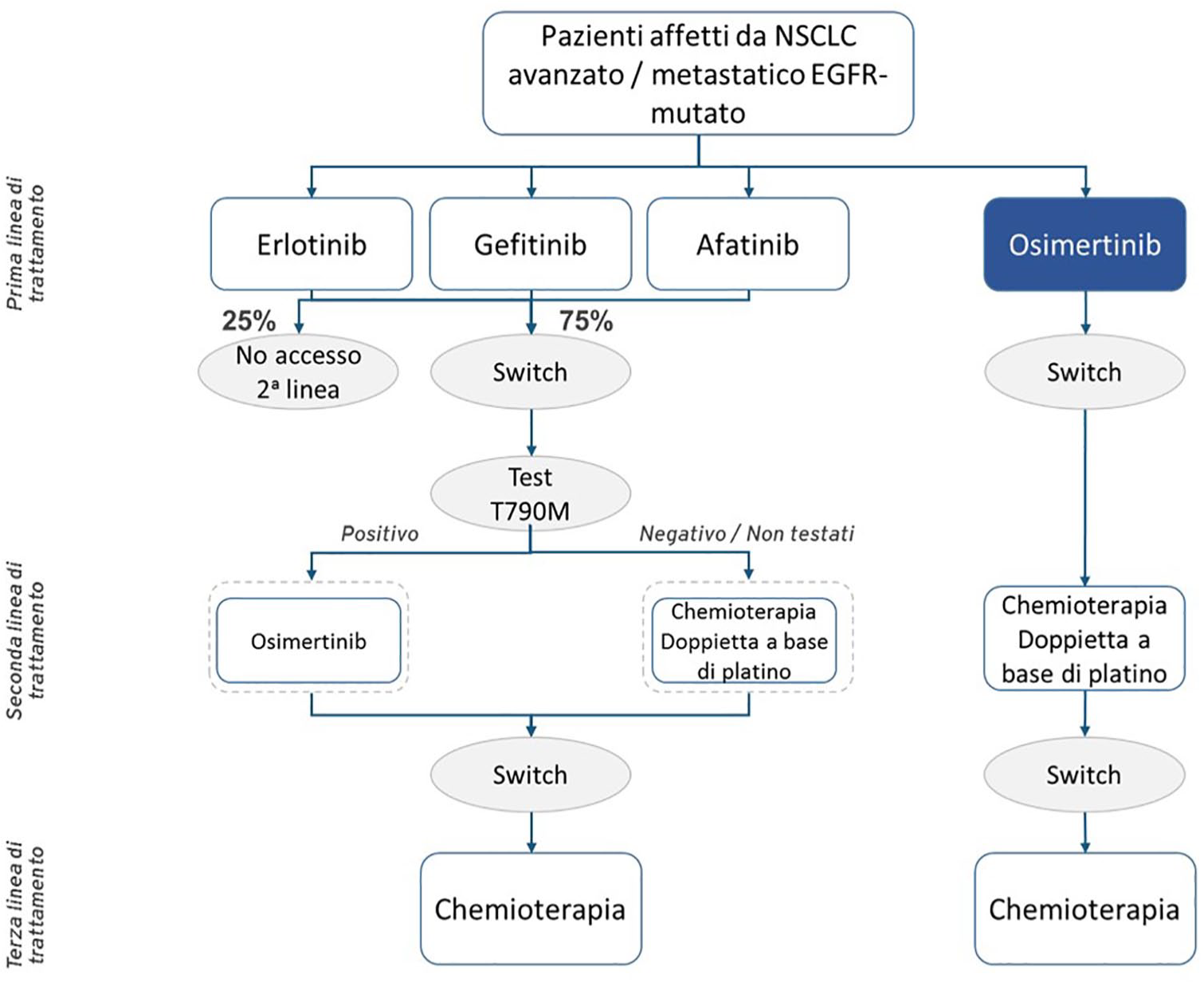
Percorso di trattamento nel tumore al polmone non a piccole cellule (NSCLC) avanzato/metastatico recettore del fattore di crescita dell’epidermide (EGFR)-mutato.
Nello studio clinico randomizzato di Fase III FLAURA 7 osimertinib in prima linea ha infatti mostrato un significativo aumento della sopravvivenza libera da progressione rispetto agli EGFR-TKI standard (18,9 vs 10,2 mesi), un tasso di sopravvivenza più elevato (83% vs 71% al mese 18), un buon profilo di sicurezza e una maggiore efficacia in pazienti con metastasi cerebrali (7% dei pazienti nel gruppo di osimertinib vs 16% nel gruppo degli standard TKI con eventi di progressione delle metastasi del sistema nervoso centrale7,9).
Secondo le ricerche di letteratura effettuate, al momento non esistono studi che valutino da un punto di vista economico la gestione del paziente affetto da NSCLC avanzato/metastatico EGFR-mutato e le relative potenziali perdite di produttività in Italia che includano osimertinib come possibile trattamento di prima linea. Pertanto, in questa sede si è deciso di prestare particolare attenzione a questi specifici capitoli di spesa, stimando il costo delle visite e degli esami, delle degenze ospedaliere, dei test diagnostici, della gestione degli eventi avversi, delle cure palliative e delle potenziali perdite di produttività in questa tipologia di pazienti.
Metodi
Disegno dello studio
Per valutare da un punto di vista economico la gestione del paziente affetto da NSCLC avanzato/metastatico EGFR-mutato e le relative potenziali perdite di produttività sono state effettuate due analisi:
Un’analisi di minimizzazione dei costi che confronta il costo annuo di gestione e la relativa potenziale perdita di produttività per ogni trattamento di prima linea in esame, per singolo paziente in Italia.
Un modello che simula il costo della gestione e le potenziali perdite di produttività per tutta la popolazione target su un orizzonte temporale di cinque anni, basato su quattro scenari di uptake delle quote di mercato di osimertinib in prima linea sui pazienti naïve. Il modello tiene conto delle durate mediane dei trattamenti, dei possibili switch tra diverse linee di trattamento e della probabilità di decesso dei pazienti ed è stato sviluppato sia a livello nazionale che regionale. È stato ritenuto opportuno considerare un orizzonte temporale di cinque anni in modo da raggiungere uno stato stazionario del modello, sulla base dei risultati clinici dei trattamenti in essere, e cogliere tutte le differenze significative in termini di costi ed effetti tra le alternative considerate.
I trattamenti considerati sono quelli riportati in Figura 1, con l’aggiunta della possibilità di effettuare una combinazione di TKI e chemioterapia come seconda linea di trattamento per i pazienti che non effettuano un test per ricercare la mutazione di resistenza T790M o che risultano negativi al test. Tale possibilità non è attualmente prevista dall’ordinamento standard italiano, ma è stata considerata sia per allineare l’analisi ai protocolli clinici dello studio FLAURA, da cui sono tratti i dati di efficacia utilizzati, sia per non escludere un trattamento che viene comunemente somministrato a questa tipologia di pazienti, come emerge dalla pratica clinica e viene confermato dai dati di mercato. Inoltre, è stata inserita la chemioterapia come possibilità di trattamento per i pazienti positivi al test T790M oltre a osimertinib, in base al dato di mercato. 10 In particolare:
Prima linea: standard EGFR-TKI – gefitinib, afatinib ed erlotinib – e osimertinib
Seconda linea: chemioterapia con doppietta a base di platino (pemetrexed e cisplatino), TKI + chemioterapia con doppietta a base di platino (pemetrexed e cisplatino) e osimertinib
Terza linea: chemioterapia
I costi considerati sono i costi di gestione e monitoraggio della patologia, i costi degli eventi avversi dovuti al farmaco, i costi delle cure palliative e le potenziali perdite di produttività (dettagli di input riportati in Appendice, nelle Tabelle Supplementari 1-7).
Gestione e monitoraggio
I costi di gestione e monitoraggio della patologia includono le visite oncologiche, le analisi del sangue, le radiografie, le tomografie, la somministrazione delle terapie endovenose, le ospedalizzazioni causate da una acutizzazione della patologia, il test diagnostico per ricercare la mutazione di resistenza T790M e la gestione delle metastasi del sistema nervoso centrale. Per la valorizzazione delle prestazioni sanitarie ambulatoriali a livello nazionale si è utilizzato il nomenclatore tariffario nazionale di riferimento, mentre per l’analisi delle singole regioni sono state considerate le tariffe a livello regionale; nel caso di mancanza del dato regionale, questo è stato assimilato a quello nazionale. Per la valorizzazione dei ricoveri ospedalieri, nell’analisi nazionale la tariffa è stata calcolata come media ponderata dei dati regionali, mentre nell’analisi regionale sono stati utilizzati i dati a livello regionale.
In conformità alla pratica clinica, è stato considerato che le visite oncologiche e gli esami del sangue vengano effettuati ogni qual volta il farmaco è somministrato/erogato al paziente 4 , mentre che le radiografie e le tomografie abbiano una frequenza trimestrale. Per calcolare l’impatto economico delle visite e degli esami, sono state considerate le tariffe nazionali/regionali per le prestazioni specialistiche ambulatoriali 11 (Tabella Supplementare 1).
Per calcolare le spese di somministrazione della chemioterapia è stato utilizzato il costo di day hospital, ridotto del 90%, in accordo con quanto appro-vato nella “Conferenza Stato-Regioni 2014,”12,13 moltiplicato per la frequenza di somministrazione del farmaco 14 (Tabella Supplementare 2).
I costi relativi alle ospedalizzazioni dovute a una acutizzazione della patologia sono stati calcolati come prodotto tra i giorni medi di degenza nella tipologia di pazienti in esame per linea di terapia, derivanti da letteratura 15 e dalla pratica clinica, e il DRG giornaliero medio per il ricovero ospedaliero a causa di neoplasie respiratorie, 16 dato dal rapporto tra il totale della spesa annua dei ricoveri in regime ordinario e il numero totale annuo di giorni di ricoveri per la specifica patologia (Tabella Supplementare 3). Considerando che il sistema di rimborso dei ricoveri ospedalieri è basato su DRG fissi, il calcolo è stato effettuato con questa metodologia per valorizzare le differenze di costo tra le varie linee di trattamento.
Per quanto riguarda le metastasi del sistema nervoso centrale, sono stati inclusi i costi dei ricoveri ospedalieri per neoplasie del sistema nervoso, 16 dei cicli di radioterpia12,17 e dei relativi eventi avversi (di grado ⩾3 e con frequenza ⩾2%)16,18 e delle radiografie cerebrali.11,19 I costi sono stati calcolati sia per l’insorgere di metastasi durante il corso della terapia sia per la progressione delle stesse nei pazienti con neoplasie cerebrali secondarie già sviluppate all’inizio del trattamento.7,9 I dettagli sono riportati nella Tabella Supplementare 4.
Relativamente al test T790M, è stato considerato che tutti i pazienti precedentemente trattati con i TKI standard ed eleggibili a una re-biopsia siano sottoposti al test (~80% dei pazienti 3 ); nessun test è stato considerato necessario per i pazienti trattati con osimertinib in prima linea, in base alle attuali linee guida.4,5 È stato assunto che tutti i pazienti siano sottoposti a una biopsia tissutale, con valorizzazione pari a €850, 20 dato medio a livello Italia utilizzato sia per l’analisi nazionale che regionale (Tabella Supplementare 5).
Eventi avversi
La tipologia e la frequenza degli eventi avversi associati al farmaco sono stati ricavati dagli studi clinici.7,14,21–24 Sono stati inclusi solo gli eventi avversi di grado ⩾3 (per i quali è indicata l’ospedalizzazione 25 ) e con frequenza ⩾2% in modo da garantire una significatività del dato sia in termini di numerosità che di entità per il Servizio Sanitario Nazionale (SSN).
Al fine di quantificare l’impatto economico degli eventi avversi sono state utilizzate le Schede di Dimissione Ospedaliera (SDO), 16 moltiplicando una volta per ogni trattamento la tariffa media del singolo evento avverso, calcolata come rapporto tra il totale della spesa annuale per ricoveri di degenza ordinaria e il totale delle dimissioni annue, per la percentuale di pazienti trattata per tale evento avverso (Tabella Supplementare 6). Nel caso di doppia opzione delle voci dei DRG, con o senza complicanze, è stato considerato il DRG con complicanze, trattandosi di eventi avversi di grado 3 e 4.
Cure palliative
È stato assunto che le cure palliative vengano somministrate a tutti i pazienti durante l’ultimo mese di vita. Il costo proviene da letteratura ed è pari a €1.472 per paziente. 26
Perdite di produttività potenziali
Lo stato avanzato/metastatico della patologia ridefinisce gli ambiti di vita dei pazienti, a partire da quello professionale, obbligandoli a smettere di lavorare o ad assentarsi dal lavoro. 27 Ciò si riflette anche sui caregiver, che si prendono cura del paziente – soprattutto nei periodi di degenza ospedaliera o nei periodi di riacutizzazione 27 – potenzialmente generando perdite di produttività a livello regionale e nazionale.
Per stimare la potenziale perdita di produttività generata dal NSCLC con mutazione EGFR avanzato/metastatico (Tabella Supplementare 7):
Sono stati inclusi nell’analisi i pazienti in età lavorativa, ossia i pazienti con più di 15 anni, in base all’età minima lavorativa in Italia, e con meno di 67 anni, in base all’età media pensionabile italiana, considerando l’incidenza del tumore al polmone specifica per questa fascia d’età.28–30
Dei pazienti in età lavorativa, solo quelli occupati sono stati inseriti nell’analisi (90% per gli uomini, 88% per le donne). 30
Si è considerata come perdita di produttività del paziente il prodotto tra lo stipendio medio in base al dato ISTAT 31 e il periodo di assenza lavorativa. Quest’ultima voce è stata eguagliata all’anno per i pazienti che hanno dovuto abbandonare il proprio lavoro a causa del tumore 27 e al numero di giorni di ospedalizzazione per eventi avversi per la restante percentuale di pazienti.7,14,16,21–24
Per quanto riguarda la perdita di produttività dei caregiver, è stata inclusa anche in questo caso solo la popolazione in forza lavoro e si è considerato che i caregiver si debbano assentare dal lavoro durante le ospedalizzazioni dei pazienti.
Analisi 1: costo annuo di gestione del singolo paziente e relative potenziali perdite di produttività tra le diverse opzioni di trattamento in prima linea
Nell’analisi del costo annuo per paziente sono stati comparati i costi di gestione e le potenziali perdite di produttività del paziente affetto da NSCLC avanzato/metastatico EGFR-mutato in prima linea, ossia trattato con EGFR-TKI standard – erlotinib, gefitinib e afatinib – o osimertinib.
Analisi 2: costo di gestione dei pazienti in trattamento e relative potenziali perdite di produttività nell’orizzonte di cinque anni
Al fine di effettuare una stima consistente del costo della gestione del paziente per il SSN e delle potenziali perdite di produttività per la società, è stato sviluppato un modello Excel con un orizzonte temporale di cinque anni che tenga in considerazione tutta la popolazione target, il percorso clinico del paziente – includendo la durata mediana dei trattamenti e la probabilità di switch di linee e di mortalità – e le quote di mercato delle terapie in esame.
Popolazione target e quote di mercato
Il target è rappresentato dai pazienti affetti da NSCLC avanzato/metastatico EGFR-mutato naïve ed eleggibili a un trattamento con EGFR-TKI in prima linea (Tabella 1). La popolazione si basa su stime ISTAT. 32 I tassi di incidenza utilizzati nel modello sono stati assunti costanti negli anni.
Popolazione target e quote di mercato.
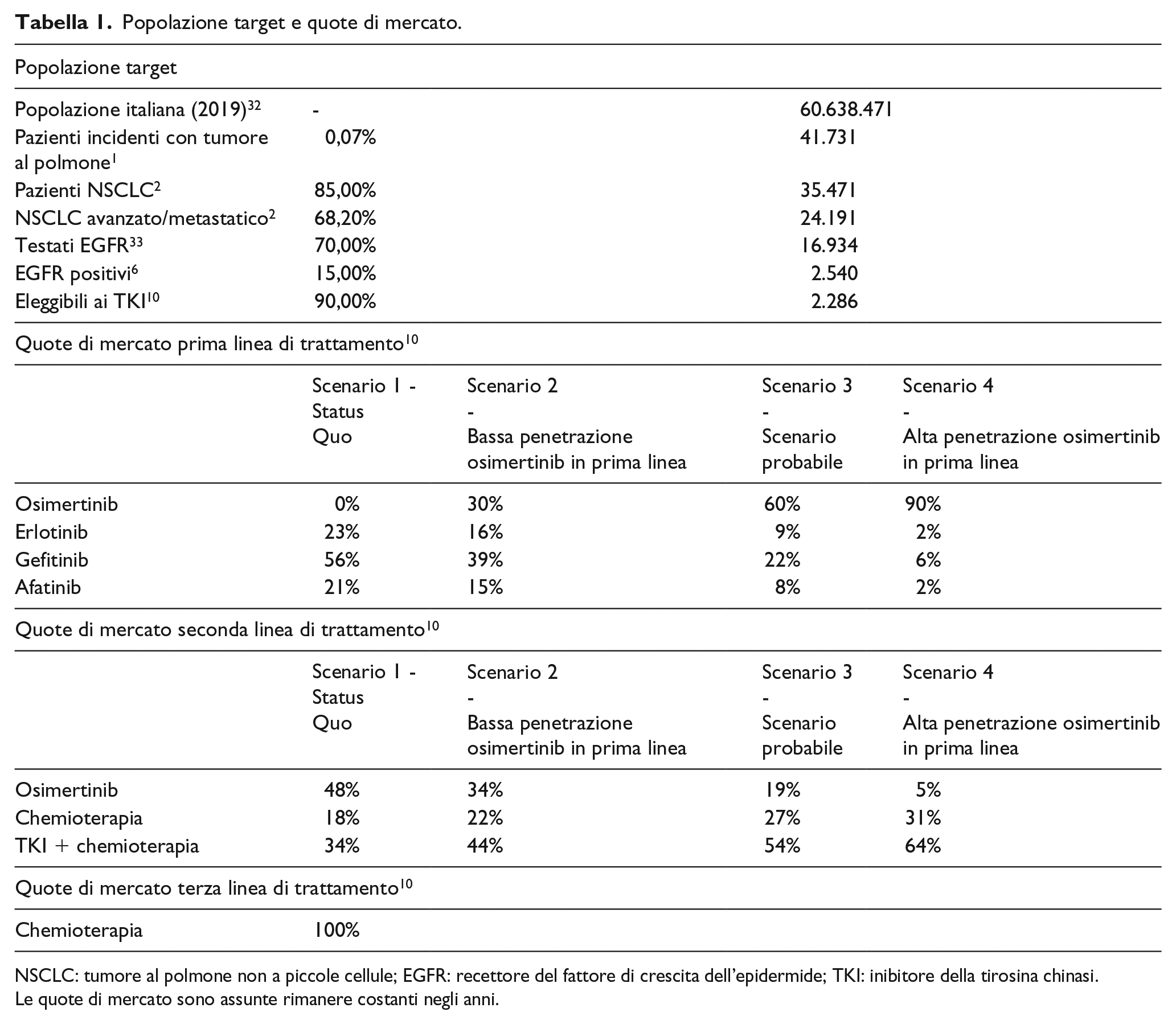
NSCLC: tumore al polmone non a piccole cellule; EGFR: recettore del fattore di crescita dell’epidermide; TKI: inibitore della tirosina chinasi.
Le quote di mercato sono assunte rimanere costanti negli anni.
Le quote di adozione dei trattamenti sono state tratte dai dati di mercato (Tabella 1) 10 e sono attese rimanere stabili negli anni. 10 Per la prima linea sono stati considerati quattro scenari di uptake di quote di mercato di osimertinib sui pazienti naïve, con un’adozione di osimertinib rispettivamente in 0%, 30%, 60% e 90% dei pazienti. I due scenari principali sono il primo, in quanto corrispondente allo status quo, e il terzo, con quote di mercato di osimertinib pari al 60%, in quanto ritenuto il più probabile in base alle stime di mercato. 10 I due scenari ulteriori sono stati analizzati per valutare la sensibilità del modello e la solidità dei risultati. Le quote di mercato di seconda linea variano al variare dell’uptake di quote di mercato di osimertinib sui pazienti naïve. Infatti, dal momento che i pazienti trattati con osimertinib in prima linea non possono assumere lo stesso farmaco in seconda linea, maggiore è l’uptake di osimertinib in prima linea, minori saranno le sue quote di mercato in seconda, mentre maggiori saranno le quote di mercato degli altri trattamenti di seconda linea, per i quali è stata mantenuta la proporzione di utilizzo corrente.
Efficacia clinica e percorsi di trattamento
I percorsi di trattamento dei pazienti sono stati sviluppati considerando che i pazienti incidenti naïve entrino ogni mese nel modello, per tutti e cinque gli anni dell’orizzonte temporale considerato. I pazienti incidenti mensili sono stati calcolati dividendo per 12 il numero di pazienti incidenti annui.
Per lo sviluppo del modello, è stato assunto che ogni mese i pazienti incidenti inizino un trattamento e ogni mese successivo al primo possano continuare con lo stesso trattamento, iniziare una seconda linea o morire. Lo stesso approccio è stato applicato alla seconda linea di trattamento. La terza linea invece è stata considerata come l’ultima linea di trattamento prima del decesso.
Durata mediana di trattamento
Al fine di calcolare la durata mediana del trattamento (Tabella 2) si è considerato il dato di tempo mediano di sopravvivenza libera da eventi (
Durata mediana del trattamento.
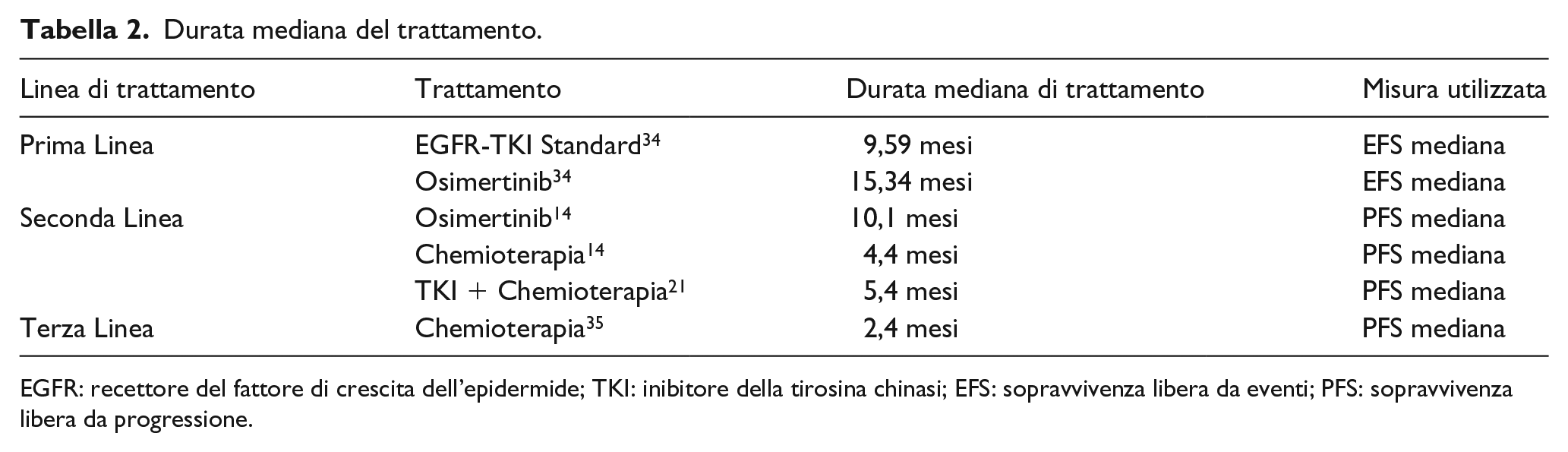
EGFR: recettore del fattore di crescita dell’epidermide; TKI: inibitore della tirosina chinasi; EFS: sopravvivenza libera da eventi; PFS: sopravvivenza libera da progressione.
Cambio di trattamento e mortalità
Per la prima linea di terapia, la probabilità di un cambio di trattamento o di morte si basa sul tempo intercorso tra l’inizio del trattamento e la prima data di progressione del tumore o di interruzione del trattamento. I dati sono tratti dallo studio clinico FLAURA 34 (Figura 2):
A 15,34 mesi il 50% dei pazienti nel braccio di osimertinib ha interrotto il trattamento di prima linea, ha registrato una progressione del tumore o è deceduto durante la prima linea di trattamento
A 9,59 mesi il 50% dei pazienti nel braccio degli EGFR-TKI standard ha interrotto il trattamento di prima linea, ha registrato una progressione del tumore o è deceduto durante la prima linea di trattamento
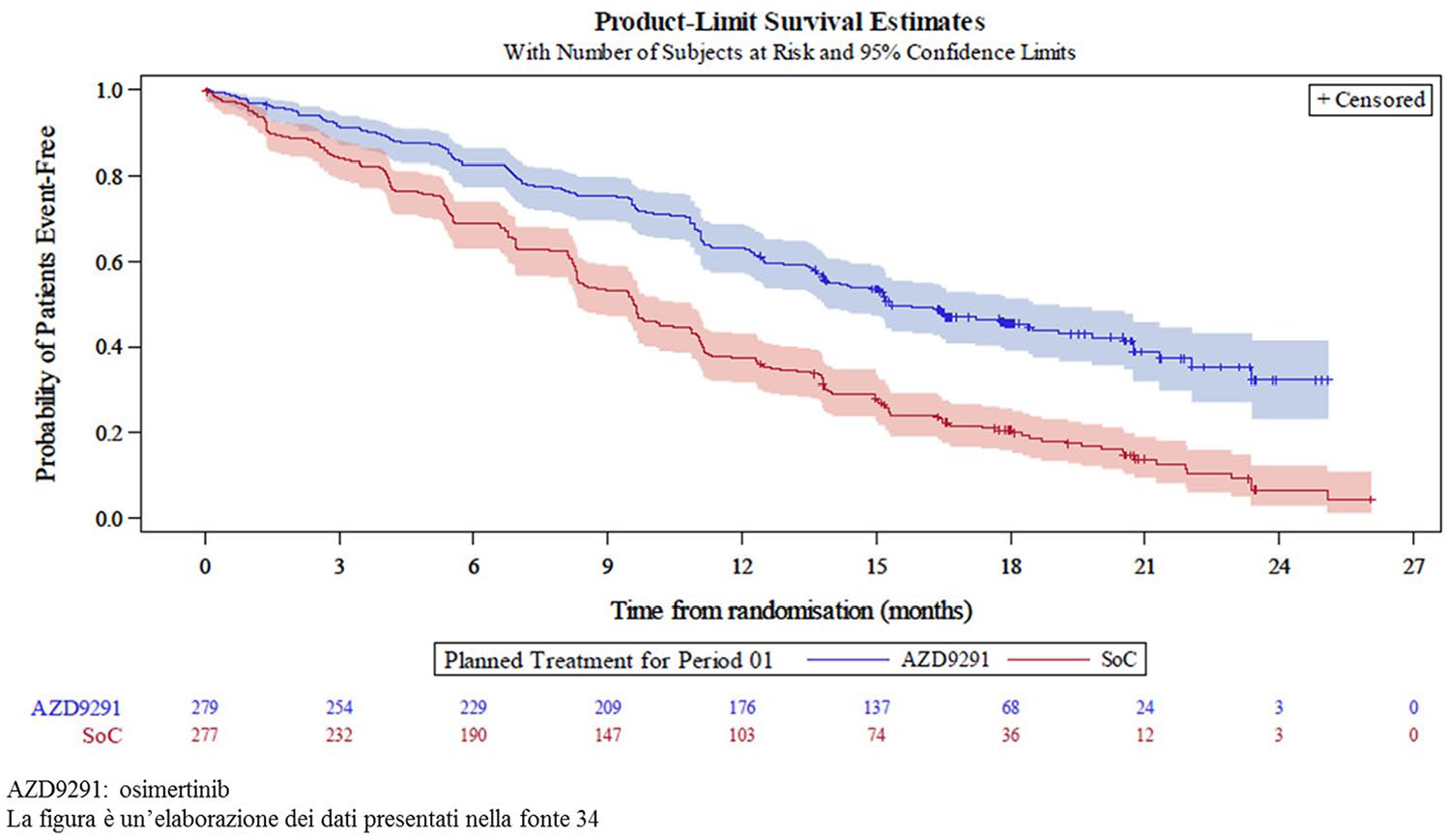
Sopravvivenza libera da eventi con i trattamenti di prima linea.
La suddivisione tra lo switch a linee successive alla prima e i decessi è stata ricavata dallo studio clinico FLAURA 34 :
Nel braccio di osimertinib 12% dei pazienti è deceduto senza iniziare una seconda linea
Nel braccio dei TKI standard 17% dei pazienti è deceduto senza iniziare una seconda linea
Per la seconda e la terza linea di trattamento è stato adottato un approccio simile, modellando le curve di cambio di trattamento o morte come curve best-fit, specifiche per ogni trattamento e basate sulla sopravvivenza libera da progressione, in particolare:
La probabilità di cambio di trattamento o morte in una linea successiva alla prima è stata calcolata interpolando le curve di PFS dei trattamenti di seconda e terza linea presi in considerazione14,21,35 con i dati presentati nello studio FLAURA 34 relativi al numero di pazienti che permangono in una linea di trattamento successiva alla prima dopo aver iniziato un trattamento di prima linea con TKI standard o con osimertinib.
Per quanto riguarda la seconda linea, ogni mese è stato calcolato il numero di pazienti che hanno effettuato uno switch in terza linea o sono deceduti, sulla base della suddivisione tra numero di switch e di decessi in seconda linea riportata nello studio clinico FLAURA 34 ; si è invece assunto che in seguito a una terapia di terza linea tutti i pazienti siano deceduti. Per differenza, la percentuale di pazienti che non ha iniziato una linea successiva di trattamento e non è deceduta è stata considerata permanere in trattamento.
I dettagli relativi alle curve di mortalità sono presentati nella Figura Supplementare 1.
Calcolo dei mesi di trattamento totali
Tramite il modello è stata effettuata un’analisi ulteriore, basata sullo studio clinico FLAURA, 34 per calcolare nei diversi scenari i mesi totali di trattamento nella popolazione target. Il calcolo è stato effettuato come prodotto tra il numero di pazienti in trattamento e il numero di mesi per cui ogni paziente permane in trattamento, sulla base delle probabilità di switch e decesso relative alle diverse sequenzialità di trattamenti e sulla base del mese di ingresso nel modello dei pazienti. Dal momento che nel modello i pazienti possono esclusivamente o essere in trattamento o essere deceduti, il totale dei mesi di trattamento può essere comparato al totale dei mesi di vita dei pazienti
Analisi del numero di pazienti con sviluppo/progressione di metastasi
Infine, dal momento che i pazienti affetti da tumore al polmone sono particolarmente soggetti allo sviluppo di metastasi al cervello, 7 è stato deciso di calcolare l’ammontare di pazienti con sviluppo/progressione di metastasi cerebrali negli scenari considerati. Il calcolo è stato effettuato considerando, in base al trattamento in atto, l’incidenza di sviluppo di metastasi nei pazienti senza metastasi a inizio trattamento7,9 sommata all’incidenza di progressione di metastasi nei pazienti con già metastasi sviluppate a inizio trattamento.7,9
Risultati
Analisi 1: costo annuo di gestione del singolo paziente e relative potenziali perdite di produttività tra le diverse opzioni di trattamento in prima linea
La Tabella 3 mostra il costo di gestione e le potenziali perdite di produttività in prima linea di un paziente affetto da NSCLC avanzato/metastatico EGFR-mutato per un anno. Dall’analisi risulta che per quanto riguarda sia il costo di gestione del paziente sia le potenziali perdite di produttività, osimertinib in prima linea minimizza i costi per il SSN e per la società, con un costo inferiore di 12% rispetto all’opzione che secondo la nostra analisi genera i costi più elevati (afatinib) e di 8% rispetto al TKI che genera l’esborso minore (gefitinib). La differenza più significativa in valore assoluto emerge nel costo di gestione delle metastasi (inferiore di 56% con il trattamento con osimertinib rispetto ai TKI standard), mentre a livello percentuale la differenza maggiore si riscontra nel costo del test per ricercare la mutazione T790M, che in seguito a osimertinib in prima linea secondo le linee guida non deve essere effettuato.
Costo di gestione e potenziali perdite di produttività annui per paziente e confronto tra osimertinib e i TKI standard – Prima linea di trattamento (€).
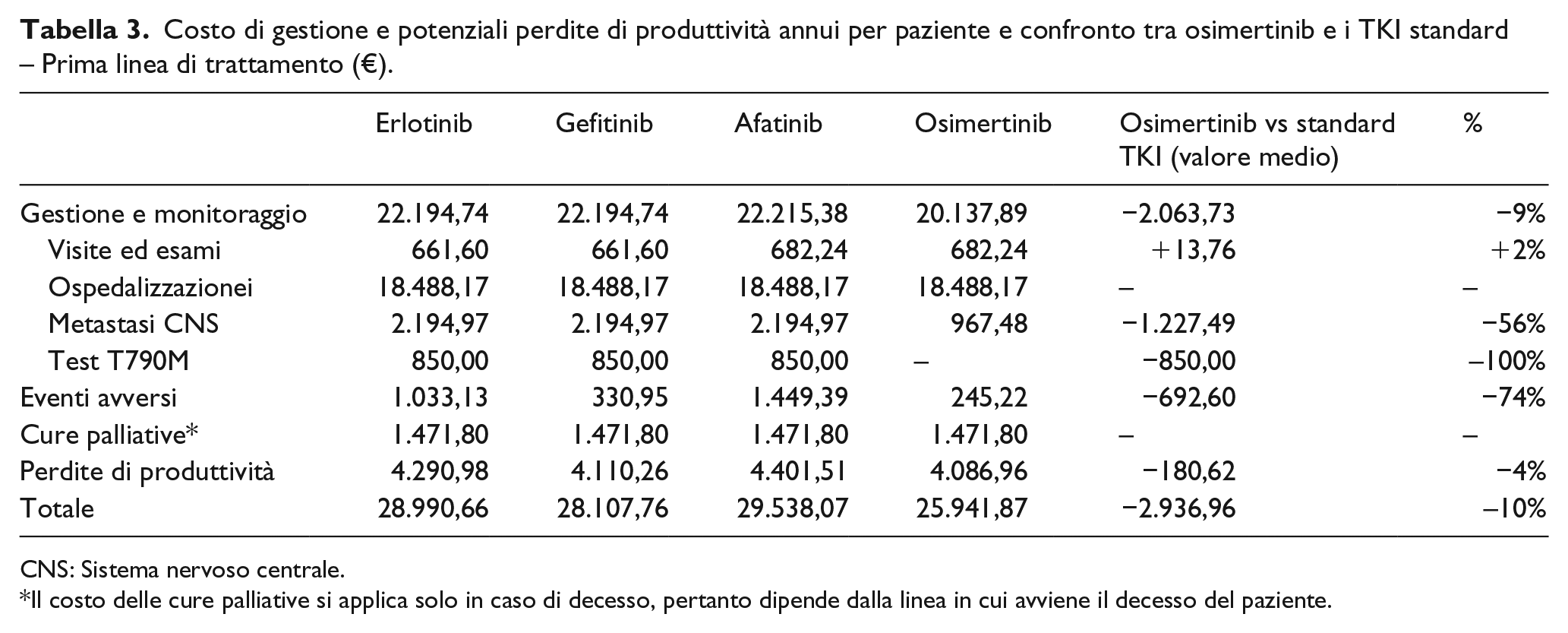
CNS: Sistema nervoso centrale.
Il costo delle cure palliative si applica solo in caso di decesso, pertanto dipende dalla linea in cui avviene il decesso del paziente.
Non si evincono differenze di costo tra osimertinib e i TKI standard per quanto riguarda le ospedalizzazioni: ciò è dovuto al fatto che, al meglio della nostra conoscenza, i dati di letteratura 15 relativi alla degenza ospedaliera in questa tipologia di pazienti sono aggregati per linea di terapia e non fanno distinzione per tipologia di trattamento.
Analisi 2: costo di gestione dei pazienti in trattamento e relative potenziali perdite di produttività nell’orizzonte di cinque anni
La seconda analisi effettuata dimostra che lo scenario più probabile di adozione di osimertinib, ossia con le quote di mercato di osimertinib in prima linea sui pazienti naïve pari a 60%, comporterebbe un risparmio di più di 7,4 milioni euro cumulati sui cinque anni rispetto a quello senza l’adozione del nuovo farmaco in termini di gestione del paziente e di relative potenziali perdite di produttività, generando un risparmio cumulato di 1,5% (Figura 4a). L’analisi di sensibilità effettuata mostra che il risparmio generato aumenta all’aumentare delle quote di mercato di osimertinib, superando 11 milioni euro cumulati con l’adozione di osimertinib nel 90% dei pazienti naïve.
Analizzando esclusivamente i costi di gestione del paziente (Figura 3a) il risultato è simile: il risparmio cumulato aumenta infatti all’aumentare delle quote di mercato di osimertinib. Tale risparmio dipende in maniera significativa dai minor costi derivanti dalla gestione delle metastasi, pari a 70% del risparmio cumulato complessivo (€8,7 milioni cumulati in meno per la gestione delle metastasi nel caso di osimertinib con quote di mercato al 60% rispetto a un utilizzo esclusivo dei TKI standard).
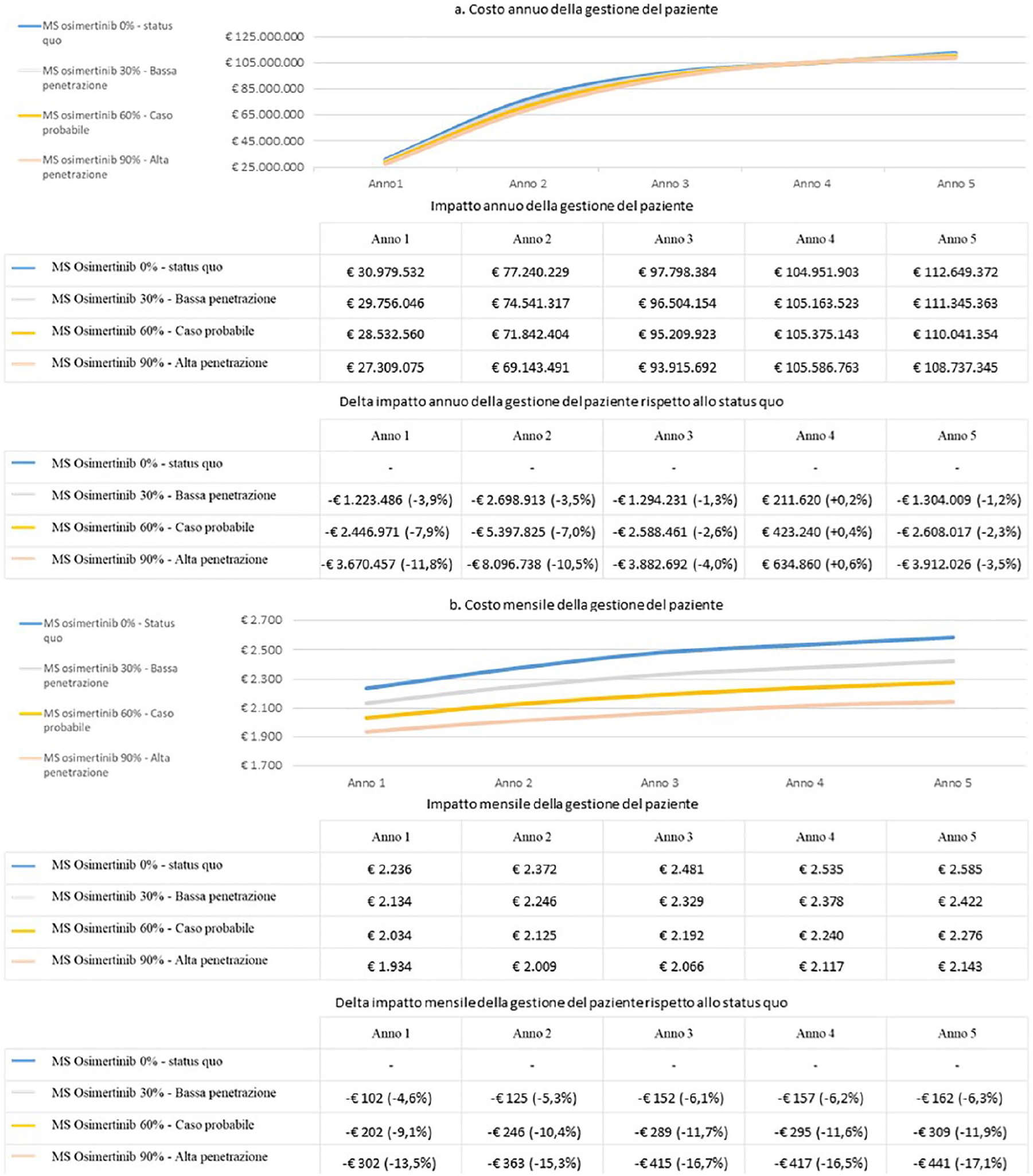
Costi di gestione del paziente affetto da NSCLC avanzato/metastatico EGFR mutato in Italia – valore assoluto e delta.
Tuttavia, come mostrano le Figure 3a e 4a, sia considerando il costo di gestione del paziente, sia aggiungendo il costo delle relative potenziali perdite di produttività, la variabilità tra i quattro scenari considerati non è elevata.
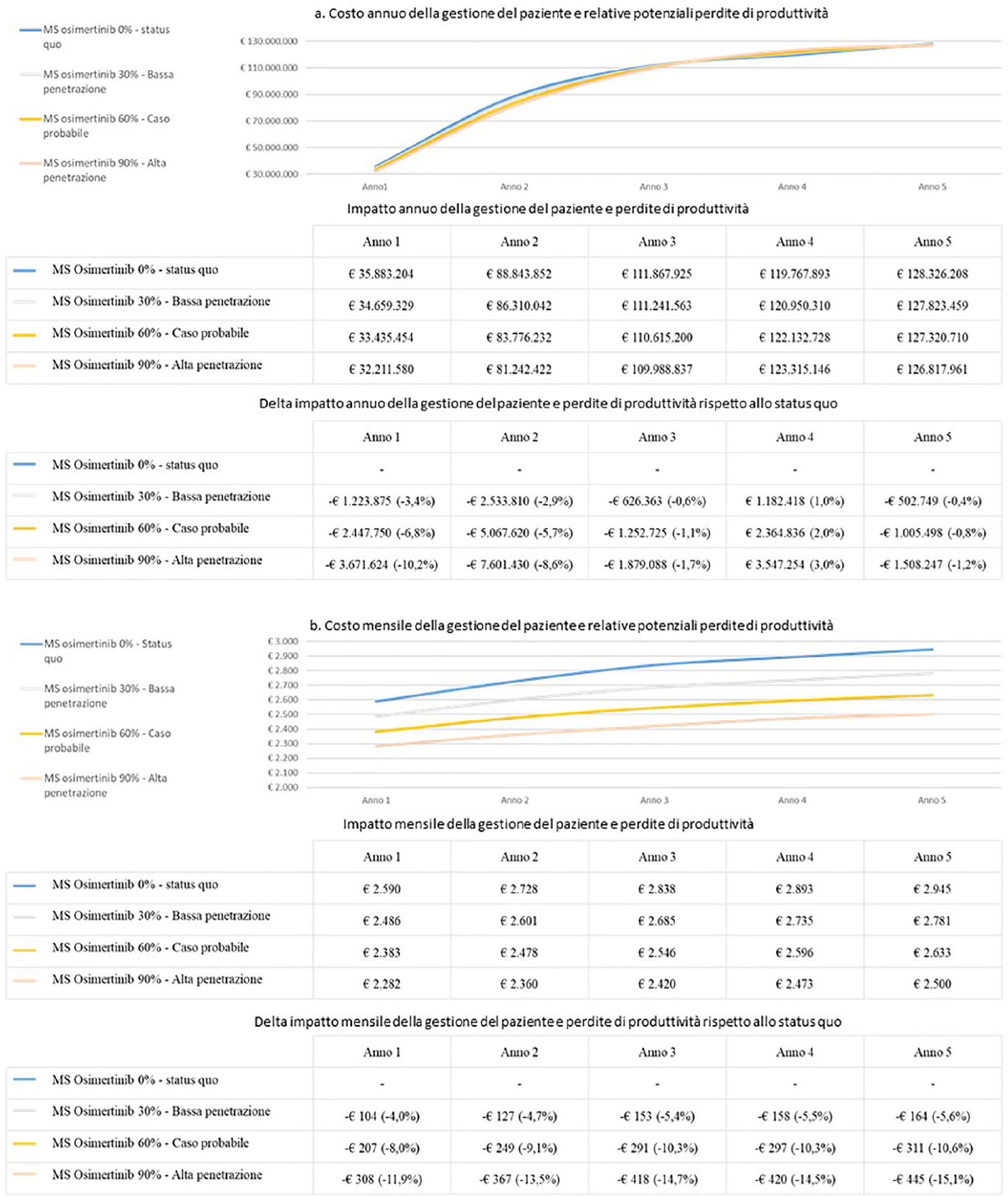
Costi di gestione del paziente affetto da NSCLC avanzato/metastatico EGFR mutato e relative potenziali perdite di produttività in Italia – valore assoluto e delta.
Analizzando invece il costo mensile della gestione del paziente e le relative potenziali perdite di produttività (Figura 4b), calcolato come rapporto tra il costo annuo della gestione del paziente e delle relative perdite di produttività e il numero di mesi di trattamento, si evidenzia un risparmio medio del 10% nel caso di quote di mercato di osimertinib pari a 60% rispetto allo scenario in cui tutti i pazienti sono trattati con gli EGFR-TKI standard. Analizzando esclusivamente il costo mensile della gestione del paziente (Figura 3b), senza considerare le relative potenziali perdite di produttività, il risparmio medio nel caso di quote di mercato di osimertinib pari a 60% rispetto allo scenario in cui tutti i pazienti sono trattati con gli EGFR-TKI standard risulta pari a 11%.
L’analisi di sensibilità effettuata mostra che il risparmio per mese di terapia sarebbe pari a 5% (6% senza considerare i costi sociali) nel caso dell’adozione di osimertinib nel 30% dei pazienti e a 14% (16% senza considerare i costi sociali) nel caso di quote di mercato di osimertinib pari a 90% (Figure 3b e 4b).
Tale risultato è dovuto al fatto che l’impatto totale è inficiato dalla maggiore sopravvivenza media dei pazienti che iniziano il trattamento con osimertinib rispetto a quelli trattati con i TKI standard e alla conseguente più lunga permanenza a carico del SSN. La sopravvivenza libera da progressione mediana che si ottiene con osimertinib è infatti pari a 19 mesi, contro i 10 mesi dei TKI standard. 7 Inoltre, la permanenza mediana in trattamento, considerando tutte le linee, è pari a più di 22 mesi per tutti i pazienti che iniziano il trattamento con osimertinib; per i pazienti che iniziano il trattamento con i TKI standard è invece pari a 22 mesi nel 50% dei casi: per l’altra metà dei pazienti si attesta attorno ai 16-17 mesi. Ciò è evidente nelle Figure 3a e 4a: fino all’anno 3 più sono elevate le quote di mercato di osimertinib, inferiori sono i costi di gestione e le potenziali perdite di produttività. L’anno 3 risulta essere un punto di pareggio: da quel momento le curve di costo diventano più elevate maggiori sono le quote di mercato di osimertinib. Dall’anno 3 infatti tutti i pazienti che hanno iniziato a essere trattati con TKI-standard all’anno 1 tendono a essere deceduti, a differenza dei pazienti trattati con osimertinib, che continuano a permanere a carico del SSN in percentuale maggiore, generando costi di gestione e potenziali perdite di produttività. Questo è valido fino alla fine dell’anno 4, anno in cui i delta di impatto riprendono il medesimo andamento dei primi tre anni analizzati: a partire dal quinto anno infatti anche la maggior parte dei pazienti che hanno iniziato il trattamento con osimertinib all’anno 1 risulta essere deceduta.
Analizzando le singole regioni il risultato è simile (dettagli nella Tabella Supplementare 8 e nella Figura Supplementare 2). Il costo di gestione del paziente e delle relative potenziali perdite di produttività cumulato sui cinque anni diminuisce all’aumentare delle quote di mercato di osimertinib; considerando invece l’impatto epurato dalla permanenza del paziente a carico del sistema sanitario a causa della maggiore sopravvivenza che si ottiene con osimertinib rispetto ai TKI standard si evidenzia, tra lo scenario con osimertinib adottato dal 60% dei pazienti e lo scenario senza osimertinib, una differenza di costo medio mensile della gestione del paziente e perdite di produttività di circa 10%. L’analisi di sensibilità conferma i risultati nazionali.
Calcolo dei mesi di trattamento totali
Tramite il modello sono stati inoltre stimati nei diversi scenari i mesi di trattamento cumulati dei pazienti, calcolati come prodotto tra il numero di pazienti in trattamento e il numero di mesi per cui ogni paziente permane in trattamento. I mesi di trattamento cumulati risultano pari a 170.830 senza l’adozione di osimertinib, 178.748 con le market shares di osimertinib pari a 30%, 186.666 con le quote di mercato pari a 60% e 194.584 con le quote di mercato pari a 90%, con una differenza tra lo scenario atteso e quello senza osimertinib di quasi 16.000 mesi (+9%), come mostrato nella Tabella 4.
Mesi di trattamento cumulati e pazienti con sviluppo/progressione di metastasi.
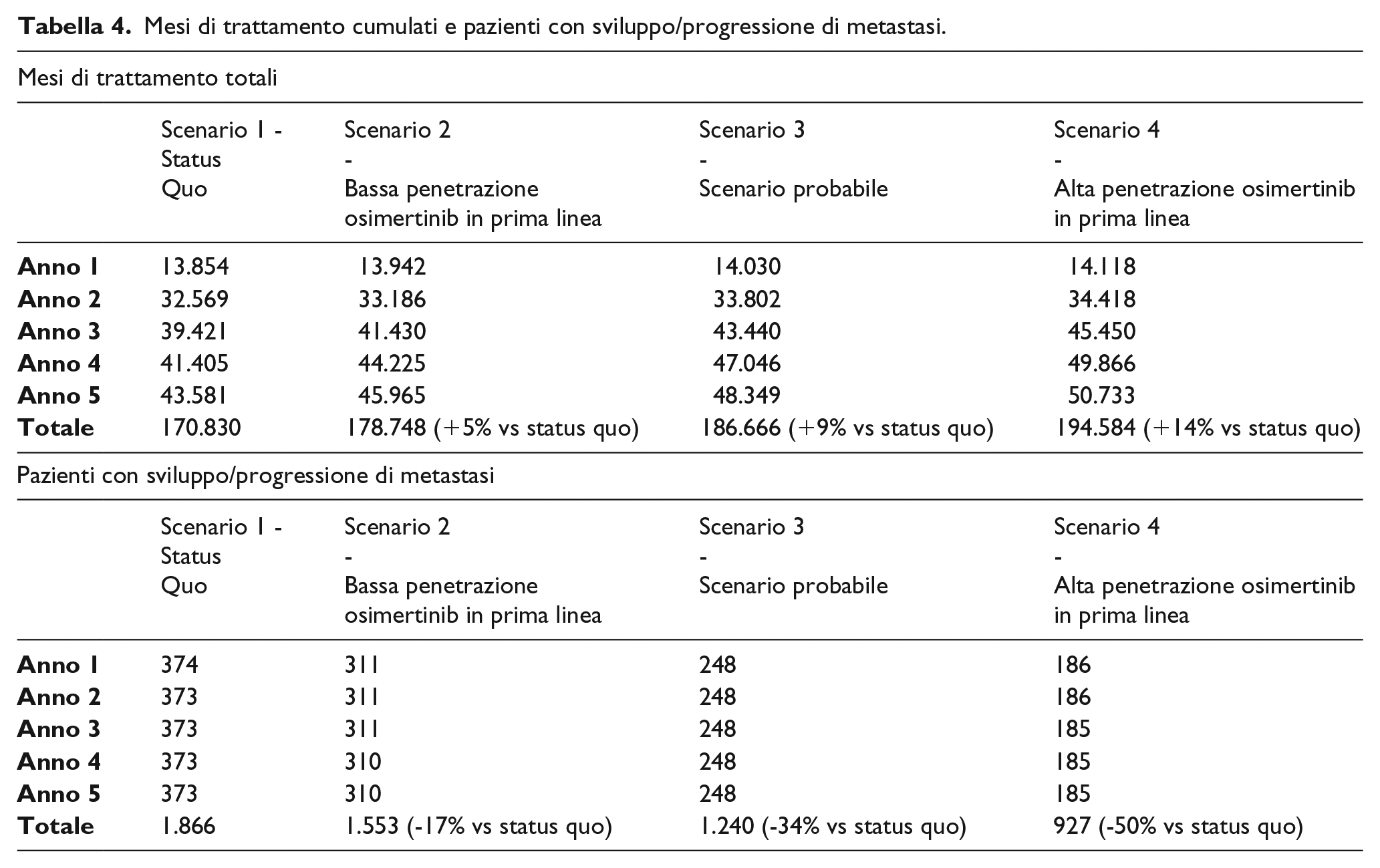
Analisi del numero di pazienti con sviluppo/progressione di metastasi
Infine, per quanto riguarda le metastasi al sistema nervoso centrale, l’adozione di osimertinib per il 60% della popolazione target prevede una riduzione di oltre 600 pazienti con sviluppo/progressione di metastasi rispetto allo scenario senza osimertinib (34% pazienti con metastasi in meno rispetto a osimertinib con 0% di quote di mercato), come evidenziato nella Tabella 4.
Discussione
Questo è a oggi, da quanto ci risulta, il primo studio in Italia relativo al costo di gestione e alle relative potenziali perdite di produttività nel paziente affetto da tumore al polmone non a piccole cellule avanzato/metastatico con mutazione EGFR che includa anche osimertinib come opzione terapeutica di prima linea.
La nostra analisi di minimizzazione dei costi dimostra che il costo di gestione e le potenziali perdite di produttività annuali in prima linea di trattamento varia da €25.942 per un paziente medio trattato con osimertinib a €29.538 per un paziente medio trattato con afatinib, generando un risparmio potenziale al primo anno di trattamento pari a 10% utilizzando osimertinib rispetto a uno standard EGFR-TKI.
La valutazione del costo di gestione del paziente e delle relative potenziali perdite di produttività a cinque anni ha mostrato un risparmio medio di 10% per mese di terapia nel caso di quote di mercato di osimertinib pari a 60% vs 0%. Data la permanenza in terapia più elevata per i pazienti trattati con osimertinib rispetto che con i TKI standard, la nostra analisi dimostra inoltre che il risparmio totale si appiana in seguito al terzo anno di trattamento considerando l’impatto totale per il SSN e la società, se pur con un risparmio di più di 7,4 milioni euro cumulati sui cinque anni tra lo scenario con osimertinib con il 60% di quote di mercato rispetto a quello senza l’adozione del nuovo farmaco.
Tuttavia, lo studio presenta alcune limitazioni. Innanzitutto, da quanto ci risulta, non ci sono dati del mondo reale italiani riguardanti l’efficacia dei trattamenti di prima linea considerati: nello studio sono stati usati dati provenienti da studi clinici randomizzati. Abbiamo infatti considerato che in mancanza di dati del mondo reale, la robustezza degli studi clinici utilizzati li renda una fonte attendibile per i dati presentati. È di interesse degli autori approfondire il tema non appena dati del mondo reale saranno disponibili.
In aggiunta, dal momento che osimertinib è stato appena approvato come prima linea di trattamento, è possibile che si assisterà a dei cambiamenti nelle linee guida per la seconda linea di trattamento sulla base dei risultati conseguenti all’adozione del farmaco. Osimertinib potrebbe infatti portare allo sviluppo di nuove forme di mutazioni nei pazienti refrattari,36,37 con conseguenti nuovi test diagnostici e differenti trattamenti da utilizzare. La nostra analisi è basata sui dati e sullo scenario più aggiornati possibile a oggi, confermati dalla pratica clinica.
Inoltre, in questo studio ci si è voluti focalizzare sul costo di gestione del paziente affetto da NSCLC avanzato/metastatico EGFR-mutato e sulle relative potenziali perdite di produttività, con l’obiettivo di spostare l’attenzione su un capitolo di spesa non sempre tenuto in considerazione. Tuttavia, un utile approfondimento futuro potrebbe essere quello di integrare l’analisi includendo anche il costo farmacologico.
Infine, parte delle curve di switch e mortalità provenienti dai risultati clinici non sono ancora definitive 7 e sono state stimate attraverso curve più adatte: sarebbe interessante effettuare un aggiornamento del modello, e quindi dei risultati qui presentati, non appena pubblicati dati definitivi.
Conclusioni
Nel complesso, al di là delle limitazioni, si ritiene che la presente valutazione riesca a presentare uno scenario attendibile del costo di gestione del paziente e delle potenziali perdite di produttività nel NSCLC avanzato/metastatico con mutazione EGFR. Osimertinib, oltre a essere il trattamento di prima linea attualmente approvato per il NSNCL avanzato/metastatico EGFR-mutato con la più lunga sopravvivenza libera da progressione e con il minor impatto sullo sviluppo/progressione di metastasi, genera un risparmio potenziale per il SSN e per la società nella gestione del paziente medio e nelle relative potenziali perdite di produttività.
Supplemental Material
Supplemental_Material – Supplemental material for Advanced-Metastatic Non-Small-Cell Lung Cancer EGFR-mutated in Italy: patient management costs and potential productivity losses
Supplemental material, Supplemental_Material for Advanced-Metastatic Non-Small-Cell Lung Cancer EGFR-mutated in Italy: patient management costs and potential productivity losses by Nicola Amedeo Mazzanti, Carolina Scauri, Bianca Domini, Chiara Vassallo, Simone Cusato, Chiara De Fino and Filippo de Marinis in Global & Regional Health Technology Assessment
Footnotes
Declaration of Conflicting Interest
Nicola Amedeo Mazzanti and Carolina Scauri are employees of AstraZeneca S.p.A. Bianca Domini, Chiara Vassallo, Simone Cusato and Chiara De Fino are employees of EY Advisory S.p.A., which received a grant from AstraZeneca S.p.A. to conduct the study and for work outside the submitted work. Filippo de Marinis received a fee from AstraZeneca S.p.A. as Advisor and Speaker.
Funding
This research was made possible by a grant from AstraZeneca, Italy
Supplemental material
Supplemental material for this article is available online.
References
Supplementary Material
Please find the following supplemental material available below.
For Open Access articles published under a Creative Commons License, all supplemental material carries the same license as the article it is associated with.
For non-Open Access articles published, all supplemental material carries a non-exclusive license, and permission requests for re-use of supplemental material or any part of supplemental material shall be sent directly to the copyright owner as specified in the copyright notice associated with the article.
