Abstract
Aim:
To assess the budget impact of the introduction of alemtuzumab in second-line treatment of active relapsing remitting multiple sclerosis (RRMS) patients, previously treated with interferon beta 1b, compared with natalizumab and fingolimod, from the Costa Rican Social Security (C.C.S.S.) perspective, with a time horizon of 5 years.
Methods:
A budget impact analysis (BIA) with a time horizon of five years was designed, considering the different percentages of administration of drugs used and forecasted by the Costa Rican Social Security (C.C.S.S.) to treat active RRMS, comparing the scenario of a base case, in which the first-line treatment with interferon beta 1-B S.C. and second-line treatments (fingolimod and natalizumab) are in place, against the alternative scenario with the introduction of alemtuzumab is included. The evaluation of the costs (in United States dollars, August2nd, 2016) (1) included most of direct medical resources (medication management, disease management, visits, diagnostic tests), excepting concurrent treatments. Unit costs were taken from the records of the C.C.S.S., specifically the Tariff Model Health Insurance First Half 2016 (2) and the Supply Management Information System (SIGES) (32). Both the National Clinical Practice Guidelines for the Treatment of Multiple Sclerosis (3),and RAND/UCLA methodology applied to an expert medical panel (4) were used to obtain the local resources used in the management of the disease. Additionally, regarding Budget Impact Models, a search and summary of evidence in PubMed database was performed (5). Finally, the ISPOR check list was selected for the evaluation of this work (6).
Results:
Considering a cohort of 118 patients with active RRMS, the mean global budget impact per five years would be $20.167.456USD$ in the base case and $19.644.090 USD$ in the scenario with alemtuzumab. The setting that includes alemtuzumab decreases the budget impact in 2,59% ($4.183USD$ per patient at 5 years). Pharmacological costs were the key drivers of total cost (82 %).
Conclusion:
The introduction of alemtuzumabrepresents a significant budgetary saving over the next five years. Higher benefits by reducing relapses, and a very manageable short-term regimen in most patients, allow recommending, both clinically and economically, the progressive and rational use of the product in this context.
Introducción
La Esclerosis Múltiple (EM) es la condición neurológica, causante de discapacidad, más común en adultos jóvenes e impone altos costos financieros y de calidad de vida en los pacientes, sus familias y la sociedad (7). Se trata de una enfermedad crónica de inicio en edades tempranas de la vida y con un curso clínico variable. Generalmente se manifiesta por un inicio con brotes caracterizados por signos clínicos de disfunción neurológica de diversa localización: trastornos visuales, alteraciones de la deambulación, trastornos sensitivos, problemas urinarios, entre otros. Los pacientes presentan una recuperación total o parcial entre los ataques. Al cabo de los años, en aproximadamente la mitad de los pacientes la enfermedad evoluciona de una forma en brotes a una fase progresiva que produce un grado de discapacidad, con importantes repercusiones en la calidad de vida y productividad de los pacientes, así como una carga para el sistema sanitario y para la sociedad (8). Las mujeres son más susceptibles que los hombres en razón de 2:1 (9). La forma de presentación más frecuente es la remitente recurrente (EMRR), que se caracteriza por la presencia de entre uno y dos episodios de déficit neurológico por año, que se resuelven, al menos parcialmente, con o sin tratamiento, en días o meses (10).
No existe un registro nacional de Esclerosis Múltiple en Costa Rica, y la información sobre su prevalencia es incompleta, razón por la cual no se la utiliza como indicador para determinar la población diana, sino los datos reales aproximados, de pacientes tratados con las terapias modificadoras de la enfermedad utilizadas en el estudio, según información proporcionada por la C.C.S.S. (11)
La Guía Nacional para el Tratamiento de la Esclerosis Múltiple indica que, para mediados del año 2015, se estaba llevando el control y tratamiento de casi 400 pacientes con Esclerosis Múltiple (3), de los cuales aproximadamente 80 reciben terapia con interferón beta-1b.
En los últimos años han surgido nuevos tratamientos para retardar la progresión de EMRR, tanto inmunomoduladores como inmunosupresores. Sin embargo, los medicamentos aprobados hasta la fecha sólo permiten la modificación del curso de la enfermedad, retrasando su progresión y evitando las recidivas.
La totalidad de los pacientes con Esclerosis Múltiple, salvo contadas excepciones, reciben atención por parte de la Caja Costarricense de Seguro Social (C.C.S.S.). Para comprender el papel protagónico de esta institución, se debe tener presente que el Sistema de Salud de Costa Rica presta servicios de salud, agua y saneamiento. El componente de servicios de salud incluye un sector público y uno privado y, a su vez, el sector público está dominado por la C.C.S.S., institución autónoma encargada del financiamiento, compra y prestación de la mayoría de los servicios personales de salud. La C.C.S.S. se financia con contribuciones de los afiliados, los empleadores y el Estado y administra tres regímenes, el seguro de enfermedad y maternidad, el seguro de invalidez, vejez y muerte, y el régimen no contributivo. (12).
Por disposición constitucional, el Servicio de Salud que presta la C.C.S.S. es universal y solidario (13) y cubre a todos los habitantes del país, con sujeción a las disposiciones reglamentarias vigentes (14). En congruencia con lo anteriormente indicado, la Ley General de Salud define a la salud de la población como un bien de interés público y estipula que es una función esencial del Estado velar por la salud de los costarricenses, garantizando el derecho a las prestaciones de salud a todos los habitantes del país (15).
Por medio de la Ley 6914, denominada “Reglamento para la compra de medicamentos, materias primas, reactivos y envases” y, adicionalmente, la Ley de Contratación Administrativa y su reglamento, la Caja Costarricense del Seguro Social adquiere los insumos y medicamentos necesarios para su gestión.
El Decreto Nº 19343-S es el instrumento normativo que contiene la relación oficial de medicamentos que deben ser utilizados por los servicios públicos en salud en la Caja Costarricense del Seguro Social. Este incluye el Formulario Terapéutico Nacional o la Lista Oficial de Medicamentos.
La Lista Oficial de Medicamentos muestra toda la medicación ofrecida por los centros de salud de la C.C.S.S. Cada uno está catalogado por tipo y clase. Este documento cuenta con 457 principios activos en 648 presentaciones farmacéuticas.
Para el tratamiento de primera línea de la enfermedad a nivel institucional, en la Lista Oficial de Medicamentos 2014 de la C.C.S.S. se encuentran disponibles los interferones beta: interferón β-1a intramuscular (IFNβ-1a im) e interferón β-1b subcutáneo (IFNβ-1b sc). Estos medicamentos son del tipo LOM almacenables, lo que quiere decir que su adquisición es por medio de licitaciones o compras anualizadas y se utiliza cuando los volúmenes de los productos son muy altos. Por otro lado, el interferón β-1a 22 μg subcutáneo (IFNβ-1a 22 μg sc) se adquiere ocasionalmente, por un trámite conocido como medicamentos LOM no almacenables (Z) o en tránsito. (16). Este mecanismo de adquisición se utiliza para cantidades mucho más pequeñas.
En la práctica médica habitual a nivel institucional, se inicia tratamiento de interferón β-1b subcutáneo e interferón β-1a 22 μg subcutáneo en alta carga lesional por Resonancia Magnética (9 o más lesiones). También consideran estas opciones si aparecen lesiones activas, aún cuando la carga lesional sea baja (en el raro caso que aun así no cumpla con criterios de Esclerosis Múltiple Clínicamente Diagnosticada). (3)
Hasta el año 2013, en Costa Rica se comenzaron a utilizar dos productos de segunda línea: natalizumab y fingolimod. Estos productos son adquiridos por medio del mecanismo de adquisición de medicamentos no incluidos en la lista oficial de medicamentos (no-LOM). Este mecanismo de compra se utiliza cuando el producto no está en la Lista Oficial de Medicamentos y cada paciente realiza el trámite.
La información recabada del Comité Central de Farmacoterapia refiere que, a julio del 2016, había 16 pacientes en tratamiento con natalizumab y 22 con fingolimod. (11)
Alemtuzumab 12 mg/1,2 ml para perfusión es un nuevo medicamento que no ha sido utilizado todavía en la Seguridad Social y es la intervención objeto de este estudio.
Aunque hay consenso de que las terapias modificadoras de la enfermedad pueden reducir la frecuencia de recaídas, su beneficio relativo (efectividad comparada entre una y otra) en la disminución de nuevas recaídas, o la progresión de la discapacidad, permanece poco claro debido al limitado número de estudios con comparaciones directas. Sin embargo, para valorar la eficacia relativa de las alternativas entre sí, en términos de tasa anualizada de recaídas, se pueden utilizar comparaciones indirectas obtenidas por un metaanálisis en red de Cochrane llevado a cabo en el 2015 (17). El metaanálisis en red mostró que, en términos del efecto protector contra la recurrencia de recaídas en EMRR, durante los primeros 24 meses de tratamiento, alemtuzumab, natalizumab y fingolimod superaron a otras drogas. La droga más efectiva fue alemtuzumab (riesgo relativo -RR- versus placebo 0,46, 95% de intervalo de Confianza -CI- 0,38 a 0,55; área bajo la curva de ranking acumulativo -SUCRA- 96%, nivel de evidencia moderado), seguido de mitoxantrona (sin interés para el caso en estudio, por no ser un producto utilizado en la Caja Costarricense de Seguro Social a la fecha), luego de natalizumab (RR 0,56, IC del 95%: 0,47 a 0,66; SUCRA 88%; nivel de evidencia alto) y fingolimod (RR 0,72, IC del 95%: 0,64 a la 0,81; SURA 71%; nivel de evidencia moderado). El metaanálisis de red concluye que, para prevenir recaídas, alemtuzumab, natalizumab y fingolimod son más efectivos que otras drogas, basado en nivel de evidencia de moderada a alta. (17).
Dada la naturaleza de la EM, estas terapias son de uso crónico, lo que supone una importante inversión para la C.C.S.S., que en el 2015 ascendió, sólo en interferones, a un monto de US$3.781.231,00. Los medicamentos de segunda línea actualmente utilizados, natalizumab y fingolimod, representaron, al primer semestre del 2016 una inversión cercana a US$1.500.000,00 anuales (11).
El objetivo del presente estudio es la estimación del impacto presupuestario de la inclusión de alemtuzumab como terapia de segunda línea en la población con EMRR activa en Costa Rica, según la perspectiva de la C.C.S.S.
Métodos
Muestra
Para la estimación de la población diana del análisis, se consideró el número aproximado de pacientes en tratamiento con interferón Beta 1B, natalizumab y fingolimod con EMRR que reciben tratamiento en la C.C.S.S. a junio del 2016, acorde con el consumo promedio determinado en el Sistema de Gestión de Suministros (SIGES) de la institución.
De acuerdo a los expertos consultados por medio del método RAND/UCLA, el 50% de la población de pacientes en tratamiento con interferón Beta 1b debería estar en otra terapia de segunda línea. Por esta razón, en el primer año, en el modelo se cambió el 50% de los pacientes bajo dicho tratamiento a las otras terapias del estudio.
La población diana de este estudio estaría constituida por 80 pacientes en tratamiento con este interferón, de los cuales el 50% cambia a segunda línea en el primer año. Asimismo, se incorporan 16 pacientes con natalizumab y 22 con fingolimod, que reciben tratamiento en el 2016 para EMRR activa (11). El crecimiento de pacientes en tratamiento a partir del primer año se ajustó de manera proporcional, aplicando la previsión de crecimiento de la población costarricense, estimada por el Instituto Nacional de Estadística y Censo. (18).
Alternativas Terapéuticas
Las alternativas terapéuticas evaluadas en el análisis incluyeron los siguientes medicamentos actualmente utilizados por la C.C.S.S. para el tratamiento de la EMRR activa:
En primera línea:
Interferón β-1b subcutáneo (IFNβ-1b sc): Betaferón®, Bayer Schering Pharma.
En segunda línea:
Fingolimod 0,5 mg cápsulas: Gilenya®, Novartis.
Natalizumab 300 mg/15 ml para uso endovenoso: Tysabri®, BiogenIdec.
Además, se incluyó el medicamento de segunda línea, para el cual se realiza el análisis de impacto presupuestario y que no ha sido utilizado todavía en la Seguridad Social, según se indica a continuación:
Alemtuzumab 12 mg/1,2 ml para perfusión: Lemtrada®, Sanofi Genzyme.
Modelo de análisis de impacto presupuestario
Un Análisis de Impacto Presupuestario predice cómo un cambio en la combinación de fármacos y otras terapias usadas para tratar una condición particular de salud tendrá un impacto en la trayectoria del gasto en esa condición. Puede ser utilizado para la planificación de presupuesto, previsión, y para calcular el impacto de los cambios en la tecnología de la salud en las primas de los seguros de salud (Mauskopf). En el presente trabajo, el desarrollo del modelo de impacto presupuestario se realizó mediante el programa Microsoft Excel 2011 para Mac, de acuerdo con las recomendaciones internacionales (27).
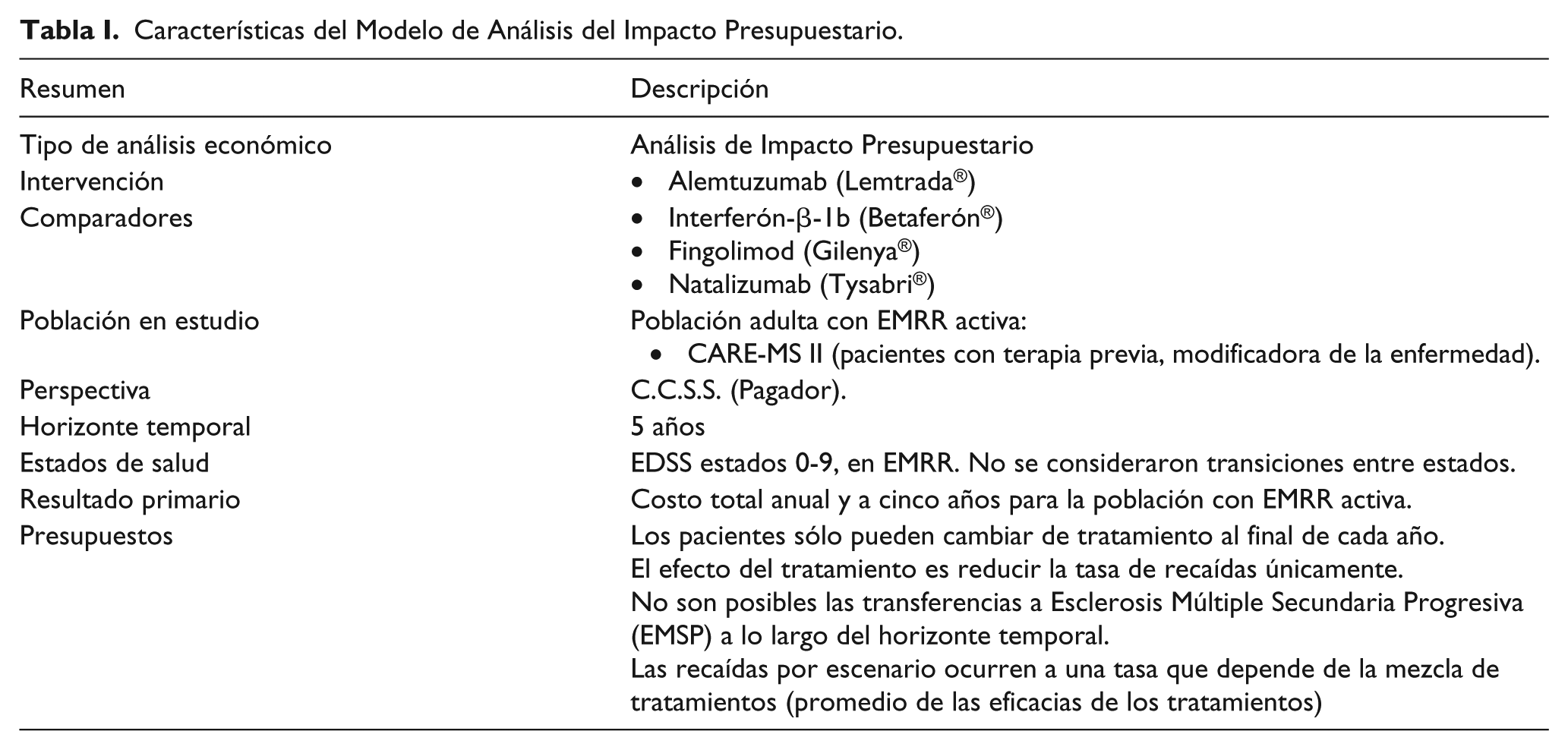
La tabla I muestra las características del modelo. Se ha utilizado una modelización estática. La tabla I resume las características básicas del modelo. Se emplea la Escala del Estado de Incapacidad Ampliada de Kurtzke (EDSS, por sus siglas en inglés) para distribuir los pacientes en el modelo. La EDSS de Kurtzke es una manera de cuantificar el avance de la enfermedad de una persona, enumerando las discapacidades relacionadas con la esclerosis múltiple, lo que permite a los neurólogos asignar una puntuación determinada a cada paciente. (Kurtzke 1983) (28). Sin embargo, el modelo asume que no hay transiciones entre los estados de EDSS a lo largo del horizonte temporal. El único efecto para las terapias modificadoras de la enfermedad incluido en el modelo es el número de brotes que requirieron o no hospitalización, experimentados. En el caso de alemtuzumab, se utiliza como referencia el estudio clínico CARE MS II, que es un estudio controlado aleatorizado de fase III de alemtuzumab en pacientes con esclerosis múltiple remitente recurrente, previamente expuestos a otra terapia modificadora de la enfermedad. (21).
Características del Modelo de Análisis del Impacto Presupuestario.
La población diana se determinó con base en el número de pacientes tratados con interferón beta 1b en el país, que son aquellos tratados en primera línea con EMRR activa (Fig. 1).
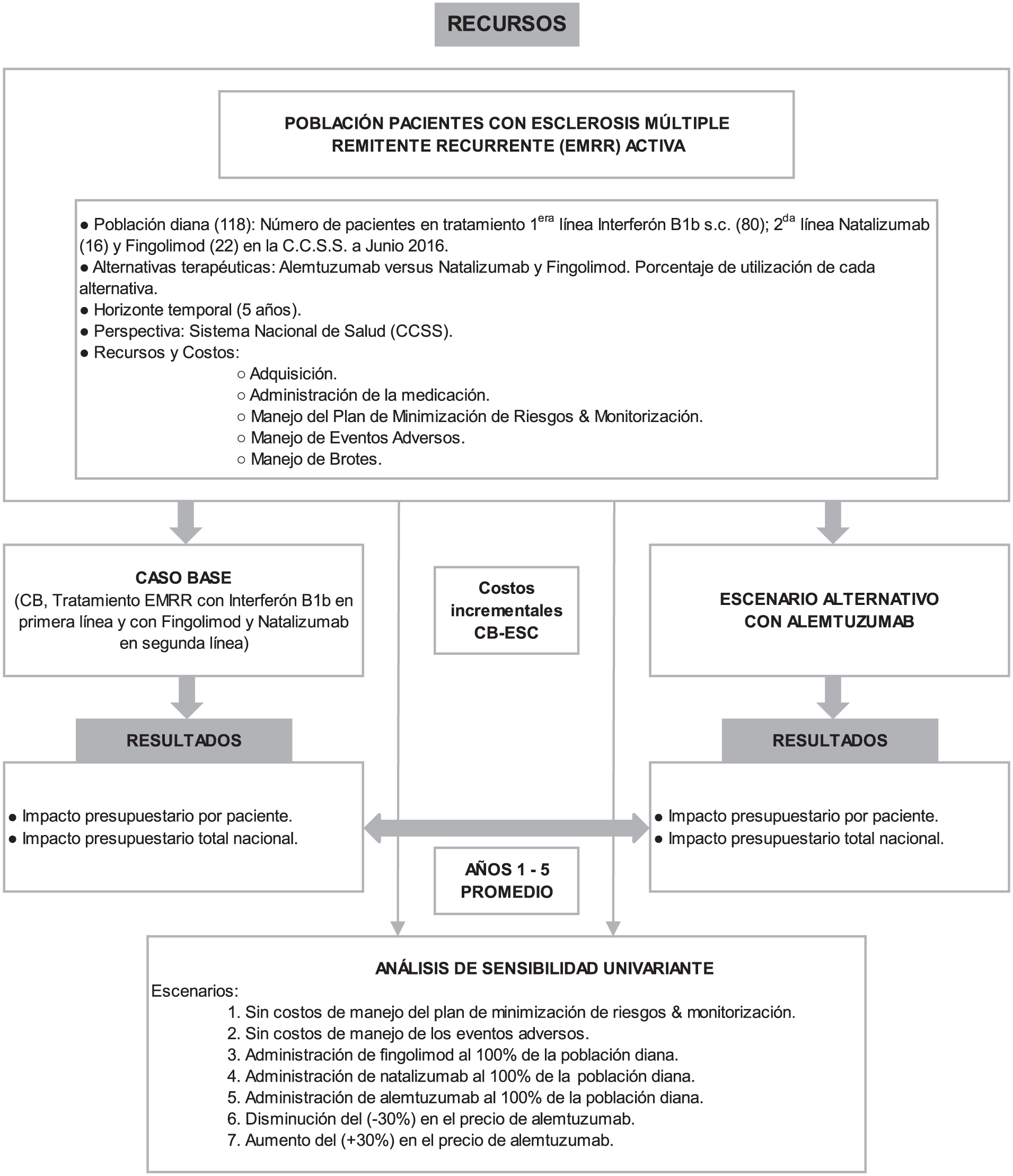
Esquema del Análisis de Impacto Presupuestario.
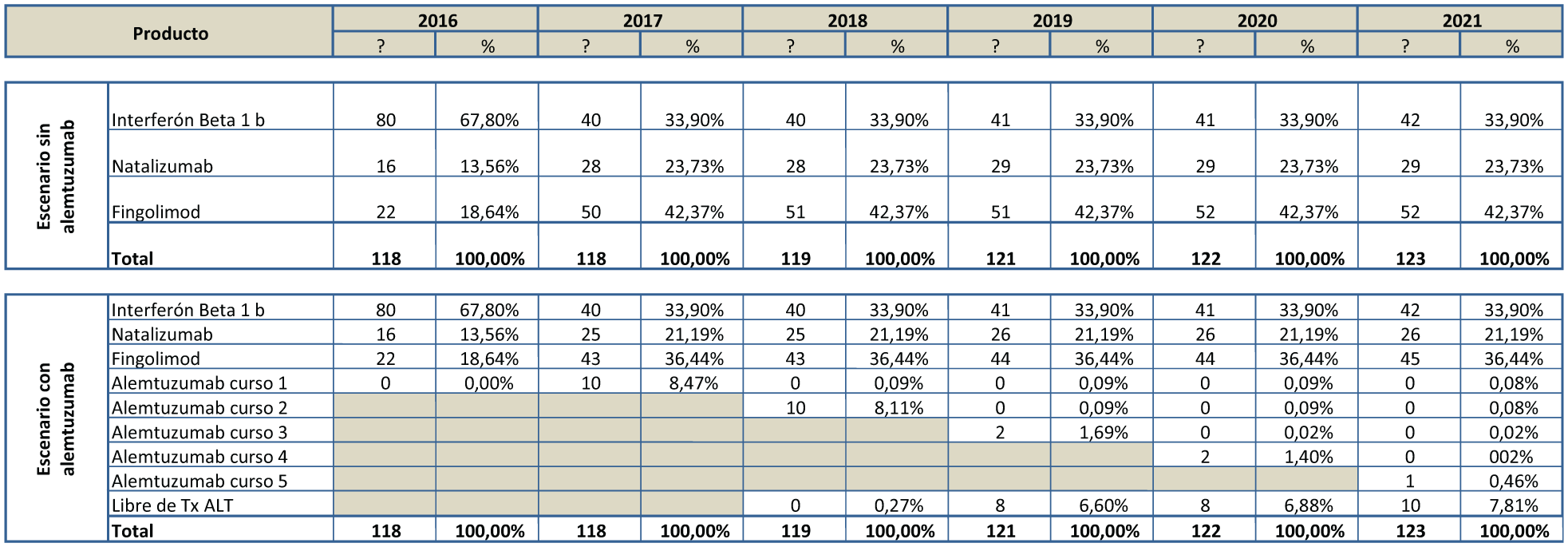
Se ha estimado un escenario de referencia o caso base, en el cual se incluyeron los porcentajes de utilización de cada uno de los fármacos indicados en primera línea y segunda línea para el tratamiento de los pacientes con EMRR activa. Este caso base se ha comparado con un escenario que recrea la incorporación de alemtuzumab, variando los porcentajes de participación de los diferentes tratamientos utilizados en la actualidad (Tabla II). De esta forma se puede calcular el costo incremental de la inclusión de alemtuzumab. En el caso base, de acuerdo con la información de la C.C.S.S., se consideró, la utilización proyectada de fingolimod y natalizumab en una proporción del 70% y 30% para los nuevos pacientes, respectivamente, los cuales son incorporados en su totalidad en el primer año. En el escenario con alemtuzumab se consideró una distribución de 25% de los nuevos pacientes con este producto, 52,5% para fingolimod y 22,5% para natalizumab. Asimismo, según la consulta a expertos, se asume la necesidad de transición a segunda línea, del 50% de los pacientes tratados con interferón beta 1b (4).
Distribución del mercado en pacientes con Esclerosis Múltiple Remitente Recurrente Activa en Costa Rica.
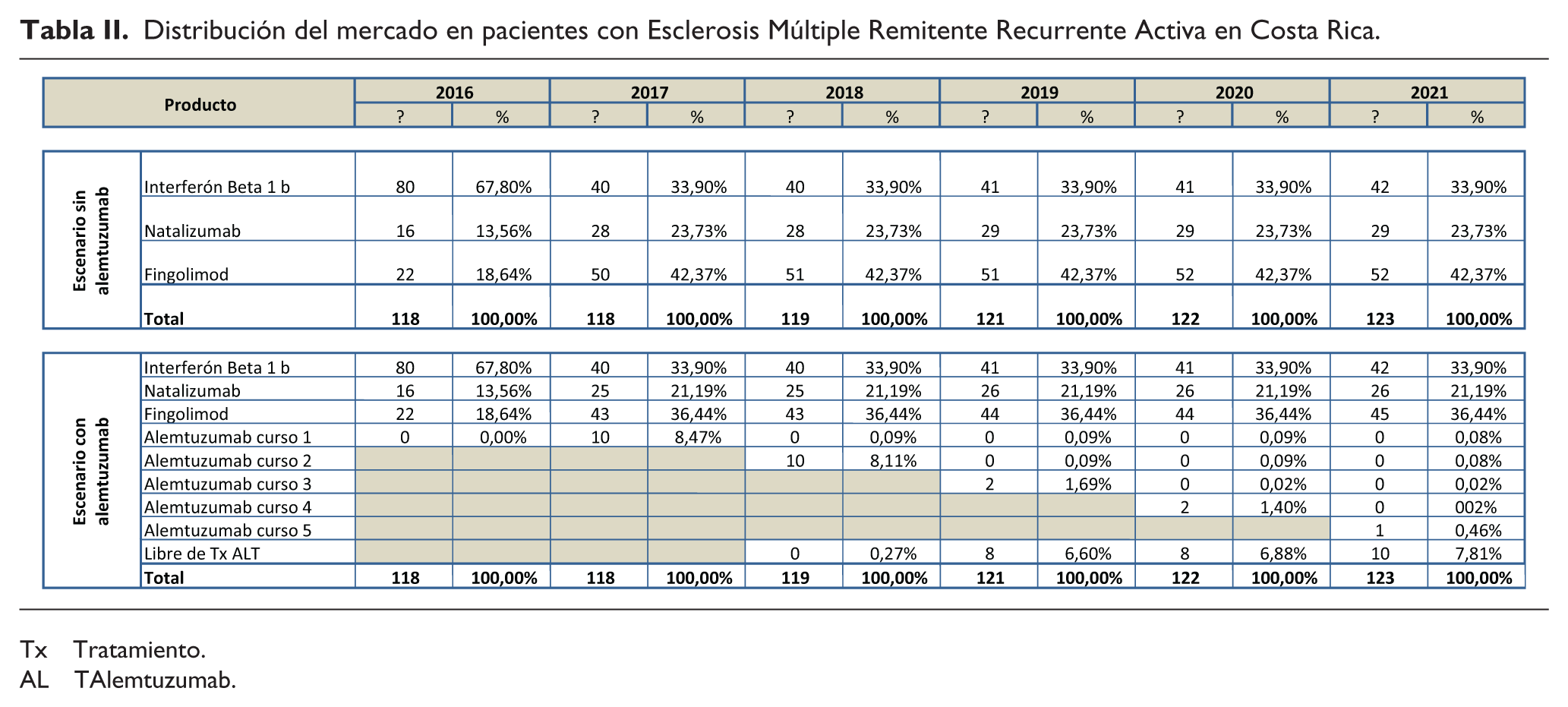
Tx Tratamiento.
AL TAlemtuzumab.
Horizonte temporal, perspectiva y tasa de descuento
El análisis se realizó utilizando un horizonte temporal de cinco años, según la perspectiva de la C.C.S.S., que es el proveedor de servicios sanitarios en Costa Rica. No se aplicó tasa de descuento ante la limitación de poder obtener el indicador más apropiado en el área sanitaria para efectos de este trabajo. (29).
Recursos
Debido a que el análisis se ha realizado siguiendo la perspectiva de la C.C.S.S., se consideraron únicamente los recursos relacionados con los costos directos sanitarios, que son los financiados por las autoridades sanitarias.
Medicamentos y costos de adquisición. (32)
Administración del tratamiento: El modelo asumió que la administración de las terapias intravenosas (natalizumab, alemtuzumab) es realizada por personal calificado, por lo que la administración intravenosa se asoció con una visita ambulatoria (en el caso de natalizumab) u hospitalización (en el caso de alemtuzumab). La terapia subcutánea (Betaferón) puede ser auto-administrada por el paciente. (4, 3, 2)
Manejo de la enfermedad: Para el manejo de la enfermedad se consideró la información obtenida de un panel de expertos y la evidencia clínica disponible. (4, 3)
Eventos adversos: Se seleccionaron los eventos adversos más frecuentes y severos de cada uno de los productos, de acuerdo a la evidencia clínica publicada correspondiente a interferón beta 1 b (19, 20), alemtuzumab (21), natalizumab (22, 23, 24) y fingolimod (25, 26). En cuanto a su manejo, se consideraron únicamente los medicamentos utilizados por el clínico para resolver los mismos, lo último basado en ProspectRx 2012 (34) y Medicaid 2012 (33).
Brotes y tasa anualizada de recaídas: Las tasas anualizadas de recaídas se basaron en la evidencia clínica de cada uno de los productos. (19, 20, 22, 23, 24, 25, 26). Para el manejo de los brotes se utilizó la información recopilada del panel de expertos consultados y la evidencia clínica disponible.
Los tratamientos concomitantes no se incluyen para efectos de este análisis.
Definiciones empleadas en el modelo
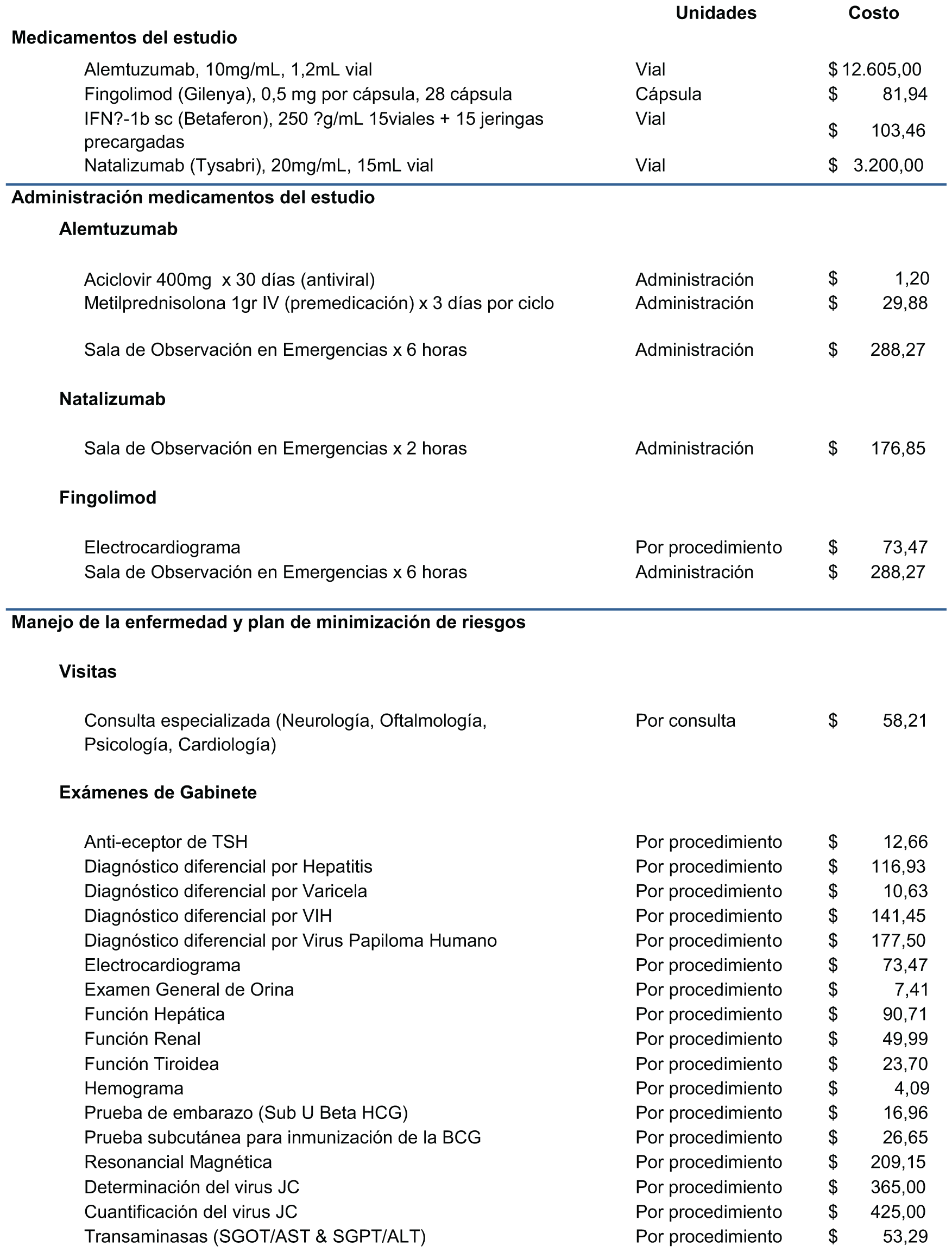
Costos Unitarios (Dólares americanos, tipo de cambio al 2 de agosto 2016).
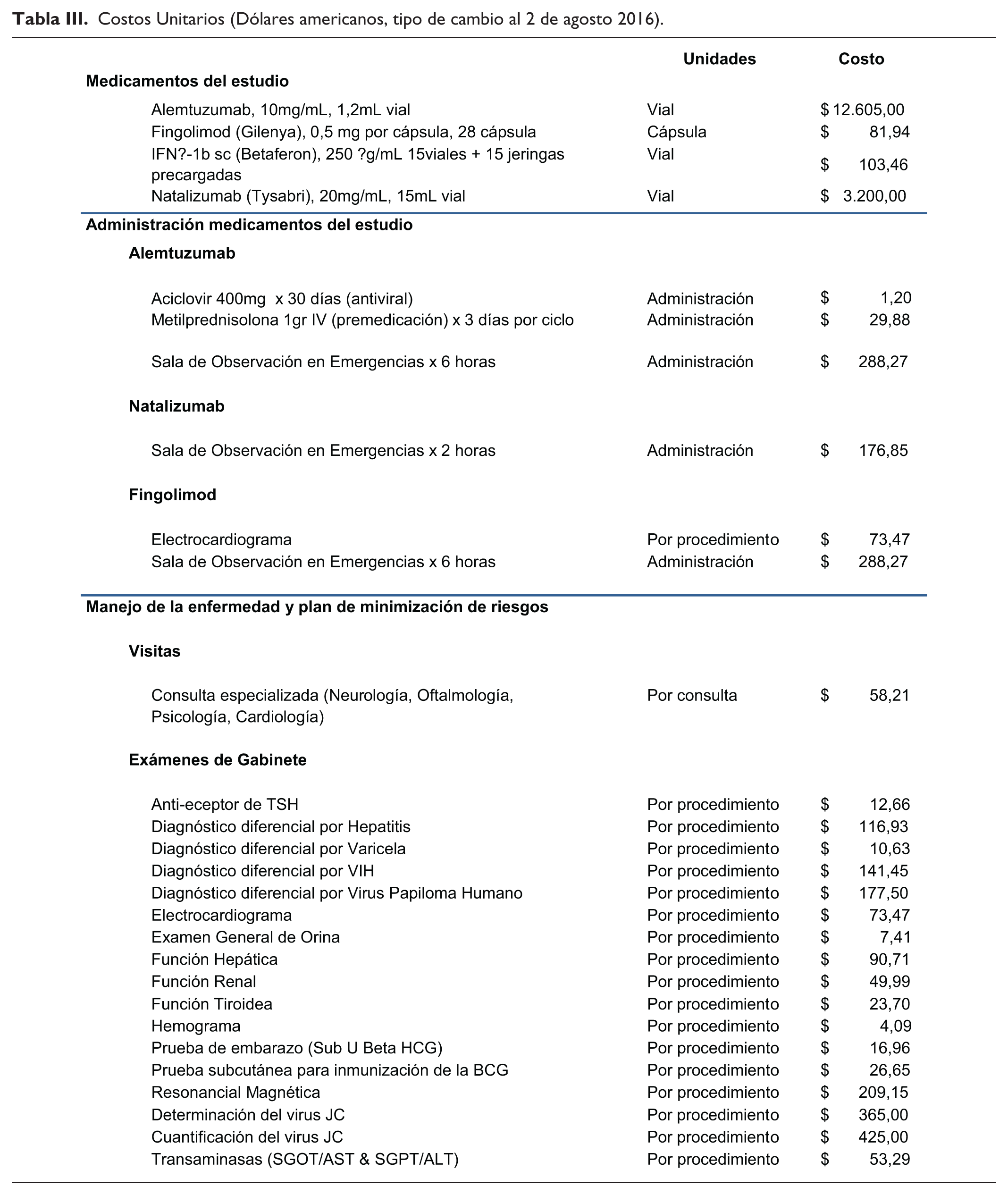
Costos Unitarios (Dólares americanos, tipo de cambio al 2 de agosto 2016).

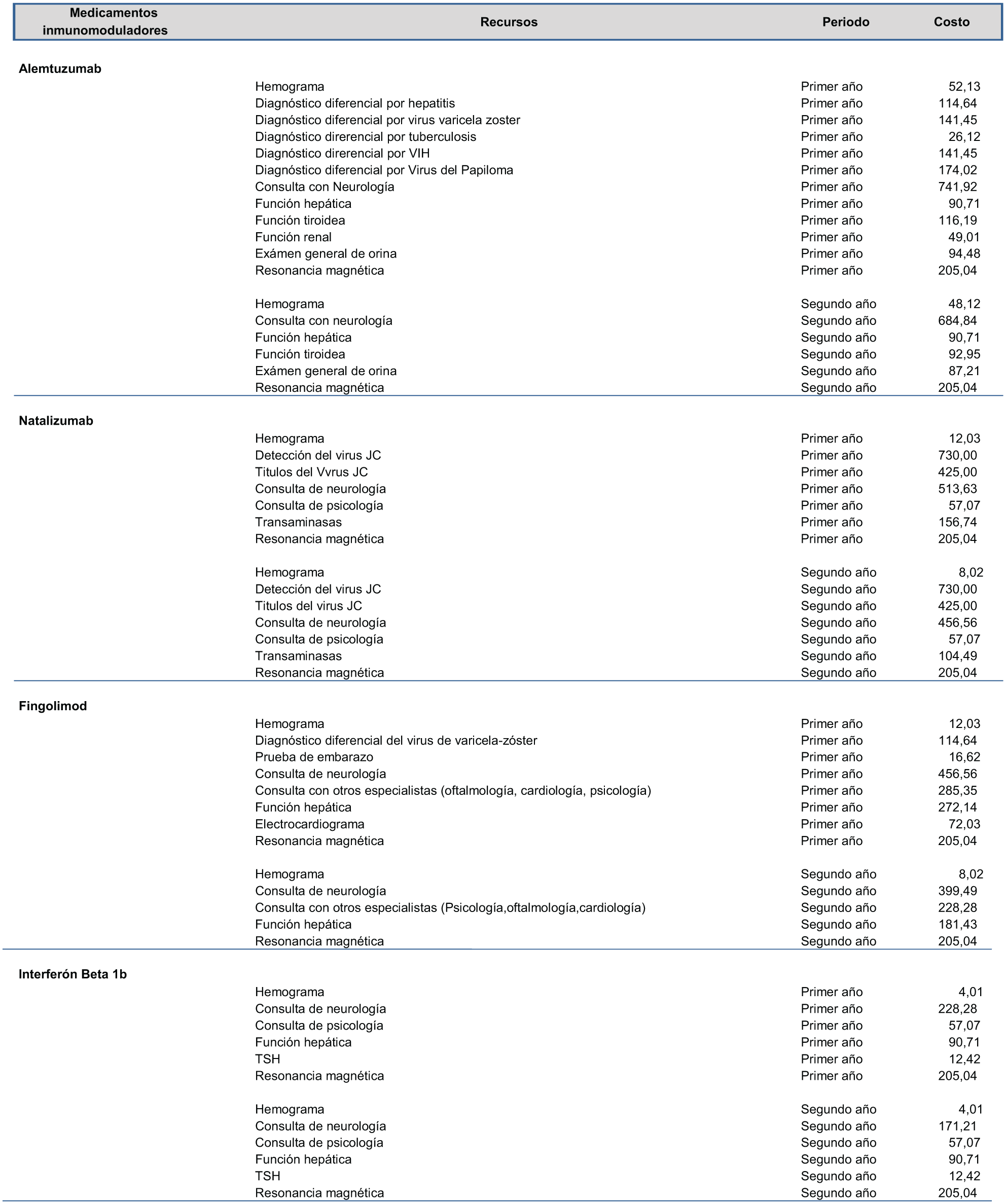
Costos unitarios de los recursos utilizados para el Plan de Minimización de Riesgos y Monitorización de las terapias modificadoras de la enfermedad, objeto de este estudio, en pacientes con EMRR Activa.(Dólares americanos, tipo de cambio al 2 de agosto 2016).

Guía Nacional.
Panel Delphi.
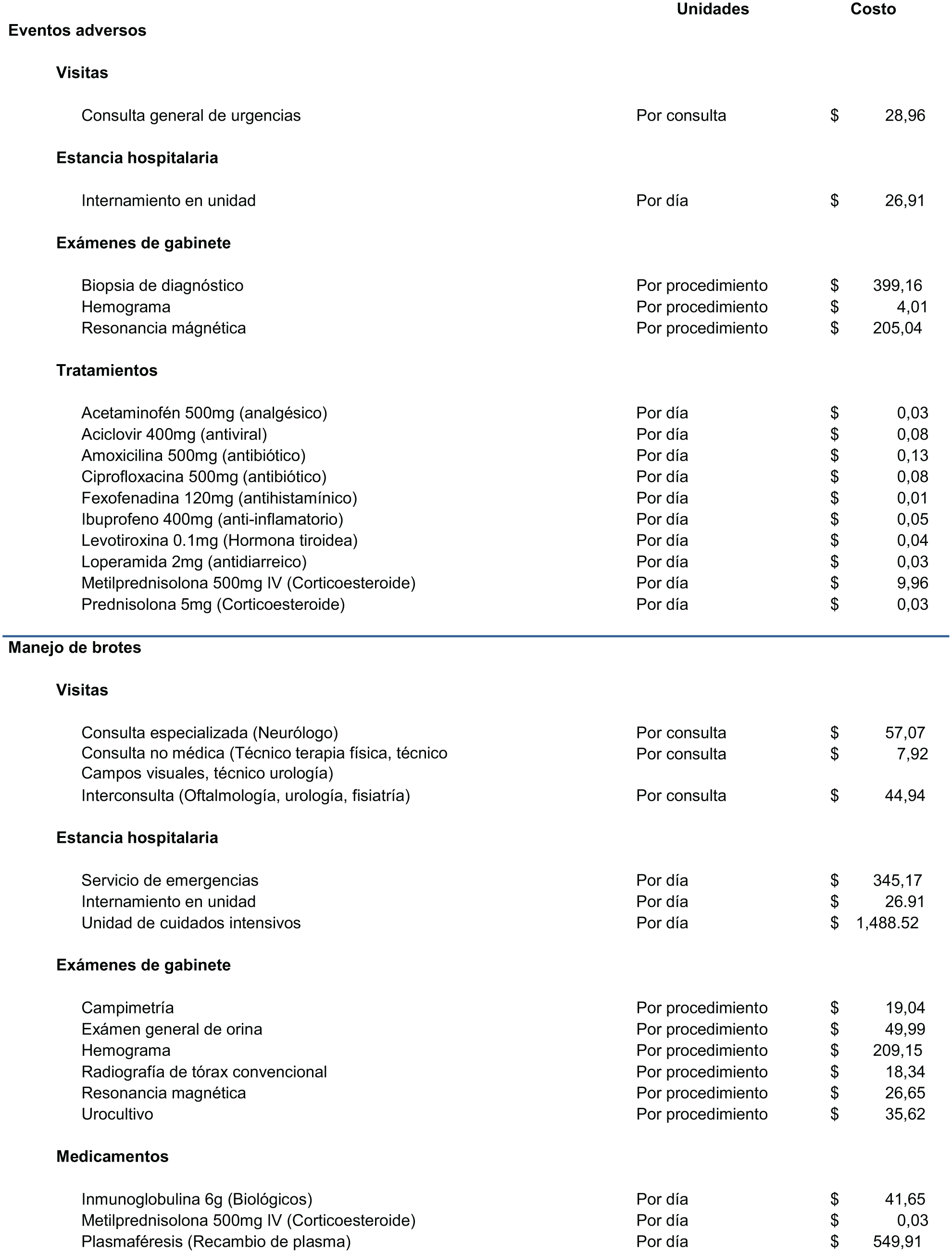
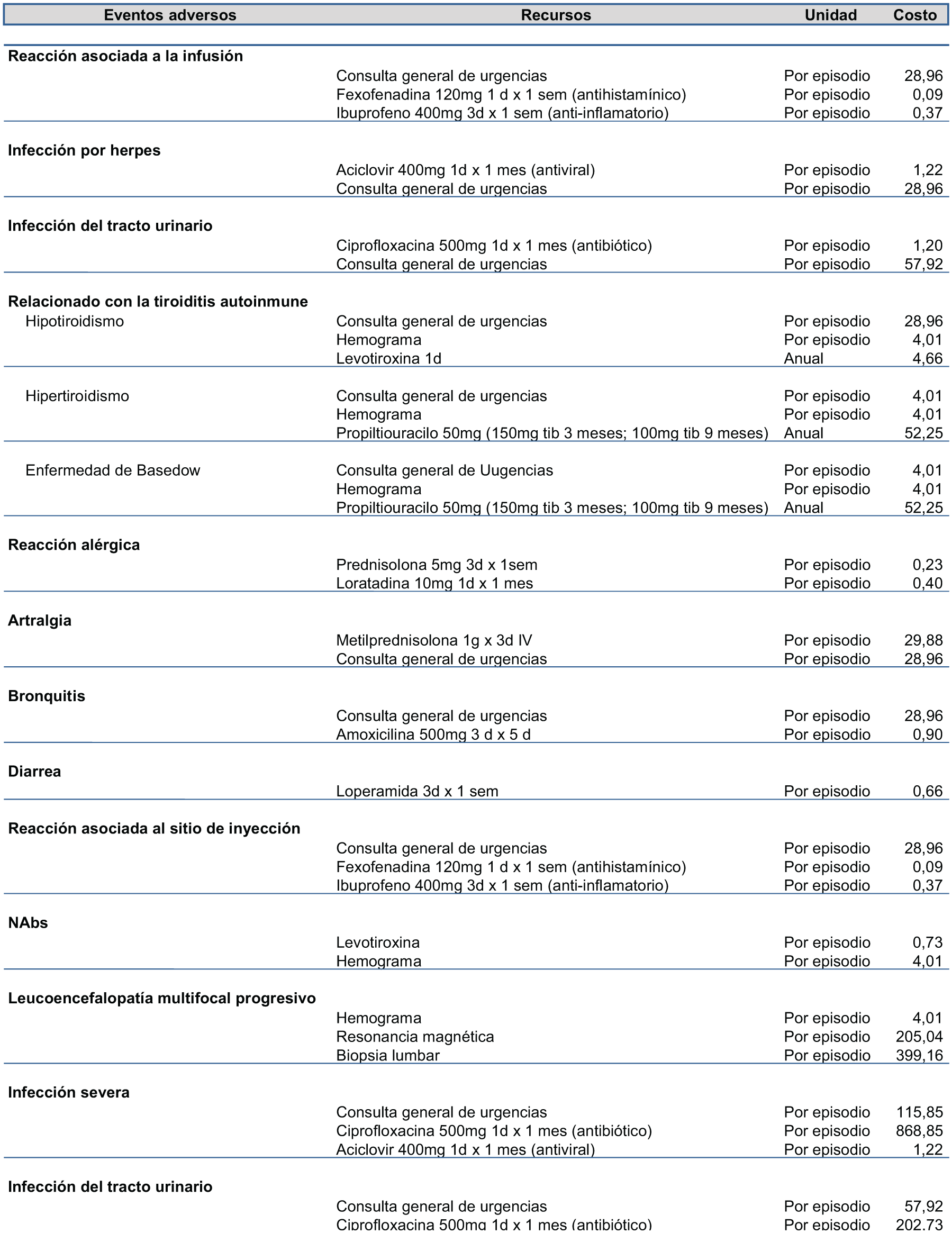
Costos unitarios de los recursos utilizados para el manejo de los eventos adversos, de las terapias modificadoras de la enfermedad, objeto de este estudio, en pacientes con EMRR Activa (Dólares americanos, tipo de cambio al 2 de agosto 2016).
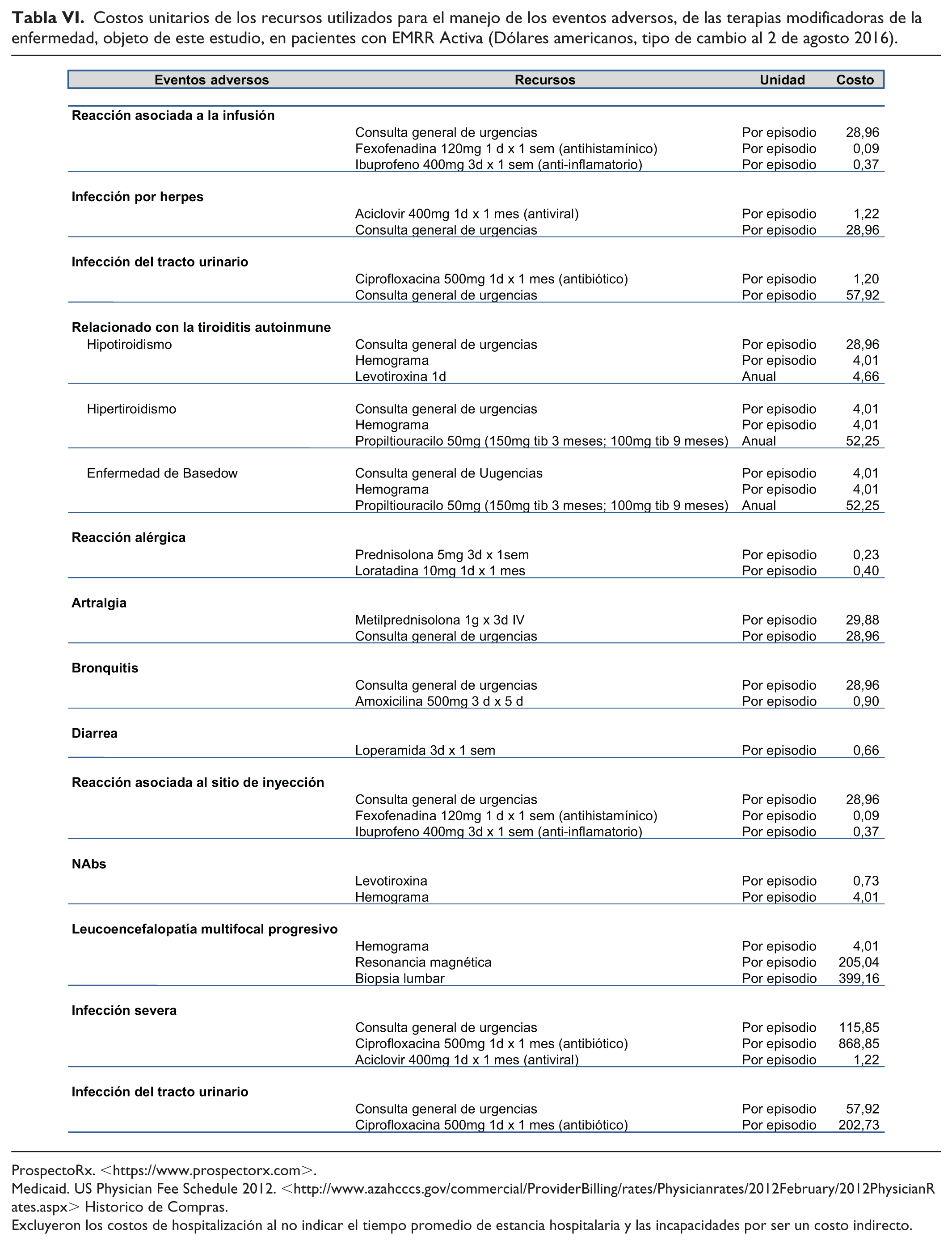
ProspectoRx. <https://www.prospectorx.com>.
Medicaid. US Physician Fee Schedule 2012. <http://www.azahcccs.gov/commercial/ProviderBilling/rates/Physicianrates/2012February/2012PhysicianRates.aspx> Historico de Compras.
Excluyeron los costos de hospitalización al no indicar el tiempo promedio de estancia hospitalaria y las incapacidades por ser un costo indirecto.
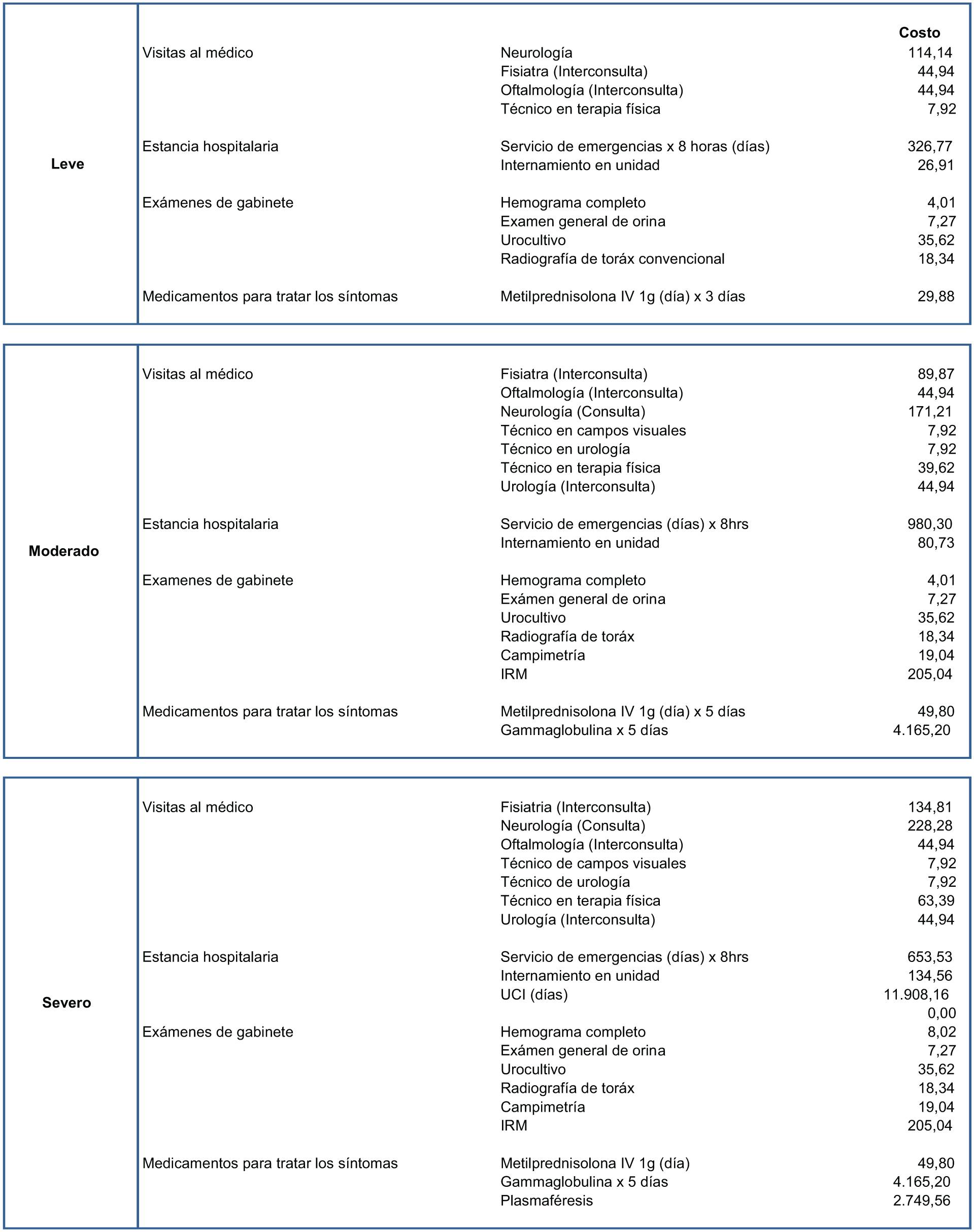
Costos unitarios de los recursos utilizados en el manejo de los brotes de EMRR Activa. (Dólares americanos del 2 agosto 2016).
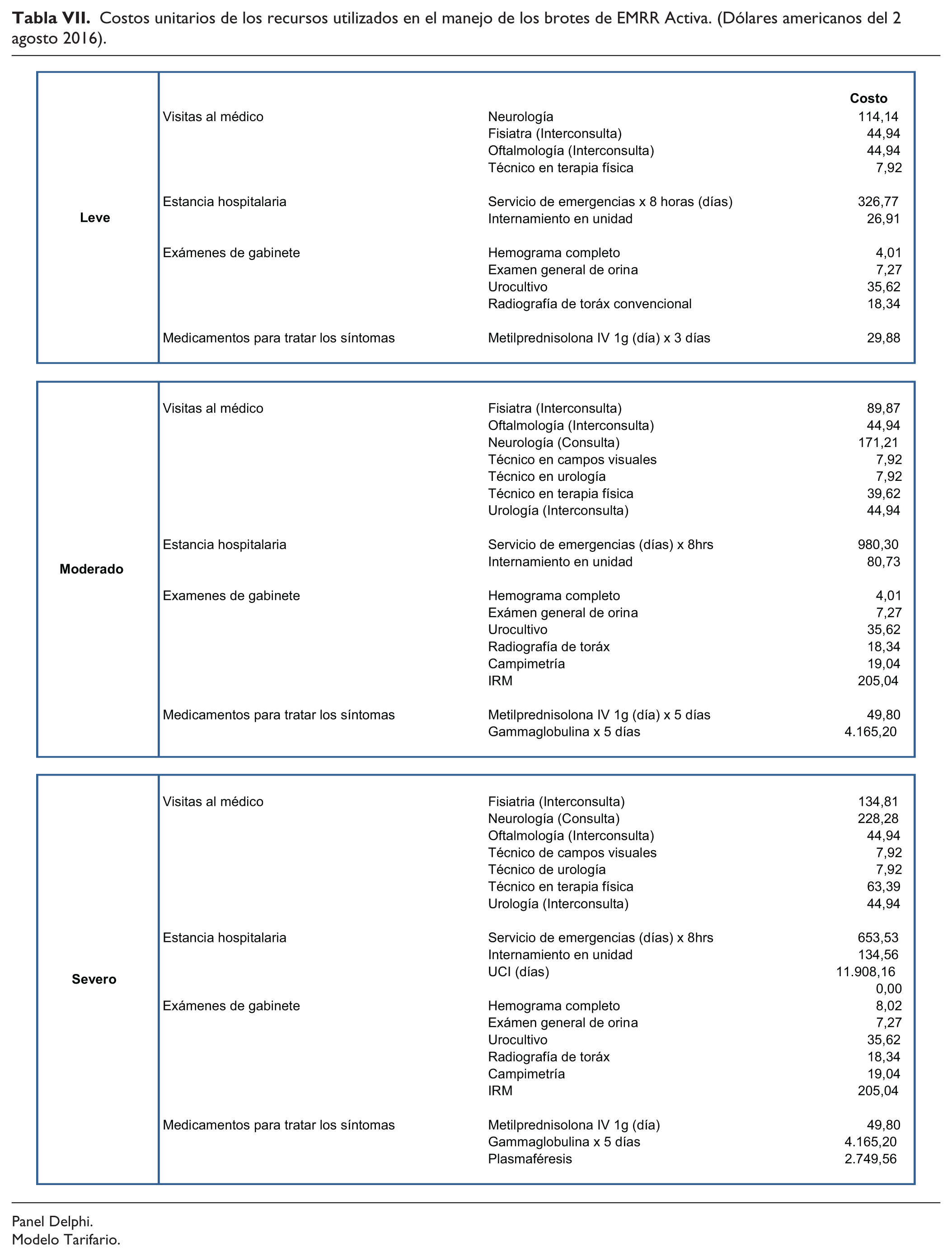
Panel Delphi.
Modelo Tarifario.
− Porcentaje de pacientes que recibe cada medicamento. Para ello, se estimó el impacto económico en el caso de que el 100% de los pacientes incluidos en segunda línea en el modelo se le administrara solamente uno de los medicamentos. Este análisis se realizó para cada una de las alternativas terapéuticas de segunda línea incluidas en el modelo.
− Precio de alemtuzumab. Se calculó el impacto presupuestario con un precio un 30% menor y 30% mayor al precio de alemtuzumab informado.
− Exclusión de costos de eventos adversos.
− Exclusión de costos de manejo de la enfermedad.
Resultados
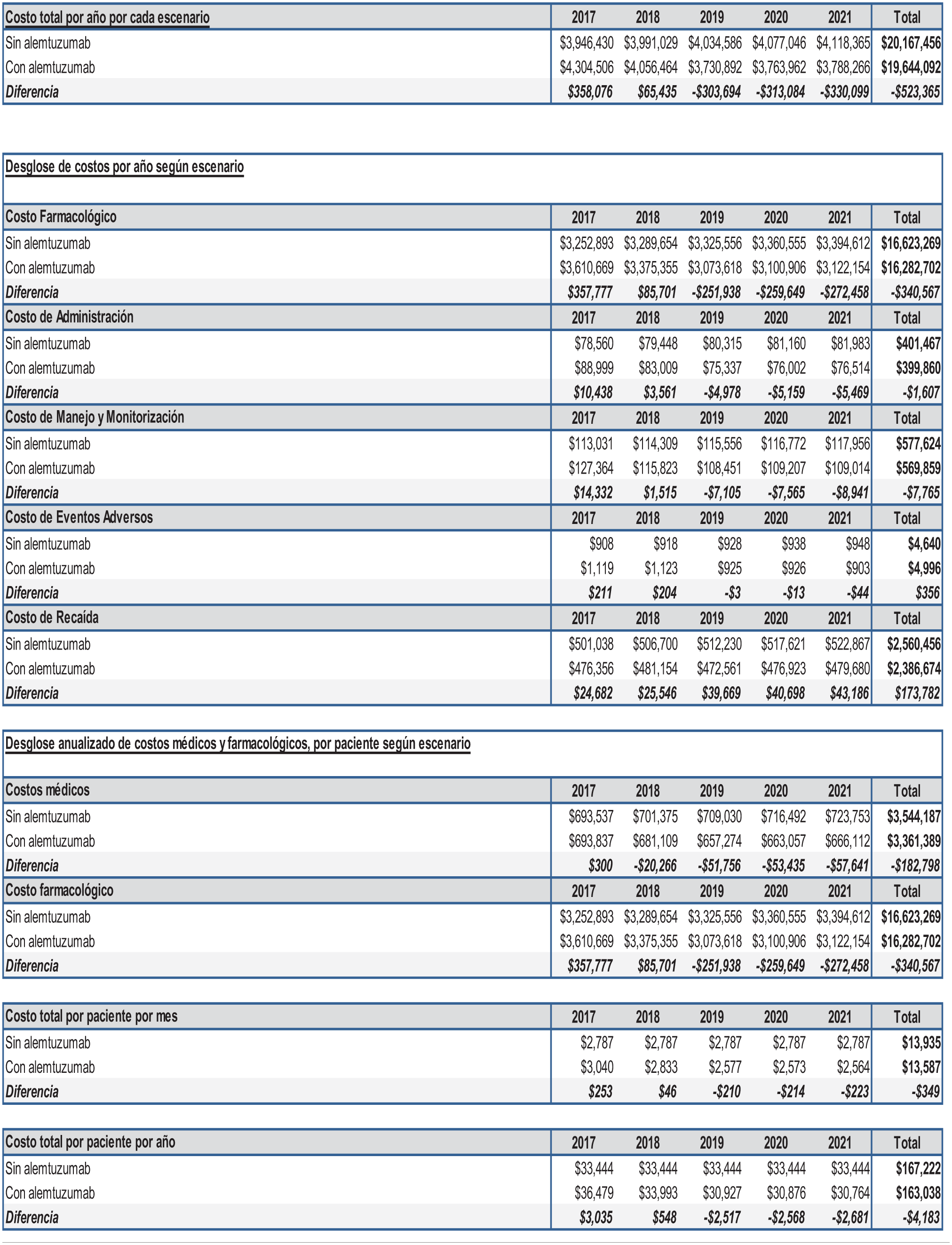
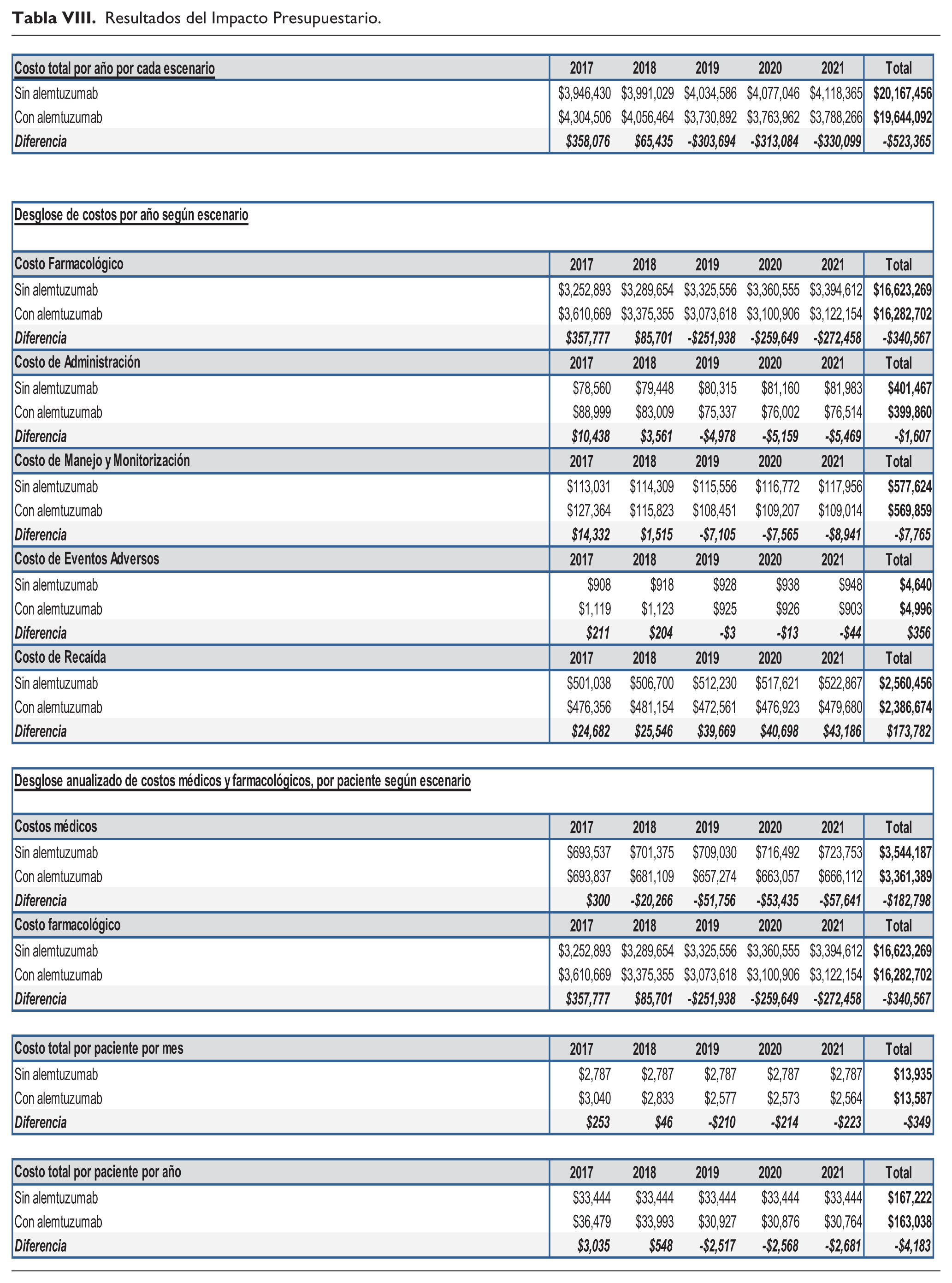
En el caso base, se consideró, de acuerdo a la información de la C.C.S.S., la utilización proyectada de fingolimod y natalizumab en una proporción del 70% y 30%, para los nuevos pacientes, respectivamente, los cuales son incorporados en su totalidad en el primer año. En el escenario con alemtuzumab se consideró una distribución de 25% de los nuevos pacientes con este producto, 52,5% para fingolimod y 22,5% para natalizumab. En la tabla VIII se detalla el impacto económico total de administración y de monitoreo, y desglosado en costos farmacológicos. El impacto presupuestario para la cohorte de pacientes con EMRR activa en tratamiento en Costa Rica, en el caso base, supone una inversión de US$20.167.456,00 y de US$19.644.090,00 en el escenario con alemtuzumab. El escenario que incluye un 25% de pacientes nuevos con alemtuzumab, disminuye el impacto presupuestario en un 2,59% a los cinco años, que representan un monto promedio de US$4.183,00 por paciente en cinco años.La figura 2 muestra el impacto presupuestario por año y se observa una tendencia decreciente anual en el impacto presupuestario en el escenario con alemtuzumab, con un impacto decreciente, siendo el primer año de US$358.076,00 más que en el caso base hasta US$330.099,00 menos que el caso base, para el año 5. La figura 3 muestra el delta entre ambos escenarios, con un claro impacto a favor del escenario con alemtuzumab a partir del año 3. La figura 4 muestra el costo promedio mensual promedio, según año, por paciente, observándose un costo menor en el escenario con alemtuzumab, a partir del año 3 del horizonte temporal. Finalmente, los costos farmacológicos suponen la mayor parte del costo global (82%), seguidos por los costos de manejo de recaídas, según se observa en la figura 5.
Resultados del Impacto Presupuestario.
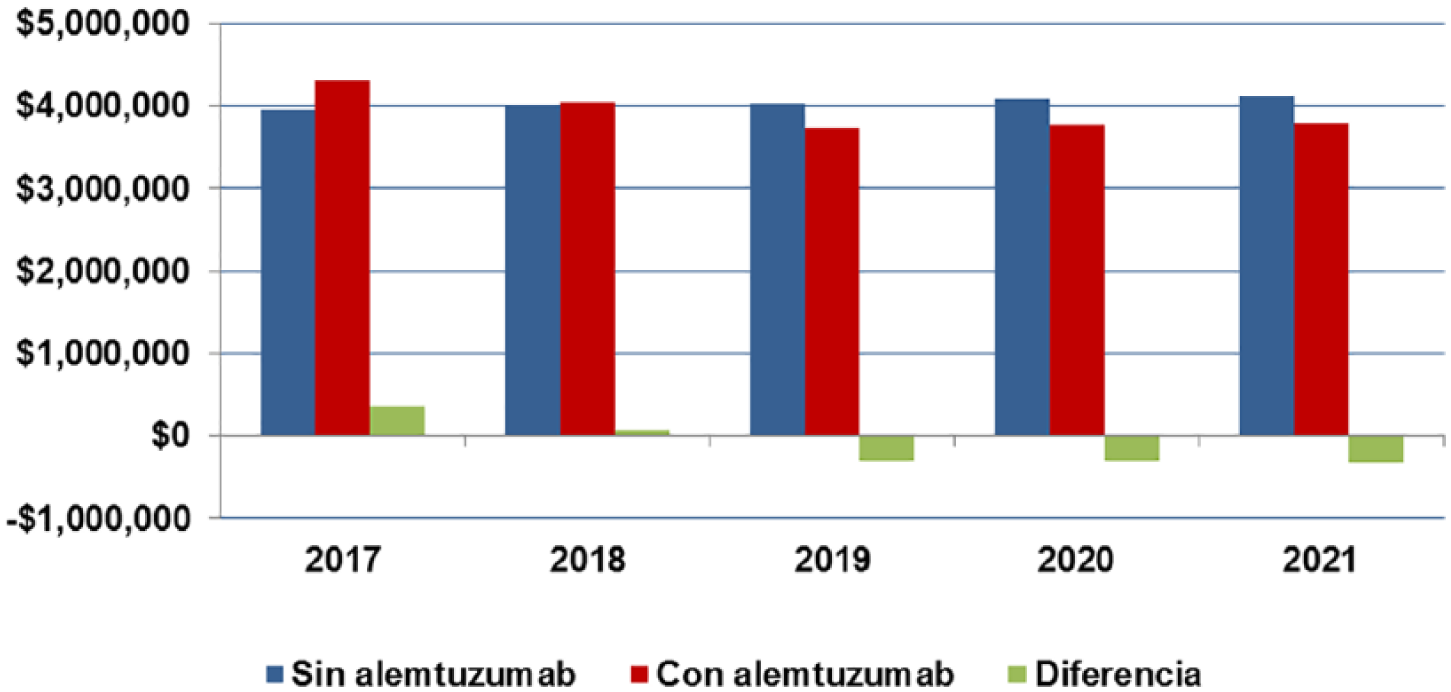
Costo Total Anual por Escenario.
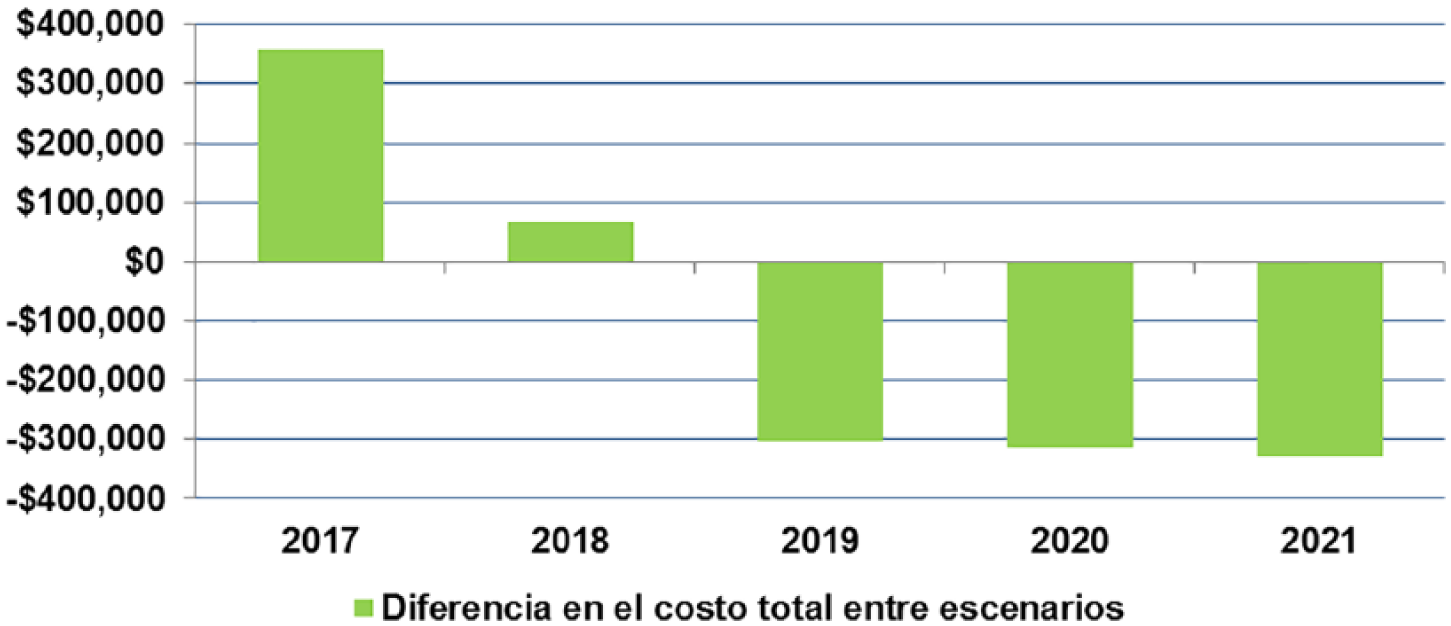
Impacto Total Anual del Presupuesto entre Escenarios.
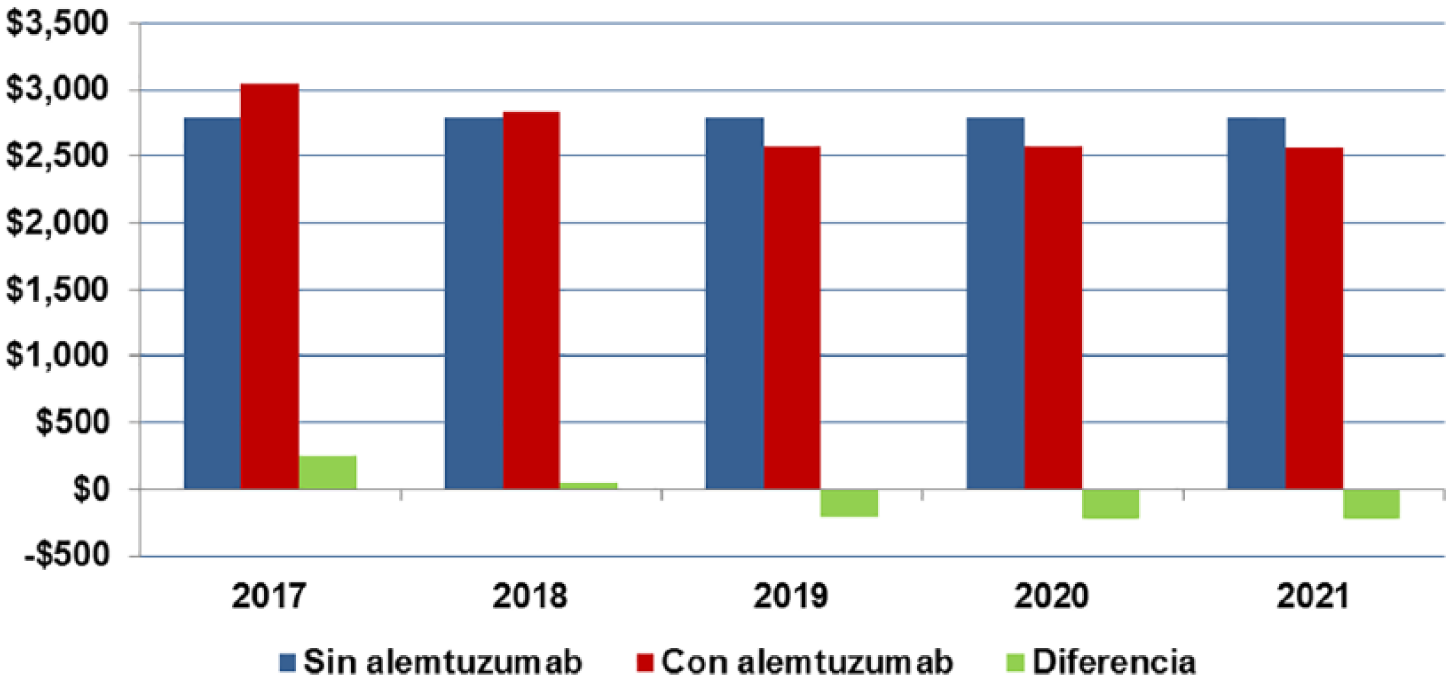
Costo Total Mensual por Paciente con EMRR Activa.
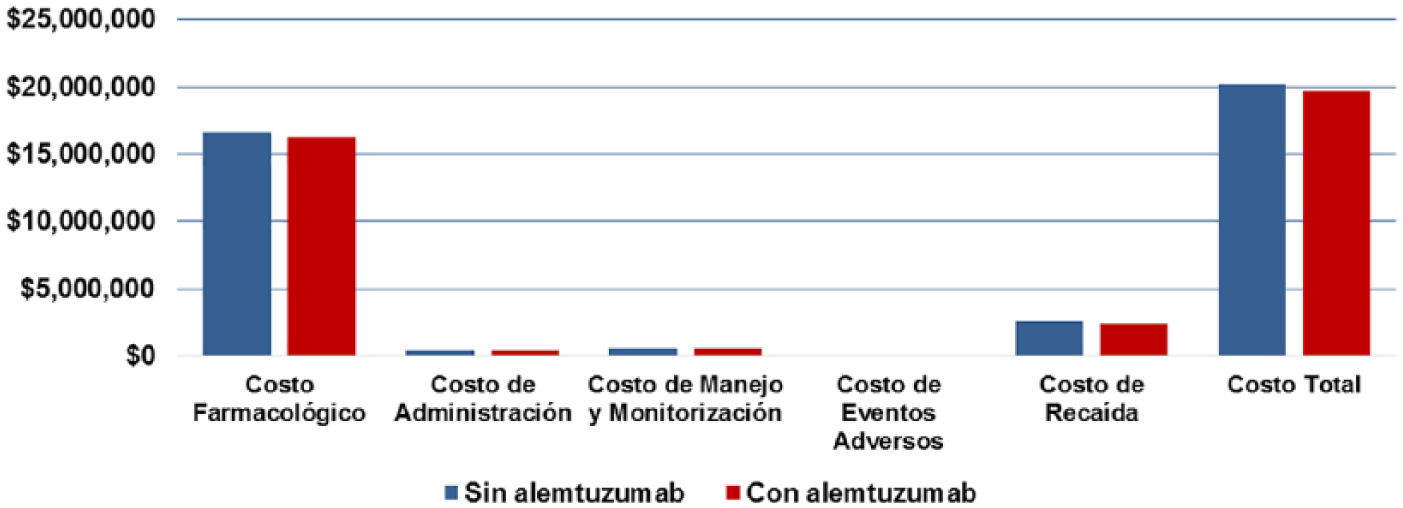
Resultados del impacto presupuestario, según la distribución por tipo de costos por escenario.
Análisis de sensibilidad
La figura 6 muestra el impacto presupuestario en cinco años en caso de modificaciones univariantes de parámetros. Se observa que, según el parámetro modificado, el impacto presupuestario está dentro de un rango que incrementa US$8.710.300,00 el caso base, en el supuesto de que todos los pacientes utilicen natalizumab desde el año 1, y disminuiría en US$6.416.900 en el supuesto de que todos los pacientes utilicen alemtuzumab desde el año 1. Si se excluyen solamente los costos de los eventos adversos, el impacto presupuestario disminuye US$528.400, y si se excluyen únicamente los costos de manejo y monitorización, el impacto presupuestario disminuye en US$1.093.200,00. Otro de los parámetros modificados para efectos del análisis de sensibilidad fue el costo farmacológico de alemtuzumab, con un ± 30% y se observa que, dentro de este rango, el impacto sigue siendo inferior al caso base. Con un precio 30% mayor, el impacto es de US$207.800 menos que el caso base, y si el precio es 30% menor, el impacto es de US$838.900.
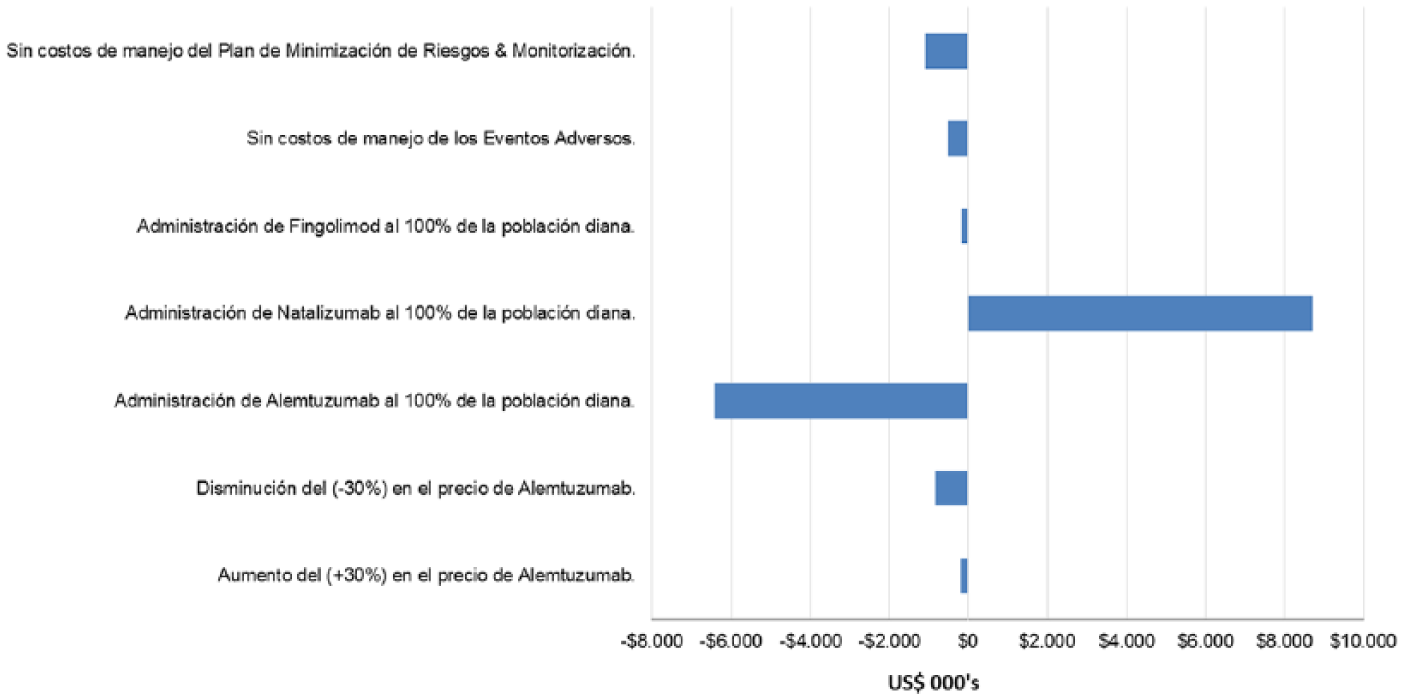
Analisis de Sensibilidad e Impacto en el caso base a cinco anos.
Discusión
El análisis del impacto económico de la incorporación de los nuevos medicamentos en el tratamiento de la Esclerosis Múltiple, podría contribuir a optimizar los presupuestos existentes (24). En Costa Rica, sin embargo, se dispone de información limitada para la realización de evaluaciones económicas en esta materia.
El presente trabajo, a través de un modelo económico parcial según la perspectiva de la Caja Costarricense de Seguro Social, aporta datos sobre el impacto presupuestario en Costa Rica, a nivel nacional, del tratamiento de la EMRR activa. Se establecen dos tipos de escenario, el de referencia o caso base, en el que se incluye un tratamiento de primera línea, Betaferón beta 1-b SC y dos medicamentos de segunda línea, fingolimod y natalizumab, en forma conjunta. La inclusión de alemtuzumab supondría un ahorro del 2,59% en comparación con el presupuesto del caso base a lo largo de cinco años.
El análisis de sensibilidad realizado demuestra que el parámetro con mayor influencia sobre los resultados es el costo farmacológico, lo que debe animar a discusiones adicionales sobre este tema concreto.
Este modelo considera tan solo los costos directos para el sistema, y no considera el impacto social de la esclerosis múltiple y el impacto económico de la progresión de la enfermedad en el largo plazo. Por otro lado, la falta de información nacional y la imprecisión de la existente obligan a asumir que los resultados de los ensayos clínicos son extrapolables en Costa Rica, en especial lo relativo a las tasas de incidencia de eventos adversos. Otra limitación implica que el modelo tampoco incluye el impacto de los estados de salud (EDSS) en virtud de que, según los expertos consultados, ellos registran el dato en los expedientes clínicos de los pacientes, pero no existe ninguna información consolidada que se haya publicado, de la distribución en cada estado, según el número de pacientes. Tampoco se incluyen las terapias concomitantes, por lo que el costo de la enfermedad es parcial, y podría ser completado en estudios posteriores. Por otra parte, aunque la recolección de los costos unitarios fue precisa, considerando que proviene de datos reales de la C.C.S.S., algunos pocos costos unitarios no pudieron ser determinados. El acceso a la información fue complejo, por reticencia a la metodología de la evaluación económica, lo que hizo que la consulta a expertos realizada a través del sistema RAND/UCLA no fuese lo suficientemente representativa, ya que solamente se recibieron respuestas de cinco neurólogos a nivel nacional, de los 12 a quienes se les envió el cuestionario. En todo caso, la variabilidad en las respuestas obtenidas con respecto al manejo de los eventos adversos determinó que, para este parámetro específico, solamente se utilizara el costo de los medicamentos utilizados para tratarlos. Debe tenerse presente que esta es la primera vez que se realiza un Análisis de Impacto Presupuestario de Tecnologías Sanitarias en Costa Rica.
Conclusión
Bajo los supuestos presentados en este trabajo se puede concluir que, desde la perspectiva de la Caja Costarricense de Seguro Social, la incorporación de alemtuzumab representa un ahorro presupuestario significativo a lo largo de los próximos cinco años. Los mayores beneficios en la reducción de recaídas y un régimen de dosificación muy manejable de corto plazo en la mayoría de los pacientes permiten recomendar, tanto clínica como económicamente, el uso racional y progresivo del producto en este contexto.
Footnotes
Financiación
Este estudio ha sido realizado por Rocío Ugalde y Luis Pastor Quirós, sin ayuda financiera de ninguna empresa, sino en su calidad de estudiantes de la Maestría de Evaluación Sanitaria y Acceso al Mercado (Farmacoeconomía) de la Universidad Carlos III de Madrid.
Declaración de Intereses
Rocío Ugalde (Doctora en Farmacia) es empleada de Lilly y trabaja en el Departamento de Acceso al Mercado, en Costa Rica. Luis Pastor Quirós (Doctor en Farmacia) es empleado de Sanofi Genzyme y trabaja como Director de Acceso al Mercado para Centroamérica y el Caribe. Esta situación no ha influido en los resultados presentados en ningún caso.
Reconocimientos
Agradecemos a los siguientes profesionales por su valiosa contribución como tutores de este trabajo.
Dr. Félix Lobo. Director Máster de Evaluación Sanitaria y Acceso al Mercado (Farmacoeconomía). Universidad Carlos III de Madrid.
Dr. Hugo Marín Piva. Secretario Técnico del Comité Central de Farmacoterapia. Caja Costarricense de Seguro Social.
Y como asesor especialista:
Dr. Miguel Ángel Barboza Elizondo. Médico neurólogo costarricense.