Abstract
Purpose
To analyse the evolution of impact on the healthcare expenditure of first and second line treatments for relapsing-remitting multiple sclerosis (RRMS) in Italy.
Methods
An economic model was developed in MSTM Excel (2010) and populated with data from three of the main Regions (Lombardy, Lazio, and Sicily) considered representative in Italy for location (North, Centre and South, respectively), population, and care organisation. Input data were retrieved from published sources and validated by a Board * of experts. The analysis considers an average from regional healthcare resource consumption, and national tariffs were used to economically quantify it. A sensitivity analysis was performed varying the market shares of second line treatments (fingolimod and natalizumab).
I nomi dei membri del Board sono riportati a fine articolo
Results
The results show that the total drug expenditure is €542,279,468 for both first and second line treatments. Among second line treatments, fingolimod showed to be less expensive than natalizumab with an annual mean saving per patient of €4,276 (of which €2,120 for routine management). The sensitivity analysis shows that, increasing the market shares of fingolimod from 59% of the base case to 80%, it is possible to achieve savings for almost €8.5 million/year.
Conclusions
Fingolimod is an affordable therapy for the Italian National Health Service. Moreover, due to a timely use of fingolimod in patients not responding to first line drugs, savings could be around €10 million due to avoided relapses.
Introduzione
La sclerosi multipla (SM) è una malattia infiammatoria demielinizzante del sistema nervoso centrale a verosimile base autoimmune con andamento cronico, caratterizzata da una sintomatologia mutevole, polimorfa, altamente imprevedibile, che può colpire qualsiasi area del sistema nervoso centrale e progredire fino alla disabilità fisica e cognitiva (1).
Si stima che la malattia colpisca circa tre milioni di persone nel mondo, di cui mezzo milione in Europa (2), e che circa l'80-90% dei pazienti sia affetto dalla forma recidivante-remittente (SMRR) (3, 4) nella quale la malattia procede con attacchi acuti successivi, o recidive, intervallati da periodi di benessere. In circa la metà dei casi, questa fase iniziale viene seguita da un fase (detta secondaria progressiva) in cui si ha progressione del deficit neurologico e l'handicap si accumula a prescindere dalla presenza o meno di recidive. Nel 50% dei casi nei pazienti con SMRR si osserva una progressione importante della disabilità a 10 anni dall'insorgenza della patologia e un'evoluzione meno rapida nel restante 50% dei pazienti (4, 5).
Da un punto di vista epidemiologico l'Italia si colloca – nel panorama europeo – in una posizione intermedia e, secondo la stima della Federazione Internazionale della Sclerosi Multipla (MSIF), la prevalenza media nel nostro Paese è di circa 113 casi su 100.000 abitanti, mentre il tasso di incidenza medio è di 4 casi per 100.000 abitanti/anno per un totale di 1800 nuovi casi diagnosticati ogni anno (2). Dati più alti di prevalenza sono invece riscontrati in Sardegna con valori compresi tra 144 e 152 casi su 100.000 abitanti (6, 7).
Nonostante i notevoli progressi, a oggi non si dispone di una cura risolutiva, ma esistono terapie farmacologiche in grado di modificare il decorso della patologia in termini sia di riduzione della frequenza e gravità delle recidive, sia (pur con evidenze più limitate) in termini di rallentamento della progressione della disabilità (5, 8). I farmaci a oggi più usati in prima linea sono gli interferoni beta (IFNβ), glatiramer acetato e i nuovi farmaci teriflunomide e dimetilfumarato, mentre in seconda linea e per le forme severe di SMRR a evoluzione più rapida i farmaci più utilizzati sono fingolimod, natalizumab e, più recentemente, alemtuzumab.
Per quanto riguarda fingolimod, i trials principali (9-11) – che hanno confrontato fingolimod vs placebo e IFNβ-1a – mostrano una riduzione dei tassi di recidiva e un rischio più basso di progressione della disabilità confermata a 3 e 6 mesi. Considerando il confronto vs IFNβ-1a, fingolimod ha significativamente rallentato la progressione dell'atrofia (10) vista come riduzione media del volume cerebrale alla risonanza magnetica (RM), e i benefici sono stati mantenuti anche durante il secondo anno di trattamento (11). Questo studio mostra inoltre una riduzione della perdita di volume cerebrale comparabile a quella osservata nella popolazione generale (11). Fingolimod ha mostrato risultati positivi vs glatiramer acetato nei pazienti che avevano fallito il trattamento di prima linea con IFNβ, mostrando una riduzione dei tassi di recidiva (12).
A oggi mancano confronti diretti vs natalizumab, ma un recente studio osservazionale (13) condotto su 437 pazienti (fingolimod, n = 190) per 1 anno ha mostrato una stabilizzazione o un miglioramento della disabilità – valutata con il punteggio della Expanded Disability Status Scale (EDSS) – leggermente a favore di fingolimod: 80,5% vs 79,3% dei pazienti trattati con natalizumab.
Inoltre una recente metanalisi ha confrontato indirettamente l'efficacia di fingolimod con quella di natalizumab (oltre che con quella di IFNβ, glatiramer acetato e placebo), mostrando per fingolimod un trend positivo in termini di minore tasso di recidive, anche se non statisticamente significativo vs il comparatore (14). Ulteriori evidenze sono tuttavia necessarie per una più attenta valutazione delle differenze tra le terapie, in particolar modo per un confronto più completo da un punto di vista clinico tra fingolimod e natalizumab.
La SM nella maggior parte dei casi colpisce giovani adulti, nel pieno delle potenzialità della vita professionale, affettiva e sociale (15) e la gestione dei pazienti comporta importanti conseguenze dal punto di vista economico sia per l'ammontare dei costi sanitari diretti a tale gestione collegati, sia per l'insorgere di costi indiretti, correlati alla ridotta o mancata produttività lavorativa dei soggetti colpiti, e dei costi intangibili, legati al deterioramento della qualità di vita (16).
L'Organizzazione Mondiale della Sanità (OMS) ha definito la SM una delle malattie socialmente più costose e nella sola Europa si stima, ad esempio, che la patologia assorba in totale 12,5 miliardi di euro (17).
In Italia i dati di una ricerca dell'Associazione Italiana Sclerosi Multipla (AISM), finanziata dal Ministero della Salute, fotografano una spesa sociale per la SM pari a 2,7 miliardi di euro nel 2011 (18), rappresentando la seconda patologia del sistema nervoso centrale (dopo il tumore cerebrale) per costo sociale per paziente (19).
Nonostante i costi sanitari rappresentino una quota minoritaria dei costi sociali complessivi nella SM, si è assistito nel corso degli ultimi 10 anni a un tendenziale aumento della loro quota, sia per la disponibilità di nuovi farmaci costosi, sia per l'effetto benefico sulla progressione della patologia di tali terapie, con conseguente possibile impatto sugli altri costi non a carico del Servizio Sanitario Nazionale (SSN). Infatti, sia i costi diretti, sia quelli indiretti aumentano con il decorso della malattia rendendo importante, dal punto di vista economico, l'utilizzo precoce delle opzioni terapeutiche maggiormente in grado di modificarne la progressione (5, 20).
Alla luce di tutto ciò, è particolarmente interessante condurre una valutazione sui costi complessivi delle terapie per la SMRR in Italia, differenziandole per linea terapeutica.
Obiettivo
Il presente studio si pone come obiettivo la valutazione degli aspetti organizzativi/gestionali e di costo legati alle terapie utilizzate nei pazienti con SMRR in Italia, con un focus particolare sui farmaci utilizzati in seconda linea (fingolimod e natalizumab). Tale analisi è finalizzata a individuare le scelte ottimali di governance che riguardano l'intera presa in carico del paziente con SMRR, anche alla luce dei valori propri del SSN.
Lo studio stima la spesa sanitaria complessiva per la SMRR in Italia nello scenario attuale e nel prossimo futuro (proiezione a 3 anni). L'analisi non si concentra sulle differenze cliniche tra le terapie, che vengono demandate ai trials clinici o alle metanalisi, ma si focalizza sulle differenze economiche e gestionali che queste comportano.
Metodi
All'interno di un processo di Health Technology Assessment (HTA) affidato a un Board multidisciplinare, composto da esperti con diverse competenze sia cliniche che economiche e gestionali, è stato sviluppato un modello in Microsoft Excel (2010), che simula il percorso del paziente con SMRR, per stimare l'impatto sulla spesa sanitaria dei pazienti in trattamento con farmaci di prima e seconda linea. A tale fine, sono stati utilizzati i dati di tre Regioni italiane (Lombardia, Lazio e Sicilia) ritenute rappresentative per posizione geografica (rispettivamente Nord, Centro e Sud), popolazione (le Regioni complessivamente comprendono circa 20 milioni di residenti, pari al 34% dell'intera popolazione nazionale) (21), pratica clinica ed economico-gestionale della malattia (diversi approcci e modalità di cura e diversa presa in carico dei pazienti con SMRR – legati ad esempio a un diverso ricorso al day-hospital o a una maggiore frequenza di esami di routine richiesti dalle terapie) (22-25). Queste differenze dovrebbero quindi permettere di rappresentare, almeno in parte, la presa in carico dei pazienti nella sfaccettata realtà nazionale, quantificando i costi associati.
Nel modello sono stati inseriti dati relativi a: (i) quadro epidemiologico; (ii) consumo e costi unitari delle risorse per un paziente con SMRR; (iii) tasso di recidive tra linee terapeutiche; (iv) quote di mercato dei farmaci. Il Board ha fornito le seguenti informazioni mediante un questionario strutturato:
convalidato i dati di input (es. percentuali di diagnosi e di pazienti messi in terapia) recuperati in letteratura;
chiarito alcuni elementi di incertezza circa il percorso diagnostico terapeutico del paziente con SMRR rispetto a ciascuna delle alternative terapeutiche disponibili e alla gestione degli eventi avversi;
individuato la percentuale di pazienti sottoposti a tali prestazioni e allo switch terapeutico dalla prima alla seconda linea;
recuperato le quote di mercato attuali dei farmaci e stimato la variazione di tali percentuali nei prossimi 3 anni anche in funzione dell'entrata nel mercato di nuovi farmaci sia in prima sia in seconda linea;
analizzato gli aspetti etici relativi alle tecnologie analizzate.
I dati sono stati raccolti nel periodo compreso tra ottobre 2013 e febbraio 2015. Per alemtuzumab, alla luce del complesso profilo di sicurezza, i componenti del Board hanno indicato un posizionamento del farmaco in una linea successiva alla seconda.
Popolazione target
Con riferimento al quadro epidemiologico, la popolazione di pazienti affetti da SMRR e in trattamento nelle due linee di terapia è stata definita in base a:
popolazione generale residente in Italia e nelle tre Regioni campione al 2013;
dati di prevalenza della malattia;
percentuali di diagnosi ed eleggibilità ai farmaci di prima e seconda linea.
II modello considera una popolazione stazionaria.
Quote di mercato
Nell'analisi, per le nuove terapie è stata considerata una quota di mercato nello scenario attuale pari a zero (perché non ancora in commercio o da troppo poco tempo al momento della rilevazione) e una penetrazione nel mercato crescente e costante. Le quote di mercato si sono mostrate diverse nelle tre Regioni campione; pertanto, nell'analisi nazionale, sia per le quote presenti sia per quelle future, si è utilizzata una media dei dati regionali. La crescita delle percentuali di mercato per i trattamenti di seconda linea è stata stimata sulla base della percentuale di recidive dei pazienti in prima linea e del peggioramento degli stessi sulla scala EDSS. I dati e le stime sono stati validati dal Board.
Costo dei trattamenti
Per il calcolo dei costi delle terapie sono stati considerati i prezzi massimi di acquisto per il SSN, al netto degli sconti (obbligatori di legge e negoziati con AIFA), e i consumi, per una durata piena della terapia di 12 mesi. Per alemtuzumab, visto il peculiare schema posologico (cinque somministrazioni il primo anno, tre il secondo e nessuna il terzo), è stato ipotizzato un costo medio annuo (a 3 anni) pari a quello di natalizumab.
Valorizzazione del consumo di risorse
Per quantificare la spesa della presa in carico dei pazienti con SMRR in Italia, lo studio ha individuato il percorso effettivo dei pazienti utilizzando, per la stima dei costi, un approccio di tipo bottom-up coerentemente con la logica dell' Activity-Based Costing (ABC) (26-28). In sostanza, l'analisi ha seguito tre fasi: 1) identificazione delle risorse assorbite; 2) misurazione; 3) valorizzazione. Tale approccio ha permesso di stimare il costo medio annuale per paziente (composto dai costi medi annui del farmaco, della gestione di routine e della gestione delle eventuali recidive) nelle Regioni selezionate.
Tutte le risorse utilizzate, consumate durante la routine terapeutica (farmaci, esami di laboratorio e strumentali, visite mediche, ricoveri), e la loro frequenza sono state individuate attraverso un questionario dal Board e sono state valorizzate utilizzando i prezzi vigenti e le tariffe ospedaliere di competenza (22-25, 29). Complessivamente per le stime a livello nazionale è stata considerata una media delle frequenze per esami e visite mediche riportate dal Board moltiplicate per le tariffe nazionali (29).
Il costo medio delle recidive è stato calcolato moltiplicandone il costo pieno per la probabilità del verificarsi delle stesse, rispettivamente del 30% per la prima linea e del 15% per le successive, così come indicato dalla letteratura (30) e validato dal Board.
Per quanto riguarda i nuovi farmaci, non avendo informazioni a disposizione al momento della rilevazione, è stato ipotizzato con un approccio conservativo:
per teriflunomide e dimetilfumarato il minore costo pieno di gestione tra i farmaci già in commercio (glatiramer acetato) e un costo medio di gestione delle recidive uguale a quello dei farmaci utilizzati in prima linea;
per alemtuzumab si è considerato un costo di gestione complessivo pari a quello di natalizumab e un costo medio per recidiva uguale a quello dei farmaci in seconda linea.
Analisi di sensibilità
Per valutare la solidità dei risultati e, in maniera più completa, l'evoluzione della spesa sanitaria, è stata sviluppata un'analisi di sensibilità, focalizzata sui farmaci di seconda linea. Tale analisi mostra quindi le variazioni di spesa in funzione di diverse quote di mercato di fingolimod, comprese tra un minimo del 20% e un massimo dell'80%.
Risultati
I dati presentati nei seguenti paragrafi fanno riferimento all'analisi condotta a livello nazionale. Come già accennato nei metodi, per condurre tale analisi è stata considerata una media delle frequenze per esami e visite mediche a seconda delle terapie analizzate, come riportato dal Board, moltiplicate per le tariffe nazionali.
Base case
La prevalenza rilevata della SM in Italia è pari a 113 casi su 100.000 abitanti (2) che, considerando una popolazione di residenti a gennaio 2013 pari a 59.685.227 abitanti (21) si traduce in 67.444 pazienti prevalenti. All'85% di questi pazienti si ipotizza venga diagnosticata la SMRR (31) e che solo il 74% di questi pazienti, in accordo con le stime degli esperti, sia effettivamente messo in terapia, per un totale di 42.422 pazienti. Di questi pazienti, in funzione dell'entrata sul mercato delle nuove molecole e dello switch di trattamento (verso i farmaci di seconda linea e successive), il modello ha stimato che 32.962 pazienti (77,7%) siano in prima linea per diminuire fino a 26.726 (63,0%) nel terzo anno (Tab. I). I pazienti in seconda linea e successive sono stati invece stimati in un numero di 9.460 (22,3%) al primo anno, per aumentare fino a 15.696 (37,0%) nello scenario al terzo anno (Tab. I). In questa analisi, come detto, si è utilizzata una popolazione stazionaria, nella quale varia soltanto la distribuzione dei pazienti.
Pazienti in terapia, quote di mercato attuali e future dei farmaci per la SMRR in Italia
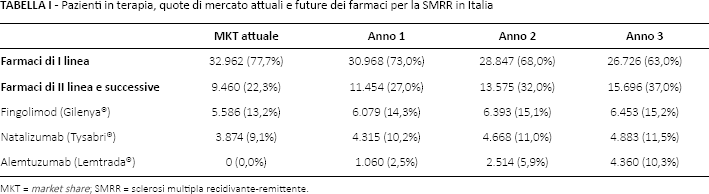
MKT = market share; SMRR = sclerosi multipla recidivante-remittente.
Considerando la prima linea, un dato che emerge con forza è quello relativo alle piccole quote di mercato per gli IFNβ-1b (circa 7,8%) che, come mostrato più avanti (Tab. II), a oggi sono i prodotti meno costosi e che, se maggiormente prescritti in prima linea di trattamento, comporterebbero un risparmio economico non indifferente.
Considerando invece le terapie successive, avendo costruito un modello con popolazione e prevalenza stazionarie, l'aumento delle percentuali di mercato è dovuto al solo switch terapeutico dalla prima linea alla seconda e alemtuzumab, con un aumento rispetto al mercato attuale, per le linee successive alla prima, di 1.994 pazienti al primo anno fino a 6.236 al terzo.
La Tabella II e la Tabella III mostrano i costi medi stimati nello studio. I costi di gestione sono stati calcolati moltiplicando la frequenza (media nelle tre Regioni) per le relative tariffe vigenti al livello nazionale. Similmente a quanto emerso in un recente studio italiano (32), la Tabella II mostra che il maggior driver di costo è legato al farmaco, che incide in media per circa l'87-95% sul costo complessivo della terapia. Altri autori hanno invece stimato un'incidenza più contenuta dei farmaci (67%) sul costo della malattia (5). Il nostro modello mostra che le terapie più economiche in prima linea sono gli IFNβ-1b, mentre la terapia più costosa rimane l'IFNβ-1a alla dose di 44 μg.
Costi medi dei trattamenti della SMRR in Italia
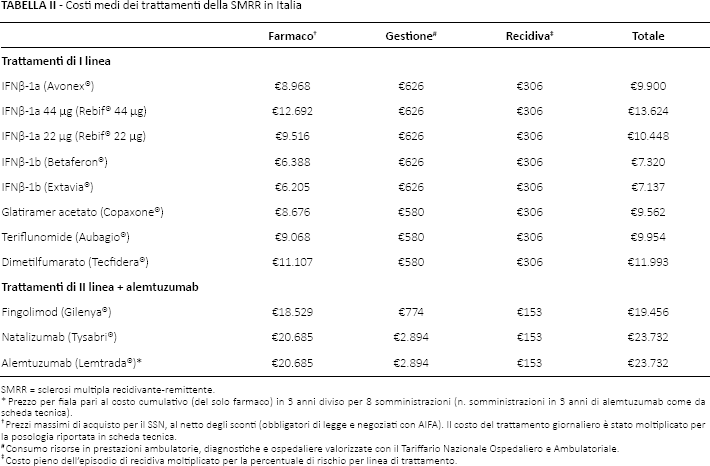
SMRR = sclerosi multipla recidivante-remittente.
Prezzo per fiala pari al costo cumulativo (del solo farmaco) in 3 anni diviso per 8 somministrazioni (n. somministrazioni in 3 anni di alemtuzumab come da scheda tecnica).
Prezzi massimi di acquisto per il SSN, al netto degli sconti (obbligatori di legge e negoziati con AIFA). Il costo del trattamento giornaliero è stato moltiplicato per la posologia riportata in scheda tecnica.
Consumo risorse in prestazioni ambulatorie, diagnostiche e ospedaliere valorizzate con il Tariffario Nazionale Ospedaliero e Ambulatoriale.
Costo pieno dell'episodio di recidiva moltiplicato per la percentuale di rischio per linea di trattamento.
Fonte dei costi: Tariffario Nazionale Ospedaliero e Ambulatoriale.
Fonte del consumo di risorse: Board multidisciplinare.
Per il costo di somministrazione di natalizumab si è considerato il costo del day-hospital.
Costo compreso nella somministrazione per il quale si è considerato un accesso in day-hospital.
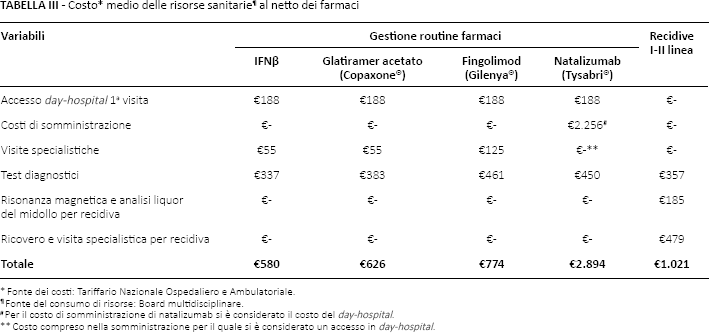
Considerando ora i costi sanitari legati alle terapie di seconda linea e successive, l'analisi ha mostrato che la differenza in termini di costo medio tra fingolimod e natalizumab è dovuta sia al costo dei farmaci (+€2.156/anno/paziente per natalizumab), sia al diverso percorso dei pazienti (Tab. III) che risulta, da un punto di vista gestionale, più oneroso e complesso per natalizumab, con un costo medio per paziente di €2.894 vs i soli €774 di fingolimod (+€2.120/anno/paziente per natalizumab). Queste differenze, nelle Regioni campione, sono state sempre favorevoli a fingolimod, con valori più alti in Lombardia, alla luce di una maggiore frequenza degli esami e di tariffe più alte. In particolare, in Lombardia è emerso un incremento del costo di gestione annuo per un paziente in trattamento con natalizumab di +€3.553 e un incremento totale di +€5.709 rispetto a un paziente in trattamento con fingolimod. Diversamente, i costi calcolati in Lazio (+€1.959 di costi gestionali e +€4.115 di costi totali con natalizumab) e in Sicilia (+€2.019 di costi gestionali e +€4.175 di costi totali con natalizumab) sono in linea con quelli stimati a livello nazionale. Le differenze in termini di costi medi tra fingolimod e natalizumab, calcolati come il prodotto tra la frequenza di esami (sia di laboratorio sia strumentali), visite e accessi in day-hospital per le tariffe nazionali associate, sono da attribuire al diverso percorso del paziente (terapia orale vs terapia iniettiva), al differente numero di esami (di laboratorio e strumentali), visite e ricoveri richiesti dalle due terapie (Tab. III). La nostra analisi ha mostrato, pur non rientrando negli obiettivi dello studio, differenze anche rilevanti tra le Regioni e che tali differenze, come evidenziato dal Board, mostrano una diversa presa in carico del paziente in termini di frequenza delle prestazioni e tariffe associate (22-25).
La Tabella IV illustra i risultati dell'impatto di spesa per il SSN. Si osserva un incremento di spesa totale compreso tra 26 e 84 milioni di euro tra il primo e il terzo anno, con un aumento del 66% dei pazienti in trattamento con farmaci più efficaci (9, 10, 13, 33-39) L'incremento di spesa nel triennio considerato è dovuto all'entrata sul mercato dei nuovi farmaci, all'evoluzione della patologia e al conseguente switch terapeutico.
Impatto di spesa a 3 anni dei trattamenti per la SMRR in Italia *
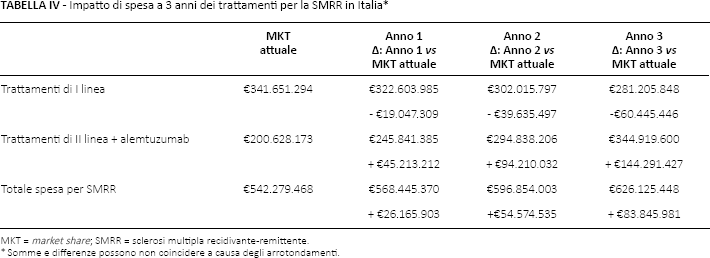
MKT = market share; SMRR = sclerosi multipla recidivante-remittente.
Somme e differenze possono non coincidere a causa degli arrotondamenti.
Il modello, come anticipato, considera una popolazione stazionaria, che non tiene conto dei dati d'incidenza, mortalità e drop-out. È stato inoltre ipotizzato che le terapie siano somministrate per 12 mesi, senza interruzioni e in piena compliance, stimando, dunque, una spesa maggiore rispetto a quella della normale pratica clinica.
Recidive
L'analisi effettuata ha stimato un costo pieno per recidiva pari a €1.021 per episodio. Tale costo medio tuttavia varia in funzione della percentuale di pazienti che vanno incontro all'evento. Per le terapie di prima linea, il Board ha stimato una percentuale di recidive del 30%, mentre, per la seconda linea e alemtuzumab, una percentuale del 15%. Moltiplicando queste percentuali per il valore pieno della recidiva si ottiene un costo per recidiva pari a €306 per i farmaci di prima linea e a €153 per le linee successive. Come già anticipato, per teriflunomide e dimetilfumarato è stato considerato un costo medio per recidiva pari a quello delle molecole di prima linea, mentre per alemtuzumab un costo medio uguale a quello delle terapie di seconda linea.
Analisi di sensibilità
La Tabella V mostra i risultati sulla spesa della variazione delle quote di fingolimod, evidenziando le differenze rispetto allo scenario attuale. Il risultato più importante dell'analisi è la chiara relazione tra la diminuzione della spesa e la maggiore quota di mercato di fingolimod: una quota di fingolimod dell'80%, rispetto all'attuale 59%, si tradurrebbe in un risparmio circa €8,5 milioni all'anno, mentre una quota pari al 20% provocherebbe un aumento della spesa complessiva di quasi €16 milioni in un anno.
Analisi di sensibilità: stima dell'evoluzione della spesa sanitaria in funzione delle quote di mercato di fingolimod *
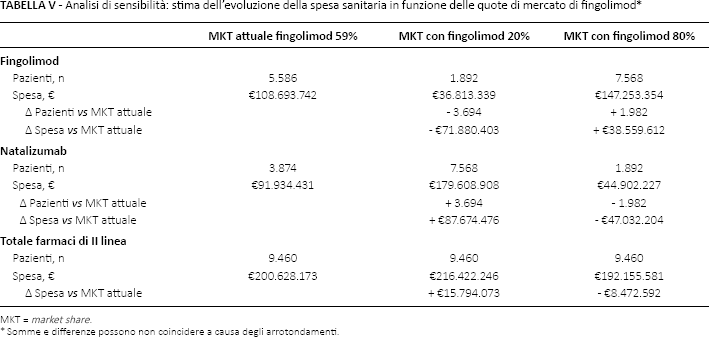
MKT = market share.
Somme e differenze possono non coincidere a causa degli arrotondamenti.
Discussione
I risultati di questo studio mostrano i potenziali incrementi di spesa nella SMRR dovuti principalmente al decorso della patologia, simulato dagli switch terapeutici e dall'introduzione sul mercato di nuovi trattamenti.
La complessità della patologia, nonché la ricca disponibilità terapeutica, potrebbero determinare una crescita dei costi correlati alla gestione della malattia. Per questo motivo, studi di farmacoeconomia multidisciplinari si rendono necessari per guidare politiche di indirizzo che garantiscano equilibrio economico e accesso alla giusta terapia per ogni paziente.
Considerando, ad esempio, i farmaci di prima linea, il nostro modello mostra che le terapie più economiche in questa linea sono gli IFNβ-1b, mentre la terapia più costosa rimane l'IFNβ-1a 44 μg. Tali rilevanti differenze di costo inducono a riflettere sul fatto che, compatibilmente con le condizioni dei pazienti e la libertà di scelta dei clinici, un maggiore utilizzo di terapie più economiche permetterebbe di liberare risorse capaci di garantire un equilibrio tra l'impiego di terapie più costose, ma più efficaci, e la sostenibilità economica.
Per quanto concerne, invece, le terapie di seconda linea, l'analisi conferma per fingolimod un profilo economico globale migliore rispetto a natalizumab, così come già evidenziato in studi precedenti.
Ad esempio lo studio di Guarrera (40) ha stimato, in Italia, costi di gestione annuali di €925 per fingolimod vs €2.196 per natalizumab. Tra il 2012 e il 2014, tre analisi di cost-minimization hanno evidenziato una differenza di costo sanitario globale a favore di fingolimod vs natalizumab pari a €6.240 in 2 anni nei Paesi Bassi (41), a €4.364 in 2 anni in Spagna (42) e a SEK124.823 [€13.719 (Cambio Euro/Corona Svedese = 9,099, anno 2014)] in 3 anni in Svezia (43). In un'analisi di costo-efficacia condotta in USA nel 2011 (44), i risultati a 2 anni si sono dimostrati favorevoli a natalizumab con un migliore profilo sia di costo che di efficacia (in termini di recidive evitate) rispetto a fingolimod. Questo lavoro non è però risultato trasferibile alla nostra realtà a causa principalmente dei prezzi dei farmaci considerati. Infatti gli autori hanno stimato dei costi annui per paziente (solo dei farmaci) completamente diversi rispetto alla realtà italiana: €39.989 per natalizumab e addirittura €47.951 per fingolimod, con una differenza in favore di natalizumab di -€7.962 e con un trend opposto rispetto all'Italia.
Analogamente a quanto emerso in un recente studio italiano (32), il nostro lavoro mostra che il maggior driver di costo è legato al farmaco, che incide in media per circa l'87-95% sul costo complessivo della terapia. Altri autori hanno invece stimato un'incidenza più contenuta dei farmaci (67%) sul costo della malattia (5).
Nel nostro studio l'utilizzo di fingolimod comporta un risparmio rispetto a natalizumab, in termini di soli costi medi gestionali, pari a €2.120/anno/paziente e un risparmio complessivo di ben €4.276/anno/paziente. Come detto, queste differenze, nelle tre Regioni campione, sono sempre state favorevoli a fingolimod, con costi e differenze più elevate per la Lombardia (-€3.553/anno/paziente di costi gestionali e -€5.709/anno/paziente di costi totali sanitari) e con valori più allineati per Lazio (-€1.959/anno/paziente di costi gestionali e -€4.115/anno/paziente di costi totali sanitari) e Sicilia (-€2.019/anno/paziente di costi gestionali e -€4.175/anno/ paziente di costi totali sanitari).
Fingolimod quindi, confrontato vs natalizumab, evidenzia differenze importanti in termini sia di costi farmaceutici (+€2.156/anno/paziente con natalizumab) che di costi gestionali. In particolare, per quest'ultimo punto si deve sottolineare che i risparmi sui costi gestionali sono collegati alla natura del farmaco e alle caratteristiche del SSN italiano e, per questo motivo, risultano particolarmente solidi e difficilmente modificabili e costanti nel tempo.
Si deve inoltre aggiungere che, nell'attuale e complesso scenario dei farmaci disponibili, il trattamento precoce della malattia rappresenta la strategia migliore per ottenere outcomes ottimali a lungo termine e garantirne la maggiore efficacia (45-47). Nella real practice relativa al trattamento con fingolimod, lo studio PANGAEA (48) ha evidenziato come i pazienti con segni di attività di malattia, passati alla terapia con fingolimod dopo terapia con disease modifying drugs (DMD), abbiano ottenuto un significativo miglioramento del tasso annualizzato di recidive in 12 mesi: 0,4 con fingolimod vs valori al basale di 1,6 per INFβ e per glatiramer acetato. Questo si traduce in vantaggi consistenti anche da un punto di vista economico: i costi delle recidive rappresentano un parametro molto importante all'interno dei costi totali della SMRR. Uno studio pubblicato in Europa ha dimostrato che un paziente con recidiva ha un costo sanitario diretto 3,5 volte superiore a un paziente libero da recidive (16), senza considerare il costo annuale della riabilitazione, che ad esempio in Italia è stimato pari a €3.418 (49).
Nel nostro modello inoltre si evidenzia che, a fronte di un costo medio stimato per la sola recidiva pari a €1.021, moltiplicato per i pazienti in prima linea che andranno incontro a un evento (30% dei pazienti per un totale di 9888 casi il primo anno), un impiego precoce dei farmaci di seconda linea si può tradurre in un risparmio di circa €10 milioni per il primo anno.
L'analisi di sensibilità ha confermato i risultati del caso base, mostrando come la spesa sia inversamente proporzionale alla crescita delle quote di mercato di fingolimod, con un risparmio che può raggiungere anche i 32 milioni di euro in un anno, qualora si confronti uno scenario con una quota di mercato di fingolimod pari al 100% (dei farmaci in seconda linea) vs uno scenario con il consumo minimo di fingolimod (20% della seconda linea).
In merito alla variazione di spesa e ai possibili risparmi, si deve sottolineare che l'analisi ha considerato una popolazione stazionaria in cui non si teneva conto dei dati di incidenza, drop-out e mortalità. Questo, se da un lato ha minimizzato i possibili effetti sulla spesa e sulle sue variazioni, d'altro lato ha messo maggiormente in risalto l'effetto di sostituzione e/o di shift tra farmaci e linee terapeutiche, in modo da valorizzarne il possibile impatto sulla spesa sanitaria.
Va inoltre sottolineato che probabilmente, in linea con quanto riportato in letteratura (42), se si fossero considerati anche i costi indiretti (spostamenti dei pazienti per le visite, giornate di lavoro perse ecc.), i risultati sarebbero maggiormente a favore della somministrazione orale (che non richiede che i pazienti si rechino regolarmente in ospedale per le somministrazioni) rispetto a quella infusionale, e dunque fingolimod risulterebbe avere un profilo economico ancora più conveniente non solo per il SSN italiano ma anche per la Società.
Conclusioni
In Italia la SM mostra una spesa pari a 2,7 miliardi di euro, rappresentando la seconda patologia del sistema nervoso centrale (dopo il tumore cerebrale) per costo sociale per paziente. Nonostante i costi sanitari rappresentino una quota minoritaria dei costi sociali complessivi nella SM, la disponibilità di nuovi farmaci efficaci, con un effetto benefico sulla progressione della patologia, ha determinato un impatto sui costi a carico del Servizio Sanitario. Per garantire dunque una spesa sostenibile nel lungo termine per il trattamento della SM, sono necessarie valutazioni multidisciplinari che prendano in considerazione diversi domini di analisi, inclusi quelli etico-sociali, e diversi drivers di costo, non limitandosi quindi ai confronti dei soli costi farmacologici.
L'analisi condotta, rispetto a una simulazione d'incremento della spesa complessiva, ha messo in evidenza alcuni aspetti economici che possono essere presi in considerazione nelle politiche di indirizzo sanitario. Ad esempio, la scelta di terapie di prima linea economicamente più vantaggiose potrebbe garantire un'adeguata disponibilità finanziaria alle terapie di seconda linea e successive, ove lo switch terapeutico si renda necessario.
Tra le terapie di seconda linea, fingolimod, grazie a un migliore profilo gestionale ed economico rispetto a natalizumab, garantisce un risparmio sia sui costi farmaceutici che su quelli sanitari. Inoltre, se utilizzato tempestivamente in pazienti che non rispondono alla prima linea, fingolimod può generare un importante risparmio sanitario. È stato infatti dimostrato che, rispetto ad altri farmaci di prima linea, fingolimod è in grado di diminuire in modo significativo le recidive in pazienti non-responders ai DMD.
La scelta di fingolimod, alla luce delle analisi disponibili, considerata la complessità della gestione della SMRR e accertata la sostenibilità economico-finanziaria, mostra un vantaggio clinico e organizzativo per il SSN. La disponibilità e la scelta di terapie sempre più precoci potrebbe consentire l'ammortamento di una parte del costo maggiore dei trattamenti di seconda linea tramite i risparmi conseguiti a fronte del minore numero di recidive.
Infine, nonostante non fosse tra gli obiettivi di questo studio, è importante sottolineare che se si fossero considerati anche i costi indiretti in termini di perdita di produttività, fingolimod, in quanto terapia orale che non richiede un accesso routinario in ospedale per le infusioni, risulterebbe avere un profilo economico ancora più conveniente sia per il SSN italiano sia per la Società.
Footnotes
Financial support: This research was made possible by an unrestricted educational grant from Novartis Farma SpA.
Conflict of interest: The Authors declare they have no conflicts of interest related to the content of this article.