Abstract
Rheumatoid Arthritis, Ankylosing Spondylitis, Psoriatic Arthritis and Psoriasis determine a high cost to the Italian National Health Service (INHS). The availability of biological drugs – among which etanercept – greatly improved treatment efficacy. The biological drugs are an expensive resource. Etanercept patent protection has expired, and biosimilar has been recently approved. Considering the perspective of the INHS, a drug budget impact (DBI) analysis was conducted to evaluate the consequences of the biosimilar availability in terms of cost containment (savings), thanks to its lower price compared to the originator’s. The DBI model expects that some patients in treatment with the originator will switch (uptake rate) to the biosimilar and that some naïve patients will directly start treatment with the biosimilar (uptake rate). Separately considering all the different diseases for which etanercept is indicated (Rheumatoid Arthritis, Ankylosing Spondylitis, Psoriatic Arthritis and Psoriasis), the number of patients who might potentially use the biosimilar is estimated – based on disease prevalence and incidence rates, the overall proportion of treated patients and the etanercept market share. The time horizon extends to five years. The results from the analysis show (in the base case) that the availability of the biosimilar would provide overall annual savings over €25 million to the INHS in the fifth year, while the cumulated savings in the five years period would be about €90 million.
Introduzione
L’artrite reumatoide (AR), la spondilite anchilosante (SA), l’artrite psoriasica (AP) e la psoriasi (Ps) fanno parte della malattie infiammatorie croniche a eziopatogenesi autoimmune e si caratterizzano per l’elevato grado di disabilità che determinano, fin dalle fasi iniziali, sulla vita dei pazienti e dei loro familiari (1). A causa della cronicità, queste malattie generano un rilevante consumo di risorse sanitarie e non a carico del Servizio Sanitario Nazionale (SSN) e della socie-tà (2). Come accade per le patologie a forte impatto sociale, anche per queste malattie infiammatorie le principali voci di spesa sono identificabili nelle assenze dal posto di lavoro e nelle cure informali (3) che, complessivamente, rappresentano oltre la metà del costo totale di trattamento (4-6).
Ad eccezione della psoriasi, prese singolarmente l’incidenza e la prevalenza di queste malattie infiammatorie non risultano particolarmente elevate, ma se considerate complessivamente ricadono su una parte considerevole della popolazione italiana (7). Le terapie farmacologiche ad oggi disponibili non sono in grado di guarire definitivamente il paziente, ma permettono di raggiungere una bassa attività della malattia o lo stato di remissione. Sul finire degli anni ’90 si è assistito ad un cambiamento nella storia delle terapie farmacologiche grazie all’immissione sul mercato dei farmaci biologici, dimostratisi efficaci in caso di fallimento o di controindicazione delle terapie tradizionali (es. metotrexato, ciclosporina). Differentemente da quelli tradizionali, i farmaci biologici determinano però maggiori costi in termini di spesa farmaceutica a carico del SSN. Nonostante diverse analisi farmacoeconomiche abbiano evidenziato il costo-efficacia dei farmaci biologici rispetto a quelli tradizionali (8-18), è possibile che, a causa dell’alto costo, pazienti aventi diritto al biologico possano avere un accesso limitato e/o ritardato a queste terapie.
Ad oggi, visto che i primi farmaci biologici hanno raggiunto, o stanno raggiungendo, la scadenza brevettuale, è presente sul mercato italiano un numero sempre maggiore di farmaci biosimilari (19). Con il termine “biosimilare” si indica un medicinale simile a un farmaco biologico di ri-ferimento, detto “originator”, già autorizzato dall’Unione Europea, per il quale sia scaduta la copertura brevettuale (19). Va sottolineato che il biosimilare e il relativo originator sono medicinali costituiti dallo stesso principio attivo che garantiscono comparabili livelli di qualità, sicurezza ed efficacia (20). L’Agenzia Europea del Farmaco (European Medicines Agency, EMA), attraverso la reda-zione di apposite linee guida (“Guideline on Similar Biological Medicinal Products”), ha provveduto a specificare il percorso (esercizio di comparabilità) che un farmaco biosimilare deve superare per ottenere l’autorizzazione all’immissione in commercio (21-23). In breve, l’esercizio di comparabilità è un confronto espresso in termini di qualità, sicurezza ed efficacia tra biosimilare e originator (21-23). La comparabilità non clinica si basa su studi pre-clinici di confronto diretto delle proprietà biochimiche, farmacocinetiche e farmacodinamiche (21-23). La comparabilità clinica viene esaminata conducendo studi clinici randomizzati e controllati relativi all’efficacia e alla sicurezza del farmaco biosimilare nei confronti del biosimilare su una patologia di riferimento (21-23).
L’esercizio di comparabilità garantisce che eventuali differenze osservate nel biosimilare rientrino all’interno del range di variabilità dimostrata per il farmaco originator e non abbiano alcun impatto su sicurezza ed efficacia. Questo percorso approvativo, infatti, non viene solamente applicato per la commercializzazione di un biosimilare, ma è stato inizialmente definito per il farmaco originator, in caso si verifichi una variazione nel processo produttivo, per garantire che eventuali variazioni delle caratteristiche chimico-fisiche non alterino efficacia e sicurezza.
Poiché secondo quanto stabilito dalle Linee Guida EMA i farmaci biosimilari non dovrebbero, per definizione, determinare differenti benefici clinici rispetto all’originator, il beneficio atteso dalla loro immissione in commercio è rappresentato dal loro minore prezzo (la negoziazione del prezzo deve garantire una riduzione di prezzo di almeno il 20% rispetto al prezzo del biologico originator) e dal conseguente effetto competitivo (eventuale riduzione del prezzo del biologico originator). Nonostante l’assenza di studi osservazionali retrospettivi finalizzati a stimare in modo sistematico gli eventuali risparmi conseguiti dal SSN grazie all’adozione dei biosimilari, recenti analisi di mercato hanno evidenziato come il loro consumo sia in costante crescita (24,25). È quindi sempre più realistico sostenere che l’utilizzo dei biosimilari contribuisca in modo importante alla sostenibilità della spesa farmaceutica pubblica. I potenziali risparmi generati dall’utilizzo del biosimilare possono infatti rappresentare un’importante risorsa economica, che potrebbe essere reinvestita per incrementare l’accesso dei pazienti alla terapia, riducendo l’impatto della spesa farmaceutica sul SSN.
Obiettivo
La scadenza della protezione brevettuale di etanercept ha portato alla recente immissione sul mercato del suo corrispettivo farmaco “biosimilare”. In accordo con tale scenario, l’obiettivo della presente analisi è valutare quale contenimento della spesa farmaceutica pubblica potrebbe derivare dai potenziali risparmi (Drug Budget Impact, DBI) determinati dall’utilizzo di etanercept biosimilare (di seguito “biosimilare”) nei prossimi cinque anni in Italia.
Materiali e metodi
Con l’obiettivo di stimare l’impatto finanziario generato dall’utilizzo del biosimilare è stato costruito uno specifico modello di simulazione, grazie al quale si ipotizza che tale farmaco, meno costoso di etanercept originator (di seguito “originator”), possa in parte sostituirsi a quest’ultimo. Va precisato che, vista la sovrapponibilità terapeutica tra biosimilare e originator, il modello di simulazione non considera eventuali valutazioni (costi di trattamento) su eventi evitati e/o effetti collaterali.
Quale principale conseguenza del processo di parziale sostituzione tra biosimilare e originator si determinerebbe un risparmio per il SSN, da quantificare grazie al confronto tra l’ipotesi di assenza e di presenza del biosimilare sul mercato. Nella prima ipotesi la spesa sarà costituita dal costo determinato dai pazienti trattati con il solo originator, mentre nella seconda ipotesi la spesa farmaceutica sarà composta dal costo dei pazienti trattati col biosimilare e da quello dei rimanenti pazienti trattati con l’originator.
La struttura del modello di simulazione è brevemente descritta dai seguenti elementi. L’analisi di Drug Budget Impact copre un orizzonte temporale di cinque anni, a partire dal primo anno di commercializzazione del biosimilare. Il costo del trattamento farmacologico è stato stimato in considerazione delle seguenti quattro indicazioni: AR, SA, AP e Ps. Con lo scopo di riprodurre uno scenario il più realistico possibile, l’adozione del biosimilare è stimata distinguendo tra due tipologie di popolazione: i) quella dei pazienti che iniziano la prima linea di trattamento biolo-gica con etanercept (di seguito naïve population), per i quali l’adozione del biosimilare potrà avvenire fin da subito al posto dell’originator e ii) quella dei pazienti già in trattamento con un biologico (di seguito switch population). Quest’ultima tipologia di popolazione viene distinta in due ulteriori sottopopolazioni: la prima è rappresentata dai pazienti in trattamento di prima linea con l’originator di etanercept (di seguito pazienti in trattamento continuativo), per i quali il passaggio al biosimilare può avvenire solo tramite switch. La seconda sottopopolazione è invece costituita da pazienti che sono già in trattamento con un farmaco biologico, ma che devono effettuare switch ad etanercept (di seguito pazienti switch win). Per questi pazienti l’adozione del biosimilare potrà avvenire fin da subito al posto dell’originator.
La scelta di distinguere tra differenti popolazioni e sottopopolazioni ha permesso di considerare differenti quote di uptake (riferite al numero di pazienti trattati) del biosimilare in funzione della popolazione valutata. Ciò ha infatti permesso, seguendo anche l’atteggiamento della pratica clinica in tema di sostituzione tra farmaci biologici e originator, di ipotizzare dei tassi di uptake per i pazienti in trattamento continuativo più prudenti rispetto a quelli adottati per la naïve population e per i pazienti switch win.
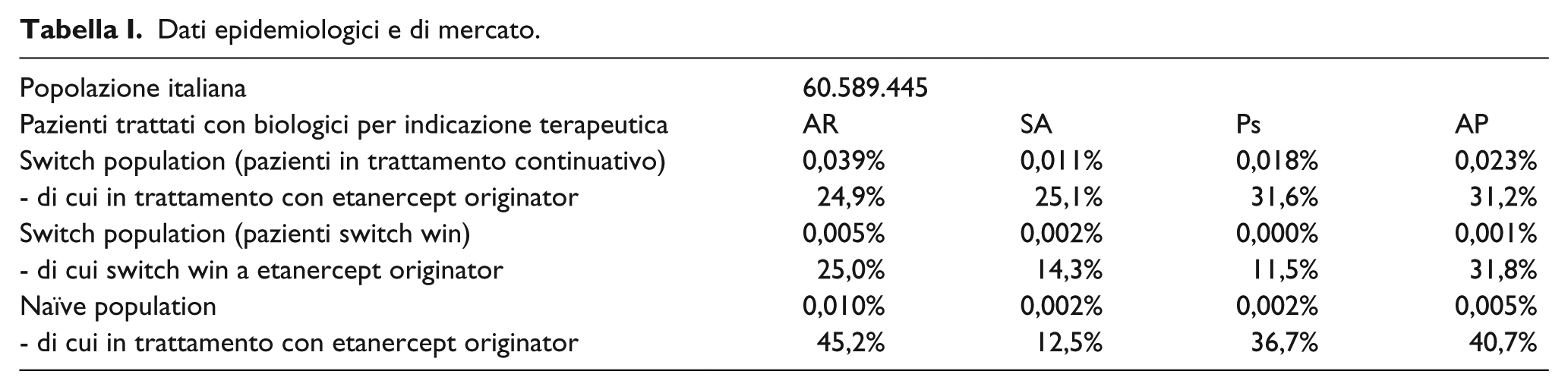
La stima del numero di pazienti in trattamento con il biologico di etanercept nel primo anno di osservazione è stata effettuata partendo dalla popolazione residente in Italia al 1° gennaio 2017 (26). Tale popolazione viene mantenuta co-stante nei successivi quattro anni. La Tabella I, distinguendo per le quattro indicazioni, riporta le percentuali considerate per stimare la quantità dei pazienti (swicth e naïve population) in trattamento con farmaci biologici e la relativa percentuale di quelli in trattamento con il solo originator di etanercept. Tali percentuali sono state calcolate facendo ri-ferimento a dati mercato IMS (MAT 09-2016) (27). La Tabella II riporta invece le ipotesi adottate per i tassi di uptake, lungo i cinque anni di osservazione, del biosimilare rispetto all’originator (28). Tali previsioni non vengono differenziate per le quattro indicazioni.
Dati epidemiologici e di mercato.
Tassi di uptake del biosimilare rispetto all’originator.

Ciò premesso, i pazienti vengono valutati nelle giuste dimensioni nel primo anno di osservazione in funzione delle percentuali associate alla switch population e alla naïve population e delle relative percentuali dei trattati con l’originator; tale popolazione viene mantenuta costante negli anni successivi. Applicando a questa popolazione i tassi di uptake si ottiene il numero di pazienti che passano al biosimilare nei relativi anni e, per differenza, quelli in trattamento con l’originator.
Il costo medio di trattamento per paziente/anno è basato sul prezzo ex-factory al netto degli sconti obbligatori, di eventuali sconti concordati e di sconti mediamente offerti in gara applicati all’originator e al biosimilare, sulla dose e sul numero di somministrazioni. I dosaggi e costi per il trattamento annuo di un paziente con etanercept originator o biosimilare sono simili per tutte le indicazioni. Il farmaco viene impiegato al dosaggio di 50 mg alla settimana (52, 1 settimane/anno) e il costo medio annuo per paziente trattato con l’originator rispetto al biosimilare è rispettivamente di € 10.672,60 e € 7.803,96.
Risultati
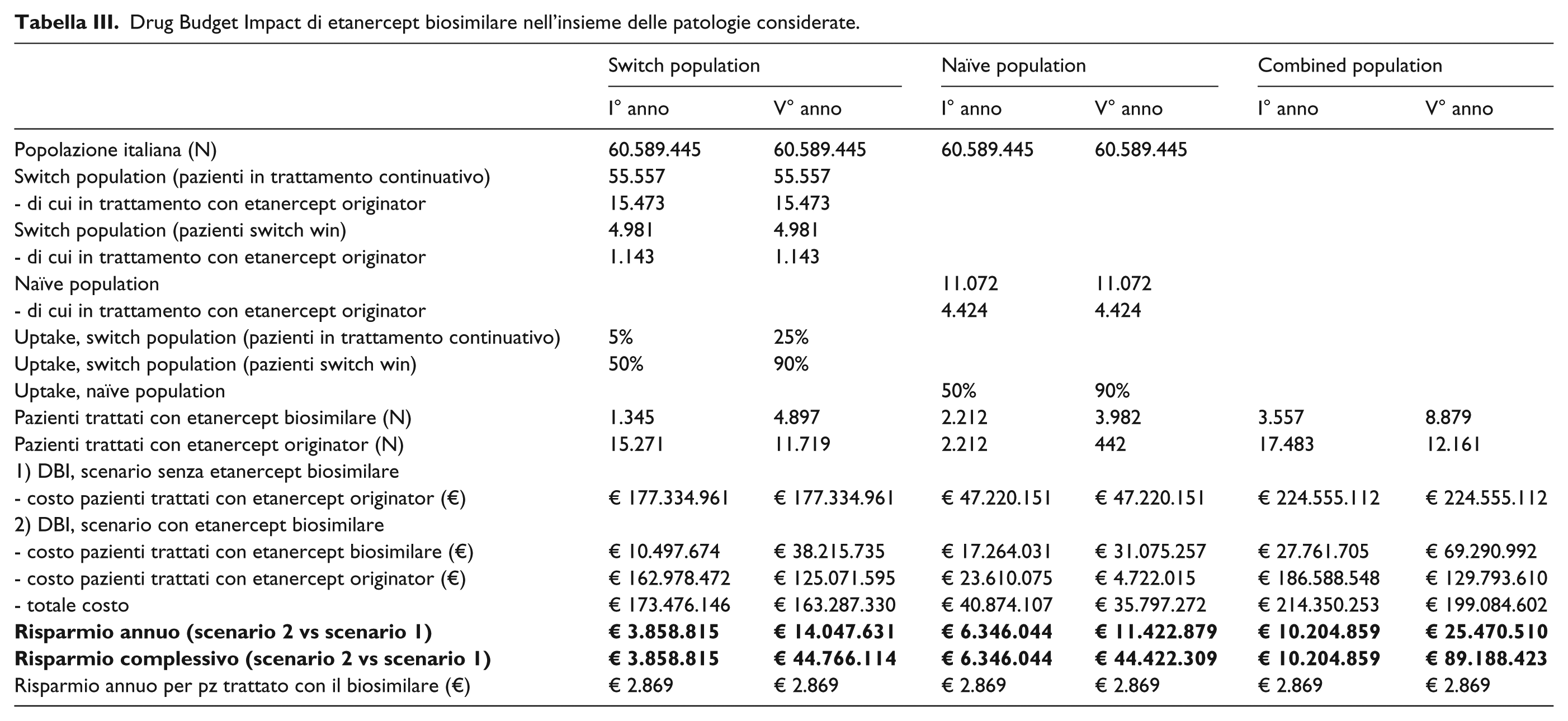
L’analisi di Drug Budget Impact del biosimilare è stata condotta sia a livello aggregato che per singole indicazioni terapeutiche. La Tabella III presenta i dati aggregati per le quattro aree terapeutiche, mentre le successive tabelle (Tabelle IV -VII) presentano i dati analitici per ognuna delle singole indicazioni. Al fine di consentire una rappresentazione leggibile nell’ambito di una pagina di testo, per ogni tabella sono riportati solo l’anno iniziale e finale del quinquennio considerato.
Drug Budget Impact di etanercept biosimilare nell’insieme delle patologie considerate.
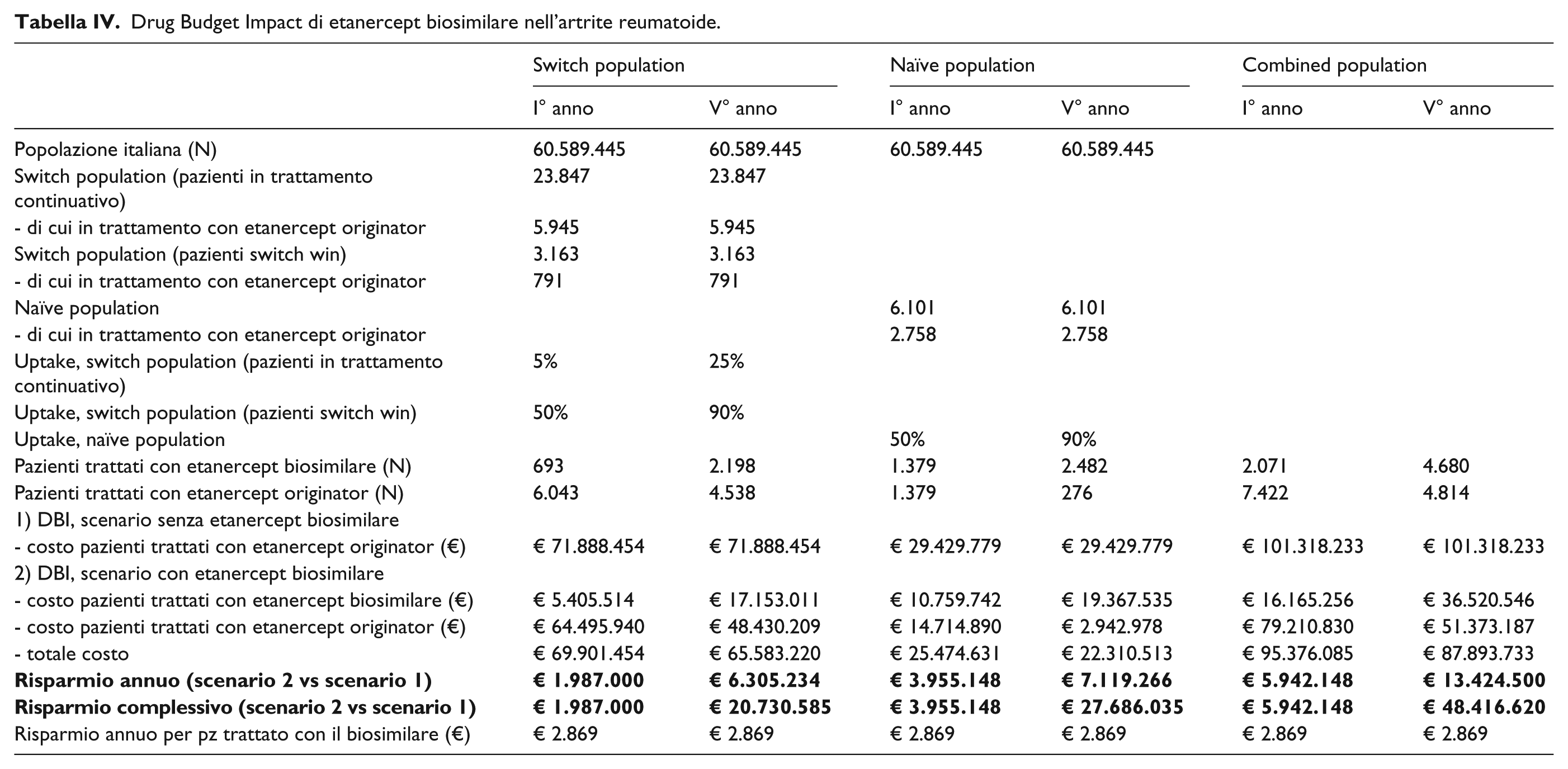
Drug Budget Impact di etanercept biosimilare nell’artrite reumatoide.
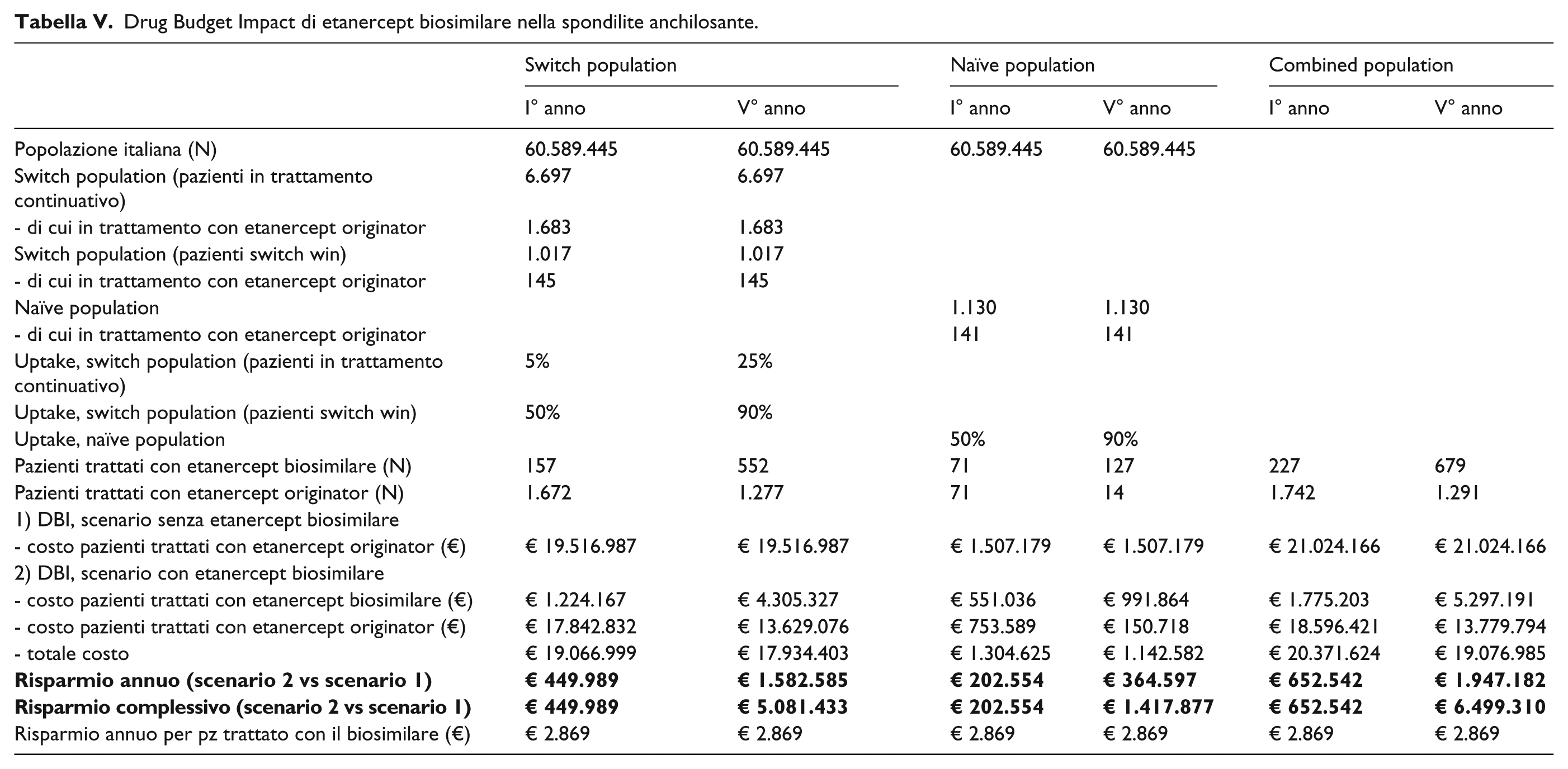
Drug Budget Impact di etanercept biosimilare nella spondilite anchilosante.
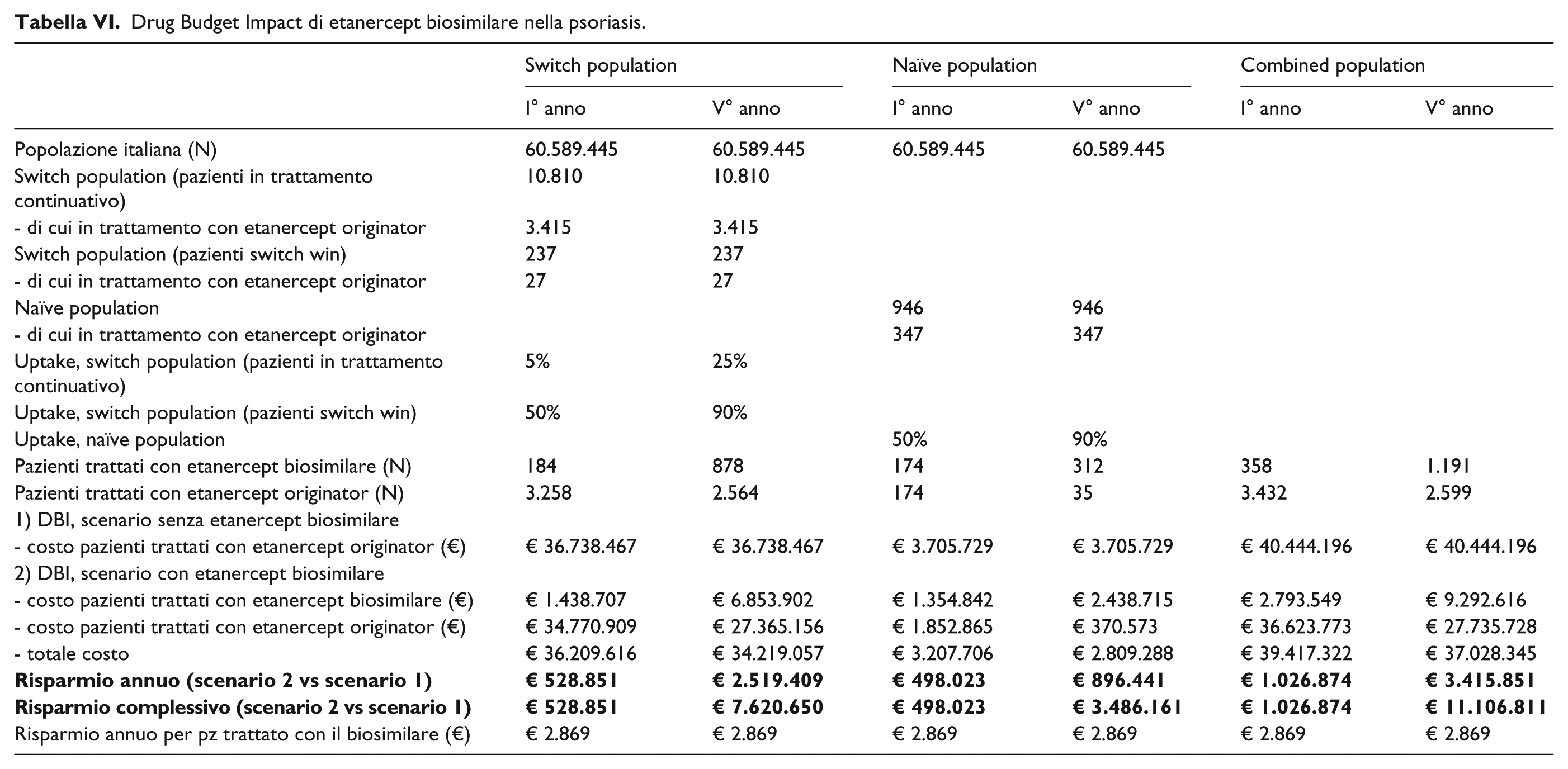
Drug Budget Impact di etanercept biosimilare nella psoriasis.
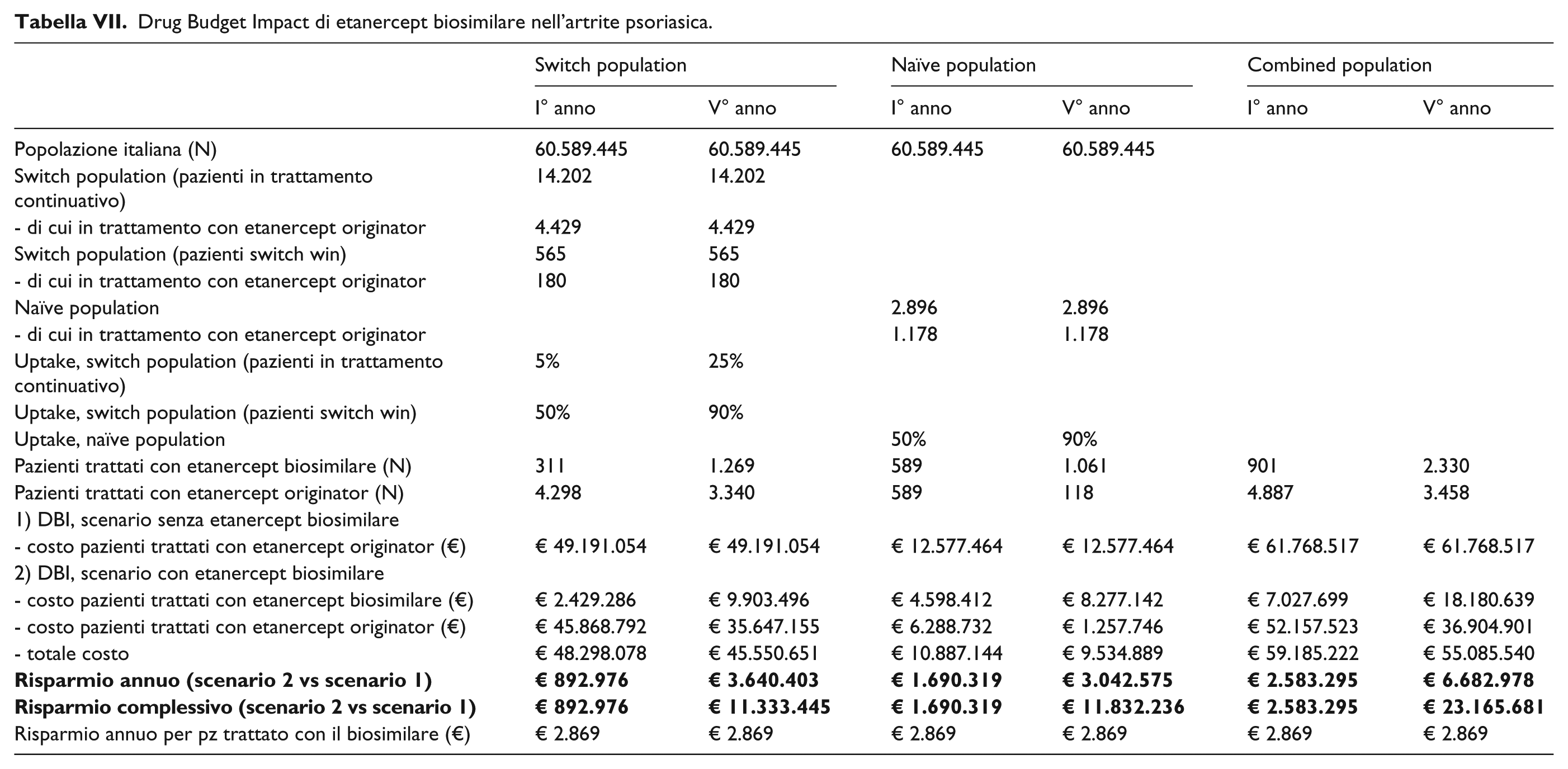
Drug Budget Impact di etanercept biosimilare nell’artrite psoriasica.
Nel primo anno di osservazione, in Italia, la popolazione in trattamento con un biologico per una delle quattro indicazioni esaminate è stimabile in 60.538 pazienti (totale switch population), di cui 15.473 trattati con l’originator (Tabella III). Nello stesso anno, i pazienti interessati sarebbero 11.072, di cui 4.424 in trattamento con l’originator (naïve population) (Tabella III). Assumendo che nel primo anno il biosimilare sia immesso sul mercato e che si realizzino i tassi di uptake ipotizzati per la switch population (Tabella II), nel quinto anno di osservazione passeranno al biosimilare 4.897 pazienti contro i 1.345 del primo anno. Mentre nel quinto anno, fra i trattati naïve (naïve population), 3.982 lo saranno col biosimilare e solo 442 con l’originator. Complessivamente in riferimento alla combined population (switch più naïve population) si prevede che a fine quinquennio 8.879 pazienti saranno trattati col biosimilare e 12.161 con l’originator. In termini di impatto sul budget a carico del SSN, il costo totale per trattare questi 21.040 pazienti, se il biosimilare non fosse disponibile, sarebbe pari a € 224.555.112. Costo che invece si ridurrebbe a € 199.084.602 grazie al minor prezzo del biosimilare, qualora questo si sostituisse parzialmente all’originator (Tabella III). In questo caso, il risparmio annuo realizzato dal SSN nel quinto annuo sarebbe pari a € 25.470.510 e quello complessivo nel quinquennio ammonterebbe a € 89.188.423. In altre parole, a ogni paziente trattato col biosimilare corrisponderebbe un risparmio annuo di € 2.869 (Tabella III).
In accordo con i dati presentati in Tabella IV sarebbero 27.011 nel primo anno i pazienti con AR trattati con un biologico, di cui 6.736 in trattamento con l’originator (Tabella IV). Sempre nel primo anno, sarebbero 6.101 i pazienti incidenti in trattamento con un biologico, di cui 2.758 in trattamento con l’originator (Tabella IV). Nel quinto anno di osservazione il modello simula che passeranno complessivamente (combined population) al biosimilare 4.680, rispetto ai 4.814 in trattamento con l’originator. Nel quinto anno, il cost-saving annuo a favore del SSN sarebbe di € 13.424.500, mentre quello cumulativo (5 anni) ammonterebbe a € 48.416.620 (Tabella IV).
Considerando invece i dati di Tabella V, a fine del pe-riodo di osservazione sarebbero 679 i pazienti con spondilite anchilosante in trattamento con il biosimilare, rispetto al totale di 1.970 pazienti trattati con etanercept (biosimilare più originator). Nel quinto anno, il risparmio annuo a favore del SSN sarebbe di € 1.947.182, mentre quello cumulato ammonterebbe a € 6.499.310 (Tabella V).
I pazienti con psoriasi in trattamento con il biosimilare nel quinto anno sarebbero 1.191 rispetto ai 2.599 in trattamento con l’originator (Tabella VI). A fine del periodo di osservazione il risparmio per il SSN sarebbe pari a € 3.415.851, mentre quello cumulativo nei cinque anni salirebbe a € 11.106.811 (Tabella VI).
Infine, in riferimento all’artrite psoriasica, ultima indicazione terapeutica esaminata, nel quinto anno salirebbero a 2.330 i pazienti in trattamento con il biosimilare rispetto ai 3.458 in trattamento con l’originator (Tabella VII). Anche in quest’ultimo caso il maggior utilizzo del biosi-milare rispetto all’originator determinerebbe una riduzione della spesa nel quinto anno di € 6.682.978, mentre il risparmio cumulativo nei 5 anni ammonterebbe a € 23.165.681 (Tabella VII).
Discussione
La presente analisi di Drug Budget Impact è stata condotta con la finalità di stimare l’impatto finanziario a ca-rico del SSN derivante dall’arrivo sul mercato del biosimilare di etanercept nelle seguenti quattro indica-zioni: artrite reumatoide, spondilite anchilosante, artrite psoriasica e psoriasi. In particolare, rispetto a queste indicazioni terapeutiche, è stata ipotizzata una duplice moda-lità di espansione del biosimilare rispetto all’originator. In un caso è stato previsto che il biosimilare possa essere somministrato a una quota di pazienti già in corso di trattamento con l’originator (switch population), nel secondo caso è stato invece ipotizzato che il biosimilare sia prescritto come prima opzione del trattamento con biologico (naïve population).
I tassi annui di uptake ipotizzati nel quinquennio, assieme al minor prezzo del biosimilare rispetto all’originator di etanercept, evidenziano come durante i cinque anni il risparmio a vantaggio del SSN passi dall’2,2% del primo anno (€ 3.858.815) all’11,3% del quinto anno (€ 25.470.510), con un risparmio cumulativo nel quinquennio di € 89.188.423. Tra le quattro indicazioni terapeutiche, a fronte del maggior numero potenziale di pazienti in trattamento con il biosimilare, è l’artrite reumatoide a determinare nel quinquennio il maggior risparmio complessivo per il SSN con circa 48,5 milioni di euro, seguita dall’artrite psoriasica con circa 23 milioni di euro.
Questi risultati trovano riscontro in quelli prodotti da due esperienze: la prima – in ordine cronologico – condotta a livello internazionale (29), la seconda in ambito nazionale (19). L’analisi internazionale, condotta lungo un orizzonte temporale di 5 anni (2016-2020), ha avuto come obiettivo la stima dell’impatto economico determinato dall’introduzione sul mercato in 5 Paesi europei (Regno Unito, Germania, Francia, Spagna e Italia) del biosimilare di etanercept nel trattamento di soggetti adulti con una delle seguenti indicazioni quattro indicazioni: AR, AP, Ps SA (29). Sono stati considerati tre tipi di popolazioni (pazienti naïve al biologico, pazienti in trattamento con il biologico, e pazienti che hanno fallito il primo biologico), mentre è stata ipotizzata una crescita del tasso di uptake del biosimilare compresa tra il 5% (primo anno di osservazione) e il 40% (ultimo anno del quinquennio). Secondo i risultati di quest’analisi l’introduzione del biosimilare determinerebbe dei risparmi (budget-saving) per tutti e 5 i Paesi europei (Regno Unito €111-284 milioni di euro, Francia € 35-81 milioni di euro, Germania € 76-187 milioni di euro, Italia € 46-111 milioni di euro e Spagna € 28-65 milioni di euro). Gli autori concludono affermando che, rispetto all’attuale scenario, tali risparmi potrebbero consentire di trattare un maggior numero di pazienti (dai 3.100 pazienti per il Regno Unito ai 17.130 per la Germania). Gli stessi autori hanno poi presentato i risultati dell’analisi di budget impact per la sola indicazione al trattamento dell’artrite reumatoide (30). In questo caso, i potenziali risparmi associati all’utilizzo del biosimilare di etanercept potrebbero arrivare nei cinque anni a € 62-162 milioni di euro per il Regno Unito, a € 19-46 milioni di euro per la Francia, a € 42-105 milioni di euro per la Germania, a € 26-62 milioni di euro per l’Italia e infine a € 16-37 milioni di euro per la Spagna. Anche in questo caso i risparmi potrebbero permettere di trattare un maggior numero di pazienti con AR (dai 1.530 pazienti per il Regno Unito agli 8.430 pazienti per la Germania) (30).
L’analisi finanziaria condotta in riferimento allo scenario nazionale ha stimato, lungo un orizzonte temporale di sei anni, l’impatto finanziario aggregato dei biosimilari di infliximab ed etanercept nel trattamento dell’artrite reumatoide, della psoriasi, delle malattie infiammatorie inte-stinali e dell’artrite psoriasica (19). Grazie alla disponibilità dei biosimilari di infliximab e di etanercept si potrebbero ottenere risparmi cumulativi compresi tra i 132 e i 296 mi-lioni di euro, in funzione di differenti ipotesi di sostituzione (tassi di uptake) adottate (19).
Avendo quale principale obiettivo la stima del contenimento della spesa farmaceutica pubblica che potrebbe derivare dai potenziali risparmi determinati dall’utilizzo del biosimilare rispetto all’originator di etanercept, il mo-dello di simulazione, qui adottato, è stato costruito semplificando alcune variabili di contesto che vengono di seguito richiamate.
Il tasso di uptake del biosimilare rispetto all’originator, ricavato dalle estrapolazioni fatte grazie ai dati di mercato, è stato ipotizzato identico per tutte e quattro le indicazioni (AR, SA, AP e Ps); tale semplificazione non ha permesso di riprodurre differenti comportamenti prescrittivi (per singola indicazione) che potrebbero essere invece adottati nella pratica clinica. Anche la quota di mercato dell’originator sul totale dei pazienti trattati con biologici è stata assunta costante nel tempo senza considerare eventuali variazioni di mix tra l’originator e altre molecole per la stessa indicazione. Così facendo è stata, di fatto, esclusa una possibile riduzione nel periodo di osservazione del numero di pazienti in trattamento con etanercept a fronte dell’introduzione sul mercato di altre molecole potenzialmente più efficaci di etanercept nel trattamento di AR, SA, AP e Ps o dell’approvazione da parte dell’European Medicines Agency (EMA) di altri biosimilari con le stesse indicazioni (es. biosimilare di adalimumab). L’inclusione di tali variabili modificherebbe verosimilmente l’effetto finanziario generato dal passaggio al biosimilare di etanercept qui presentato.
Con l’obiettivo di fornire una stima nazionale dell’impatto finanziario del biosimilare di etanercept, i tassi di uptake e le quote di mercato, qui utilizzate, sono state stimate senza tenere in considerazione la presenza di eventuali politiche regionali quali possibili determinanti di mercato e/o di spesa, poiché fortemente differenziate da regione a regione. Politiche regionali che favoriscono alti tassi di penetrazione del biosimilare ne massimizzerebbero l’impatto finanziario, differentemente da ciò che accadrebbe in regioni con un basso tasso di penetrazione del biosimilare.
Nel presente modello di budget impact, la switch population è stata distinta in pazienti in trattamento continuativo con etanercept, per i quali il passaggio al biosimilare può avvenire solo tramite switch, e in pazienti switch win, per i quali, già in trattamento con un farmaco biologico, l’adozione del biosimilare può avvenire fin da subito al posto dell’originator. Per questi ultimi soggetti, rispetto a quanto ipotizzato nel modello, nella partica clinica potrebbe accadere che, a seguito del fallimento di una prima linea biologica con un anti-TNFα, la scelta di una seconda linea possa ricadere su un farmaco con un differente meccanismo d’azione. Anche questo elemento influenzerebbe l’impatto finanziario del biosimilare di etanercept qui stimato.
Ci sono infine alcune variabili che incidono sul prezzo che non sono state incluse nell’analisi. Nel modello non è stato valutato l’impatto economico che eventuali gare regionali potrebbero determinare sul prezzo di acquisto dei farmaci qui considerati. A giustificazione di tale scelta si fa presente che l’obiettivo della presente analisi è stato quello di presentare una panoramica nazionale e generale dell’impatto finanziario del biosimilare di etanercept, a prescindere dalla presenza di differenti politiche di prezzo adottate in ambito regionale e/o locale. L’analisi finan-ziaria non ha inoltre preso in considerazione né l’effetto competitivo che il prezzo del biosimilare potrebbe esercitare sulle politiche di prezzo adottabili da parte dell’azienda titolare dell’immissione in commercio dell’originator, né quello generato dalla presenza di più biosimilari di etanercept (ad oggi sono due quelli approvati dall’EMA) che potrebbe causare una riduzione più rapida dei prezzi.
Conclusioni
Si può concludere che l’analisi di Drug Budget Impact abbia messo in luce gli apprezzabili risultati positivi che si potrebbero avere in termini di risparmio della spesa farmaceutica pubblica conseguenti l’utilizzo del biosimilare di etanercept. Oltre a ciò, grazie al minor costo del biosimilare rispetto all’originator, sarebbe possibile iniziare prima il trattamento biologico per i pazienti che presentano una risposta non ottimale ai DMARD convenzionali. Ipotizzando una maggiore penetrazione del biosimilare rispetto al tasso considerato in questa analisi si potrebbero ulteriormente incrementare i potenziali risparmi per il Servizio Sanitario Nazionale. Il reinvestimento di queste risorse consentirebbe di incrementare ulteriormente l’accesso dei pazienti al trattamento delle patologie infiammatorie croniche.
Footnotes
Declaration of Conflicting Interest
The authors declare that there is no conflict of interest.
Funding
This research was made possible by an educational grant from Sandoz S.p.A.
