Abstract
Economic impact of biosimilar drugs in Italy: past, present and future of infliximab and etanercept
Purpose
The objective of this study is to estimate the impact of the Anti-TNF monoclonal antibodies that are currently approved in Italy (etanercept ed infliximab) on healthcare expenditure between 2014 and 2020.
Methods
The prediction model was developed considering the standard unit consumption and equivalent patients from IMS database. Drug costs were calculated using official hospital reimbursement prices reported by the Italian Pharmaceutical Agency. By analysing the number of treated patients between 2014 and 2016, clinical experts develop three alternative scenarios and provide estimating the number of patients that they expect to treat during the next 4 years with biosimilars or originator in Italy.
Results
Considering the number of standard units dispensed each year, the model estimated a total number of 28.000 patient/year that are treated with infliximab or etanercept (28% for AR, 17% for psoriasis, 26% for psoriatic arthritis, 18% for IBD and 11% for other indications). In 2020, drugs expenditure is expected to decline between €42 and €90 billion as compared to 2014, (12% and 26% of total spending in 2014 respectively). Overall, the cumulative savings are estimated between €132 and €296 billions.
Conclusions
The estimated savings may constitute an economic resource that could be re-invested for achieving improvements within the healthcare system.
Keywords
Introduzione
I progressi della biologia molecolare, dai primi anni ’80 a oggi, hanno permesso di introdurre in commercio più di 150 prodotti biotecnologici che sono stati registrati a livello mondiale, rappresentando una nuova frontiera per il trattamento di patologie complesse, invalidanti, spesso fortemente limitative della vita di relazione dei pazienti (1). È indubbio, alla luce dei risultati emersi negli ultimi anni, che questi farmaci abbiano rappresentato e stiano tuttora rappresentando un notevole progresso nelle alternative terapeutiche a disposizione del medico (1).
Ad oggi, la prima generazione di farmaci biologici sta raggiungendo, o ha già raggiunto, la scadenza brevettuale e un gran numero di biosimilari si sta affacciando nel mercato farmaceutico italiano. Il termine biosimilare indica un medicinale simile a un farmaco biologico di riferimento già autorizzato nell'Unione Europea, per il quale sia scaduta la copertura brevettuale. Un biosimilare e il suo prodotto originator sono ottenuti mediante processi produttivi differenti, ma rappresentano alternative simili in termini di qualità, sicurezza ed efficacia (2).
Entro il 2018 scadrà il brevetto di almeno 45 farmaci biotecnologici, per un fatturato mondiale di 58 miliardi di dollari. Un vasto numero di altri prodotti è tuttora in fase di registrazione o sviluppo clinico: i biologici costituiranno una quota significativa del mercato farmaceutico nel prossimo futuro.
Da alcuni anni, per malattie infiammatorie croniche di forte impatto economico e sociale, come l'artrite reumatoide (AR), la spondilite anchilosante, la malattia di Crohn, l'artropatia psoriasica e la psoriasi, sono disponibili alcuni inibitori del tumor necrosis factor-α (anti-TNF), come etanercept, infliximab, adalimumab ecc. (3). Tali farmaci hanno determinato un significativo miglioramento nell'evoluzione della patologia, associato a un incremento della qualità di vita di questi pazienti (4). Negli anni 2013-2016, l’European Medicines Agency (EMA) ha approvato nove nuovi farmaci biosimilari, tra cui i primi tre biosimilari di infliximab (Remsima® e Inflectra®, autorizzati nel corso dell'anno 2013, e Flixabi®, nel maggio 2016) e il primo biosimilare di etanercept (Benepali®, nel gennaio 2016) (4).
In generale, si prevede che l'arrivo dei biosimilari possa generare importanti risparmi per i Sistemi Sanitari e offrire, in questo modo, la possibilità di estenderne l'accesso a un maggior numero di pazienti e di disporre di un maggiore quantitativo di risorse economiche da reinvestire in innovazione (2). Ma a quanto ammonterebbe il risparmio atteso nei prossimi anni da parte del Servizio Sanitario Nazionale (SSN) italiano grazie all'introduzione dei biosimilari? Qual è l'impatto che i biosimilari di etanercept ed infliximab avranno sulla spesa farmaceutica nazionale e regionale?
Il presente studio si è posto come obiettivo quello di sviluppare un modello economico in grado di fornire una quantificazione degli impatti economici che i biosimilari degli anticorpi anti-TNF attualmente disponibili in Italia (etanercept e infliximab) avranno sulla spesa sanitaria nazionale e regionale tra il 2015 e il 2020. Il modello si basa sui dati di consumo IMS e sulle stime di costo al netto degli sconti trasparenti previsti per legge.
Metodi
Fonte dei dati
La base dati da cui è stato sviluppato il modello di previsione di spesa è stata quella della dispensazione dei farmaci biologici e biosimilari del database IMS (5). In particolare, in questo database vengono riportate le unità standard dispensate (siringhe o flaconi) attraverso tutti i canali, e i pazienti stimati in base alle unità ipotizzabili per paziente a livello mensile. La Figura 1 (A e B) riporta le unità standard dispensate sull'intero territorio nazionale e il corrispettivo numero di pazienti stimati per ciascun trattamento. I pazienti vengono stimati sulla base del rapporto di unità per paziente riportate nella Tabella I.
Unità standard/mese per molecola per paziente
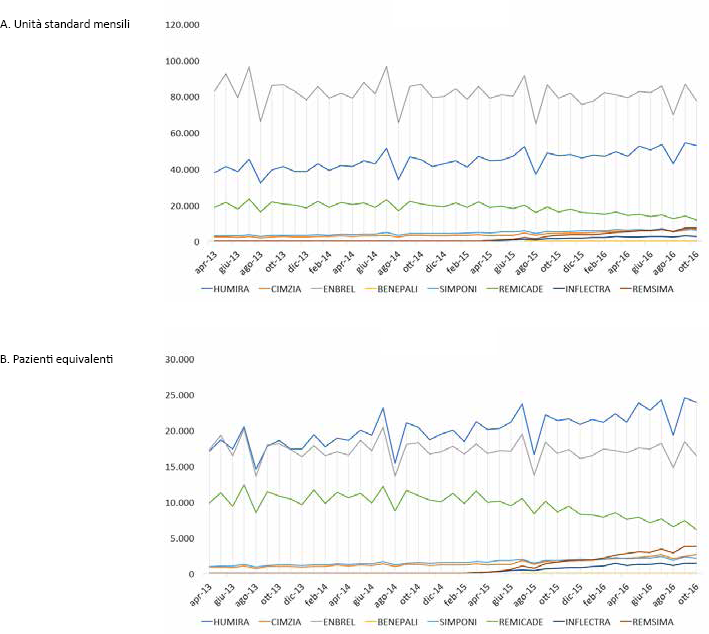
Unità standard dispensate e pazienti corrispondenti trattati sul territorio nazionale – Italia aprile 2013-ottobre 2016.
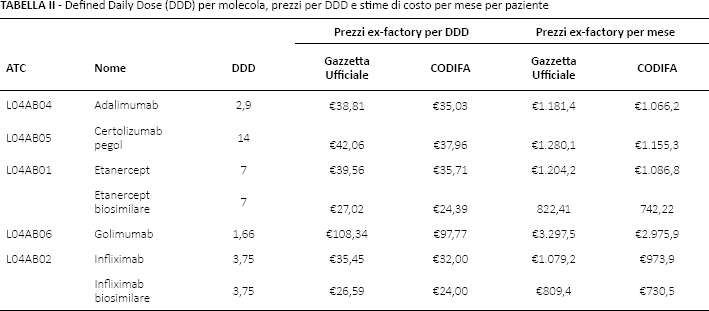
Sulla base delle informazioni derivanti dai consumi per unità standard e pazienti equivalenti è stata stimata la spesa mensile per gli anti-TNF considerati nel modello previsivo. La spesa farmaceutica, nello specifico, è stata calcolata sui prezzi di cessione ospedaliera al netto degli sconti trasparenti previsti per legge e visibili da Prontuario (6). I costi sono stati calcolati sulla base dei prezzi per Defined Daily Dose (DDD) di ciascuna molecola disponibili in Gazzetta Ufficiale (GU) e poi scontati al netto degli sconti trasparenti visibili da Prontuario (Tab. II). Il costo mensile è stato stimato utilizzando il costo per DDD moltiplicato per 365,25 gg/12 mesi.
Defined Daily Dose (DDD) per molecola, prezzi per DDD e stime di costo per mese per paziente
Infine, i risultati di dispensazione e di costo sono stati stratificati sulla base dei principali raggruppamenti terapeutici, in linea con le indicazioni a oggi approvate per gli anti-TNF in Italia. In particolare sono stati considerati per etanercept e infliximab i seguenti sottogruppi di analisi:
Artrite reumatoide (infliximab ed etanercept)
Artrite psoriasica (infliximab ed etanercept)
Psoriasi (infliximab ed etanercept)
Malattia infiammatoria intestinale (IBD) – Colite Ulcerosa e Malattia di Crohn (infliximab)
Altro (indicazioni residuali).
Scenari di previsione della spesa farmaceutica
Sono stati sviluppati tre scenari alternativi sulla base delle percezioni di tre esperti clinici coinvolti nello studio e co-autori del lavoro. In particolare, gli esperti hanno analizzato le stime dei pazienti trattati nel periodo 2014-2016 e hanno espresso la loro percezione sulla percentuale di pazienti che, ipotizzano, verranno trattati a livello nazionale con un farmaco biosimilare o con l'originator di infliximab (Tab. III) ed etanercept (Tab. IV) nel corso dei successivi 4 anni.
Scenari di analisi per tipologia di paziente e indicazione terapeutica secondo l'expert opinion: percentuale di pazienti in trattamento con infliximab biosimilare sul totale dei pazienti trattati con infliximab – Scenario caso-base, minimo e massimo – Italia
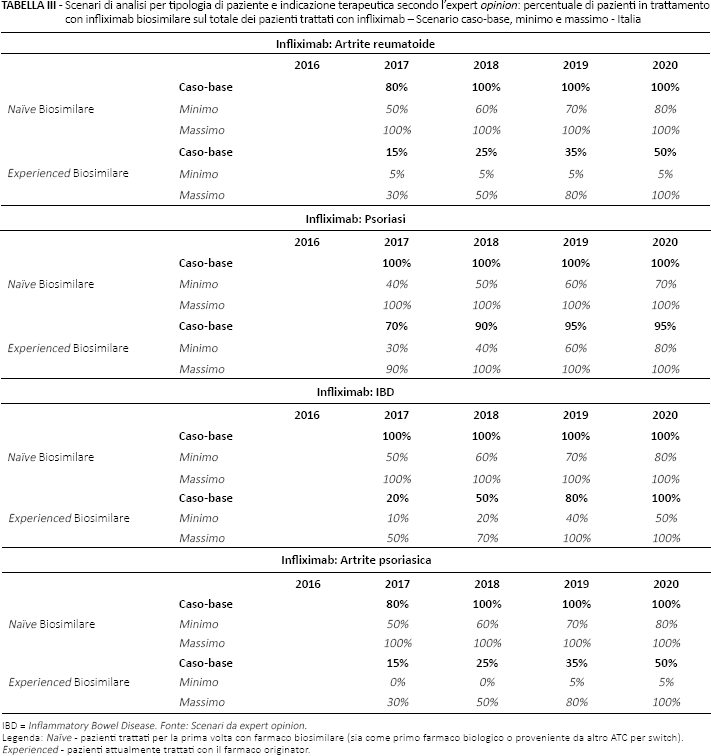
IBD = Inflammatory Bowel Disease. Fonte: Scenari da expert opinion.
Legenda: Naïve - pazienti trattati per la prima volta con farmaco biosimilare (sia come primo farmaco biologico o proveniente da altro ATC per switch).
Experienced - pazienti attualmente trattati con il farmaco originator.
Scenari di analisi per tipologia di paziente e indicazione terapeutica secondo l'expert opinion: percentuale di pazienti in trattamento con etanercept biosimilare sul totale dei pazienti trattati con etanercept - Scenario caso-base, minimo e massimo – Italia
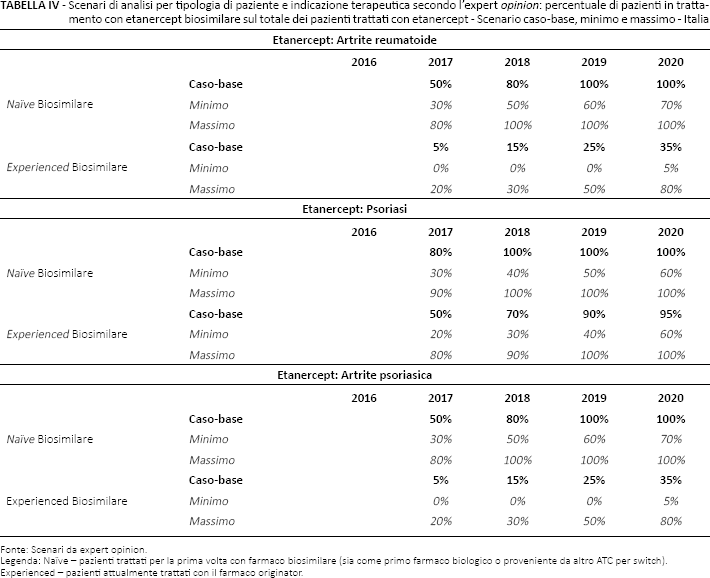
Fonte: Scenari da expert opinion.
Legenda: Naïve – pazienti trattati per la prima volta con farmaco biosimilare (sia come primo farmaco biologico o proveniente da altro ATC per switch).
Experienced – pazienti attualmente trattati con il farmaco originator.
Gli scenari sono stati costruiti sulla base dell’expertise dei clinici coinvolti, suddividendo tali scenari per indicazione terapeutica, tipologia di paziente (naïve o experienced) e considerando un'ipotesi di minimo e massimo della penetrazione del biosimilare in Italia nel corso del tempo. Nello specifico, il paziente naïve è stato definito come un paziente che per la prima volta inizia un trattamento con farmaco biologico o che per la prima volta viene trattato con la molecola in analisi (effettuando quindi uno switch terapeutico da un altro farmaco biologico con altra ATC alla molecola in analisi), mentre i pazienti experienced vengono definiti come i pazienti che sono già in trattamento con il farmaco biologico originator. La Tabella III riporta gli scenari considerati nell'analisi secondo le indicazioni degli esperti. In particolare, i clinici hanno riportato la percentuale di pazienti (sul totale dei pazienti naïve o experienced in trattamento per ciascun anno) che a loro avviso verrà trattata con farmaci biosimilari. Per l'anno 2016, sono state considerate le percentuali di farmaco biosimilare registrato dai dati IMS tra gennaio e ottobre 2016 (ultimi dati disponibili), applicando un trend lineare crescente per gli ultimi 2 mesi dell'anno.
Stima delle riduzioni di spesa
Tutte le riduzioni di spesa sono state stimate attraverso la differenza netta (e percentuale) tra la spesa sostenuta nel 2014 – anno in cui non erano ancora presenti biosimilari degli anti-TNF in Italia – e la spesa sostenuta negli anni successivi secondo scenari analizzati. Nel dettaglio verranno riportate le differenze nette di spesa per ciascun anno di analisi e i risparmi cumulativi nei 4 anni di introduzione dei biosimilari, distinguendo per molecola e indicazione.
Il modello non prevede alcuna assunzione di switch dei pazienti da altre molecole a etanercept (biosimilare o originator) e non sono considerati altri tipi di modificazione dell'evoluzione dei pazienti (stessi pazienti trattati con anti-TNF nei differenti scenari) tra il caso-base e lo scenario al fine di individuare l'effetto netto del biosimilare oggetto di studio. Infine, il modello assume che il numero dei pazienti in trattamento con i due farmaci in analisi sia costante nel tempo e che il saldo tra pazienti naïve e switch/decessi sia pari a zero.
Risultati
Stima dei pazienti
Il modello, considerando le unità standard vendute per ciascun anno, stima che vi siano circa 28.000 pazienti/anno in trattamento con infliximab o etanercept. Di questi, il 28% è costituito da pazienti trattati per AR, il 17% per psoriasi, il 26% per artrite psoriasica, il 18% per IBD e la restante quota parte percentuale per le altre indicazioni (Tab. V).
Distribuzione dei pazienti per tipologia di farmaco e indicazione terapeutica – Italia, 2014-2016
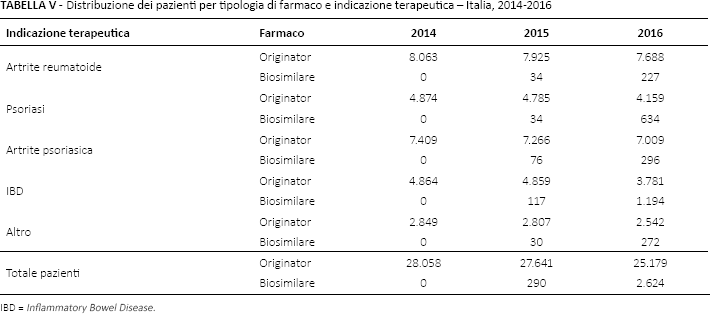
IBD = Inflammatory Bowel Disease.
Osservando la distribuzione dei pazienti per farmaco biologico e biosimilare in Italia registrata nei primi anni dopo la loro commercializzazione, si osserva come solo le IBD, al 2016, avessero in media nel corso dell'anno più del 2% di pazienti effettivamente trattati con biosimilare (di infliximab). Le altre indicazioni avevano una stratificazione al di sotto dell’1,2% di pazienti trattati con biosimilare. Nel corso del 2016 l'incremento nell'utilizzo dei biosimilari ha consentito di poter trattare circa il 24% di pazienti affetti da IBD con farmaci biosimilari e, anche se a ritmi meno elevati, anche per i pazienti con psoriasi la percentuale è salita al 13,2%. Per quanto riguarda i pazienti trattati per AR e artrite psoriasica, il numero dei pazienti è rimasto piuttosto basso anche nel corso del 2016, con meno del 5% (2,9% per l'AR e 4,1% per l'artrite psoriasica) dei pazienti trattati con biosimilare (Tab. V).
Seguendo le ipotesi di distribuzione dei pazienti tra originator e biosimilare costruite attraverso le opinioni degli esperti coinvolti, la Figura 2 (A-F) mostra l'andamento dei pazienti per indicazione terapeutica e tipologia di farmaco. Secondo tali scenari il numero di pazienti che, al 2020, arriverà a essere trattato con farmaci biosimilari per AR o artrite psoriasica sarà di circa il 56% (55,8% per AR e 57,3% per artrite psoriasica). Viceversa, per i pazienti con IBD o psoriasi gli esperti prevedono una penetrazione del biosimilare ben più rilevante, con addirittura il 90% dei pazienti trattati con biosimilare (87% per la psoriasi e 97% per IBD). Mediamente, degli oltre 27.800 pazienti che si prevede saranno trattati in Italia nel 2020 con etanercept o infliximab, circa il 71% verrà trattato con un farmaco biosimilare (Fig. 2).
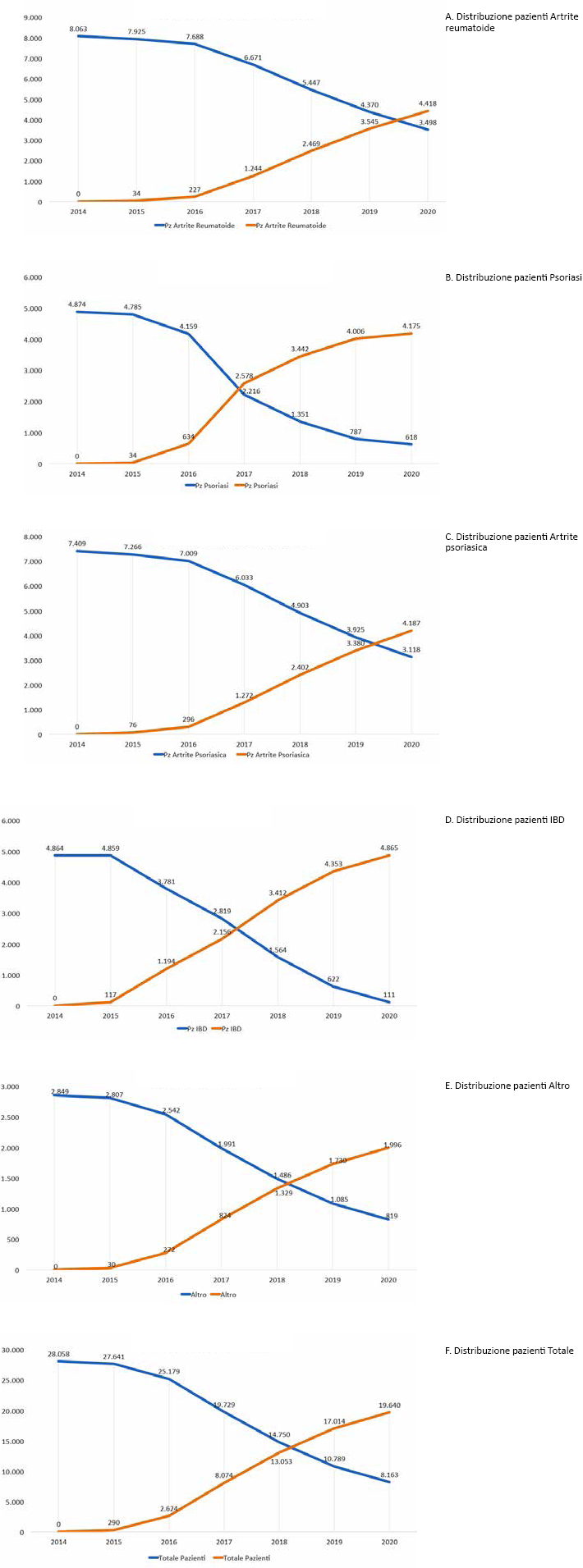
Distribuzione dei pazienti in trattamento con originator o biosimilare – Italia 2014-2020.
Risultati di spesa
L'utilizzo del biosimilare, sulla base degli scenari ipotizzati, consentirebbe una riduzione media di spesa, rispetto a quanto registrato nel 2014, di oltre 73 milioni di euro (pari al 21% di quanto è stato speso nel corso del 2014 per i medesimi farmaci) considerando solo etanercept e infliximab (Fig. 3, A–B–C–D–E–F). Tali riduzioni vanno dai quasi 19 milioni di euro di riduzione generati dalla psoriasi (-31% rispetto alla spesa del 2014) ai 12 milioni di euro di riduzione nei pazienti trattati per IBD (-23% rispetto alla medesima spesa del 2014).
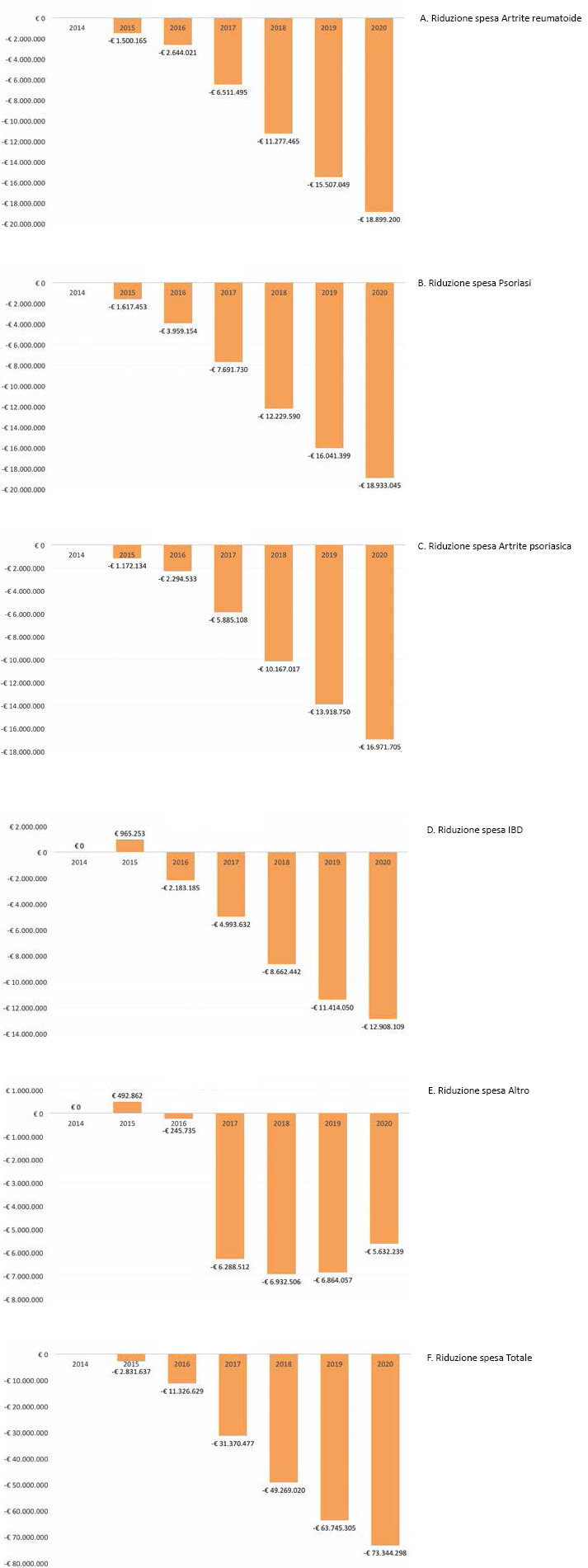
Riduzioni di spesa rispetto al 2014 per indicazione terapeutica – Italia 2014-2020.
La Figura 4 mostra le riduzioni complessive generate dai due farmaci in esame fino al 2016 e i possibili risparmi ottenibili secondo le ipotesi di minimo e massimo proposte dagli esperti (linee tratteggiate). Al 2020 la spesa per i pazienti trattati con etanercept o infliximab potrebbe ridursi tra i 42 e 90 milioni di euro in base al numero di pazienti che effettivamente verranno trattati con farmaci biosimilari (Fig. 4). Complessivamente, nel corso dei 6 anni di disponibilità dei biosimilari delle molecole considerate, si potrebbero ottenere risparmi cumulativi tra i 132 e i 296 milioni di euro.
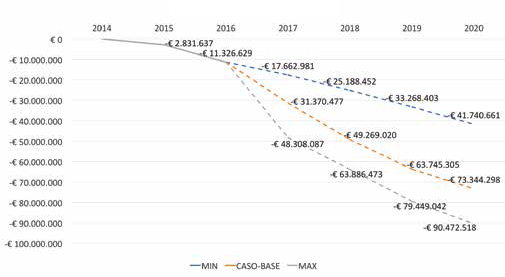
R iduzioni d i s pesa c omplessive per scenario di analisi.
Discussione e conclusioni
Il modello permette di stimare l'impatto economico che i biosimilari di etanercept e infliximab consentiranno di ottenere nella spesa farmaceutica per gli anti-TNF in Italia nei prossimi 5 anni, qualora venga garantita la pari efficacia rispetto all'originator. Partendo dai dati di consumo registrati tra il 2013 e il 2016, sono state effettuate assunzioni di evoluzione del mercato degli anti-TNF per orizzonti temporali di breve-medio periodo. I differenti scenari indagati hanno dimostrato che la spesa farmaceutica per i biologici, nonostante sia in crescita in termini di pazienti trattati e di costi sostenuti, può essere rallentata (e in molti casi ridotta) grazie all'introduzione tempestiva di trattamenti con efficacia non inferiore e costi ridotti rispetto agli originator.
Nel corso del 2016 in Italia la spesa per gli anti-TNF ha superato i 741 milioni di euro, con un incremento del 7% rispetto all'anno precedente e del 12% rispetto al 2014 (5). Le stime prodotte dal modello economico proposto e derivanti dagli scenari definiti dagli esperti consentono di prevedere una riduzione di circa il 6% della spesa complessiva per anti-TNF al 2017 e addirittura un risparmio cumulato superiore al 31% della spesa annua. Tali cifre diventano ancora più importanti nel momento in cui analizziamo le riduzioni di spesa per gli specifici farmaci in analisi. Ad esempio, i biosimilari di infliximab hanno già fatto registrare un decremento del 4% della spesa complessiva per questa tecnologia tra il 2014 e il 2016 (5). In futuro il nostro modello ha stimato una riduzione di spesa annua per un ulteriore 20% rispetto al 2016 e un impatto cumulato tra il 2016 e il 2020 che supererà gli 80 milioni di euro (74% della spesa annua per infliximab nel corso del 2016).
Conclusioni simili si possono trarre analizzando le riduzioni di spesa stimate per etanercept. Il rapporto OSMED (7) ha individuato una spesa annua per il solo etanercept superiore a 193 milioni di euro nel 2014. Il modello economico ha stimato una riduzione di spesa al 2017 (primo anno completo di introduzione del biosimilare) di circa 20 milioni di euro, pari al 9% della spesa sostenuta al 2014. Complessivamente le riduzioni ottenute secondo i nostri scenari potrebbero generare risparmi per oltre 148 milioni di euro tra il 2016 e il 2020 (78% di quanto stimato dal report OSMED).
Il modello, come ogni proiezione statistica, presenta dei limiti metodologici. In primo luogo considera delle proiezioni basate su assunzioni che non derivano da studi osservazionali, ma da interviste face to face ed expert opinion. Tuttavia, il consulto con il board di esperti è stata l'unica via che ha permesso di individuare il potenziale prescrittivo che i biosimilari hanno all'interno di ciascuna area terapeutica in Italia. Tali scenari sono stati ottenuti consultando i co-autori dello studio, i quali hanno fatto riferimento a centri eterogenei tra loro e possono rappresentare uno spaccato verosimile delle differenze territoriali esistenti in Italia. Inoltre, le analisi di sensibilità hanno consentito delle stime intervallari in grado di rappresentare un minimo e un massimo di impatto di spesa credibile.
In secondo luogo, i prezzi considerati per le stime di spesa fanno riferimento a dati non perfettamente allineati con la reale spesa sostenuta dal SSN. Di fatto, il modello si basa sui prezzi ex-factory, che prevedono ulteriori sconti non trasparenti al pubblico. Questo risulta ancora più vero se consideriamo che il prezzo tanto degli originator quanto dei biosimilari sono spesso legati a effetti di contrattazione regionale (8, 9). Tuttavia, le stime consentono di ottenere una scala di risparmi realistica, ipotizzando che gli sconti siano costanti per le differenti molecole in analisi e che la negoziazione regionale consenta delle riduzioni di spesa costanti. Inoltre, anche in questo caso l'analisi di sensibilità consente di tenere conto della variabilità intrinseca nei dati di prezzo.
Infine, un'assunzione importante del modello riguarda la sua staticità. Infatti, non vengono considerati gli effetti dell'entrata di nuovi biosimilari nell'arco di tempo preso in considerazione né tantomeno le modificazioni demografiche della popolazione trattabile con i differenti farmaci in analisi o l'introduzione di farmaci innovativi ad alto costo nella stessa area terapeutica (ustekinumab, secukinumab, apremilast, ixekizumab). Effettivamente, quest'ipotesi non rappresenta la realtà terapeutica, tuttavia è utile per evitare confondimenti da effetti che non appartengono ai trattamenti in analisi.
In conclusione, i biosimilari rappresentano uno strumento per liberare risorse a supporto di terapie innovative, ma devono essere usati con piena consapevolezza, criterio e con le necessarie attenzioni per poter gestire al meglio le risorse economiche in questo campo. Il modello per la sua semplicità nella definizione degli scenari e per l'elasticità di adattamento rappresenta un buono strumento per la quantificazione dei risparmi garantiti dalle variazioni del mercato degli anti-TNF in Italia che si verificheranno nei prossimi anni, consentendo di distinguere gli effetti in base ai periodi di introduzione e alle quote di pazienti che passano da un farmaco originator a prezzo più elevato a un biosimilare a prezzi minori ed efficacia comparabile. Inoltre, per la prima volta nel contesto nazionale vengono quantificati i risparmi potenziali stratificati sulla base delle principali indicazioni terapeutiche e basati sui differenti specialisti che effettuano prescrizioni nella real practice italiana. Ovviamente, l'impatto stimato dal nostro modello fa riferimento a soli due farmaci biosimilari degli anti-TNF, a cui seguiranno nel corso degli anni molte altre molecole che potranno contribuire alla reale sostenibilità della spesa farmaceutica (adalimumab, trastuzumab, rituximab, bevacizumab, insulina aspart, insulina glargine). Tuttavia, a nostro avviso, il presente lavoro rappresenta un utile strumento per i decisori nazionali e regionali al fine di facilitare le decisioni allocative e gestionali delle risorse specifiche per la cura di malattie infiammatorie croniche con anticorpi anti-TNF. Futuri lavori fondati sugli stessi criteri potrebbero fornire informazioni aggiuntive in grado di fornire stime reali di spesa e sostenibilità delle future politiche del farmaco in Italia.
Footnotes
Financial support: No grants or funding have been received for this study.
Conflict of interest: None of the authors has financial interest related to this study to disclose.
