Abstract
In Peru, Hypothenemus hampei or the coffee berry borer, (CBB) is the most important pest, causing specific damage to coffee crops, because it causes fruit to fall during feeding. On the other hand, Beauveria bassiana is an entomopathogenic fungus widely used in biological control. This study determine the induction of chitinase and laminarinase of B. bassiana in presence of H. hampei powder and how it relates to pathogenicity in order to promote the development of biological control agents and replace the use of pesticides. Three different liquid media cultures were prepared to induce the enzymatic production and growth of B. bassiana; and biomass, total proteins, conidia, enzymatic activities and enzymatic specific activities were evaluated. Data were analyzed using SPSS 19.0. Significant differences (P<0.05) for biomass (F = 5.30; df = 35; P < 0.05), conidia (F = 190.87; df = 35; P<0.05), total proteins (F = 91.04; df = 35; p < 0.05), laminarinase activity (F = 27.61; df = 35; P<0.05), specific laminarinase activity (F = 25.31; df = 35; P < 0.05), chitinase activity (F = 32.66; df=35; P<0.05) and specific chitinase activity (F = 26.91; df=35; P < 0.05) were determined between each treatment evaluated. Levels of chitinase and laminarinase determined that induction of these enzymes is possible in liquid media cultures supplemented with powdered H. hampei extract. Results require further evaluation for application in vivo but are fundamental and constitute a contribution to knowledge about the pathogenic mechanism of B. bassiana.
Introducción
La broca del café Hypothenemus hampei Ferrari, 1867 (Coleoptera: Curculionidae) proviene del África Ecuatorial y es reportada en el Perú desde 1962 (SENASA 2014). H. hampei es considerado el insecto plaga más importante que, causa daño específico a los cerezos del café produciendo la caída de los frutos (Bustillo 2006) y según Colonia (2014) puede afectar la producción en más del 50 %, dependiendo de la altitud, clima y condiciones naturales.
El control de esta plaga resulta difícil de ejecutar debido a que pasa la mayor parte de su ciclo de vida dentro del fruto (Damon 2000). Los métodos más comunes para su control recurre al uso de insecticidas que penetran en el fruto y resultan tóxicos para la salud y el medio ambiente (Liceras y Farge 2011). En consecuencia, su uso viene siendo estrictamente regulado, sobretodo, en los mercados de exportación donde los Límites Máximos de Residuos de Plaguicidas (LMR) disminuyen cada vez más para evitar la contaminación de los alimentos; es en este contexto que, el uso de productos biológicos es cada vez más importante (Posada et al. 2007).
Una de las principales estrategias de control biológico de la broca se basa en el uso de hongos entomopatógenos (Monzon et al. 2008) como Beauveria bassiana (Bals. - Criv.) Vuill. 1912 (Hypocreales: Clavicipitaceae) aunque no se ha determinado completamente el mecanismo de su virulencia se sabe que producen enzimas extracelulares que degradan los componentes de la pared del insecto permitiendo la penetración hifal a través de la cutícula (Fan et al. 2007). Delgado et al. (2001) han indicado la posible relación entre la actividad enzimática de estos hongos y su patogenicidad al insecto sobre el cual se dirige el control; por lo que es necesario evaluar la actividad catalítica de las enzimas producidas por los hongos entomopatógenos y favorecer el desarrollo de agentes controladores que reemplacen a los químicos sintéticos.
Este estudio evaluó el mecanismo de acción de B. bassiana sobre broca del café mediante la evaluación in vitro de la actividad quitinasa y laminarinasa inducidas con sustratos de H. hampei. Se postuló que la presencia de compuestos presentes en la pared del insecto podrían estimular el mecanismo de virulencia de B. bassiana y de esta forma, hallar marcadores de virulencia relacionados a la expresión de las enzimas laminarinasa y quitinasa que estén asociadas a características de su desarrollo (número de conidios, biomasa y proteínas totales del exudado) en diferentes tiempos de crecimiento en cultivo in vitro.
Materiales y métodos
Obtención de la muestra
La cepa de B. bassiana de código CCB-LE 262 se obtuvo del Servicio Nacional de Sanidad Agraria (SENASA). La cepa se cultivó en un medio GPL (glucosa 4%, peptona 1 % y extracto de levadura 1% a pH 5,6) para su mantenimiento y recuperación antes de iniciar los ensayos.
Establecimiento de los cultivos suplementados con sustrato de H. hampei
Se prepararon tres medios de cultivo líquido diferentes: (1) medio mínimo (MM), (2) MM + glucosa 0,1% (MMG) y (3) MM + extracto en polvo de H. hampei 0,1% (MMB). El MM se preparó según Fernandes et al. (2012). Los medios se ajustaron a pH 5,6 y se esterilizaron en autoclave (Greetmet, YX-280D) a 121 °C por 15 minutos a una presión de 15 psi. Todos los tratamientos se realizaron por triplicado. Cada uno contenía 20 mL del medio de cultivo, con una concentración final de 1,3 x 106 conidios de B. bassiana. Cada tratamiento se incubó a 25 °C +/- 2 °C en agitación constante de 130 rpm (Orbital GenieTM- EEUU) durante los tiempos establecidos para cada evaluación.
Determinación de conidios, biomasa, proteínas totales
A las 0, 24, 96 y 216 horas después de la inoculación, se tomó un mililitro de extracto crudo de cada cultivo para el conteo de conidios mediante microscopía (Olympus®-Japón). Otro mililitro se centrifugó a 10.000 rpm para determinar la cantidad de proteínas totales del sobrenadante a 280 nm en un espectrofotómetro (Shimadzu, UV-1700, Japón), el valor del mismo se multiplicó por el factor de calibración (y = 0,0006x + 0,0004, R2 = 0,9999) de la curva de albúmina de suero bovino (BSA, Sigma), la cual se estableció previamente para calcular la concentración de proteínas en µg/µL. El resto de cultivo se centrifugó a 10.000 rpm en microtubos y se obtuvo el peso seco del precipitado. Los sobrenadantes se almacenaron a -20 °C para la evaluación de las actividades enzimáticas.
Ensayos enzimáticos
Se determinó la actividad enzimática laminarinasa según Sigma, con algunas modificaciones en los volúmenes. 170 µl de sobrenadante se transfirió a un tubo con 500 µl de tampón citrato de sodio 0,1 M (Merck) + NaCl 0,2 M (Backer) a pH 5,6 y 170 µl de la solución de laminarina 1% (p/v) (Sigma). Se incubó a 37 °C por 180 minutos y se detuvo la reacción a 100 °C durante 5 minutos. Posteriormente, se desproteinizó diluyendo 250 µl de la muestra en 1.250 µl de H2O esteril, mezclándola con 250 µl Ba(OH)2 (Merck) y 250 µl de ZnSO4 (Merck) durante 5 minutos, para finalmente ser centrifugada a 5.000 rpm por 5 minutos. La concentración de azúcares reductores se determinó utilizando el método de Somogy (1952) y Nelson (1944) y se leyó la absorbancia de la muestra a 540 nm. La ecuación para determinar la cantidad de glucosa liberada siguió la ecuación: y = 0,1164 x +0,0316, con R2 = 0,998. Una unidad de enzima, libera 1,0 µmol de azúcar reductor (glucosa) a partir de la laminarina por minuto a pH 5,0 a 37 °C. La actividad específica se expresa u moles glucosa.mg proteína-¹.min-¹.
Para la determinación de la actividad enzimática quitinasa se utilizó el protocolo de Sigma modificado en los volúmenes: 100 µl de muestra de sobrenadante se mezcló con 400 µl tampón citrato de sodio 0,1 M (Merck) + NaCl 0,2 M (Merck) pH 5, que contenía como sustrato el 4-nitrofenil N-acetil-B-D-glucosaminida (Sigma 9376), a 1mg/ml. Se incubó a 37 °C durante 30 minutos. La reacción se detuvo con 1 ml de NaCO3 400 mM (Merck) y se leyó a 405 nm. La ecuación para determinar la cantidad de p-nitrofenol liberado fue: y = 0,0127x + 0,0037 con Rβ = 1. Se define que una unidad de enzima es capaz de hidrolizar 1 µmol de 4-nitrophenil N-acetil-ẞ-D-glucosaminida a 1 µmol p-nitrofenol + 1 µmol N-acetilglucosamina por minuto a 37 °C y pH 5. La actividad quitinasa específica se expresa como µmoles de p-nitrofenol. mg proteína-¹.min-¹
Diseño experimental
Los datos de cantidad de conidios, biomasa y proteínas, así como las actividades específicas quitinasa y laminarinasa, se colectaron en Excel. El ensayo se basó en un modelo aditivo lineal de dos vías (tres tratamientos por cuatro tiempos) para cada una de las variables:
Resultados
En la tabla 1, se determinan las diferencias significativas (P < 0,05) para la biomasa (F = 5,30; df = 35; P < 0,05), conidios (F = 190,87; df = 35; P < 0,05), proteínas totales (F = 91,04; df=35; P<0,05), actividad laminarinasa (F = 27,61; df=35; P < 0,05), actividad específica laminarinasa (F = 25,31; df = 35; P < 0,05), actividad quitinasa (F = 32,66; df = 35; P < 0,05) y actividad específica quitinasa (F = 26,91; df = 35; P < 0,05) del factorial originado por cada uno de los tratamientos (MM, MMG y MMB) y todos los tiempo de evaluación (0, 24, 96 y 216 horas).
El medio MMB (MM + extracto en polvo de H. hampei) a las 24 horas de evaluación, indujo la mayor cantidad de biomasa (0,0026 µg/µl), proteínas (2,11 µg/µl), actividades enzimáticas laminarinasa (2,22 x 10-9 µmol glucosa.min⁻¹) y quitinasa (1,61 x 10-4 µmol pNF.min⁻¹). Así mismo, el medio MMB obtuvo la mayor actividad específica quitinasa (3,03 x 10-9 µmol pNF.min¯¹.mg proteína¹) apartir de las 96 horas, en comparación a los otros medios (Tabla 1). Se observa que las mayores cantidades de conidios están en los tratamientos MMG96 (46 x 106) y MMG216 (61,3 x 106). La mayor actividad específica laminarinasa se obtuvo en MMG216 (3,30 X 10-9 µmol Glucosa.min-¹.mg proteína⁻¹).
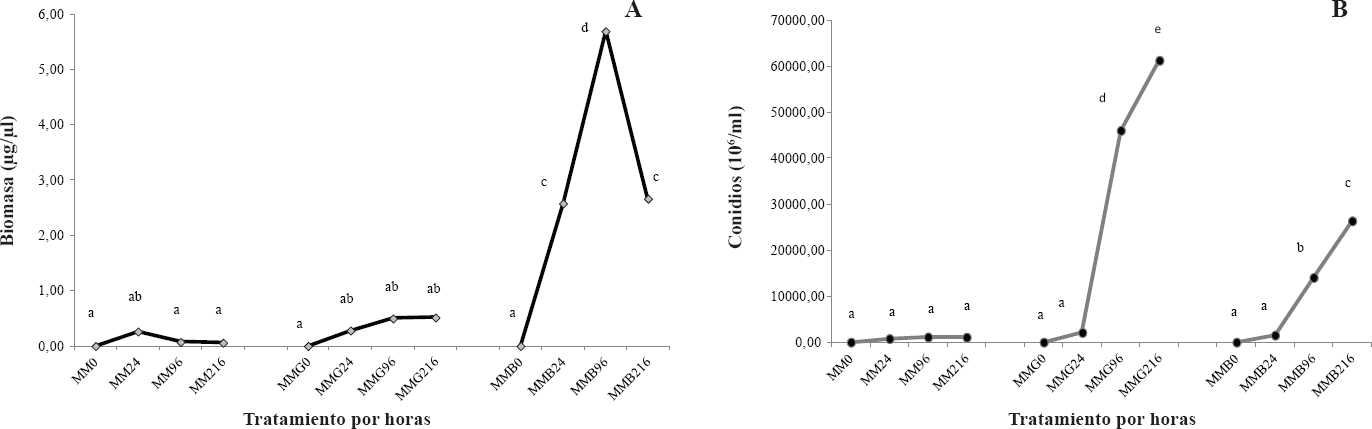
(A) Comparación de biomasa (µg/µl) y (B) número de conidios (x 106/ml) de los tratamientos según las horas de evaluación. P < 0,05. Los valores de cada media son obtenidos por triplicado. Diferencias significativas entre tratamientos tienen letras diferentes (P < 0,05).
En la Figura 1A se observa que la mayor producción de biomasa se obtuvo con el medio suplementado MMB96 (0,0057 µg/µl, Tabla 1). No se presentaron diferencias significativas (P > 0,05) entre la cantidad de biomasa que se produce en el medio mínimo (MM) y el medio con glucosa (MMG). Se observó una relación inversa entre los medios MMG y MMB. El primero fomenta la mayor producción de conidios (61,3 x 106 en MMG216) pero no el mayor desarrollo de biomasa (Fig. 1A-B, tabla 1).
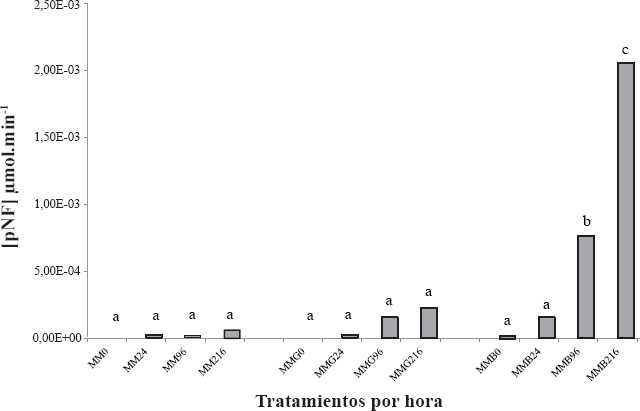
Actividad quitinasa de B. bassiana de diferentes tratamientos a distintos tiempos de evaluación. Los valores de cada media son obtenidos por triplicado. Diferencias significativas entre tratamientos tienen letras diferentes (P < 0,05).
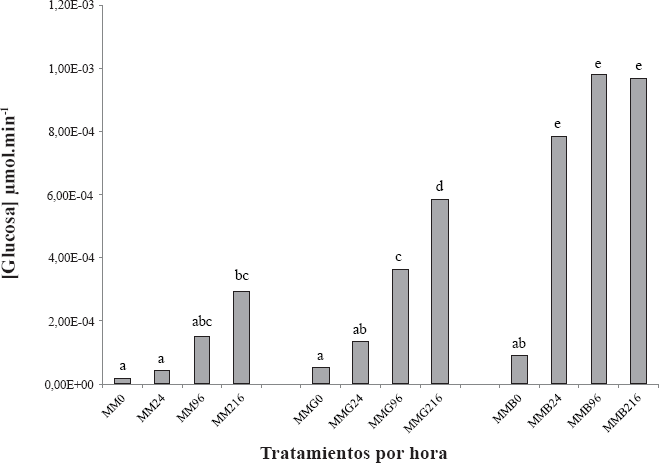
Actividad laminarinasa de B. bassiana de los diferentes tratamientos a distintos tiempos de evaluación. Los valores de cada media son obtenidos por triplicado. Diferencias significativas entre tratamientos tienen letras diferentes (P < 0,05).
La actividad de enzimas quitinasa y laminarinasa (Fig. 2 y 3, respectivamente), que se detallan en la tabla 1, determinan que la inducción de enzimas si es posible en el medio suplementado con extracto en polvo de H. hampei. Sin embargo, al analizar la actividad específica enzimática de cada enzima evaluada, se observa que laminarinasa cambia su comportamiento respecto a lo observado para los medios MM y MMG, en los cuales se incrementa con el pasar de las horas; en el medio MMB, el comportamiento revela una inducción específica desde el inicio y luego se mantiene sin diferencias significativas entre los tiempos (P = 0,372).
Biomasa [B], conidios [C], proteínas totales [PT], actividad quitinasa [Q], actividad específica laminarinasa [QE], actividad laminarinasa [L] y actividad específica laminarinasa [LE] de B. bassiana en los tratamientos MM, MMG y MMB evaluados a diferentes tiempos.
Los valores son la media de ensayos triplicados. Las medias con las mismas letras no son significativamente diferentes. Test de Duncan (α = 0,05).
Se encontró correlación positiva (Tabla 2) entre los elementos biomasa, proteínas totales, actividad enzimática y actividad específica laminarinasa. Las actividades enzimáticas específicas de quitinasa y laminarinasa no se correlacionaron junto a las otras debido a los bajos valores considerados como constantes. No obstante, se determinaron diferencias significativas entre ellas (Tabla 1).
Correlación de Pearson de las variables biomasa, conidios, proteínas totales, actividad laminarinasa y actividad quitinasa.
La correlación es significante al nivel 0,05 (bilateral).
La correlación es significativa al nivel 0,01 (bilateral).
Discusión
Al analizar la biomasa que en su mayor parte está representada por el desarrollo de masa hifal, reportamos que el medio MMB produjo la mayor cantidad de biomasa (Tabla 1; Fig. 1A). Esto sugiere que el desarrollo de hifas es estimulado por los nutrientes obtenidos del insecto desde las primeras 24 h en contacto con éste, estimulando un comportamiento patógeno, a diferencia del cultivo con glucosa el cual más bien promueve un crecimiento saprófito y acelera la curva de crecimiento lo que representa una mayor producción de conidios. Estudios sobre la biomasa generada por B. bassiana se han realizado con la finalidad de comprender los aspectos básicos del desarrollo de los hongos entomopatógenos y el conocimiento detallado de los requerimientos nutricionales para su crecimiento y esporulación, esencial para la producción masiva y comercialización (Gandarilla et al. 2013). Pedrini et al. (2007) mencionan que 24 h post infección del hospedero hay una proliferación masiva de crecimiento micelial en ambas superficies del insecto por partes de conidios crecidos sobre el medio inductor con quitina, mientras hongos crecidos en glucosa, muestran una baja densidad de crecimiento de conidios en la cutícula del insecto. Para el crecimiento hifal, representado por la cantidad de biomasa obtenida en MMB se requiere nitrógeno, N-acetilglucosamina, quitina, almidón, y ácidos grasos entre otros; que no estarían presentes en el medio de glucosa, pero que estarían suministradas por el integumento de broca (Smith y Grula 1981).
Como mencionan Pedrini et al. (2007) la germinación de los conidios de los hongos es el primer y más crucial evento en el proceso de infección. Un alto porcentaje de germinación puede ayudar a aumentar la probabilidad de infección de los conidios sobre la superficie del insecto antes de que sean removidas de la cutícula del insecto una vez que se pierda la capacidad de retención. En la Figura 1B, el medio MMB (MM + extracto en polvo de H. hampei) obtuvo una producción de conidios significativamente más alta (26,4 x 106 conidios a las 216 h) que el medio de control MM (1,1 x 106 conidios a las 216 h) en todos los tiempos de evaluación. Lo anterior se reporta por Smith y Grula (1983) en cuyos tratamientos con B. bassiana cultivado en SDA más integumento de broca del café se observó un crecimiento más rápido y una producción más abundante de conidios. Como era de esperarse el MM (medio control) sin fuente de carbono o nitrógeno, como nutriente, no desarrolló conidios, a diferencia del MMG (61,3 x 106 conidios a las 216 h) que presentó la más alta germinación de estos, el cual se explica, porque este medio posee la fuente de azúcares disponible y de fácil asimilación para promover su crecimiento acelerado.
Aunque las proteínas totales no han sido identificadas como un parámetro importante para el estudio de la patogenicidad de B. bassiana, deben ser tomadas en cuenta para el cálculo de la actividad específica de las enzimas (Peteira et al. 2011). Los más altos niveles de síntesis de proteínas totales de B. bassiana se expresaron en el medio MMB (suplementado con integumento de broca), detectándose un incremento de más de 500% (Tabla 1) a las 96 h en comparación con MM (medio control). Este resultado aventaja al ensayo de Peteira et al. (2011) quienes determinaron mayores valores al quinto día sobre un medio suplementado con quitina como sustrato sintético de integumento de insecto. Este incremento se encontraría condicionado a la composición del extracto en polvo de H. hampei el cual aporta los nutrientes al medio debido a su composición: proteínas, quitina y lípidos (St. Leger 1995). La cantidad y composición de las proteínas segregadas en el medio involucra la presencia de componentes proteicos estructurales de la pared del insecto generados por acción de las enzimas secretadas por B. bassiana. Así mismo, St. Leger (1995), afirma que el rango de actividades de proteinasas secretadas por varias especies de entomopatógenos pone en relieve la importancia de estas enzimas (quitinasa y laminarinasa) para el crecimiento y la supervivencia de estos organismos.
Se conoce que durante la germinación del conidio, el área de la procutícula alrededor de la penetración, aparecen síntomas de histólisis producida por enzimas. Estudios con Metarhizium anisopliae (Metchnikoff) Sorokin (1883) (Hypocreales: Clavicipitaceae) demostraron claramente que una proteasa es el factor clave en la penetración de la cutícula del insecto por el hongo (St. Leger 1995). La cutícula está formada en un 70 % aproximadamente de proteínas, lo que explica que las proteasas sean más importantes que las quitinasas. Sin embargo, la quitina es un componente de la cutícula y la primera barrera contra los patógenos (Fan et al. 2007). De tal forma, en el micoparasitismo no sólo participan las quitinasas y las β-1,3-glucanasas, sino también las β-1,6-glucanasas, α-1,3-glucanasas y proteasas.
La evaluación de laminarinasa en medio suplementado con broca es apoyada por Noronha y Ulhoa (2000) quienes reportan el desarrollo de β-1,3-glucanasas de Trichoderma harzianum Rifai, 1969 (Hypocreales: Hypocreaceae) en presencia de quitina como fuente de carbono. Una de estas enzimas se purificó y se caracterizó como una endo-β-1,3-glucanasa con una masa molecular de 36 kDa. Las enzimas gluconolíticas están ampliamente distribuidas entre las plantas superiores, bacterias y hongos y tienen varias funciones fisiológicas en dependencia de su procedencia. Las β-glucanasas fúngicas son enzimas que degradan β-glucanos y se clasifican en dos grandes grupos según los mecanismos que utilizan para hidrolizar el sustrato, identificados por los productos de hidrólisis: (i) las exo-β-glucanasas, las cuales hidrolizan el sustrato por ruptura secuencial de residuos de glucosa desde el extremo no reductor, y (ii) las endo- β-glucanasas, que rompen aleatoriamente los sitios de enlace β de la cadena polisacarídica, liberando pequeños oligosacáridos. La degradación de los β-glucanos por los hongos se acompaña frecuentemente de la acción sinérgica de la endo y exo-β-glucanasa (Pitson et al. 1993).
Nuestro ensayo confirma de manera significativa que un medio suplementado con extracto en polvo de H. hampei, consigue activar la producción de enzimas quitinoliticas por su mayor presencia como componente principal de la pared de los insectos, además de otras asociadas a la patogenicidad (Zhang et al. 2008). Lubeck (2004) menciona que el aumento del nivel de enzimas β-1,3-glucanasas en cultivos con ninguna o poca fuente de carbono se debe al papel que desempeñan en los procesos autolíticos, cuando a falta de nutrientes parece inducir la secreción de estas enzimas glucanasas para la movilización de β-glucanos presentes en la pared celular realizando la autolisis, lo cual sería importante para la sobrevivencia del hongo a medida que regiones de cultivo continúan creciendo en respuesta al reciclaje de los productos de la degradación. En nuestro trabajo en el medio suplementado con glucosa (MMG) se detectaron actividades laminarinasa 8,29; 1,47 y 1,66 mU/mg de proteína a las 24 h, 96 h y 216 h respectivamente, observándose que los resultados son más altos a las 24 h; frente a esto, Severgnini (2006) menciona que la acumulación de glucosa en el sobrenadante como resultante de la degradación de quitina y laminarina puede ser un auto limitante hacia la actividad enzimática, lo que puede explicarse debido a que, al tener en presencia un monosacárido fácilmente metabolizable como la glucosa, éste puede ser absorbido directamente por el hongo para nutrirse sin necesidad de segregar enzimas que digieran el polímero de β-glucanos (laminarina) y posteriormente esta actividad se puede dar mientras se extingue el nutriente del medio de cultivo (Lubeck 2004).
Los valores de la actividad enzimática quitinas y laminarinasa resultaron mayores en MMB de manera altamente significativa (Tabla 1) lo cual confirma la inducción de producción enzimática utilizando integumento de broca. Este resultado fue inicialmente demostrado por Smith y Grula (1983) quienes logran la inducción de quitinasa con sustratos sintéticos que sustituyen al integumento como quitina o quitobiosa. Sin embargo, los valores no son comparables debido a las condiciones de cultivo y el volumen de muestra evaluado.
Los sustratos enzimáticos de quitina y laminarina son comúnmente usados para el establecimiento de micoparasitismo simulado (Severgnini 2006). Existen estudios sobre el modo de acción de los agentes de control biológico en los cuales el medio de cultivo es suplementado con macerados provenientes del organismo que el controlador infecta. El integumento de los insectos (constituido por quitina como parte de su cutícula) ha sido empleado como fuente de nutrición para hongos especializados. Los valores de actividad quitinasa que determinamos en nuestros ensayos son comparables a los obtenidos por González et al. (2011) en Serratia Bizio, 1823 (Enterobacteriales: Enterobacteriaceae) y Svedese et al. (2013), quienes hallaron que la mayor producción de quitinasa se obtuvo a las 96 h del cultivo para todas las cepas probadas. Los niveles de enzimas específicas que degradan la cutícula, tales como proteasas, correlacionaron positivamente con los parámetros específicos de virulencia.
Existen ensayos que utilizan sustratos sintéticos para simular parasitismo; los resultados hallados en el género Trichoderma por González et al. (2012) y Ting y Chai (2014) difieren de nuestros resultados debido a que estos ensayos obtuvieron como sustrato inductor quitina 0,5 % para inducir la producción de una mayor cantidad de quitinasas.
Para el caso de enzimas quitinasas, Dhar y Kaur (2010) señalan que la presencia de fuentes de carbono fácilmente disponibles como la dextrosa, son las que al inicio pueden suprimir la producción de esta enzima, sin embargo en la última fase del crecimiento habría una mejora de la producción cuando la dextrosa ha sido utilizada total o parcialmente. Estas aseveraciones pueden ser demostradas si observamos que en nuestro estudio, en el medio de glucosa, la lectura más alta de actividad laminarinasa se da a las 24 horas, disminuyendo gradualmente por el consumo del hongo (Fig. 3A).
Gupta et al. (1994) encontraron una correlación positiva entre la producción de altos niveles de quitinasas y/o proteasas con la virulencia de B. bassiana contra Galleria mellonela L., 1756 (Lepidoptera: Pyralidae) y Trichoplusiani Hübner, 1803 (Lepidoptera: Noctuidae). Además, Fan et al. (2007) demostraron que una sobreexpresión de un gen de quitinasa (Bbchit1) mejoró la virulencia de B. bassiana para áfidos [Myzus persicae Sulzer, 1776 (Homoptera: Aphididae)], en comparación con una cepa de tipo salvaje. Sólo unos pocos documentos se han centrado en la producción de estas enzimas por cepas de B. bassiana sobre la presencia de la cutícula del hospedero, así tenemos a Campos et al. (2005) quienes detectaron la presencia de quitinasas y proteasas en la cutícula de Rhipicephalus microplus Canestrini; 1888 (Ixodida: Ixodidae) y Montesinos et al. (2011) que evaluaron la producción de quitinasas después de crecer el hongo en presencia de Tenebrio molitor L., 1758 (Coleoptera: Tenebrionidae). Estos trabajos sugieren que las enzimas de B. bassiana se expresan de forma diferente según el tipo de cutícula del insecto y que los niveles específicos de enzimas que la degradan, como proteasas, correlacionan positivamente con los parámetros específicos de virulencia. Este hecho contribuye a la comprensión de la relación parásito-hospedero y a la importancia en la selección de cepas de B. bassiana para el control biológico de insectos.
No se han detallado estudios sobre la correlación entre la cantidad de conidios o biomasa, de B. bassiana, producidas por medios inductores, y las actividades enzimáticas implicadas en su patogenicidad. Según la Tabla 2, se determinó la correlación altamente positiva con las actividades quitinasa (P < 0,01) y laminarinasa (P < 0,01) por lo cual, se podría estimar que a mayor producción de biomasa por parte del hongo entomopatógeno, la producción de enzimas asociadas a la infección e invasión del insecto, como las ya mencionadas e incluso otras aún no estudiadas, será mayor. No se determinó correlación entre los valores de número de conidios y proteínas totales exudadas. Probablemente, este resultado negativo se debe a que cuando existe mayor cantidad de conidios no hay síntesis de enzimas a gran escala sino hasta después de la fase germinativa; caso contrario sucede en los medios con menor cantidad de conidios puede representar la mayor presencia de hifas recién formadas e inicio de mayor actividad enzimática y actividad metabólica que la síntesis a proliferación de proteínas.
Conclusiones
Los resultados revelan la inducción positiva de quitinasa y de manera similar de laminarinasa en un medio suplementado con integumento de H. hampei. El comportamiento observado bajo condiciones in vitro simula las condiciones naturales y la activación del mecanismo de respuesta del agente entomopatógeno es expresado. La correlación positiva entre las actividades enzimáticas quitinasa, laminarinasa, la biomasa y la cantidad de proteínas totales, así como los días de mayor expresión constituyen factores fundamentales a seguir estudiando puesto que esto contribuye al conocimiento de elementos relacionados a la patogenicidad de B. bassiana y su control sobre H. hampei.
Footnotes
Agradecimientos
El presente proyecto Convenio N°189-FINCyT-IB-2013 se financió por el Programa Nacional de Innovación para la Competitividad y Productividad (PNICP), conjuntamente con el laboratorio de Bioquímica y Biología Molecular de la Universidad Nacional Federico Villarreal. El Agustino, Lima, Perú.
