Abstract
Carbonic anhydrase (CA) catalyzes the reversible conversion of CO2 to bicarbonate and participates in mechanisms of alkalinization in the intestine of mosquitoes. The toxicity of four CA inhibitors (CAI): acetazolamide (AZM), methazolamide (MZM), ethoxzolamide (ETX) and dorzolamide (DZA) were evaluated in larvae of Anopheles albimanus by monitoring mortality 24, 48 and 72 hours post application, at a concentration of 50 ug/ml diluted in dimethyl sulfoxide previously. All IAC reduced the population of larvae in variable proportions. ETX showed the highest toxicity, achieving more than 80% mortality after 24 hours and 98% after 72 hours of application. The CAI, AZM, MZM and DZA showed less toxicity (<50% mortality). Our results indicate that the CAI, including ETX in particular, is a worthy candidate as an alternative for the control of An. albimanus, which is considered a primary vector of malaria in Colombia.
Introducción
Anopheles (Nyssorhynchus) albimanus (Wiedemann, 1820) (Diptera: Culicidae) es uno de los vectores principales de Plasmodium de humanos en Centro y Sur América (Zimmerman 1992; Sinka et al. 2010; Montoya-Lerma et al. 2011). En Colombia, An. albimanus es considerado vector primario de malaria en áreas rurales y periurbanas de la Costa Pacífica y probablemente en la Costa Caribe (Gutiérrez et al. 2008). En el control de la malaria se presentan algunas limitaciones que incluyen el desconocimiento de actividades adecuadas para la protección y prevención de la transmisión; resistencia de algunas poblaciones de Plasmodium a los medicamentos de uso actual para el tratamiento de la malaria; errores en la aplicación de insecticidas o aun, resistencia de los vectores a los insecticidas; polución del medio ambiente y efectos adversos de los insecticidas en humanos y otros organismos (Georghiou y Taylor 1977, Olano et al. 1997; Hemingway y Ranson 2000; Carmona-Fonseca 2003, 2004; Nauen, 2007). Por esta razón, es fundamental la vigilancia de la resistencia a los insecticidas en uso (Fonseca-González et al. 2010) y la susceptibilidad de los estadios inmaduros a los insecticidas.
El control de inmaduros es una estrategia más factible que el de los adultos, dado que limita la capacidad de dispersión de los mosquitos (Blanco et al. 2002). El control de formas inmaduras de anofelinos, requiere el conocimiento de las condiciones de calidad de agua que puede ocupar una especie (Sinka et al. 2010). Además, se debe conocer aspectos biológicos básicos que permitan el descubrimiento de blancos necesarios para el desarrollo de nuevos y mejores larvicidas. Un aspecto fundamental en larvas de mosquitos es la alcalinización, la cual es indispensable para la supervivencia (Corena et al. 2004). Las enzimas relacionadas con este proceso pertenecen a la familia de las anhidrasas carbónicas (AC), las cuales catalizan la conversión reversible del CO2 a bicarbonato (Corena et al. 2002; Smith et al. 2007). La AC es inactivada por dos clases de compuestos: aniones complejos de metales y sulfonamidas no sustituidas, las cuales se unen al ión de zinc de las AC. Algunos de estos compuestos, como la acetazolamida (AZM) y metazolamida (MZM), en larvas de mosquitos como Aedes aegypti, Ae. albopictus, Culex quinquefasciatus, Cx. nigripalpus, Ochlerotatus taeniorhynchus, An. quadrimaculatus, ocasionan un efecto letal variable de acuerdo con la especie (Corena et al. 2004). Sin embargo, hasta el momento se desconoce el efecto de estos compuestos en larvas de An. albimanus. El objetivo de este trabajo fue evaluar el efecto letal de cuatro IAC en larvas de esta especie, bajo condiciones de laboratorio.
Materiales y métodos
Resultados
El tratamiento de larvas An. albimanus con los IAC produjo una toxicidad variable siendo ETX el que mostró mayor toxicidad y mortalidad. Ésta fue mayor al 80% después de 24 horas de aplicación y después de 48 y 72 horas alcanzó su valor máximo de 98% (Fig. 1). Este porcentaje fue significantemente diferente (P < 0,0001), con respecto a los otros IAC y el control sin tratamiento. En contraste, las mortalidades con AZM, MZM y DZA fueron menores al 60%. El control con DMSO no arrojó diferencias estadísticamente significativas con respecto al control. El control positivo registró una mortalidad de 100% en larvas 24 horas después de la aplicación (datos no mostrados).
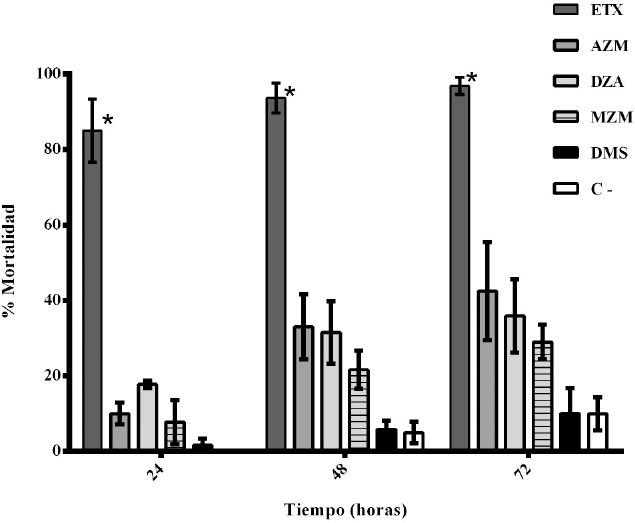
Mortalidad en larvas An. albimanus expuestas a los IAC en tres tiempos de evaluación (24, 48 y 72 postaplicación). Concentración 50 µg/ml. Valores promedio de tres ensayos experimentales incluyendo 420 larvas en cada uno. ETX= Etoxzolamida, AZM = Acetazolamida, DZA = Dorzolamida, MZM = Metazolamida, DMS = Dimetil sulfóxido, C- = Control sin compuestos, n=1260. * P < 0,0001.
Discusión
El efecto de mortalidad de algunos IAC sobre estadios inmaduros de insectos ha sido estudiado en pocas especies como Ae. aegypti, An. quadrimaculatus, Cx. quinquefasciatus, Cx. nigripalpus, Oc. taeniorhynchus y Ae. albopictus (Corena et al. 2004). Nuestros hallazgos indican que la MZM produjo el menor efecto tóxico (< 40% mortalidad), contrario a lo encontrado por Corena et al. (2004), donde MZM causó una mortalidad del 80% en larvas del mismo género a una concentración similar a la utilizada en el presente estudio (10−4 M). La mortalidad en larvas se atribuye al desequilibrio en el pH del intestino medio y la inhibición de los procesos de transporte de iones (Corena et al. 2004). Las diferencias en el porcentaje de mortalidad para cada especie, pueden obedecer a un mecanismo de respuesta específico o la presencia de una familia particular de AC (Corena et al. 2004). Una de las formas de comprender mejor el efecto de los IAC, es el análisis de los productos de excreción liberados en el agua. Si bien este aspecto no se incluyó en este trabajo, sería interesante considerarlo para estudios futuros dado que se pueden esperar variaciones de acuerdo no solo con la especie sino con el estadio evaluado (Corena et al. 2004). El efecto tóxico de ETX (mortalidad cercana al 100%) después de 24 horas, es un resultado importante, comparable al efecto larvicida logrado por compuestos como el temefos®, utilizado en el control de Ae. aegypti y An. nueztovari en condiciones laboratorio y campo (González y Palacio Mosquera, 2009; Maestre et al. 2009). La inclusión del temefos sirvió exclusivamente como un control positivo y no con el propósito de establecer comparaciones con los IAC. ETX posee propiedades inhibitorias sobre el dominio soluble de la alfa-AC1 que se encuentra en Ae. aegypti, mostrando afinidad a nivel nanonolar (Fisher et al. 2006). Es muy probable que un dominio homólogo exista en An. albimanus y, por tanto, el efecto de ETX en larvas se observe en mayor medida. Además, de acuerdo con las propiedades físicas de la ETX, se indica que es un compuesto prácticamente insoluble en el agua, hecho que favorece su permanencia en la superficie del agua, lugar donde se alimentan y permanecen la mayor parte del tiempo las larvas del género Anopheles logrando de esta forma una mayor mortalidad.
Por otro lado, la ETX en los insectos produce un desequilibrio en el pH del intestino y además causa la inhibición de procesos de transporte de iones (Corena et al. 2004). Las propiedades letales de la ETX sobre la fisiología de las larvas propende su uso en el control, no sin antes considerar su efecto en organismos no blanco.
Según nuestros resultados la ETX es un compuesto importante que puede ser utilizado como una estrategia complementaria con las medidas de control. El alto porcentaje de mortalidad observado en larvas expuestas a ETX, señala que podría considerarse como un compuesto promisorio en la búsqueda de nuevos blancos larvicidas para An. albimanus.
Agradecimientos
A Evencio Mosquera por su valiosa ayuda en la cría del material biológico empleado en este estudio, a María Fernanda Flórez, María Alejandra Duque, Catalina Marín y Esteban Marín por su colaboración en la ejecución de los bioensayos. Este trabajo fue financiado por Colciencias y la Universidad de Antioquia.
