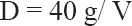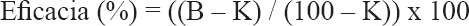Abstract
One of the principal problems of potato cultivation in Colombia is the Guatemalan moth Tecia solanivora, which causes damage in the field and during tuber storage. For its biological control under storage conditions, products have been developed based on the granulovirus denominated "Baculovirus Corpoica", the only one registered in Colombia. However, with the isolation of a native granulovirus known as VG003, two biopesticide prototypes were formulated as a dispersible granular (WG) and as an emulsifiable concentrate (EC), designed for control of the insect under field conditions. Considering that the stability of biopesticide under storage is a determining parameter for their registration and commercialization, the objective of the present study was to evaluate the physicochemical, microbiological and biological stability of the products over six months of storage at 6°C, 20°C and 28°C. Insecticidal activity of both formulations remained stable at 6°C and 20°C, with efficacies that ranged between 60% and 70%. Contaminant content increased during storage but was maintained within the established acceptance limits. However, physicochemical characteristics were affected by elapsed time and high temperature, which is why storage at 20°C is recommended, and which would also reduce costs during commercialization since it would eliminate the necessity for refrigeration during transport and commercialization.
Introducción
Uno de los mayores problemas sanitarios que presenta el cultivo de papa es el ataque del tubérculo por parte de la polilla guatemalteca de la papa Tecia solanivora (Povolny, 1973) (Lepidoptera; Gelechiidae); insecto oriundo de América Central que se reportó por primera vez en Colombia (Norte de Santander) en el año 1985 (Herrera 1998) que se ha adaptado a diferentes condiciones agroecológicas, favoreciendo su diseminación por todo el país y causando grandes pérdidas económicas (Araque y García 1999). Con el fin de controlar este insecto plaga, a nivel mundial se han usado de forma indiscriminada una gran cantidad de plaguicidas químicos que a menudo presentan altos niveles de toxicidad y en muchos casos son aplicados sin el uso de protección. El resultado es un alarmante nivel de intoxicación en las comunidades campesinas y la contaminación ambiental (FAO 2008).
Como alternativa "ambientalmente amigable" para el control de este insecto plaga, se encuentra la aplicación de agentes como los granulovirus. Este virus de la familia Baculoviridae ha sido hallado en forma natural afectando larvas de las polillas Phthorimaea operculella (Zeller, 1873) (Lepidoptera: Gelechiidae) y T. solanivora en varios países de América y África (Zeddam et al. 1999). Todos los granulovirus sintetizan al final del proceso infeccioso grandes cantidades de granulina, proteína que cristaliza formando una matriz o cuerpo de inclusión (CI) con forma de gránulo. Durante su morfogénesis, queda incluido un virión dentro del CI, lo que les permite preservar su capacidad infecciosa. Los CIs son insolubles en agua y resistentes a la putrefacción y desintegración por agentes químicos y también a tratamientos físicos como la congelación, la desecación o la liofilización, características que les confieren persistencia en el ambiente (Caballero et al. 2001).
La producción de estos virus se realiza normalmente en su hospedero, lo que genera contaminación microbiana en la suspensión viral, proveniente de la microflora normal de los cadáveres de los insectos (Lasa et al. 2008). Esta contaminación puede afectar la estabilidad fisicoquímica y las propiedades insecticidas del producto, e incluso representar riesgos para la salud si se presentan patógenos humanos dentro del formulado (Grzywacz et al. 1997).
Dos productos de origen latinoamericano han sido registrados para el control de esta plaga en papa almacenada; uno de ellos desarrollado por el Centro Internacional de la Papa (CIP) en Perú, formulado como un polvo para espolvoreo cuyo ingrediente activo es un granulovirus aislado de P. operculella llamado "Baculovirus de la polilla de la papa" (Alcázar y Raman 1992) y el producto colombiano denominado "Baculovirus Corpoica", formulado también como un polvo para espolvoreo (Chaparro et al. 2010). Recientemente se desarrollaron dos prototipos de bioplaguicida a base de un granulovirus colombiano aislado de larvas de T. solanivora y codificado como VG003, que según el trabajo de Barrera et al. (2009) corresponde a un granulovirus de P. operculella (PhopGV). Estos productos se diseñaron para el control de la polilla en campo y fueron formulados como un granulado dispersable (WG) y un concentrado emulsionable (EC), los cuales incluyen en su formulación un filtro ultravioleta del grupo de los abrillantadores ópticos y deben ser reconstituidos en agua para su posterior aplicación por aspersión dirigida al suelo (Chaparro et al. 2010).
Teniendo en cuenta que las características fisicoquímicas, microbiológicas y la actividad insecticida de los formulados pueden afectarse negativamente durante el almacenamiento y que la estabilidad de los productos puede verse influenciada por la temperatura y el tipo de formulación; el objetivo del presente trabajo fue realizar un estudio de estabilidad acelerada para determinar características susceptibles de optimización en los dos productos que permitan avanzar en el desarrollo de los prototipos y seleccionar las condiciones óptimas de almacenamiento para los mismos.
Materiales y Métodos
El estudio contó con un diseño experimental completamente al azar, con medidas repetidas en el tiempo y todas las mediciones se realizaron por triplicado. Los resultados del estudio de estabilidad de las características fisicoquímicas, microbiológicas y biológicas se sometieron a un análisis de varianza y posteriormente a comparaciones de medias mediante la prueba de Tukey (95%). En el caso de la estabilidad de la densidad apisonada, los resultados se analizaron mediante una prueba no paramétrica de Kruskal-Wallis ya que los datos no cumplieron con los principios de normalidad y homogeneidad de varianzas.
Donde K es el porcentaje de mortalidad del testigo y B es el porcentaje de mortalidad en el tratamiento.
Resultados y Discusión
El WG almacenado a 28°C redujo significativamente su pH desde los dos meses de almacenamiento, es decir que a mayor temperatura, el cambio químico se evidenció más rápido. Sin embargo, el pH del producto durante todo el almacenamiento a las tres temperaturas se mantuvo entre 5 y 8, rango adecuado para el granulovirus utilizado como ingrediente activo. De esta forma se asegura la estabilidad física de los cuerpos de inclusión, ya que se ha establecido que solo valores de pH mayores a 9 y menores a 4 afectan la integridad de los baculovirus (Caballero et al. 2001).
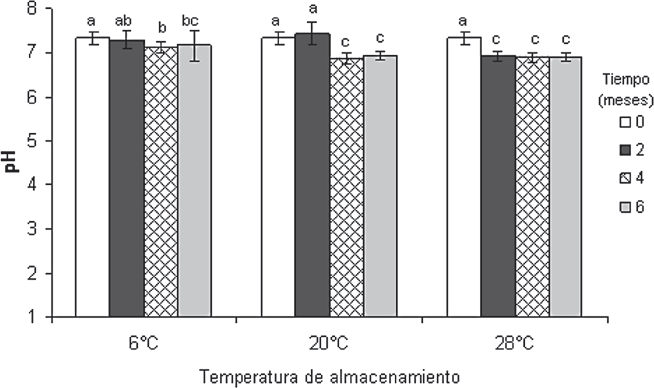
Estabilidad del pH del WG durante seis meses de almacenamiento a tres temperaturas. Tratamientos con la misma letra no presentan diferencias según la prueba de Tukey con un 95% de confianza.
Cuando el almacenamiento se realizó a 28°C, no hubo diferencias significativas entre el porcentaje de humedad del producto antes de ser almacenado y el valor obtenido a los dos y cuatro meses de almacenamiento, pero la humedad obtenida a los seis meses fue significativamente inferior a la inicial. Estos resultados podrían sugerir que el sello al calor usado en los empaques no fue totalmente hermético y permitió la entrada de humedad a las dos temperaturas más bajas y posiblemente la salida de ésta cuando se utilizó la temperatura más alta.
Cuando el almacenamiento se realizó a 6°C y 20°C, la humedad de los prototipos sobrepasó el valor máximo del 5% recomendado para este tipo de productos (Lawrie et al. 2001; Santos et al. 2008), considerando que humedades altas podrían dar lugar a la compactación de los gránulos, con la consecuente aparición de grumos y aglomerados de difícil dispersión, además de facilitar el crecimiento de microorganismos contaminantes (Salazar 2003). El crecimiento de organismos contaminantes puede afectar la estabilidad del virus, ya que estos pueden degradar los compuestos orgánicos presentes en la cubierta viral y generar radicales libres que podrían afectar la integridad del ingrediente activo (Burges 1998).
Los resultados sugieren la necesidad de revisar el sellado utilizado para los empaques, o de buscar otro sistema que garantice la hermeticidad y de esta forma, la calidad del producto terminado y su estabilidad durante el almacenamiento.
Estabilidad del tiempo de mojabilidad (segundos) del granulado almacenado durante seis meses a tres temperaturas.
Tratamientos con la misma letra no presentan diferencias según la prueba de Tukey con un 95% de confianza.
El porcentaje de estabilidad presentado por el producto recién manufacturado (78,88%) y después del almacenamiento fue superior al límite mínimo recomendado correspondiente al 60% (SENASA 2002; Chemical Regulation Directorate 2009). La alta suspensibilidad del producto posiblemente se debe a que el granulado desintegra completamente al entrar en contacto con el agua y no hay agregación de las partículas en suspensión (Allen et al. 2005), ya que según la ley de Stokes, a mayor tamaño de partícula o mayor diferencia de densidad entre la partícula y el medio dispersante, mayor será la velocidad de sedimentación (Aulton 2004).
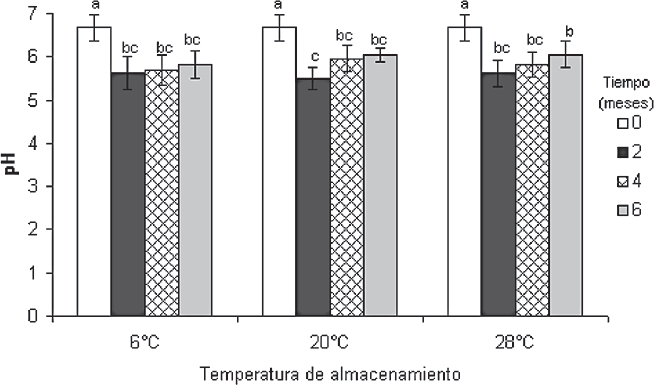
Estabilidad del pH del EC, durante seis meses de almacenamiento a tres temperaturas. Tratamientos con la misma letra no presentan diferencias según la prueba de Tukey con un 95% de confianza.
La prueba cualitativa también mostró que la emulsión obtenida al reconstituir el EC fue estable, ya que no se presentaron separación de fases, ni formación de flóculos en los ensayos realizados al prototipo almacenado a 6°C, 20°C y 28°C durante seis meses. Lo anterior indica que la temperatura y el tiempo de almacenamiento no afectaron la diferencia de densidad entre las fases (Cubero et al. 2002) y que la estructura química del surfactante que compone la formulación fue estable durante el tiempo, ya que facilitó la extensión de la interfase y estabilizó la emulsión retardando la coalescencia de las gotas de la fase dispersa (Graciani 2006).
El producto reconstituido presentó un cremado de 6 mL fácilmente dispersable, fenómeno de inestabilidad que normalmente es reversible con una pequeña agitación y que se presenta con más frecuencia en emulsiones agua en aceite (O/W) (Nehal et al. 1999). A pesar de esto, el cremado debe evitarse ya que puede originar errores en la dosificación, mal aspecto y mayor proximidad de los glóbulos, lo que puede conducir a una agregación o coalescencia de la emulsión (Allen et al. 2005).
Comportamiento de la estabilidad de la emulsión formada al reconstituir el EC almacenado durante seis meses a tres temperaturas, expresada como porcentaje.
Tratamientos con la misma letra no presentan diferencias según la prueba de Tukey con un 95% de confianza.
El WG recién manufacturado presentó un contenido de contaminantes 17 veces mayor que el del EC (Tabla 3). Esto podría deberse a diferencias en la carga microbiana de los auxiliares de formulación empleados en la elaboración de los dos productos, ya que éstos no fueron esterilizados antes de la manufactura. Cabe destacar que el contenido de contaminantes inicial en los dos formulados es bajo (3,00x103 UFC/g para el WG y 1,77x102 UFC/mL para el EC) en comparación con los descritos en la literatura para productos virales como la formulación del nucleopoliedrovirus de Spodoptera exigua (Hübner, 1808) evaluada por Lasa et al. (2008), que mostró un contenido de microorganismos aerobios de 1,4 x107 UFC/mL y el producto comercializado en Estados Unidos con el nombre comercial Elcar, cuyo ingrediente activo es el nucleopoliedrovirus de Helicoverpa zea (Boddie, 1850) que presenta un contenido de contaminantes de 107 UFC/g (Shied 1989).
Comportamiento del contenido de contaminantes del WG y del EC (UFC/g) almacenados durante seis meses a tres temperaturas.
Tratamientos con la misma letra no presentan diferencias según la prueba de Tukey con un 95% de confianza.
No se detectaron diferencias significativas entre el contenido de contaminantes del producto recién manufacturado y el de éste durante los seis meses de almacenamiento a 6°C (F=2,56, df=3, P=0,071), lo que indica que no hubo crecimiento microbiano a temperatura de refrigeración. El uso de temperaturas bajas es un mecanismo utilizado para estabilizar las células, debido a que disminuye su metabolismo y en consecuencia la velocidad de crecimiento de los microorganismos (Rodríguez 1998). Sin embargo, se pudo observar un aumento al sexto mes de almacenamiento que pudo haberse favorecido por un incremento de la humedad del WG.
Cuando la temperatura de almacenamiento fue de 20°C y 28°C, se observó un aumento significativo (F=9,66, df=11, P<0,005) en la concentración de contaminantes del WG a partir del cuarto y el segundo mes respectivamente, que en el producto almacenado a 20°C pudo verse favorecido por el incremento de la humedad del producto. Sin embargo, el incremento de la contaminación fue mayor cuando el bioplaguicida se almacenó a 28°C, posiblemente debido a que dicha temperatura es adecuada para el crecimiento de diversas bacterias contaminantes (Burges 1998).
El aumento de la población microbiana contaminante podría relacionarse con las propiedades higroscópicas de los productos liofilizados (Voigt y Bornshein 1982), ya que el WG fue sometido a dicho proceso de deshidratación; lo que sumado a un sello no hermético posiblemente favoreció un incremento de la humedad y en consecuencia el crecimiento microbiano. Este tipo de contaminación es muy frecuente ya que los sistemas actuales de producción viral se realizan in vivo, lo que genera una carga importante de bacterias y hongos que naturalmente colonizan las dietas, la superficie del insecto, su intestino y sus heces. La gran mayoría de estos microorganismos son especies comunes de los géneros Pseudomonas, Enterococcus y especies coliformes de la familia Enterobacteriaceae (Jenkins y Grzywacz 2000).
Para el EC, la temperatura y tiempo de almacenamiento no afectaron el contenido de contaminantes a 6°C. Sin embargo, el análisis estadístico detectó diferencias significativas entre la cantidad de contaminantes presentada por el EC almacenado a 20°C y 28°C después de seis meses de almacenamiento, con respecto al contenido de contaminantes presentado por el producto recién manufacturado (F=35,9, df=11, P<0,005).
Dicho comportamiento sugiere que estas temperaturas favorecieron el crecimiento microbiano, posiblemente debido a que algunos componentes de la formulación oleosa podrían ser utilizados como sustrato por los microorganismos (Aulton 2004), especialmente por bacterias de la familia Enterobacteriaceae. Dentro de éstas se destaca Enterobacter gergoviae (Brenner et al. 1980) aislado por Kuzina et al. (2002) en el intestino de Pectinophora gossipiella (Saunders, 1844) (Lepidoptera; Gelechiidae), que también fue encontrada por Pinto et al. (2007) en el tracto digestivo de dos lepidópteros de la familia Saturniidae, Rothschildia lebeau (Rothscild, 1907) y Automeris zugana (Druce, 1886) y además demostraron su actividad lipolítica.
Durante todo el tiempo de almacenamiento a las tres temperaturas los dos prototipos de bioplaguicida (WG y EC) presentaron una concentración de microorganismos contaminantes que estuvo por debajo del límite máximo de calidad establecido previamente en el Laboratorio de Control de Calidad biotécnica de Corpoica, que exige que la concentración de contaminantes sea inferior a 1x106 UFC/g o mL.

Larvas de Tecia solanivora el ejemplar de la izquierda muestra su condición sana mientras que los demás dejan ver la sintomatología típica de la infección con granulovirus PhoGV.
Estos resultados pueden atribuirse a la alta estabilidad que presentan los baculovirus a diferentes temperaturas, ya que existen estudios que demuestran su tolerancia a condiciones de congelamiento por varios años y a temperaturas de hasta 50°C por varias horas (Ignoffo y García 1992), aunque Támez et al. (2006) observaron una reducción significativa de la eficacia de cuatro granulados a base del NPV de Anagrapha falcifera (Kirby, 1837), almacenados a 25°C durante ocho meses. Este comportamiento se atribuyó a un incremento en la concentración de contaminantes, debido a un aumento de la humedad desde el tercer mes de almacenamiento, los cuales pudieron degradar la cubierta viral.
La estabilidad del granulovirus formulado como un WG sugiere que los excipientes utilizados en la formulación fueron adecuados y mantuvieron la integridad viral durante el almacenamiento, criterio de gran importancia cuando se seleccionan los auxiliares de formulación (Támez et al. 2002). Sin embargo, es necesario mejorar el sistema de sellado y tomar medidas para reducir la concentración de contaminantes desde el inicio de la producción, ya que la presencia de microorganismos saprófagos, puede afectar severamente la viabilidad del virus a largo plazo (Gipson y Scott 1975). Lo anterior facilitará el almacenamiento del producto a temperatura ambiente y por lo tanto ahorrará costos de producción y transporte, evitando un costo adicional por el uso de una cadena de frío.
En cuanto al EC no se detectaron diferencias significativas entre la eficacia del producto recién manufacturado y la presentada después de seis meses de almacenamiento a 6°C y 20°C (Tabla 4), mientras que a 28°C se presentó una reducción significativa del 20% (F=5,77, df=5, P=0,006). Este comportamiento podría estar relacionado con el aumento en la concentración de contaminantes que se evidenció desde el segundo mes del estudio en el EC almacenado a 28°C. Estos contaminantes pudieron afectar la estabilidad del virus por efectos de proteólisis de los cuerpos de inclusión o inactivación por la producción de radicales libres (Jones y Burges 1997). Adicionalmente, esta menor actividad insecticida del EC almacenado a 28°C podría también deberse a la formación de torta o "caking" (sedimento compacto de difícil dispersión) que se produjo en dicho tratamiento. Este sedimento posiblemente atrapó y aglomeró algunas partículas virales impidiendo su homogénea distribución en el momento de la reconstitución y en consecuencia afectando la dosis aplicada.
Batista et al. (2001) obtuvieron resultados similares quienes observaron una reducción de la eficacia del 18,3% para un concentrado emulsionable a base del nucleopolihedrovirus de Anticarsia gemmatalis Hübner, 1818 (AgMNPV) después de 20 meses de almacenamiento a 24,5°C. En un trabajo similar, se estudió la estabilidad del baculovirus de Spodoptera littoralis (Boisduval, 1833), almacenado en diferentes aceites minerales y vegetales y a bajas temperaturas no se observaron diferencias en la eficacia en los dos grupos de aceites, pero si se presentó una pérdida de la infectividad del virus almacenado durante 15 meses a 26°C en aceite vegetal, lo que atribuyeron al deterioro de los componentes de la formulación por interacciones con el oxígeno (Cherry 1994).
Para el virus liofilizado sin formular no se detectaron diferencias significativas entre los valores de eficacia obtenidos antes y después de seis meses a las tres temperaturas evaluadas (F=1,77, df=5, p=0,1943) (Tabla 4).
Para muchos autores, los baculovirus son considerados los mejores agentes biológicos para desarrollar bioplaguicidas, ya que pueden ser almacenados en preparaciones secas en oscuridad a temperaturas ambientales de 20°C y 25°C durante varios años. Un ejemplo, es el producto comercial llamado TM Biocontrol-1, el cual tiene una vida de almacenamiento de cinco años a temperaturas ambientales (Martignoni 1978). La estabilidad de la actividad insecticida del WG y el virus sin formular podría atribuirse a la estabilidad innata de los baculovirus en un amplio rango de temperaturas, hecho que fue comprobado por Pokharkar y Kurhade (1999), quienes observaron que temperaturas entre 20°C y 35°C no tuvieron un efecto significativo en la infectividad del granulovirus de P. operculella.
Eficacia biológica (%) del WG, del EC y del virus liofilizado durante seis meses de almacenamiento a tres temperaturas.
Tratamientos con la misma letra no presentan diferencias según la prueba de Tukey (95%).
Footnotes
Agradecimientos
Los autores manifiestan sus agradecimientos al Ministerio de Agricultura y Desarrollo Rural por el apoyo financiero.