Abstract
The Guatemalan potato moth Tecia solanivora (Lep.; Gelechiidae) is one of the most limiting pests of this crop in Venezuela, Colombia and Ecuador and its control through the use of chemical insecticides has not been very effective. Its biological control with the granulovirus Phthorimaea operculella (PhopGV) has been one of the principal components of its management in Colombia and other Andean countries. Corpoica has a plant, registered through the Colombian Agricultural Institute, for manufacturing a biopesticide based on this virus. Given the importance of confirming product quality, the objective of this work was to standardize and implement quality control tests during the manufacturing process. Virus identity and concentration, physical-chemical characteristics of the product and biopesticide efficacy were established as critical parameters; methodologies for evaluating these parameters were then standardized and implemented in the production process. Virus identity was confirmed as P. operculella by microscopic, immunological, and molecular techniques. To control viral concentration, lethal viral concentrations were determined and acceptable limits for this variable were established. The biopesticide was elaborated based on these results. The lethal concentration (LC90) was 8 x 105 occlusion bodies (OB).mL−1 and based on this result, the final product was adapted to give a concentration of 105 OB.g1. Three batches of the product were manufactured and quality control showed low variability, indicating the repeatability of the process. Mean product characteristics were concentration 105 OB.g−1, moisture content 0.57%, voluminosity 0.93 mL.g−1, pH 9.52 and efficacy 97.25%.
Introducción
La “Polilla guatemalteca de la papa” Tecia solanivora (Povolny) 1973, originaria de Centroamérica, pertenece al complejo de polillas o palomillas que ataca al cultivo de la papa y es considerada como una de las principales plagas de dicho cultivo en la región Andina si se tiene en cuenta el daño que ocasiona al tubérculo tanto bajo condiciones de campo como de almacenamiento (Niño y Notz 2000).
Frente a esta problemática, se han generado varios componentes para su control, dentro de un Programa de manejo Integrado de Plagas de la Papa (MIPP), tales como el control cultural, el etológico y el químico. Sin embargo, la medida más utilizada por los agricultores sigue siendo el uso indiscriminado de productos químicos, de los cuales muchos son de categoría toxicológica I, es decir extremadamente tóxicos y la mayoría son ineficientes para el control del insecto (Niño y Notz 2000).
Una alternativa promisoria para su control es el uso del granulovirus de Phthorimaea operculella, un virus perteneciente a la familia Baculoviridae, el cual es altamente específico y ha sido considerado con otros virus por la Organización para la Agricultura y la Alimentación (FAO) y la Organización Mundial de la Salud (OMS) como la herramienta más promisoria para el control de plagas (CIP 2000).
Este virus interactúa inicialmente con su hospedero a nivel intestinal lo que implica que para que se infecten las larvas es necesario que las partículas virales sean ingeridas. Posteriormente, las larvas se vuelven lentas en sus movimientos, se retrasa su crecimiento, toman una coloración blanca, se produce la desintegración de los tejidos internos y la muerte ocurre entre los 12 y 21 días, no llegando ninguna larva al estado de pupa (CIP 2000).
Para la multiplicación del virus se emplean larvas del hospedero, las cuales cuando están infectadas, se muelen en fresco, congeladas, secas o liofilizadas. El Centro Internacional de la Papa (CIP), desarrolló una formulación en forma de polvo seco para protección de semilla en almacenamiento, la cual consiste en macerar 20 larvas infectadas y diluirlas en un litro de agua. Esta preparación se mezcla manualmente con un kilo de material inerte tal como talco, caolín, etc., hasta obtener una pasta que se extiende sobre un plástico en una superficie horizontal protegida de la luz para secarla al ambiente y después de dos semanas, se muele con un rodillo manualmente hasta obtener un polvo que es empacado y distribuido para su uso (CIP 2000). Sin embargo, este proceso artesanal puede dar origen a productos de calidad variable ya que no se conoce la concentración viral del producto, no se conocen sus concentraciones efectivas y las operaciones de manufactura no incluyen ningún tipo de control durante el proceso (Zeddam et al. 2003).
En Corpoica, desde su existencia, se estableció el Laboratorio de Control Biológico como apoyo al Programa Nacional de Manejo Integrado de Plagas (MIP). La función de este laboratorio es la de hacer investigación y desarrollar bioplaguicidas. En el año 2000, este Laboratorio se enfrentó al reto de producir el producto a base de baculovirus, para responder a la emergencia sanitaria causada por la polilla guatemalteca. Inicialmente se obtuvo la cepa del virus proveniente de la Secretaría de Agricultura de Boyacá y se adoptó la tecnología de formulación desarrollada por el CIP. Sin embargo, dicho proceso artesanal no permitía asegurar la calidad de los diferentes lotes de producción, presentándose inconsistencias en los resultados de eficacia del producto. Por tales razones y con miras a producir cantidades comerciales del bioinsecticida que permitieran suplir las necesidades del sector, se planteó como meta la tecnificación del proceso productivo, dentro de una filosofía de “calidad total”, para lo cual fue necesario construir una planta de producción que cumpliera con las especificaciones técnicas para este tipo de industrias, se adquirieron los equipos para realizar cada parte del proceso como una operación unitaria independiente y estandarizable; todas las operaciones unitarias se estandarizaron y se determinaron los puntos críticos de cada una de ellas. Así mismo, se corroboró la identidad del agente biocontrolador, se ajustó su concentración efectiva en el producto y se validaron y documentaron las técnicas de control de calidad en los Procedimientos Operacionales Estándar (POES).
Materiales y Métodos
Identificación viral
La identificación del virus se realizó en el Instituto de Investigaciones para el Desarrollo de Francia (IRD). Para tal fin, larvas infectadas provenientes de la unidad de propagación viral de la Planta Semicomercial de Baculovirus fueron liofilizadas y analizadas en dicho instituto.
Microscopía electrónica
Larvas frescas se fijaron con glutaraldehido al 2% y fijadas nuevamente con tetraóxido de osmio al 2%; estas dos soluciones se prepararon en tampón cacodilato (pH6.8, 0.1M). Las muestras fueron deshidratadas en concentraciones crecientes de etanol (20 a 100%) y luego fijadas en parafina y cortadas con micrótomo en tajadas de 10 micras de espesor. Secciones del insecto fueron cubiertas con oro con un micrótomo Reichert Jung, modelo 2030 y observadas en un microscopio electrónico Phillips 515.
Purificación viral y análisis molecular del ADN
Larvas infectadas con el virus fueron homogeneizadas en solución de sodio dodecil sulfóxido (SDS) al 0,1% en agua destilada. El homogeneizado se filtró a través de una tela y la suspensión resultante se ubicó sobre un gradiente de sacarosa de 45% a 80% y se centrifugó por una hora a 32.500g. La banda blanca formada por los cuerpos de inclusión se recuperó, se diluyó en tres volúmenes de agua destilada y se centrifugó por 1 hora a 20.000g. El sedimento que contenía los cuerpos de inclusión fue suspendido en 1 mL de agua destilada. Se tomó 1 mL de la suspensión de virus purificado y se mezcló con el mismo volumen de una solución de carbonato de sodio (1M, pH 11) por 30 minutos, seguido de la adición de 2mL de tampón Tris (1M, pH 8.0). La solución resultante se centrifugó por 1 hora a 75.000g. El sedimento (viriones) se resuspendió en 1 mL de tampón Tris y se extrajo sucesivamente tres veces con fenol, dos veces con cloroformo: alcohol isoamílico (1:24) y dos veces con éter. La fase acuosa fue recuperada y precipitada toda la noche (-20°C) con 2.5 volúmenes de etanol absoluto en presencia de acetato de sodio (pH 5.5) a una concentración final de 0.3M. El ADN sedimentado se lavó con etanol al 95%, se secó y disolvió en tampón Tris. Posteriormente, se aplicaron las enzimas de restricción Eco RV, BgI II, Sal I, Eco RI, Pvu II, Sac I, Cla I y Bam HI, según las recomendaciones del fabricante (Boehringer). Terminada la digestión se corrió una electroforesis del ADN digerido usando un gel de agarosa al 1% en tampón TEP (9 mM Tris-fosfato, 2 mM EDTA, pH 8.0) (Zeddam et al. 1999). Los tratamientos consistieron en larvas provenientes de la Planta Semicomercial de Baculovirus y un tratamiento control consistente en ADN de PhopGV patrón.
Inmunodifusión
El virus purificado se analizó en un gel de agarosa mediante la técnica de inmunodifusión (Ouchterlony 1948). El antisuero utilizado se produjo sobre ratón por inyección de cuerpos de inclusión de PhopGV previamente disueltos con carbonato de sodio. Los tratamientos fueron los cuerpos de inclusión de larvas provenientes de la Planta Semicomercial de Baculovirus y un tratamiento control consistente en cuerpos de inclusión de larvas infectadas con PhopGV patrón.
Validación de la técnica de cuantificación viral
De la suspensión viral preparada en la Planta Semicomercial de Baculovirus se tomaron ocho muestras que fueron filtradas usando una jeringa de filtración con un filtro de 0,8 micras. Posteriormente, con una micropipeta se tomó un volumen de la muestra y se colocó en la cámara de Neubauer, la cual se cubrió con su respectiva laminilla de cuarzo y observada en el microscopio de campo oscuro a 400X, ajustando la cuadrícula central de la cámara. Se tomó una fotografía de la imagen con una cámara digital acoplada al microcopio y se imprimió para realizar el conteo de cuerpos de inclusión. El conteo de las partículas virales se realizó en cada uno de los 25 cuadrados que conformaron el cuadrante. Los resultados se promediaron y se utilizó el factor de conversión de la cámara para calcular el número de cuerpos de inclusión por mL.
El procedimiento descrito se repitió con cada muestra. Para la evaluación de repetibilidad, las ocho muestras evaluadas se tomaron de la misma suspensión viral y se evaluaron con los mismos equipos, en el mismo día y con el mismo analista.
Determinación de las concentraciones letales
Para determinar la concentración letal media y noventa del PhopGV, tres larvas muertas de T. solanivora con síntoma viral fueron maceradas y llevadas a 100mL con una solución de Tween 80 al 0,1%, consistiendo ésta en la dilución 10°, a partir de la cual se prepararon 100mL de las diluciones decimales 10−1, 10−2, 10-³ y 10−4, determinando su concentración mediante conteo en cámara de Neubauer en microscopio de campo oscuro siguiendo la metodología descrita anteriormente después de haber sido validada. En cada dilución se sumergieron tres tubérculos de papa pastusa lavada durante 1 minuto, momento en el cual las papas fueron retiradas del líquido y puestas sobre un papel servilleta al ambiente para permitir el secado. Cada papa seca se ubicó en un recipiente plástico de 16 onzas y fue infestada con 20 larvas de T. solanivora de primer ínstar. Los recipientes se cerraron y se ubicaron aleatoriamente en un estante ubicado en un cuarto con temperatura promedio 25°C. Se contó con un testigo absoluto en el cual los tubérculos no fueron inoculados. Pasados 30 días, se registró la mortalidad de las larvas en cada unidad experimental mediante una evaluación destructiva de los tubérculos. Los insectos se clasificaron como vivos (larvas con movimiento y pupas) y muertos (larvas sin movimiento y larvas desaparecidas, lo que sugiere que murieron en estado neonato). Los resultados se utilizaron para calcular el porcentaje de eficacia mediante la fórmula de Schneider-Orelli (Ciba Geigy 1973) y se empleó el análisis Probit para determinar las concentraciones letales.
Elaboración del bioplaguicida
Una vez determinadas las concentraciones letales del aislamiento, se ajustó el proceso de manufactura del bioplaguicida para que la concentración final del producto fuera la concentración letal noventa (CL50) determinada. Para tal fin se calculó la concentración requerida en la suspensión viral a partir de la cual se elaboró la formulación y basados en la desviación estándar de los resultados de la validación de la técnica de cuantificación viral se fijaron los límites de aceptación para dicha variable. Una vez fijado este parámetro, se elaboraron tres lotes del bioplaguicida en la Planta Semicomercial de Baculovirus.
Validación de técnicas de control de calidad
Con los productos se validaron las pruebas de control de calidad para el producto terminado. Dichas pruebas consistieron en la determinación del pH, la voluminosiad, el tamaño de partícula y la eficacia biocontroladora.
Resultados y Discusión
Identificación viral
Microscopía electrónica
En las imágenes de microscopía electrónica de las muestras se observaron estructuras ovoides que coincidieron con la descripción típica de los cuerpos de inclusión del granulovirus de Phthorimaea operculella (Fig. 1). Los cuerpos de inclusión aparecieron como corpúsculos de forma de bastón con un ancho aproximado de 260 a 280 nm y un largo aproximado de 460 a 480 nm. Estas características coincidieron con las reportadas para los granulovirus, los cuales han sido descritos como estructuras de esta forma con un tamaño entre 160 y 300 nm de ancho y entre 300 y 500 nm de largo (Caballero et al. 2001).
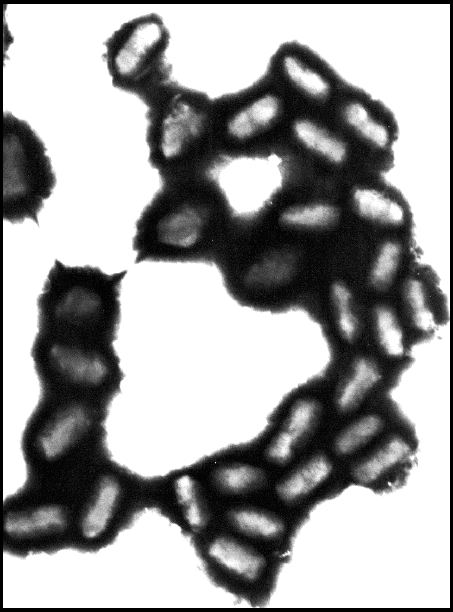
Microscopía electrónica de cuerpos de inclusión del granulovirus de Phthorimaea operculella (10.000 x)
Análisis molecular del ADN
Los patrones de distribución de los fragmentos de ADN generados por la muestra digerida con las ocho enzimas de restricción, coincidieron con los obtenidos con el tratamiento control para las diferentes enzimas utilizadas. Este resultado confirma la identidad del virus como el granulovirus de Phthorimaea operculella.
La gran similitud en el ADN de diferentes aislamientos de este virus facilita su identificación por este método. La razón para la alta conservación de los sitios de restricción en las secuencias de ADN viral es desconocida, esta conservación además no es única de los granulovirus (Zeddam et al. 1999). A pesar de que se han reportado algunas pequeñas variaciones, como en el caso de granulovirus patógenos de Pieris brassicae y Pieris rapae, los cuales mostraron algunas diferencias en los patrones de distribución de los fragmentos de ADN, las diferencias mínimas encontradas no han dificultado su identificación por esta técnica molecular (Crook 1986).
Inmunodifusión
La reacción de inmunodifusión mostró bandas idénticas en los dos tratamientos consistentes en la muestra proveniente del principio activo del bioplaguicida y del tratamiento control (Fig. 2). Esto sugiere que el virus presente en la muestra es antigénicamente estrechamente relacionado con el PhopGV.
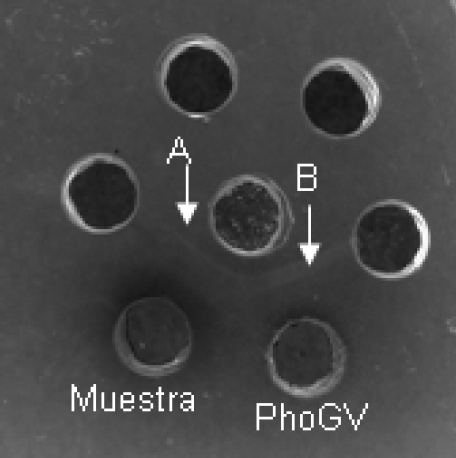
Evaluación serológica de la muestra. (A) y (B) bandas de reacción antígeno anticuerpo positivas para PhopGV.
Los resultados de la aplicación de las técnicas de microscopía, serología y biología molecular son coherentes y permiten concluir que las larvas de Tecia solanivora examinadas estaban infectadas masivamente por un granulovirus. Las características establecidas por éste permitieron concluir que se trataba del granulovirus de Phthorimaea operculella descrito por primera vez en 1967 por Steinhaus y Marsh.
Validación de la técnica de cuantificación viral
Al observar las muestras en el microscopio de campo oscuro se observaron los cuerpos de inclusión (CI) como puntos brillantes con un ligero movimiento Browniano. Los resultados de concentración expresada como CI.mL−1 para cada una de las ocho muestras evaluadas fueron 3,61 x 106, 4,75 x 106, 6,73 x 106, 4,23 x 106, 4,40 x 106, 5,71 x 106, 6,49 x 106 y 4,47 x 106 y el valor medio fue de 5,04 x 106. Los resultados se transformaron calculando el logaritmo decimal de cada valor y con dichos valores se calcularon la desviación estándar, la varianza y el coeficiente de variación de los datos. El coeficiente de variación expresado como porcentaje fue del 1,38%, indicando baja variabilidad y alta repetibilidad; en consecuencia, éstos sugieren que la técnica utilizada para evaluar la variable concentración de cuerpos de inclusión en la suspensión viral es precisa y confiable, por lo que puede utilizarse para el control de calidad del producto en proceso. Este método es el más utilizado para la cuantificación de cuerpos de inclusión en suspensiones acuosas puras o semipuras y se recomienda para facilitar la lectura un número de cuerpos de inclusión entre 20 y 40 por cuadrícula (Caballero et al. 2001). La implementación de dicho control en la manufactura del bioplaguicida permitió establecer una concentración fija y constante del virus en el producto.
Determinación de las concentraciones letales
Una vez validada, la técnica de cuantificación viral se utilizó para ajustar la concentración de diferentes suspensiones virales. Al evaluar las diferentes concentraciones del virus se encontró que a mayor concentración viral inoculada en los tubérculos, mayor número de larvas muertas y las pocas que se encontraban vivas, presentaron la sintomatología típica de la infección viral expresada como retardo en el crecimiento, disminución de la movilidad y una coloración blanca lechosa a través del integumento, la cual fue más notoria en la zona ventral (Fig. 3). A menor concentración del virus se encontró mayor número de pupas y larvas vivas de mayor tamaño. En el tratamiento control, en el cual no se aplicó virus, se obtuvo un 5% de mortalidad, 88% de los individuos se encontraban en estado de pupa y el 7% como larvas vivas y sanas sin sintomatología viral. Los porcentajes de eficacia para las diferentes concentraciones del virus correspondientes a 10β, 10³, 104 105 y 106 CI.mL−1 fueron del 5,26%, 14%, 59,5%, 59,7% y 92,9% respectivamente. Estos resultados indican que la concentración del virus es directamente proporcional a la mortalidad de las larvas de la Polilla guatemalteca de la papa.
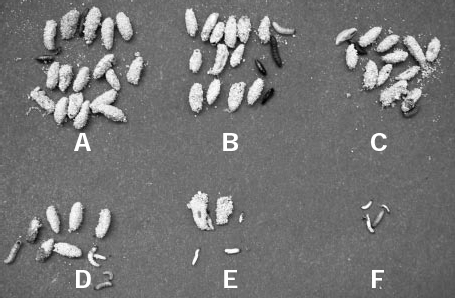
Pupas y larvas sobrevivientes a la infección con diferentes concentraciones del virus. (A) Testigo, (B) 10β CI.mL−1, (C) 10³ CI.mL¹, (D) 104 CI.mL−1, (E) 105 CI.mL−1, (F) 106 CI.mL−1.
El programa Probit determinó como concentración letal media 1.4x104CI.mL−1 y como concentración letal noventa 8.0x105 CI.mL−1 (Tabla 1). Existen algunos trabajos en los que se ha buscado determinar las concentraciones letales de aislamientos de baculovirus, sin embargo, en la mayoría de los casos se ha utilizado el número de larvas o equivalentes larvales (E.L.) para medir las concentraciones y no la cuantificación de partículas virales por lo que los resultados han sido inconsistentes. Al trabajar con equivalentes larvales las concentraciones virales son variables pues cada larva puede tener un contenido diferente de cuerpos de inclusión dependiendo de cómo se haya desarrollado la infección.
Concentraciones letales de Baculovirus sobre la polilla de la papa Tecia solanivora.
Con un aislamiento de PhopGV procedente de Yemen se estableció como concentración letal media un valor de 7.3 x 104 CI.mL−1, mediante un experimento en el cual se expusieron neonatos de P. operculella a tubérculos tratados con diferentes concentraciones del virus (Kroshel et al. 1996 citado por Zeddam 1999). Esta concentración es similar a la obtenida en el presente trabajo con T. solanivora, a pesar de que el virus empleado en los dos estudios es un granulovirus de Phthorimaea operculella, por lo que se esperaría que presentara mayor patogenicidad contra su hospedero natural.
Alcázar et al. (1992) establecieron la CL50 para un aislamiento de PhopGV para el control de P. operculella en 3.83 x 10³ CI.mL−1, resultado aproximadamente 10 veces menor del encontrado en el presente estudio. Esto podría sugerir que dicho aislamiento es más patogénico que el evaluado en este trabajo o que P. operculella es más susceptible a este virus que T. solanivora.
Zeddam et al. (1999), establecieron la CL50 de diferentes aislamientos de PhopGV en Phthorimaea operculella para lo que prepararon diferentes dosis del virus utilizando como variable los equivalentes larvales. Con dichas suspensiones inocularon tubérculos de papa que infestaron con larvas de segundo o tercer ínstar de la polilla. Los autores concluyeron que todos aislamientos virales presentaron la misma patogenicidad y sus CL50 oscilaron entre 15.6 y 18.5 E.L.100mL−1.
Después de determinar la CL50 del virus, se realizaron los cambios necesarios en el proceso de manufactura del bioplaguicida para ajustar en el producto una concentración final equivalente por unidad de peso, ésta fue de 8.0x105 CI.g−1 y se estableció como concentración óptima en el producto con la cual se fijaron los límites de aceptación para la concentración de la suspensión viral utilizada para elaborar el formulado entre 2.0 x 106 y 6.2 x 106 CI.mL−1. De esta forma, cada vez que se elabora un lote de bioplaguicida, se realiza como control de calidad la determinación de la concentración de la suspensión viral. Así el producto solo se usaría cuando se encuentra dentro de dicho rango. Esto ha permitido asegurar que todos los lotes de producto tengan la misma concentración viral y en consecuencia una eficacia biocontroladora constante.
Validación de técnicas de control de calidad
Para la variable pH se obtuvieron resultados que oscilaron entre 9.33 y 9.64 (Tabla 2), valor que se debe al soporte inerte utilizado como vehículo de la formulación. Los valores obtenidos presentaron baja variabilidad entre las diferentes muestras, con un bajo coeficiente de variación del 1.47%, que sugiere que la técnica es confiable y precisa y puede ser utilizada como un control de calidad para el producto. Con el resultado promedio y la desviación estándar de los datos se estableció como límite de aceptación para esta característica un rango entre 9.38 a 9.66.
Valores de pH en diferentes muestras del producto a base de Baculovirus. SD: Desviación estándar, C.V.: Coeficiente de variación.
Para la voluminosidad del bioplaguicida, característica que determina la facilidad en la manipulación del producto durante los procesos de llenado de empaques (Voight y Bomschein 1982), se obtuvieron valores entre 0.88 mL.g−1 y 0.96 mL.g−1 (Tabla 3) que se consideran bajos y están determinados por la voluminosidad del vehículo inerte. Estos valores se consideran adecuados según la industria farmacéutica, la cual recomienda voluminosidades inferiores a 3 mL.g−1 para asegurar que no presentará problemas de manipulación durante el proceso de manufactura y empaque (Voight y Bomschein 1982). Los resultados presentaron una baja variabilidad entre réplicas, con un coeficiente de variación del 3.59%, el cual indicó que esta técnica también es altamente repetible y puede ser utilizada como un control de calidad confiable. Los límites de aceptación para esta característica se fijaron entre 0.60 mL.g−1 y 1.26 mL.g−1 y se estableció que dicho control debe realizarse al producto antes de iniciar la operación de llenado sde envases.
Valores de voluminosidad en diferentes muestras del producto a base de Baculovirus. SD: Desviación estándar, C.V.: Coeficiente de variación.
En la determinación del tamaño de partícula del producto, la mayor cantidad de peso retenido se obtuvo en el tamiz con tamaño de poro 59 micras (Tabla 4). También se observó que en el colector de polvos finos quedó retenido un 40.72% del material, resultado que indica que un alto porcentaje de las partículas presentan un tamaño inferior a 59 micras. Este aspecto asegura una buena adherencia sobre la superficie de los tubérculos. Los resultados de las diferentes muestras presentaron coeficientes de variación inferiores al 5%, valores bajos que indicaron que la técnica es precisa, con alta repetibilidad y es adecuada como control de calidad del producto.
Distribución de tamaños de partícula del producto a base de Baculovirus. SD: Desviación estándar, C.V.: Coeficiente de variación.
En cuanto a la evaluación de la eficacia del bioplaguicida, los resultados con las cuatro muestras oscilaron entre 89.2% y 100% (Tabla 5), valores que muestran que el producto es eficiente para el control de la plaga. Estos resultados además presentaron un coeficiente de variación del 5.5%, considerado bajo para este tipo de ensayos biológicos; este indica que la metodología empleada para el bioensayo es precisa y de alta repetibilidad. Si se tiene en cuenta que la técnica desarrollada es sencilla, rápida y económica, puede considerarse óptima para el control de calidad del producto.
Actividad biocontroladora de diferentes muestras del producto a base de Baculovirus. SD: Desviación estándar, C.V.: Coeficiente de variación.
La validación de estas técnicas permitió elaborar Procedimientos Operativos Estándar (POE's) que describen la metodología detallada de cada prueba y un formato para el registro de los resultados parciales y finales de cada evaluación. Con base en dicha documentación el laboratorio de control de calidad Biotécnica adscrito al laboratorio de Control Biológico de Corpoica se registró ante el ICA. Este presta el servicio de control de calidad a la Planta de Producción de Baculovirus y es el único laboratorio registrado en el país para desarrollar dichos análisis.
Footnotes
Agradecimientos
Los autores expresan sus agradecimientos a Colciencias por su apoyo financiero para el desarrollo del presente trabajo.
