Abstract
The corn armyworm, Spodoptera frugiperda, is a polyphagous insect that causes important economic losses worldwide. Its control with highly toxic chemical insecticides is inefficient given the generation of resistance. Biological control with nucleopolyhedroviruses emerges as an alternative considering the efficacy and high specificity of these agents. However, baculoviruses are affected by environmental conditions, ultraviolet solar radiation being the most limiting factor for field efficacy. For this reason, the present work aimed to determine the susceptibility of a S. frugiperda nucleopolyhedrovirus to type UVA, UVB and UVC monochromatic ultraviolet radiation. Five concentrations of purified virus were exposed to each type of UV radiation over different times for a maximum of one hour. A negative effect of the three radiation types was observed on insecticidal activity, being greatest at higher exposure time and UV radiation energy. These results confirmed the need to develop a formulation which includes solar protectors for ensuring biopesticide efficacy under field conditions.
Introducción
El gusano cogollero Spodoptera frugiperda (J. E. Smith, 1797) (Lepidoptera: Noctuidae), es la plaga más importante del cultivo del maíz; las pérdidas que este insecto ocasiona son cuantiosas considerando que se encuentra ampliamente distribuido y reduce los rendimientos hasta en un 35%. Para el control químico de este insecto a nivel mundial se gastan aproximadamente $4,2 millones de dólares en plaguicidas químicos por año, lo cual incide negativamente en los costos de producción (Fernández 2003).
La creciente necesidad de reducir el uso de agroquímicos para el control fitosanitario de los cultivos, hace necesario desarrollar tecnologías que permitan de forma fácil, económica y efectiva obtener productos a partir de microorganismos, insectos o nemátodos con alta calidad y en cantidades suficientes para su aplicación en las zonas cultivadas (Ferrer 2001). Por tales razones, el control biológico mediante virus entomopatógenos como componentes de una estrategia de manejo integrado de plagas, se acerca más a una solución duradera y efectiva, debido a su reducido efecto sobre el ambiente.
La infección viral en los insectos ocurre por vía oral, a través de la ingestión del alimento contaminado con cuerpos de inclusión virales (CIs). La replicación del virus en los tejidos susceptibles del insecto causa desintegración de éstos y las larvas se tornan blandas y muy frágiles (Burges 1981). Según Alves (1986) los insectos afectados por virus presentan falta de apetito, cambios en la coloración y alargamiento del tiempo del estado larval. Además, hay una disminución de la actividad de las larvas y en los estados más avanzados de la infección se produce su muerte.
Una de las familias de entomovirus más estudiada es la familia Baculoviridae a la cual pertenecen los géneros de la Granulovirus (GV) y de la Nucleopoliedrovirus (NPV). Estos se caracterizan por presentar CIs que los protegen contra los factores ambientales y por afectar sólo a invertebrados, especialmente insectos, no representando riesgos para otros organismos (Burges 1981; Tanada y Kaya 1993). Dichos virus han sido reportados en 600 especies hospederas, de las cuales la mayoría pertenecen al orden Lepidoptera y en menor proporción a los órdenes Diptera e Hymenoptera (Federici 1997).
La efectividad y alto potencial de los baculovirus para el control de diferentes insectos plaga han sido demostrados en diversos trabajos (Valicente y Da Costa 1995; Batista et al. 2001; Barreto et al. 2005; Villamizar et al. 2005; Murillo y Caballero 2006). Sin embargo, a pesar de que estos virus son una herramienta eficiente para el control de insectos plaga, su evaluación en campo ha presentado resultados inconsistentes (Mascarenhas et al. 1996), posiblemente por el efecto deletéreo de las condiciones ambientales sobre los CIs (Ignoffo et al. 1977).
La inactivación causada por la radiación solar bajo condiciones de campo es el principal factor ambiental que limita el uso masivo de estos agentes de biocontrol (Ignoffo et al. 1977). La luz solar afecta negativamente las partículas virales, particularmente la radiación comprendida en el espectro ultravioleta y especialmente la radiación entre 280 nm y 310 nm (Asano 2005).
Actualmente el Laboratorio de Control Biológico del Centro de Biotecnología y Bioindustria de Corpoica cuenta con un aislamiento de nucleopoliedrovirus de S. frugiperda (SfMNPV) codificado como NPV001, el cual tiene alto potencial para ser desarrollado como un bioplaguicida. Sin embargo, cuando el virus formulado sea aplicado bajo condiciones de campo se verá expuesto a condiciones ambientales deletéreas como la radiación ultravioleta del sol. Por tales razones, surgió la necesidad de caracterizar ecofisiológicamente este aislado del SfMNPV con miras a determinar si requiere la inclusión de protectores solares en la formulación.
Materiales y Métodos
El insecto
Los insectos utilizados para la presente investigación fueron obtenidos a partir de una cría ubicada en el Centro de Investigaciones Tibaitatá y establecida a partir de larvas recolectadas en campo en el municipio de Cereté (Córdoba). Los insectos se mantuvieron en un cuarto a 28°C y 60% de humedad relativa, con un fotoperíodo de 12 horas. Las larvas fueron manejadas de manera individual en recipientes plásticos de 25 mL que contenían 15 mL de dieta artificial (harina de maíz 8,3 g, levadura de pan 8,3 g, harina de fríjol 41,6 g, 1 mL de formaldehído al 10%, metilparabeno 0,6 g, ácido ascórbico 0,8 g, ácido sórbico 0,7 g, 2 ml de aceite de linaza, caseína 0.8 g, agar 4,0 g y 300 mL de agua destilada estéril).
El virus
El aislamiento viral (NPV001) fue obtenido a partir del Banco de Germoplasma de Microorganismos con Interés en Control Biológico de Corpoica, el cual fue aislado de larvas de S. frugiperda infectadas naturalmente en campo.
Producción viral
La superficie de la dieta artificial dispensada en recipientes plásticos de dos onzas fue inoculada con 100 µL de una suspensión viral ajustada a una concentración de 106 CIs/mL. En cada recipiente se ubicó una larva de tercer ínstar de S. frugiperda, sometidas a seis horas de ayuno. Los recipientes plásticos con las larvas inoculadas fueron incubados a 25°C y 80% de humedad relativa (HR). Cada dos días se revisaron las larvas y aquellas que presentaron la sintomatología típica de infección (tegumento frágil, coloración parda y poca movilidad) fueron recolectadas y almacenadas en congelador a -20°C.
Purificación viral
Se utilizó el método modificado de Valicente et al. (1989). Cincuenta larvas con sintomatología típica de infección fueron homogeneizadas en un mortero de porcelana estéril con 10 µL de solución de SDS al 0,1% estéril y posteriormente se filtraron por una muselina para retirar el tejido del insecto. El líquido se centrifugó a 1000 rpm durante un minuto y se recogió el sobrenadante, el cual se centrifugó a 12.000 rpm por 30 minutos a 10°C. El sedimento fue resuspendido en 1 µL de tampón Tris (pH 7,4; 0,1M) y ubicado sobre un colchón de sacarosa del 60%, posteriormente se centrifugó a 12.000 rpm durante 30 minutos. Se retiró la banda que contenía el virus y se realizaron dos lavados con el mismo tampón.
Susceptibilidad del virus a la radiación ultravioleta
Con el virus purificado se preparó una suspensión y a partir de ésta, diluciones ajustadas a cinco concentraciones correspondientes a 2 x 105, 2 x 106, 2 x 107, 2 x 108 y 2 x 109 CIs/mL, revisadas mediante recuento en cámara de Neubauer. Posteriormente, se colocaron 20 µL de cada concentración en cinco pozos de una fila de tres microplacas de 96 pozos de fondo plano. Cada microplaca fue expuesta a 30 cm de una lámpara ultravioleta monocromática con longitudes de onda de 365 nm (UVA), 302 nm (UVB) y 254 nm (UVC). Antes de iniciar la exposición a la luz se cubrió un pozo de cada concentración de la primera columna de pozos de la microplaca con papel aluminio, consistiendo este tratamiento en el virus no expuesto a la radiación. Cada 15 minutos durante una hora se cubrió la columna de pozos siguiente, representando cada columna de la microplaca un tiempo diferente de exposición a la radiación ultravioleta. Posteriormente se adicionó a cada pozo 200 µL de una solución de sacarosa al 4% y colorante azul de alimentos Tuska® (Azul No 1 y Azul No. 2) al 1% y se desarrolló un bioensayo.
Para la inoculación de los insectos se tomó el contenido de cada pozo previamente homogeneizado con una micropipeta de 10 µL y se dispensaron gotas de 2 µL en forma circular en un disco plástico de color blanco. Posteriormente se ubicaron 40 larvas neonatas de S. frugiperda en el interior del círculo y se esperó hasta que las larvas bebieran el tratamiento, lo que se evidenció por la coloración azul en el cuerpo de las mismas como consecuencia de la ingestión del tratamiento (virus + colorante). Dicha coloración fue detectada mediante observación en un estereoscopio Olympus SZ40. Se seleccionaron 30 larvas con coloración azul que fueron ubicadas individualmente en la dieta artificial, e incubadas en un cuarto a 28°C y 60% de humedad relativa.
Se contó con un testigo absoluto en el que las larvas no fueron sometidas a ningún tratamiento. Los resultados de mortalidad al día siete fueron corregidos con respecto al testigo utilizando la fórmula de Schneider - Orelli para el cálculo de la eficacia (Zar 1999). El diseño experimental fue completamente al azar con medidas repetidas en el tiempo y 30 individuos por tratamiento. Los resultados de mortalidad fueron sometidos a un análisis Probit (Finney 1952) mediante el programa Polo-PC (LeOra Sofware Inc. Berkeley, CA, USA) para la determinación de las concentraciones letales.
Se calculó adicionalmente el porcentaje de actividad original remanente (%AOR) (Shapiro 1989) = (C/A) x 100 donde: A: Eficacia del virus no expuesto, C: Eficacia del virus expuesto a la radiación UV. Los resultados de %AOR se sometieron a un análisis de varianza ANAVA y una prueba de comparación de medias de Tukey con una confiabilidad del 95%.
Resultados y Discusión
Los resultados del ensayo de dosis-mortalidad del nucleopoliedrovirus de S. frugiperda, aislamiento NPV001 expuesto a la radiación ultravioleta tipo A, tipo B y tipo C, presentaron para todos los tiempos de exposición, un valor de P > 0,05 y valores de xβ (Tablas 1, 2 y 3), que indican que la nube de puntos se ajustó a la línea de regresión y permitieron aceptar la hipótesis de que existe una correlación lineal entre la dosis y la mortalidad de las larvas. Las líneas de regresión para cada tratamiento (tiempo de exposición) evaluado para cada tipo de radiación UV, no fueron paralelas, por lo que para determinar diferencias estos, se utilizaron los límites de confianza del cociente de la CL50 obtenida para el virus sin exponer a la radiación UV, sobre la CL50 determinada para el virus irradiado.
Valores de la concentración letal media (CL50) del nucleopoliedrovirus de Spodoptera frugiperda, no expuesto y expuesto a radiación UVA en larvas neonatas de S. frugiperda.
Valores de la concentración letal media (CL50) del nucleopoliedrovirus de Spodoptera frugiperda, no expuesto y expuesto a radiación UVB, en larvas neonatas de S. frugiperda.
Efecto de la radiación ultravioleta tipo A
Hubo una relación directa entre la concentración viral y la mortalidad de las larvas. La concentración letal media (CL50) para el virus no expuesto fue de 2,2 x 106 CI/mL. Ésta se incrementó progresivamente a medida que aumentó el tiempo de exposición a la radiación UVA, obteniéndose valores de CL50 de 4,6 x 106; 5,0 x 106; 7,6 x 106 y 1,9 x 107 CIs/mL para los tiempos de exposición 15, 30, 45 y 60 minutos respectivamente (Tabla 1).
Las CL50 del virus expuesto a la luz durante 15 y 30 no fueron estadísticamente diferentes entre sí, pero si fueron significativamente inferiores que las obtenidas para el virus irradiado por 45 y 60 minutos. Estos resultados indican que la radiación ultravioleta tipo A causó una pérdida significativa de la actividad insecticida del virus a partir de los 45 minutos de exposición. La exposición de este aislamiento viral a la radiación UVA por 45 y 60 minutos incrementó 3,45 y 8,6 veces respectivamente, la CL50 del virus no irradiado.
Esta radiación no es absorbida por el ozono atmosférico, por tanto penetra directamente a la biosfera. Aunque de los tres tipos de radiación ultravioleta ésta es la de menor energía y por ende la menos perjudicial, está presente en mayor intensidad en los rayos solares y puede ser absorbida por muchas proteínas incluyendo importantes fotorreceptores (Niegel y Dylan 2003), razón por la que causa lesiones indirectas en la molécula de ADN (Wakefield et al. 2004). El daño indirecto se debe principalmente a la formación de especies reactivas de oxígeno (peróxido de hidrógeno, oxígeno molecular y radicales hidroxilo) que oxidan las pentosas presentes en el ADN y rompen la cadena de la molécula (Diffey 1991, en Devotto y Gerding 2003).
Otros aislamientos de baculovirus han mostrado susceptibilidad similar a la radiación UVA. Ignoffo et al. (1989) evaluaron el efecto de dicha radiación (350 nm) sobre partículas virales ocluidas y no ocluidas (viriones liberados por disolución del CI) de un nucleopoliedrovirus de Helicoverpa sp. (HzSNPV). En dicho trabajo se determinó que la vida media de los virus ocluidos y no ocluidos expuestos a la radiación UVA fue de 5,8 y 6,3 horas respectivamente, concluyendo que los dos tipos de partículas virales son igualmente susceptibles a la luz ultravioleta tipo A.
El efecto de la radiación ultravioleta tipo A también ha sido evaluado sobre otros agentes de biocontrol como bacterias y hongos entomopatógenos. Por ejemplo, Saxena et al. (2002) reportaron una pérdida del 90% en la viabilidad de Bacillus thuringiensis subsp. kurstaki después de 16 minutos de exposición a la radiación ultravioleta tipo A (λ = 366 nm), disminución que estuvo relacionada con una pérdida del 90% de su actividad insecticida para Helicoverpa armigera (Hübner, 1805).
De igual forma, Braga et al. (2001), evaluaron la viabilidad de los conidios de tres aislamientos del hongo entomopatógeno Metharhizium anisoplie (Metschnikoff), obteniendo una reducción del 10% para el aislamiento ARSEF 324, del 40% para el aislamiento ARSEF 23 y del 60% para el aislamiento ARSEF 2575, después de cuatro horas de exposición a la radiación UVA (320 a 400 nm). En otro estudio realizado por Pavone (2003), se demostró que la radiación UVA (λ= 365 nm) no ejerció ningún efecto negativo sobre los conidios de Nomuraea rileyi (Farlow) Samson luego de una hora de exposición. Estas diferencias permiten sugerir que el efecto de esta radiación es dependiente del género, especie y aislamiento del microorganismo.
Efecto de la radiación ultravioleta tipo B
Las concentraciones letales medias del virus expuesto a la radiación UVB fueron 6,6 x 106; 5,4 x 106; 1,5 x 106 y 2,8 x 108 CI/mL para los tiempos de exposición 15, 30, 45 y 60 minutos respectivamente (Tabla 2). La CL50 media para el virus expuesto durante 45 minutos fue más baja que las determinadas para el virus irradiado durante menores lapsos. Sin embargo, los límites de confianza para esta concentración fueron muy amplios, cruzándose con los determinados para el virus no expuesto y expuesto durante 15 y 30 minutos, lo que sugiere que aunque el valor medio es menor, no fueron diferentes entre sí. La amplitud de los límites de confianza para este tratamiento sugiere una alta dispersión de los datos utilizados para el análisis Probit. Las CL50 obtenidas para el virus expuesto a la radiación UVB durante 15, 30 y 45 minutos no fueron diferentes entre sí, pero el virus irradiado por 60 minutos presentó un aumento significativo de la CL50 (Tabla 2).
Estos resultados sugieren que si las partículas virales son expuestas a la radiación UVB por un tiempo de 60 minutos, será necesario incrementar 127 veces la concentración viral con respecto a la requerida para el virus no expuesto con miras a alcanzar el 50% de mortalidad de larvas neonatas. Este incremento en la CL50 indica que la radiación ultravioleta tipo B afecta negativamente las partículas virales, causando una reducción en la actividad insecticida del agente infeccioso después de 60 minutos de exposición.
Esta franja del espectro ultravioleta es la radiación con más energía que tiene la propiedad de penetrar la biosfera aunque es absorbida en parte por el ozono atmosférico (Niegel y Dylan 2003). La radiación ultravioleta B es absorbida por muchas moléculas biológicas incluyendo macromoléculas como el ADN, provocando lesiones directas. El daño directo resulta de la formación de fotoproductos tales como dímeros de pirimidinas (aparición de enlaces covalentes entre bases pirimidímicas adyacentes: citosina-citosina o citosina-timina), hidratos de pirimidina y entrecruzamientos entre el ADN y las proteínas (Diffey 1991, en Devotto y Gerding 2003).
Varios estudios han demostrado el efecto deletéreo de la radiación ultravioleta tipo B sobre la viabilidad de microorganismos biocontroladores. Griego et al. (1985) determinaron el efecto de la radiación ultravioleta monocromática sobre el NPV de Orgya pseudotsugata McDunnough, 1921, exponiendo partículas virales a las longitudes de onda del espectro del ultravioleta B 290 nm, 300 nm, 310 nm y 320 nm. Todas las radiaciones causaron inactivación del virus, pero dicho efecto fue inversamente proporcional a la longitud de onda, debido a que a una menor longitud de onda se tienen fotones con mayor energía y mayor capacidad de causar daños directos en los organismos. También se han realizado estudios con hongos, tal es el caso de Paecilomyces fumosoroseus (Wize, 1904), para el cual la viabilidad de sus conidios fue reducida a la mitad luego de la exposición a la radiación ultravioleta tipo B (280 a 320 nm) por 34 minutos (Smits et al. 1996). De igual forma, para Beauveria bassiana y N. rileyi, se encontró una completa inactivación de sus conidios, cuando estos fueron expuestos por 20 segundos y 10 minutos respectivamente, a la radiación ultravioleta tipo B (λ= 302 nm) (Edgington et al. 2000; Pavone 2003).
Efecto de la radiación ultravioleta tipo C
Las concentraciones letales medias del virus expuesto a la radiación UVC fueron 4,1 x 106; 1,7 x 107; 4,7 x 107 y 1,6 x 108 CI/µL para los tiempos de exposición 15, 30, 45 y 60 minutos respectivamente (Tabla 3). El análisis de los límites de confianza detectó un incremento significativo de la CL50 a partir de los 30 minutos y a medida que aumentó el tiempo de exposición a la radiación UVC. Pasados 60 minutos de irradiación, la concentración letal media se incrementó 72,7 veces, confirmando la pérdida de actividad insecticida a causa de los efectos nocivos de la radiación. La CL50 determinada para el virus irradiado durante 60 minutos a la luz ultravioleta tipo C fue superior a las obtenidas para el virus expuesto durante el mismo período a la luz tipo B y A, lo que sugiere que la radiación UVC causa una mayor inactivación, resultado que está relacionado con la mayor energía de sus fotones (WHO 1994).
Valores de la concentración letal media (CL50) del nucleopoliedrovirus de Spodoptera frugiperda, no expuesto y expuesto a radiación UVC en larvas neonatas de S. frugiperda.
La radiación UVC cuya longitud de onda oscila entre 100 y 280 nm es la de menor longitud de onda y por ende, mayor energía dentro del rango ultravioleta, razón por la cual es la más nociva dentro del espectro ultravioleta. Sin embargo, es absorbida por el oxígeno y el ozono en la atmósfera, impidiendo que penetre y cause su efecto deletéreo sobre los seres vivos (Niegel y Dylan 2003).
El tiempo de exposición a la radiación UVC (λ= 254 nm) requerido para afectar significativamente la viabilidad de algunos agentes de biocontrol normalmente es muy corto. Devotto y Gerding (2003) reportaron para un aislamiento de Metharhizium anisoplie (Metchsnikoff) Sorokin, una reducción del 93% en la germinación de los conidios luego de 40 segundos de exposición a la radiación UVC. Saxena et al. (2002) observaron una pérdida del 80% de viabilidad de Bacillus thuringiensis subsp. kurstaki después de dos minutos de exposición a este tipo de radiación. El efecto de la radiación UVC sobre los baculovirus ha sido evaluado para diferentes especies virales encontrándose respuestas variadas dependiendo del aislamiento viral. Batista et al. (2001) determinaron que la exposición de un aislamiento de nucleopoliedrovirus de Anticarsia gemmatalis Hübner, 1818 AgMNPV durante cinco minutos a una lámpara germicida UVC (253,7 nm) causó una pérdida del 73% de la actividad biocontroladora del virus. Estos resultados demostraron la alta susceptibilidad de este virus a dicha radiación.
Actividad después de la exposición a la radiación
Cuando se evaluó la concentración viral más alta (109 CIs/mL) o las concentraciones más bajas (106 y 105 CIs/mL) con los tres tipos de radiación, el efecto del tiempo de exposición se traslapó, debido posiblemente a las muy altas o muy bajas mortalidades causadas por dichas concentraciones. La concentración 107 CIs/mL fue entonces seleccionada para establecer los porcentajes remanentes de actividad original del virus expuesto a la radiación (Fig. 1), como una medida de la inactivación de las partículas virales por efecto de la luz ultravioleta, debido a que con esta concentración se logró observar claramente el efecto negativo de las tres radiaciones y su relación directa con el tiempo de exposición.
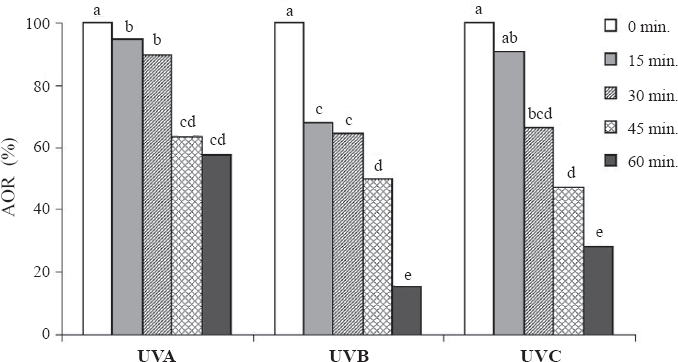
Actividad original remanente (AOR) después de la exposición del aislamiento NPV001 a la radiación ultravioleta tipo A, B y C. Tratamientos con la misma letra no presentan diferencias según prueba de Tukey 95%.
El virus expuesto a la radiación UVA presentó una actividad original remanente del 57,89% después de 60 minutos de irradiación, es decir, un 42,11% de inactivación. Con las longitudes de onda en el espectro B y C se obtuvieron actividades originales remanentes del 15,30% y del 28,57%, las cuales no fueron significativamente diferentes (P > 0,05), sugiriendo que el aislamiento NPV001 de nucleopoliedrovirus es igualmente susceptible a los dos tipos de radiación UV. Por el contrario, la actividad original remanente del virus expuesto durante 60 minutos a la radiación tipo A fue estadísticamente superior (P < 0,05) a la obtenida con las radiaciones tipo B y C, resultado que indica que aunque la radiación UVA afectó las partículas virales, su efecto fue significativamente menor al causado por la radiación UVB y UVC, lo que posiblemente está relacionado con que es la radiación con menor energía (Griego et al. 1985).
La actividad viral se redujo progresiva y significativamente a medida que aumentó el tiempo de exposición a los tres tipos de radiación ultravioleta (Fig. 1), lo que indica que posiblemente el aislamiento NPV001 es susceptible a longitudes de onda dentro de todo el espectro ultravioleta. Este resultado sugiere la necesidad de incluir en la formulación, coadyuvantes que protejan las partículas virales de la radiación tipo A y B, a las cuales se verá expuesto el virus bajo condiciones de campo.
En trabajos similares se ha evaluado el efecto de la radiación UV utilizando todo el rango de radiación y evaluando inclusive algunas alternativas de protección. Por ejemplo, Martignoni y Iwai (1985) evaluaron el efecto de la radiación ultravioleta cubriendo el rango entre 250 nm y 360 nm, es decir los tres tipos de radiación UV, sobre un NPV de Orgya pseudotsugata (OpMNPV). Después de cuatro horas de exposición del virus a la radiación se presentó una inactivación total de las partículas virales, evidenciada en una pérdida de la actividad insecticida. Sin embargo, cuando el virus fue mezclado con melaza o con el abrillantador óptico Tinopal DCS, el virus mantuvo el 94,80% y el 96,67% de su actividad insecticida inicial respectivamente, sugiriendo que dichas sustancias brindaron una efectiva protección frente a la radiación UV. Ignoffo y Batzer (1971) determinaron la susceptibilidad de un aislamiento de nucleopoliedrovirus de Helicoverpa zea (Boddie, 1850) (HzNPV) a la radiación ultravioleta artificial (215 nm a 400 nm) y natural, determinando que el virus expuesto a los dos tipos de radiación presentó un comportamiento similar con un 70% de inactivación después de cuatro horas de exposición. A partir de las cuatro horas la velocidad de inactivación se redujo, manteniendo el virus, un 10% de la actividad original después de 192 horas de exposición.
Agradecimientos
Los autores expresan su agradecimiento al Ministerio de Agricultura y Desarrollo Rural por el apoyo financiero para la presente investigación y al Dr. Miguel López-Ferber por su acertada y generosa asesoría.
