Abstract
Entomopathogenic nematodes (EPN) of the groups Heterorhabditidae and Steinernematidae are used as potential control agents of soil pests, being found in many habitats worldwide according to studies of their distribution. We collected soil samples in four Colombian departments (Quindío, Risaralda, Caldas, and Cauca) in order to isolate and identify native EPN strains associated with whitegrub (Coleoptera: Melolonthidae) and burrower bug (Hemiptera: Cydnidae) Cyrtomenus bergi soil pests. EPN isolation was done through the Galleria mellonella (Lepidoptera: Pyralidae) bait method. After verifying the entomopathogenicity of the samples using Koch's postulates, we multiplied, stored and identified the EPN. We analyzed 284 samples (300 g of soil each) collected in 23 sites in 15 crops. Pathogenic and saprophytic nematodes were present in 17 samples. PCR technique lead to the identification of Steinernema kraussei Steiner (Rhabditida: Steinernematidae) coming from of two samples, one from Cassava (ex Manihot esculenta L.) in Cauca and the second one from Inga spp. in Risaralda, being these the first record of the species for the country.
Introducción
El chinche de la viruela Cyrtomenus bergi Froeschner, 1960 (Hemiptera: Cydnidae) y algunos géneros del complejo de chisas (Coleoptera: Melolonthidae) como Astaena, Barybas, Ceraspis, Clavipalpus, Isonychus, Macrodactylus, Manopus, Phyllophaga y Plectris han sido registradas en los últimos 20 años en Colombia por su importancia agrícola (Bellotti et al. 1999), siendo consideradas plagas polífagas que atacan cultivos como cebolla (Allium cepa L.), maíz (Zea mays L.), maní (Arachis hypogaea L.), caña de azúcar (Saccharum officinarum L.), café (Coffea arabica L.), espárragos (Asparagus officinalis L.), yuca (Manihot esculenta Crantz), sorgo (Sorghum bicolor L.), palma de aceite (Elaeis guineensis Jacq.), papa (Solanum tuberosum L.), pastos, forestales, hortalizas, frutales, ornamentales y leguminosas, entre otros (Lacerda 1983; Bellotti y García 1983; Herrera 1988; Rueda et al. 1993; Pardo-Locarno et al. 1995; Riis y Esbjerg 1998) y ocasionando disminución en el rendimiento, calidad y cantidad de estos productos (Bellotti et al. 1999; Pardo 2002; CIAT 2004).
El control químico de estas plagas se descarta como única forma de manejo a causa de los altos costos económicos, ecológicos y por la destrucción de los enemigos naturales que controlan otras plagas asociadas al cultivo, lo que muestra que a pesar de que puede reducir la población del insecto, no es muy efectivo ni recomendable (Carballo y Saunders 1990; Robertson et al. 1997; Bellotti et al. 1999; Pardo 2002), por lo que existe gran interés en buscar técnicas de control efectivas como son los agentes de control biológico, que no vayan en contra de la salud humana y el ambiente.
El control microbiológico de plagas de la familia Scarabaeidae fue propuesto hace más de 100 años. Las bacterias, hongos, virus y entomonematodos han sido usados en la actualidad en programas de control biológico, pero el uso de estos para escarabajos es reducido. Esta limitación se debe a carencia de filtrados apropiados, métodos de producción inadecuados, métodos de aplicación y su uso inapropiado. A comienzos del siglo pasado aumentó el interés en control microbiológico y aunque su aplicación en campo encontró muchas dificultades, actualmente los programas de control microbiano más exitosos se basan en patógenos con alta especificidad. Aunque existe variabilidad en la virulencia de los patógenos es posible encontrar variantes apropiadas para el control de las plagas mencionadas, mediante avances tecnológicos de producción, reducción de costos y desarrollo de métodos de aplicación apropiadas para el uso de los patógenos, que faciliten al control microbiológico extenderse y establecerse como un método adecuado para los escarabajos plaga (Jackson 1993). Uno de estos agentes de control son los nematodos entomopatógenos (NEP's), especialmente de las familias Steinernematidae y Heterorhabditidae (Rhabditida). Estos presentan una serie de atributos ventajosos como controladores, por lo cual son una excelente alternativa para ser empleados en el Manejo Integrado de Plagas (Luque 2001).
Un ejemplo del uso de los entomonematodos es el caso de la introducción de Popillia japonica Newman, 1841 en Estados Unidos, plaga que se multiplicó rápidamente, devastando árboles frutales y plantas ornamentales y que se encontró infectada con el nematodo Steinernema glaseri (Steiner, 1932) (Rhabditida: Steinernematidae) cerca de Haddonfield, New Jersey en el año 1929. Experimentos con este nematodo se realizaron en los años 30, culminando con un programa de cría masiva donde 3,6 billones de nematodos fueron liberados a través del estado de New Jersey, recuperándose larvas infectadas en 72 de 73 parcelas dos semanas después de la aplicación, registrándose un parasitismo que osciló entre 0,3 a 81%, adicionalmente se determinó una persistencia de 8,5 años en las parcelas tratadas (Jackson 1993; Glaser et al. 1940; Glaser 1931; Glaser y Farrell 1935; Glaser y Fox 1930).
En Colombia, aproximadamente en los últimos 13 años se han realizado investigaciones con especies nativas y foráneas, destacándose entre estos trabajos el control del chinche C. bergi con Heterorhabditis bacteriophora Poinar, 1975 (Rhabditida: Hetrorhabditidae) (Barberena y Bellotti 1998), Steinernema carpocapsae (Weiser, 1955) (Rhabditida: Steinernematidae) (Caicedo y Bellotti 1994) y S. feltiae (Filipjev, 1934) y H. bacteriophora en invernadero (Melo et al. 2006b). También se usó para el control de la plaga Sagalassa valida Walker, 1735 (Lepidoptera: Glyphipteridae) en plantaciones de palma de aceite (Ortiz 1994), para el control de chisas Ancognatha scarabaeoides Erichson, 1847 (Navarro y Vélez 1999), y contra Phyllophaga obsoleta Blanchard, 1850 y Cyclocephala sp. (Londoño 1999), sobre Phyllophaga sp., P. menetriesi (Blanchard, 1850) y Anomala cincta Say, 1835 (Melo et al. 2006b). En el control de broca del café Hypothenemus hampei (Ferrari, 1867) (Coleoptera: Scolytidae) con los nematodos S. feltiae y H. bacteriophora (Molina-Acevedo y Núñez-López 2003) y S. feltiae sobre Tecia solanivora Povolny, 1973 (Lepidoptera: Gelechiidae) en campo (Luque et al. 2006).
Una de las formas de captura de estos nematodos es por medio del insecto cebo Galleria mellonella (L., 1758) (Lepidoptera: Pyralidae), el cual presenta más susceptibilidad ante estos patógenos que los insectos hospederos comunes. Este provee un excelente medio tanto para detección de nematodos en el sitio, como para procesar muestras en laboratorio (Bedding y Akhurst 1975) o hacer multiplicación a pequeña escala. Aún así, los nematodos presentan adaptaciones que obligan a iniciar nuevos muestreos y registro de especies, así como a mejorar los procedimientos y técnicas de extracción e incremento, además de las de fijación y preservación de los ejemplares; dirigiendo estos esfuerzos a la tenencia de individuos jóvenes y adultos para su identificación. Se debe tener en cuenta que los mejores sitios para hacer muestreos son los relacionados con el nicho de posibles hospedantes, al igual que áreas de descomposición orgánica activa y abundante, como compost, madera envejecida, bajo cortezas de troncos, estiércol y en caso de cultivos, sitios de ataque de los insectos. Suelos de áreas boscosas frecuentemente contienen parásitos obligados tipo Rhabditidae, Steinernematidae y Heterorhabditidae, así como predadores y omnívoros tipo Mononchida o Dorylaimida (Luque et al. 2006).
Por lo anterior el Proyecto de Control Integrado de Plagas Subterráneas, desarrollado en el Centro Internacional de Agricultura Tropical (CIAT), situado en Palmira, consideró usar estos controladores como alternativa para el manejo de plagas, desarrollando metodologías para hallar cepas o especies nuevas en campos con plagas blanco; adaptando procedimientos de multiplicación y almacenamiento en condiciones de laboratorio. Para esto se planteó la siguiente investigación que tiene como objetivo, buscar e identificar nematodos entomopatógenos en regiones de Colombia con cultivos atacados por plagas subterráneas de importancia económica.
Métodos
Ubicación y cultivos
Las muestras de suelo se tomaron de varias localidades de los departamentos colombianos de Quindío, Risaralda, Caldas y Cauca (Fig. 1), a inicios del año 2002; con estos sitios abarcaron amplios rangos de altitud, temperatura y precipitación (Tabla 1). Por reportes de ataque de las plagas citadas en la introducción, se seleccionaron cultivos como cebolla (Allium fistulosum L.), yuca (Manihot esculenta L.), pastos, maíz (Zea mays L.), maní (Arachys hipogaea L.), fríjol (Phaseolus vulgaris L.), y cultivos que no presentaban aplicaciones de insecticidas como son maracuyá (Passiflora edulis L.), mango (Manguifera indica L.), árbol del pan (Artocarpus altilis L.), guamo (Inga spp.), plátano (Musa sp.), mandarina (Citrus sp.), limón (Citrus sp.), café y aguacate (Persea americana L.).
Datos de los sitios de colección de las muestras de suelo y cultivos asociados para la búsqueda de nematodos entomopatógenos en cuatro departamentos de Colombia.
Mapa de los departamentos de Quindío, Risaralda, Caldas y Cauca (en color gris), donde se tomaron muestras de suelo para búsqueda de nematodos entomopatógenos.
Muestras de suelo
Un total de 10 muestras por lote con tres submuestras de cada sitio (1000 cm³), se tomaron a una profundidad entre 15 a 20 cm. Para la extracción del suelo se utilizaron barrenos de 4,5 cm de diámetro. Estas muestras se mantuvieron en incubadora, en oscuridad y a 15°C, para ser procesadas. Para el análisis fisicoquímico de cantidad de materia orgánica, pH y textura se tomaron muestras a una profundidad de 15 a 20 cm, recuperando un mínimo de 500 g de suelo. Estas muestras fueron analizadas en la unidad de suelos del Centro Internacional de Agricultura Tropical (CIAT) en Palmira, Colombia.
Insecto Cebo
Para la captura de NEP's del suelo se utilizaron larvas de último instar de G. mellonella (Bedding y Arkhust 1975), insecto muy susceptible al ataque de estos organismos. La cría se mantenía en una cámara con 67% de humedad relativa y 29°C de temperatura, se alimentó con una dieta constituida con: 500 g salvado de trigo, 145 g de levadura de cerveza, 72 g de cera de abejas, 150 ml de glicerina, 270 ml de miel de abejas y formaldehído. Los adultos se mantuvieron en frascos grandes de vidrio para la oviposición; y, los huevos y larvas en recipientes de acrílico rectangulares de uso doméstico (24 x 32 x 11 cm). El tiempo de obtención de estas larvas fue aproximadamente 40 días.
Búsqueda, reactivación y almacenamiento de NEP's en laboratorio
Se dispusieron 300 g de suelo en vasos plásticos de 500 ml alcanzando el 90% de su capacidad donde se colocaron 10 larvas de G. mellonella manteniéndolas en oscuridad total a 23°C por cinco días. Este procedimiento se repitió tres veces. Posteriormente las larvas se extrajeron del suelo, y se colocaron en cajas de Petri (60 x 15 mm) sobre papel filtro humedecido y se dejaron por aproximadamente cinco días en cámara de maduración, para luego ser colocadas en una pequeña trampa White modificada (Kaya y Stock 1997), esperando a que los nematodos salieran de la larva y migraran al agua. La suspensión obtenida se lavó con formaldehído al 0,05% y se colocó en tubos de ensayo. Los nematodos rescatados se colocaron en cajas de Petri con arena, donde se introdujeron larvas de G. mellonella para verificar si a los cinco días había reinfección de acuerdo con los postulados de Koch. Este procedimiento se repitió dos veces.
Identificación de los NEP's
Tradicionalmente se ha usado morfometría, morfología y cruces para identificación métodos que necesitan especialistas y que además de ser complicados, toman mucho tiempo (Poinar 1990; Kaya y Stock 1997; Nguyen y Smart 1997). En la actualidad se usan técnicas moleculares como RAPD y RFLP que han sido exitosas para la identificación de NEP's de la familia Steinernematidae (Stock et al. 2001). Para este caso se usó el método de PCR.
La extracción del ADN de los NEP's se realizó con el kit Qiagen (GMBH Alemania). Una muestra de 200 µl (ca. 2500-3500 Infectivos juveniles) de los nematodos almacenados fue tratada en 2 ml del kit. Después de esto el ADN se almacenó a -30 °C. La amplificación del ADN extraído se hizo en un volumen de reacción de 100 µl para cada cepa. Las muestras se amplificaron en un termociclador (Perking Elmer Cetus). Para la fijación se graduó el termociclador a 42°C para H. bacteriophora y 55°C para S. feltiae, por 1 minuto y a 72°C por 1,5 minutos, respectivamente. Como paso final se dejó la muestra 1 minuto a 94°C, seguido de 3 minutos en temperatura de fijación y 5 minutos a 72°C, para asegurar que los últimos productos de la amplificación se alargaran completamente. Al finalizar los 40 ciclos en el termociclador las muestras se almacenaron a 4°C, según la metodología de Reid y Hominick (1993). Se realizaron electroforesis de las muestras de ADN y de la amplificación de PCR para estar seguros de la confiabilidad del método en un gel de agarosa a 180 V por 35 minutos.
La digestión del amplificado se realizó con aproximadamente 200 µl del producto de PCR con enzimas y sus buffers a 37°C por 3 horas en el termociclador. En este estudio se usaron las enzimas Ali I, Hae III (Haemophilus aegytius), Hind III (Haemophilus influenzae) (Eurogentec inc.), y Dde I (Desulfovibrio desulfuricans), Hha I (Haemophilus haemolyticus), Hinf I (Haemophilus influenzae), Hpa II (Haemophilus aphrophilus), Rsa I (Acidiphilium facilis) y Sau 3Al (Staphylococcus aureus) (Amersham Biosciences). Los fragmentos resultantes fueron separados en gel de agarosa (2%), se fotografiaron y compararon con los patrones para esta especie, considerándose iguales las bandas que coincidieron al 100% (Fig. 2).
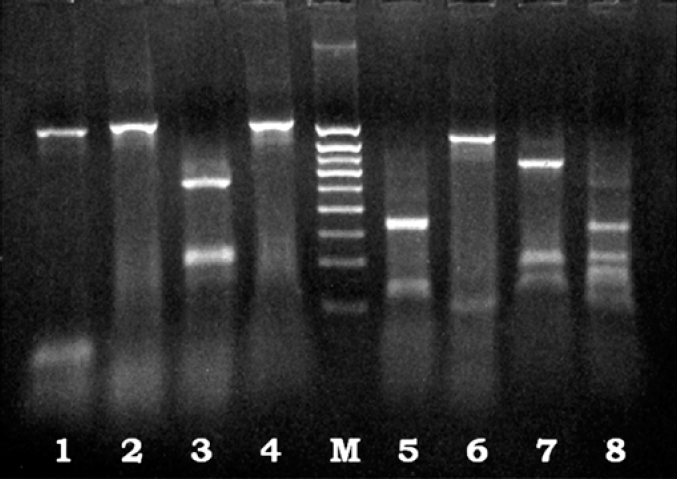
PCR de Steinernema kraussei de productos de la región ITS digerida con ocho enzimas de restricción: 1. Dde I: Desulfovibrio desulfuricans, strain Norway; 2. Hae III: Haemophilus aegytius; 3. Hha I: Haemophilus haemolyticus; 4. Hind III: Haemophilus influenzae Rd; M. Marcadores de peso molecular de las bandas (1000, 800, 700, 600, 500, 400, 300, 200, 100 pares de bases); 5. Hinf I: Haemophilus influenzae Rf; 6. Hpa II: Haemophilus aphrophilus; 7. Rsa I (Afa I): Acidiphilium facilis; 8. Sau 3 AI.: Staphylococcus aureus 3A.
Resultados y Discusión
De los 23 sitios muestreados en los seis municipios 74% presentaron nematodos encontrándoseles en 17 cultivos (Tabla 2). Al evaluar el porcentaje mortalidad producida por los nematodos sobre las larvas de G. mellonella, se observaron valores relativamente bajos, siendo aparentemente un comportamiento normal en cepas recién aisladas de campo (Parada pers. com.) (Tabla 3).
Número de muestras de suelo con nematodos asociados a la rizósfera de cultivos comerciales en cuatro departamentos de Colombia.
Síntomas en larvas de Galleria mellonella, infectadas con los nematodos aislados. *: Muestras positivas para Steinernema kraussei.
Una muestra del Cauca (en yuca) y otra de Caldas (en guama) pertenecían a la especie Steinernema kraussei (Steiner, 1923) (Rhabditida: Steinernematidae), constituyéndose en el primer registro para Colombia. Esta especie encontrada originalmente sobre Cephaleia abietis L. (Hymenoptera: Pamphiliidae) en Alemania, está asociada simbióticamente a la bacteria Xenorhabdus bovienii (Enterobacteriaceae) y fue el primer nematodo entomopatógeno descrito por Steiner en 1923, inicialmente como Aplectana krausse. Posteriormente Travassos, en 1927, lo transfirió al género Steinernema. El diagnóstico de los infectivos juveniles (IJ3), muestra un cuerpo con 797 a 1102 micrómetros de longitud, envuelto en la cutícula del estado J2. Presenta cuatro papilas cefálicas, papilas labiales indistintas, abertura oral cerrada, esófago colapsado, bulbo basal más alargado que en adultos y poro excretorio que se abre cerca de la mitad del esófago. Esta especie de nematodo se encuentra comercialmente distribuida para el control de plagas como el gorgojo negro del vino Otiorhynchus sulcatus (F., 1775) (Coleoptera: Curculionidae) en diferentes partes del mundo (Boemare 2002; Adams y Nguyen 2002). Larvas de G. mellonella de estas muestras infectadas con los NEP's se tornaron de color crema, y la mortalidad fue del 100% después de 96 h de inoculación
Según el análisis de suelo las regiones donde se identificó la especie S. kraussei presentan pHs de 6,4 en el Cauca y entre 5,2 a 5,8 en Caldas, con una textura franco arcillosa para Cauca y desde franco hasta franco-arcillo-arenosa, para Caldas; la cepa se encuentra en suelos con características que están dentro de los rangos de pH de 4,0 a 8,0, registrados por otros autores como óptimos para los steinernemátidos (Koppenhöfer et al. 1996; Palacios 2002; Parada 2006), lo que muestra que estos NEP's presentan condiciones que les permiten adaptarse dentro del rango de los 2086 y 1799 msnm y los 23,5°C promedio.
Footnotes
Agradecimientos
Este trabajo fue financiado por el Ministerio de Cooperación Económica (BMZ) de Alemania. Los autores agradecen a Carlos Julio Herrera, Rodrigo Zúñiga, Catalina Ramírez y Rómulo Riascos por su colaboración en la realización de esta investigación.
