Abstract
The use of entomonematodes (EN) as a biological control, is a very valuable tool within an Integrated Pest Management program. The mass production in laboratory is a limiting factor and is necessary to develop studies about behavior, pathogenicity and biological activity on insect pest populations in laboratory, needed to seek an easy and economic alternatives of in vivo mass production. This paper describes an in vivo production technique of three EN (Rhabditida: Steinernematidae) Steinernema carpocapsae Brasil, Steinernema carpocapsae All strain and Steinernema cubanum, in two insect host: Galleria mellonella (Lepidoptera: Pyralidae) and Bombyx mori (Lepidoptera: Bombycidae) and two infection systems: topical and injection, to standardize parameters of production and to realize pathogenicity proofs. A randomized experimental design in a factorial arrangement 3x2x2, 12 treatments each one composed by ten larvae was evaluated. Daily and accumulative production of EN stages (JI, J4, males and females/larvae) and host production percent were observed every 24 hours, from EN emergency to depletion host. The treatments S. carpocapsae Brasil by topical system in G. mellonella and S.carpocapsae All strain by injection system in B. mori, presented the highest accumulative production 149.258 JI/larvae and 139.756 JI/larvae respectively. It also did obtain the highest production for S. carpocapsae All strain in B. mori by injection system (139.880 JI). S. cubanum was not reproduced under any infection system in B. mori, but in G. mellonella, being an specific host. G. mellonella by topical system and B. mori by injection system, registered the highest level of production of JI between third to fifth day after infection time to harvest the EPN production. G. mellonella is ratified as the most effective host to reproduce EN, however B. mori can be used as an alternative of production in vivo of EN.
Keywords
Introducción
La efectividad demostrada de los agentes microbianos, como hongos y bacterias, en el control de plagas para la protección de cultivos, el descubrimiento de otros agentes y la implementación de técnicas para su producción, formulación y control de calidad, unidas con la necesidad de minimizar el impacto negativo que causa el uso de insecticidas en el medio ambiente, han permitido que los insecticidas microbianos se posicionen a un nivel alto en programas de Manejo Integrado de Plagas (MIP) (Lacey y Goettel 1995; Georgis 1997), llegando a ser más competitivos con el control químico tradicional (Georgis 1997). Los entomonemátodos (EN), principalmente de los géneros Steinernema y Heterorhabditis, representan una parte importante del espectro de los más recientes biocontroladores, con resultados satisfactorios en el control de insectos plaga habitantes del suelo (Ehlers 1996).
Uno de los principales insectos hospedantes que ha sido probado comúnmente para producción in vivo, de numerosas especies de los géneros Steinernema y Heterorhabditis, es Galleria mellonella (Lepidoptera: Pyralidae) (Dutky 1959). Este hospedante ha mostrado características buenas para la infección, parasitismo y penetración de EN (Poinar Jr y Himsworth 1967, Stock 1998), ratificándose hasta hoy como hospedante por su producción alta de EN. La producción in vivo de EN para propósitos comerciales en larvas de G. mellonella permite obtener promedios de producción de 30.000 a 50.000 juveniles infectivos (JI) por larva (Poinar 1979), llegando a promedios de producción de 200.000 JI por larva (Dutky et al. 1964). Sin embargo, este sistema de producción ofrece volúmenes mínimos en comparación con la producción masiva in vitro con el uso de medios artificiales (Wouts 1981); no obstante, se debe continuar mejorando su producción in vivo estandarizándola e implementando el almacenamiento y conservación de EN (Flanders et al. 1996). Con base en lo anterior y con el fin de conocer algunos parámetros de producción de EN en laboratorio para la realización de estudios básicos, se evaluaron en Bombyx mori y G. mellonella dos sistemas de infección que permitieran obtener principalmente JI para bioensayos en laboratorio.
Materiales y Métodos
Material biológico
Las especies de EN utilizados, Steinernema carpocapsae Brasil, S. carpocapsae All strain y S. cubanum, fueron suministrados por el Dr. Bernard Briscoe del CABI (Centre for Agriculture and Biosciences International. CABI Biosciences, Lane, Egham. Surrey. Inglaterra).
Se utilizaron larvas de Galleria mellonella de último ínstar con un promedio de peso de 0,20 ± 0,018 g, obtenidas de la cría del laboratorio de la Disciplina de Entomología de Cenicafé y larvas de cuarto ínstar de B. mori, con un peso de 2,31 ± 0,12 g, suministradas por la empresa Cokosilk de Pereira, Colombia.
Producción de JI para el bioensayo
Los JI se multiplicaron y activaron de acuerdo con la metodología descrita por Poinar (1979), donde se infectaron larvas de último ínstar de G. mellonella (Fab.) (polilla mayor de las colmenas) con JI, mediante el sistema de infección topical por cada EN, se incubaron a 25°C y se colocaron en cámara seca; finalmente, se emplearon las trampas White (White 1927) en las mismas condiciones. Los JI emergidos se almacenaron a una temperatura de 12°C durante un tiempo no mayor a 5 días.
Desinfección superficial y ajuste de concentraciones de JI
Los JI se dejaron a temperatura ambiente entre 20 y 24°C, durante 24 horas (tiempo y temperatura de acondicionamiento). Posteriormente, a 1.000 JI/ml, se adicionó 1,5 ml de solución desinfectante (Timerosal, Sigma®) al 0.1% en agua destilada estéril (ADE) durante 10 minutos; lo anterior permite la desinfección superficial del JI. Finalmente, se retiró el volumen máximo del desinfectante y se reemplazó por solución salina en ADE (NaCl 0,5%) ajustando a las concentraciones deseadas determinadas mediante conteos directos de JI, para el caso del sistema de infección topical e inyección.
Infección de hospedantes
La infección se realizó mediante dos sistemas; topical, aplicando una concentración por EN utilizado de 200 JI/ml por caja de Petri de 9 cm de diámetro x 1.5 cm, sobre papel filtro Whatman # 1 humedecido con 1 ml de ADE y luego colocando 10 larvas de cada hospedante por caja de Petri. El segundo fue por inyección, utilizando una jeringa de 1 ml, inyectando JI con una concentración de 25 ± 5 JI/20ml por larva en los últimos segmentos de la región posterior ventral de la larva. Todas las larvas una vez infectadas, se llevaron a 23°C en oscuridad constante durante 48 horas, de acuerdo con la metodología de Taylor y Shields (1990).
Desarrollo de síntomas, emergencia y conteos diarios de entomonemátodos
Las larvas de los hospedantes se colocaron en cajas de Petri sobre papel filtro (cámara seca), manteniendo una temperatura de 23°C de 96 hasta 120 horas, tiempo en el cual se observó la sintomatología típica de infección por EN del género Steinernema: coloración amarilla a marrón. Las larvas que no presentaron dicha sintomatología se descartaron.
Al final de las 120 horas, mediante el uso de trampas de White, las cuales facilitan la emergencia y recuperación de EN, se colocaron individualmente las larvas de G.mellonella y B. mori que presentaron sintomatología, llevándolas a una temperatura de 23°C. Una vez se registró la emergencia de JI, se colectaron diariamente, realizando conteos hasta observarse un agotamiento en su producción. Mediante lavados sucesivos con agua destilada de los hospedantes de cada trampa "White", se vertió el agua de lavado en una probeta graduada para establecer el volumen total empleado en la recuperación de JI y otros estados de EN que se colectaron en el agua de lavado (J4 "preadultos", hembras y machos). Posteriormente, el volumen total se agitó uniformemente y se tomó un volumen de 100 µl, llevándose a una cámara de recuentos en acrílico de 4 x 3 cm con 49 cuadrantes, para contabilizar el número de JI, lo anterior se hizo seis veces por repetición. Conociéndose el volumen total y el número total de estados en 100 µl, determinándose el número de estados por ml, se procedió a hacer el cálculo del número de estados de EN por larva/día.
Diseño experimental y variables evaluadas
Se utilizó un diseño completamente aleatorio, dispuesto en arreglo factorial 2x3x2, cuyos factores fueron los dos hospedantes, tres especies de EN y dos sistemas de infección, para un total de 12 tratamientos (Tabla 1). Diferencias significativas entre tratamientos, para las variables producción diaria y producción acumulada por larva se evaluaron mediante análisis de varianza y prueba de comparación de promedios de Tukey al 5% de significancia. Dichas variables por tratamiento fueron halladas mediante promedios. Como variable adicional se tuvo en cuenta el porcentaje de producción por hospedante.
Resultados y Discusión
En general, las variables evaluadas, producción diaria y producción acumulada de JI, mostraron diferencias entre hospedantes, sistemas de infección y especies de EN. Las producciones mayores de los dos EN de mayor multiplicación, S. carpocapsae Brasil y S. carpocapsae All strain, no coincidieron por hospedante, ni por sistema de infección; sin embargo, el hospedante G. mellonella, bajo el sistema topical para todas las especies evaluadas, se ubicó dentro de las producciones mayores. En este orden de ideas, la producción varió en los hospedantes de acuerdo con la especie de EN utilizada, donde S. carpocapsae Brasil obtuvo su máxima producción en G. mellonella y S. carpocapsae All strain obtuvo su máxima producción en B. mori (Tabla 2).
Tratamientos constituidos para la producción in vivo de entomonemátodos
Producción de juveniles infectivos
Para la variable producción acumulada de JI por larva, se presentaron diferencias estadísticas significativas entre tratamientos (p < 0,05). Al realizar la prueba de comparación de promedios, se encontró que el tratamiento con mayor producción S. carpocapsae Brasil / topical / G. mellonella, fue estadísticamente igual a los tratamientos con las mayores producciones (Tabla 2a). No obstante, los tratamientos S.carpocapsae Brasil / Topical / G. mellonella y S. carpocapsae All strain / inyección/ B. mori por el volumen de producción obtenido de JI por larva, con 149.258 y 139.756 respectivamente, registran producciones cercanas a las encontradas por Dutky et al. (1964), con 160.000 JI y 190.000 JI para Steinernema carpocapsae Mexican strain en G. mellonella. Es importante resaltar que la máxima producción total por larva, la obtuvieron estos mismos tratamientos S. carpocapsae Brasil / topical / G. mellonella y S. carpocapsae All strain / inyección / B. mori, con 270.000 y 395.880 JI por larva, respectivamente, producciones que están incluso por encima de las registradas por Jansson (1996) quien obtuvo en larvas de G. mellonella un máximo de 238.692 JI por larva con dos especies del género Heterorhabditis (Bacardis y FL2122) con 137.229 y 238.692, respectivamente. Esta producción se refleja en la producción diaria máxima por larva con 67.800 y 108.200 JI/día respectivamente, siendo los tratamientos de mejor comportamiento para su implementación. Las producciones acumuladas para cada tratamiento (Fig. 1) se ajustaron a diferentes modelos lineales, siendo el modelo cuadrático, con los mayores coeficientes de correlación para todos los tratamientos, el que mejor explicó el comportamiento de producción, sin necesidad de incurrir en transformación de datos (Tabla 3), presentando los tratamientos S. carpocapsae Brasil / topical / G. mellonella y S. carpocapsae All strain / inyección / B. mori, las mayores tasas de producción de JI (55.528 y 31.247 respectivamente, ratificando sus posibilidades de ser utilizadas en producción masiva in vivo.
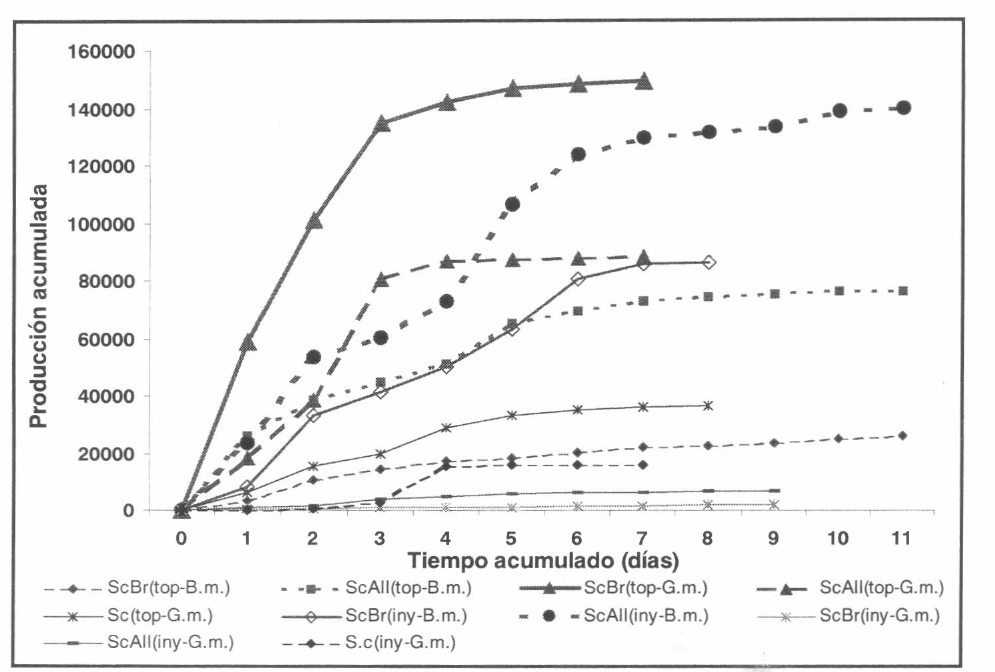
Producción acumulada en el tiempo de JI/larva por hospedante y sistema.
Promedio de producción acumulada de JI.
Promedios seguidos por distintas letras difieren significativamente, Tukey (0,05).
Promedio de producción diaria de JI.
Ecuaciones de promedios de producción acumulada
S. cubanum obtuvo una de las producciones acumuladas más bajas de las especies de EN evaluados (Fig. 1), con 36.583 JI/ larva en G. mellonella con el sistema topical, estando incluso, por debajo del promedio de producción por larva estimado para Steinernematidos, el cual fluctúa entre 70.000 y 90.000 JI (Poinar 1979).
En cuanto a producción diaria, se presentaron diferencias significativas entre tratamientos (p < 0,05) (Tabla 2b), al igual que la anterior variable, presentándose en general entre el primer y tercer día, las mayores concentraciones de emergencia de JI (56% al 96%), para el 80% de los tratamientos evaluados; disminuyendo hasta su agotamiento entre el octavo y duodécimo día, tendencia general observada para la mayoría de los tratamientos (Fig. 2). La razón de este detrimento en la producción depende del tamaño del hospedante, el cual influye en el agotamiento rápido de la reserva alimenticia para la multiplicación del nemátodo, disminuyendo su producción a través del tiempo hasta el total agotamiento del hospedante (Fig. 2). Para este caso, claramente se observa que la producción de JI es dependiente del tamaño del hospedante ya que G. mellonella con un agotamiento entre 8 y 10 días (Fig. 3b) produjo un máximo de 270.000 JI/ larva y B. mori con agotamiento entre 9 y 12 días, lo hizo con 395.880 JI/larva, corroborando lo encontrado por Dutky et al. (1964), quienes establecen que las diferencias de producción de nemátodos entomopatógenos están determinadas por el tamaño del hospedante.
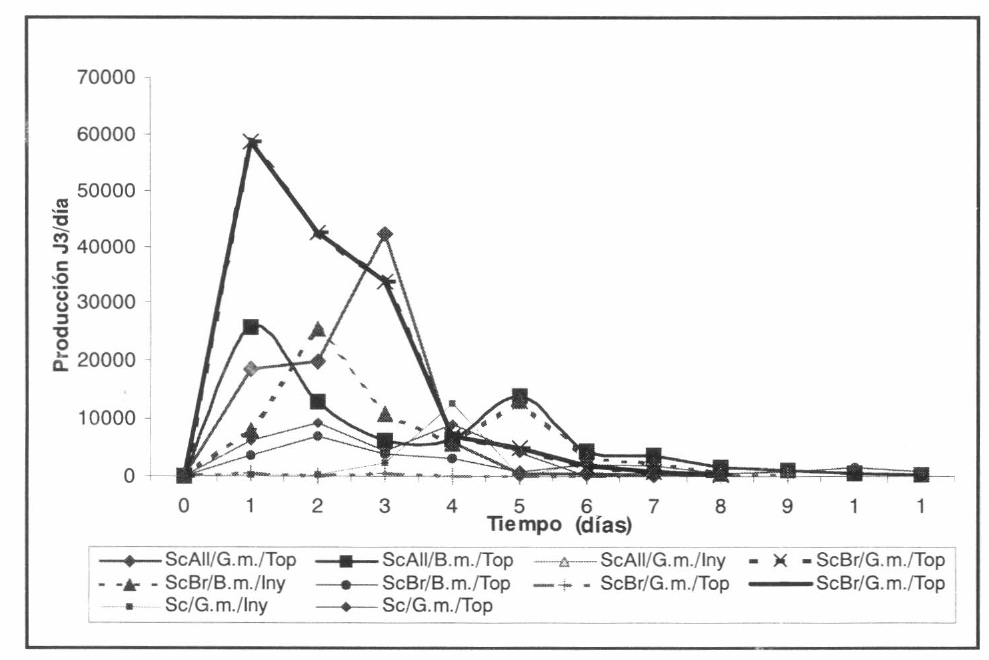
Producción diaria de JI por larva para los hospedantes y sistemas.
Para la máxima producción diaria obtenida no hay un patrón definido entre especies hospedantes y sistemas de infección; cada especie de EN por sistema de infección, en el mismo hospedante y entre hospedantes, presenta características particulares en producción.
Al realizar la prueba de comparación de promedios, se encontró que S. carpocapsae Brasil/G. mellonella, con el sistema de infección topical, fue estadísticamente diferente a los demás, presentando la mayor producción diaria de todos los tratamientos (Tabla 2b), con un pico importante en el primer día (58.650 JI/larva), concentrando el 90% de su producción (134.950 JI), en los primeros tres días de emergencia (Fig. 2). A diferencia de lo anterior, al evaluar la misma especie de EN y hospedante por el sistema de infección inyección, se obtuvieron las producciones más bajas durante el experimento (Tabla 2b). En contraste con lo anterior, B. mori, con el sistema de infección por inyección, presentó producciones importantes, donde S. carpocapsae All strain produjo la mayor producción en este hospedante, concentrando el 72% (106.586 JI / larva) de su producción al quinto día, siendo la segunda producción de los tratamientos evaluados. Así mismo, S. carpocapsae Brasil / inyección en B. mori presentó un promedio de producción diaria de 8.592 JI por larva (Tabla 2 b), colectando en los tres primeros días el 64% de su producción (44.360 JI / larva) (Fig. 2). No obstante lo anterior, en este mismo hospedante el sistema de infección topical fue eficiente, donde S. carpocapsae All strain en B. mori concentró el 60% de su producción en los tres primeros días (44.800 JI / larva), con una producción promedio diaria de 6.915 JI por larva.
Obtención de otros estados de entomonemátodos
La obtención de otros estados de EN (J4, hembras y machos) se debió al sistema de recuperación empleado (lavado diario de cada cámara de White), pues el agua de arrastre desprende algunos estados diferentes a JI, que solamente se desarrollan dentro del hospedante. No obstante, la medición de esta variable permitió obtener parámetros de comparación entre las especies evaluadas.
La obtención de J4 constituyó el segundo estado contabilizado de EN después los JI. En general, el mayor número acumulado obtenido lo presentaron los tratamientos S. carpocapsae Brasil y S. carpocapsae All strain / topical / G. mellonella (14.075 y 12.081 J4/larva respectivamente), coincidiendo con los tratamientos de mayor producción de JI. Esta cantidad de J4 indica un buen desarrollo de la segunda generación de las especies de EN evaluadas de EN, particularmente S. carpocapsae Brasil y S. carpocapsae All strain en ambos hospedantes. Posiblemente este volumen alto de J4 desarrollados se deba a que por un reducido número de JI que penetraron en las larvas de los hospedantes en el proceso de infección, se presentó una densidad poblacional baja de EN en el interior de los hospedantes y se desarrollaron adecuadamente estados (J1, J2) y los JI sin salir del hospedante, pasan a J4 continuando el ciclo con una segunda generación en el hospedante (Sáenz 1998).
En los lavados se presentó una cantidad alta de hembras y machos de segunda generación. Tratamientos como S. carpocapsae All strain/ topical/ G. mellonella y S. carpocapsae Brasil /inyección / B. mori presentaron un número alto de hembras con 4.311 y 3.696 con el sistema de infección inyección en B. mori aunque no hubo diferencias significativas entre tratamientos (p>0.05). Así mismo el tratamiento S. carpocapsae Brasil /inyección / B. mori presentó un número importante de machos con 1.372 por larva. Todo esto deja entrever que puede haber una segunda generación de las especies S. carpocapsae Brasil y S. carpocapsae All strain en los dos hospedantes evaluados B. mori y G. mellonella. Para este último, Sáenz (1998) registra que puede permitir hasta tres generaciones, caso particular para la especie Steinernema feltiae cepa Villapinzón. Caso contrario lo presentó la especie S. cubanum que no produjo J4, hembras y machos, produciendo JI en los primeros cinco días y agotando a su hospedante en el noveno día, sin dejar entrever una segunda generación (Fig. 3b).
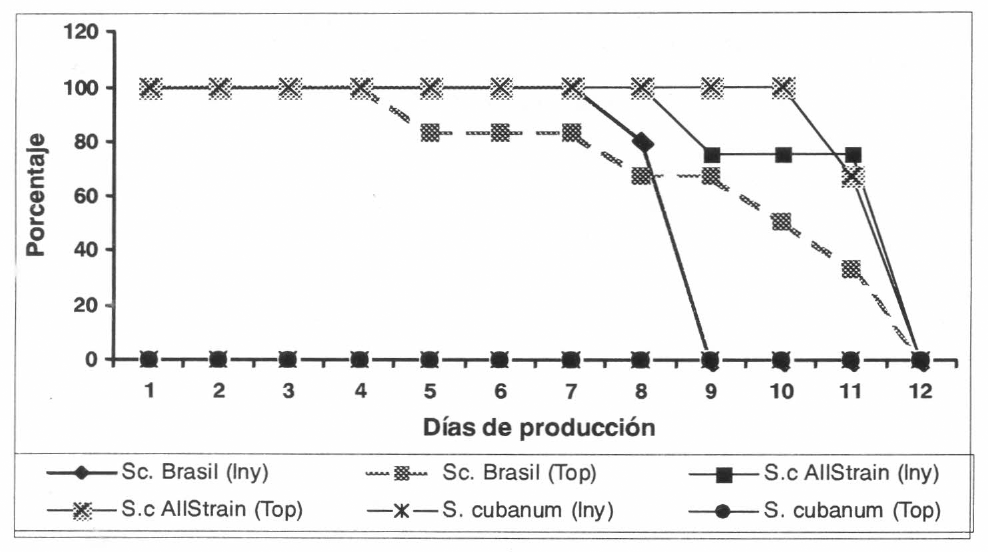
Agotamiento de B. mori por los sistemas inyección y topical.
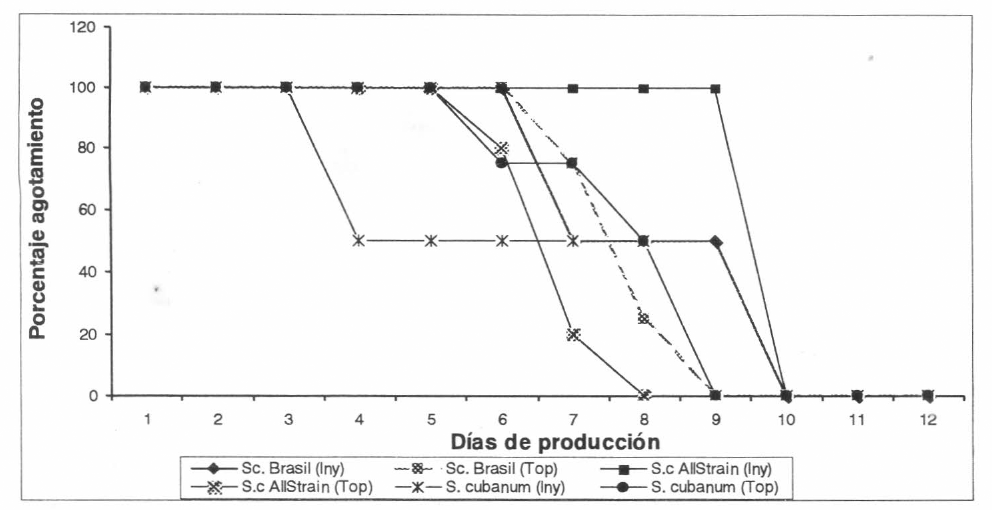
Agotamiento de G. mellonella por el sistema inyección.
Especificidad del hospedante
S. cubanum no se multiplicó en B. mori bajo ningún sistema de infección (T11 y T12), aunque algunas larvas de B. mori presentaron sintomatología de afección por bacteriosis y posiblemente éste sea un caso de especificidad de especie de EN por hospedante tal como lo registraron De Doucet et al. (1999), quienes encontraron que algunas especies de EN sólo se multiplican en cierto rango de hospedantes insectiles. Maxwell et al. (1994) afirman que la bacteria simbionte, Xenorhabdus spp., al no producir cantidades suficientes de antibióticos como xenocoumacina, bacteriocina o xenorhabdinas en el proceso de infección, no inhibe suficientemente las defensas del hospedante, lo cual afecta directamente la septicemia de la bacteria y la multiplicación del EN en el mismo hospedante.
Porcentaje de producción de hospedantes
En general, B. mori presentó los porcentajes más altos de producción de EN, para los dos sistemas de infección evaluados y para las dos EN de mayor producción, oscilando entre un 30 y 60% de producción de sus larvas, a excepción de S. cubanum que no se multiplicó bajo los sistemas de infección en este hospedante. G. mellonella se encuentra en un rango de producción más bajo, entre 10 y 50%; sin embargo, presenta diferencias en porcentaje de producción entre sistemas, siendo mucho más efectivo el sistema de infección topical para los tres EN evaluados (Fig. 4).
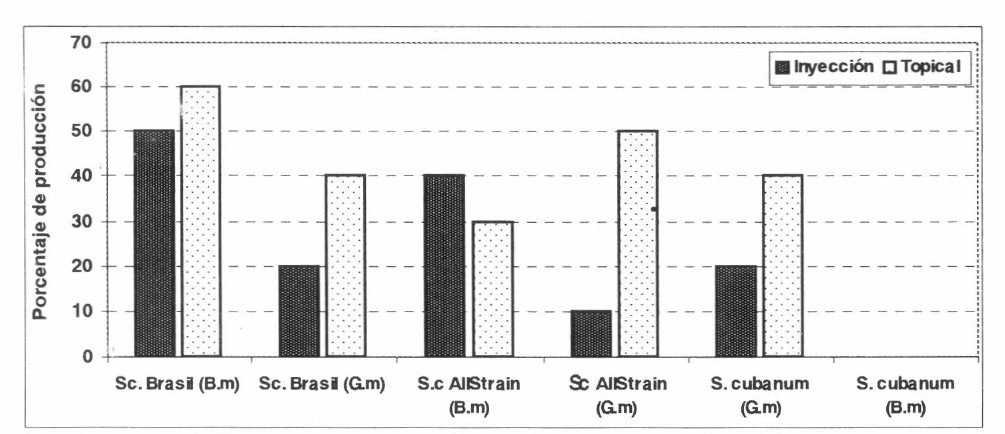
Porcentaje de producción de estados de larvas de G. mellonella y B. mori.
Conclusiones
El hospedante G. mellonella se ratifica como el principal en producción in vivo de JI para las especies de EN evaluadas especialmente empleando el sistema de infección topical; así mismo, se registra a B. mori como hospedante alternativo en la producción in vivo para determinados EN y sistemas de infección, como es el caso de la producción de la especie S. carpocapsae All strain empleando el sistema de infección por inyección.
Los tratamientos S. carpocapsae Brasil / topical en G. mellonella y S. carpocapsae All Strain / inyección en B. mori se mantuvieron dentro de la máxima producción acumulada de JI/larva, estimada para Steinernematidos, con 149.258 y 139.757 JI/larva. En cuanto a la máxima producción obtenida por larva, el tratamiento S. carpocapsae All Strain / inyección en B. mori superó los registros encontrados (395.880 JI/larva).
Para producción in vivo de EN se debe tener en cuenta la especificidad del hospedante para la multiplicación de las especies de EN; caso concreto en el experimento, la especie S. cubanum no se multiplicó bajo ningún sistema de infección en larvas de B. mori, pero si logró multiplicarse utilizando los dos sistemas de infección en larvas de G. mellonella.
La producción de JI, en general, para todos los tratamientos se concentró entre el segundo y quinto día, período en que se debe realizar la colección de EN ya que se presentan los picos de producción más altos, disminuyendo la producción entre el octavo y duodécimo día.
Los sistemas de infección topical e inyección garantizan la multiplicación in vivo; sin embargo, la infección topical en general muestra una mayor eficiencia en cuanto a producción, posiblemente por presentarse libremente todos los procesos de infección en su hospedante, accediendo a éste por los orificios naturales (boca, ano o espiráculos), lo que pudo facilitar el desarrollo libre del nemátodo en su interior, por lo que se recomienda su uso. Sistemas de infección inducidos, como el de inyección en este caso, aunque pueden tener éxito en multiplicación, se recomienda principalmente para realizar estudios genéticos de especies de entomonemátodos o de especificidad al hospedante, ya que permite conocer con mayor exactitud el número de unidades infectivas o JI por insecto.
Finalmente, ante la masiva y fácil obtención de estados diferentes a JI durante la multiplicación in vivo, se considera su utilización en la producción masiva implementando técnicas de producción in vitro, especialmente en reactores.
Footnotes
Agradecimientos
Al personal de la Disciplina de Entomología, en especial al Sr. Uriel Posada Posada por la ayuda en el laboratorio, y al Sr. Gonzalo Hoyos y al Dr. Alex Bustillo por la revisión final del documento, al Centro Nacional de Investigaciones de Café "Cenicafé" que con su colaboración permitieron la realización de la investigación y a los revisores por sus valiosos aportes.
