Abstract
The fungus Metarhizium anisopliae was obtained from two dead queens of the ant species Atta cephalotes collected in Colombia. The isolates were grown on PDA, and identified as 136 and 137. Their pathogenicity was evaluated against workers of A. cephalotes and compared with isolates obtained from other insect sources. Mortality and infection of ant workers were monitored during 9 days. Half infective concentration (CI₅₀) and half sporulation time (TE₅₀) was determined by probit analysis. Strains 136, 137 and 77 at the minor dose 5.4x10⁵ conidia/ml, presented the lowest TE₅₀ (200.3, 180.7 and 197.7 hours) compared with the other strains that varied in a range of 237.3 to 672.7 hours post-inoculation. The CI₅₀ after 144 hours post exposure was 9.93x10⁷ conidia/ml and 4.5x10⁷ conidia/ml for the isolates 136 and 137 in contrast with the isolates 82 and 77 with 7.5x10⁸ conidia/ml and 1.7x10⁵ conidia/ml respectively. Molecular characterization by PCR-RFLP. produced a fragment of 1.2 kpb of ADN that digested with restriction enzymes generated a banding pattern in agarose gel that permitted to locate the interest isolates in a group with 60% of similarity among them, accompanied by other three isolates. The evaluation of the ADN by RAPD's generated two groups, in one of them are isolaties 136 and 137 with 71% percentage of disagreement, demonstrating high genetic variability between them.
Introducción
Las hormigas cortadoras de hojas de los géneros Atta y Acromyrmex son plagas de cultivos económicamente importantes en varios países suramericanos (Cortés 1986; Dichl-Fleig y Valim-Labres 1993; Velez y Gallego 1992). El control de estas ha sido complicado, debido a la complejidad de sus nidos, lo que dificulta la llegada del producto al lugar donde se encuentra la reina, blanco ideal en el control del nido (Cortes 1986). Se han usado insecticidas químicos para el control de las hormigas; sin embargo, su baja especificidad, su alta toxicidad, sus efectos adversos en el ambiente y la generación de poblaciones de insectos resistentes (Dichl-Fleig et al. 1993), han llevado a considerar el uso de agentes biológicos para su control (Da Silva y Diehl-Fleig 1988; Dichl-Fleigy Valim-Labres 1993; Leal et al. 1997; Leathers et al. 1993; Specht et al. 1994). Debido a su acción específica relativa, los hongos se han considerado buenos candidatos para el control de plagas agrícolas importantes, incluyendo malezas e insectos; algunos son producidos industrialmente y en la actualidad se encuentran disponibles en el mercado. M. anisopliae es un hongo patógeno de insectos que muestra especialización considerable con respecto a su amplio rango de hospederos lo cual es una indicación de la variación genética que está ocurriendo naturalmente en esta especie (St. Leger et al. 1992). Estudios relacionados con la penetración de la cutícula del huésped indican que este hongo produce enzimas extracelulares de familias catalíticamente distintas, proteasas como subtilisina (PR1) tripsina (PR2), y metaloproteasas, así como también otras proteasas que son secretadas por el hongo durante el proceso patogénico y de degradación de la cutícula del insecto (Leal et al. 1997; St Leger et al. 1998).
En este trabajo se describen algunas propiedades de M. anisopliae que ha sido encontrado por primera vez parasitando reinas de la hormiga cortadora de hojas A. cephalotes. Se realizó la caracterización de las dos cepas que incluye la evaluación de su patogenicidad contra obreras de A. cephalotes y se comparó con aislamientos obtenidos de otros insectos. También se realizó análisis genético por medio de RAPD del ADN genómico y PCR-RFLP del gen Prl, en el que se encontraron algunas diferencias genéticas entre las cepas que podrían estar en relación con la adaptación del hongo al huésped.
Materiales y Métodos
Obtención y mantenimiento de los insectos
Se colectaron hormigueros recién fundados de A. cephalotes en el municipio de San Luis. Antioquia. Posteriormente se trasladaron al laboratorio de la CIB en Medellín para ser colocadas en hormigueros artificiales que se alimentaron con hojas frescas de plantas y hojuelas de avena. Los hormigueros se mantuvieron en cuartos especiales en el insectario con una temperatura promedio de 25°C y con un fotoperiodo de 12:12 horas (luz: oscuridad). Los recipientes donde se encuentran los jardines de hongo se mantienen cubiertos con papel oscuro para simular la penumbra del interior de los hormigueros naturales.
Condiciones de aislamiento y cultivo de M. anisopliae
Los aislamientos de M. anisopliae, sus códigos, origen geográfico y el huésped de donde se obtuvieron se muestran en la tabla 1. Para los bioensayos se realizaron cultivos en PDA a un pH 4.5 a 25°C y se mantuvieron en oscuridad por 14 días. Las suspensiones de conidias utilizadas para cada bioensayo se obtuvieron por un raspado suave de la superficie del medio de cultivo y se suspendieron en agua destilada estéril. La concentración de conidias se determinó usando la cámara de Neubauer bajo microscopía de luz y se hicieron diluciones seriadas en un rango entre 5.4x10⁵ a 5.4x10⁸ conidias/ml.
Aislamientos de Metarhizium anisopliae utilizados en este estudio
Bioensayos
Se realizaron tres ensayos de laboratorio con hormigas obreras de A. cephalotes de la siguiente forma. Las hormigas se sumergieron durante tres segundos en diluciones consecutivas de conidias de cada aislamiento de M. anisopliae y se transfirieron a cajas de petri con papel filtro húmedo, mientras que los controles se sumergieron en agua destilada estéril. Los tratamientos se realizaron por duplicado y en días diferentes (Jones et al. 1996). La mortalidad de las hormigas se registró cada 24 horas durante nueve días. Las hormigas muertas se incubaron en cámara húmeda a 25°C en oscuridad para permitir el desarrollo del hongo y la esporulación sobre sus cadáveres. Por análisis probit se determinó la concentración infectiva media (CI₅₀) y tiempo medio de esporulación (TE₅₀). Los datos de esporulación sobre los cadáveres de las hormigas fueron sometidos a análisis de varianza (ANOVA. Statistica. StatSoft. Inc., Tulsa. USA).
Extracción de ADN
Las diferentes cepas del hongo se cultivaron a 300 rpm, 30°C por 7 días en un medio líquido que contenía por litro, 25 gr de extracto de levadura y 25 gr de sacarosa. El micelio se colectó por centrifugación durante 15 minutos a 4000 rpm. se lavó tres veces con agua destilada estéril y se almacenó a -70°C. El ADN se extrajo siguiendo el método de Johanson (1995). El micelio se maceró en nitrógeno líquido, posteriormente se le adicionó el tampón de extracción (200 mM Tris HCl pH 8,5. 250 mM NaCl, 25 mM EDTA, 0.5% SDS), se incubó a 65°C por una hora. Esta mezcla se colocó en tubos de microcentrífuga de 1.5 ml, se agregaron 600 µl de fenol: cloroformo y el tubo fue centrifugado nuevamente a las mismas condiciones; el sobrenadante se pasó a un nuevo microtubo y se incubó con RNAsa A, se agregaron 600µl de cloroformo: alcohol isoamílico (24:1) y se centrifugó bajo las mismas condiciones. El sobrenadante se retiró y el ADN se precipitó por la adición de 20 µl de acetato de sodio 3M y 700 µl etanol absoluto frío: y se incubó toda la noche a -20°C y se centrifugó a 13000 rpm, 4"C por 10 min. El botón de ADN se lavó con etanol al 70%. se secó y luego se resuspendió en 100 µl agua destilada estéril.
Análisis por PCR-RFLP del gen Prl
La reacción en cadena de la polimerasa (PCR) anidada se realizó usando Taq ADN polimerasa y los pares de cebadores publicados por Leal et al. (1997): METPR1: 5' CAC TCT TCT CCC AGC CGT TC 3', METPR2: 5' AGG TAG GCA GCC AGA CCG GC 3'. METPR4: 5' GTA GCT CAA CTT CTG CAC TC 3', METPR5: 5' TGC CAC TAT TGG CCG GCG CG 3'. En la primera PCR se usó ADN extraído de la muestra como molde y el par de cebadores METPR1 y METPR4. Mientras que la segunda PCR utiliza una alicuota de la primera PCR como molde y el segundo par de cebadores METPR2 y METPR5. Las PCR se efectuaron en 50 mM KCl, 1.5 mM MgCl₂, 10 mM Tris HCl pH 8,5, 10 mM de cada dNTP, 25 pmoles de cada cebador, 0.5 µl Taq polimerasa, 25 ng de ADN en un volumen final de 50 µl. Las reacciones se efectuaron un termociclador Perkin Elmer 9600, como se indica a continuación: 4 min a 94°C, seguido por 38 ciclos de 1 min a 94°C. 1 min a 58°C y 2 min a 72°C; y un ciclo de extensión final de 4 min a 72°C. La segunda PCR se hizo usando 1 µl de la primera PCR como molde con los correspondientes cebadores y bajo las mismas condiciones de temperatura y tiempo (Leal et al. 1997).
Restricción de los productos de PCR
Se usaron cinco endonucleasas con el fin de detectar polimorfismos entre los productos amplificados del gen Pr1 por PCR de cultivos de M. anisopliae. Las digestiones se hicieron con DdeI, RsaI, AluI, HinfI y HaeIII como se indica a continuación: 10 µl de producto de PCR, 5 unidades de enzima (0.5 µl), 2 µl de tampón apropiado para la enzima y 7.5 µl de agua destilada. Las reacciones se incubaron a 37°C toda la noche. Después de la digestión, los productos de reacción fueron analizados por electroforesis a través de un gel de agarosa al 2% tamponado con TBE (Tris-Borato-EDTA) 0.5X conteniendo bromuro de etidio (Leal et al. 1997).
Amplificación aleatoria de ADN polimórfico (RAPD)
Las reacciones se hicieron usando el juego de cebadores OPM (Operon Technologies Inc., Alameda, USA) y se efectuaron en 50 mM KCl, 1.5 mM MgCl₂, 10 mM Tris HCl pH 8.5, 10 mM de cada dNTP, 5 pmoles de cada cebador, 0.2 µl de Taq polímerasa, 50 ng de ADN en un final volumen de 50 µl. Las reacciones se realizaron en un termociclador Perkin Elmer 9600 programado como se indica a continuación: 3 min a 95°C, seguido por 40 ciclos de 1 min a 95°C, 1 min a 36°C, 2 min a 72°C. después el último ciclo de extensión final de 5 min a 72 °C. Los productos amplificados fueron corridos por electroforesis en un gel de agarosa al 1,2% con bromuro de etidio (Sambrook et al. 1989).
Cada banda correspondiente a un fragmento de ADN obtenido por PCR o restricción fue tratado como un carácter con dos posibles estados, presente o ausente. Los perfiles de ADN se valoraron y generaron dendrogramas por análisis de grupos de jerarquías genéticas basadas en el método UPGMA, la distancia de ligamiento se calculó como porcentaje de desacuerdo con el paquete estadístico Statistica (StatSoft, Inc., Tulsa, USA).
Resultados
Bioensayos
No se encontraron diferencias estadísticas significativas entre los datos de mortalidad de las hormigas tratadas con las distintas cepas y dosis de M. anisopliae y las hormigas empleadas como control.
En la dosis mas baja utilizada (5.4x10⁵ conidias/ml) el TE₅₀ de los aislamientos 136 y 137 (obtenidos de reinas de A. cephalotes naturalmente infectadas) y el aislamiento 77 fue de 200.3, 180.7 y 197.7 horas respectivamente, después de la exposición a las conidias del hongo. Período de tiempo más corto que el empleado por los otros aislamientos obtenidos a partir de otros insectos que presentaron valores de TE₅₀ en un rango de 237.3 a 672.7 horas. En la concentración mas alta 5.4x10⁸ conidias/ml, las diferencias en el TE₅₀ de las cepas de M. anisopliae se hicieron mas pequeñas con cerca de 138 horas para los aislamientos 136 y 137 comparado con las otras cepas, las cuales estuvieron en un rango de 167.1 a 238.3 horas, lo que indica una tendencia a disminuir el TE₅₀ a medida que se incrementó la concentración del inoculo (Fig. 1).
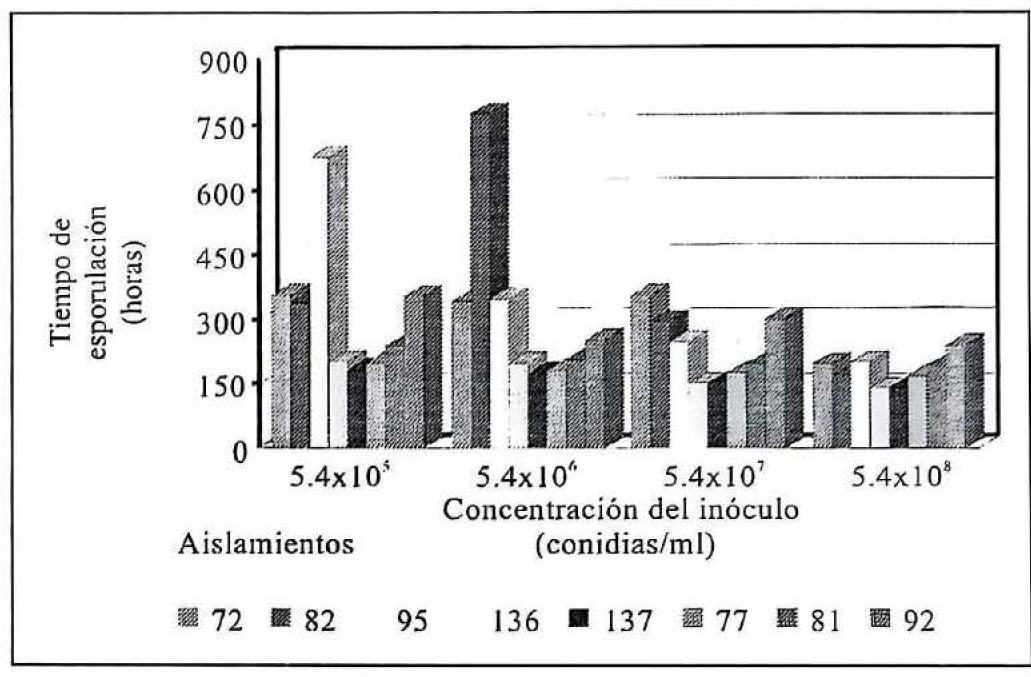
Efecto de la concentración del inóculo sobre el tiempo medio de esporulación de Metarhizium anisopliae infectando obreras de Atta cephalotes (determinado por análisis Probit).
El seguimiento de la infección de las hormigas demostró que los individuos sometidos a todos los tratamientos mostraron algún grado de infección, mientras que ninguna de las hormigas utilizadas como control se vió invadida por M. anisopliae. El tiempo de evolución de los bioensayos mostró que 144 horas después de la exposición al inóculo, se observó esporulación del hongo sobre algunas hormigas muertas y se determinó para éstas una CI₅₀ de 9.9x10⁷ y 4.4x10⁷ conidias/ml para los aislamientos 136 y 137, respectivamente, siendo ésta una concentración baja comparada con las cepas 82 y 77 que tuvieron 7.5x10⁸ y 1.2x10⁵ conidias/ml respectivamente. En el tiempo final de monitoreo de los bioensayos, 216 horas, la CI₅₀ disminuyó para los aislamientos 136, 137 y 77 calculando para éstas 6.5x10³, 2.1x10⁴ y 2.8x10³ conidias/ml, respectivamente, mientras que para las otras cepas del hongo la concentración fue del orden de 1.7x10⁷ y 2.1x10⁸ conidias/ml (Fig. 2).
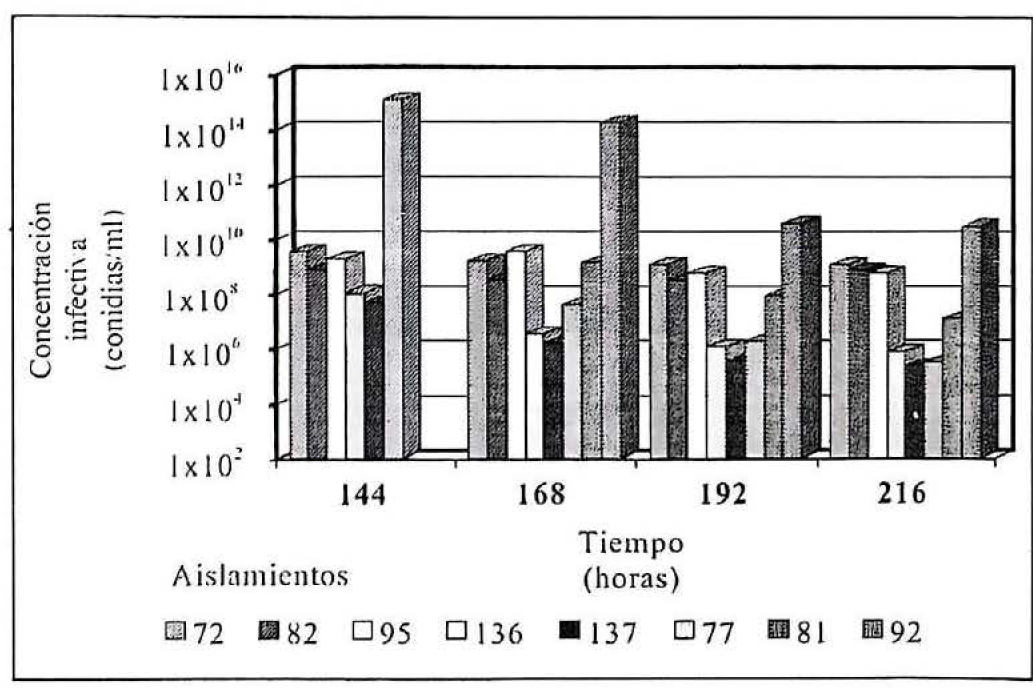
Efecto del tiempo de incubación sobre la concentración infectiva media de Metarhizium anisopliae sobre obreras de Atta cephalotes (determinado por análisis Probit).
El análisis de varianza y la prueba de Tukey realizada a los datos de esporulación obtenidos en los bioensayos indican que las cepas 136 y 137 producen un mayor número promedio de insectos esporulados, en las diferentes dosificaciones utilizadas y en los diferentes tiempos de lectura de los bioensayos (Tabla 2).
Número promedio de hormigas obreras de Atta cephalotes esporuladas despues del tratamiento con diferentes cepas y dosis de Metarhizium anisopliae e incubadas a diferentes tiempos
Los promedios de hormigas esporuladas seguidos de la misma letra en cada tiempo y dosis no son significativamente diferentes (α=0.05, DF=40). El dato promedio para las hormigas control para todas los tiempos y dosis fue igual a cero.
Análisis por PCR - RFLP
Mediante la PCR anidada se determinó la presencia del gen Pr1 en todas las cepas de M. anisopliae evaluadas produciendo un fragmento de ADN caracteristico de 1.2 kpb (Leal et al. 1997). La digestión de este ADN con enzimas de restricción generó un total de 38 bandas (Fig. 3) con un tamaño variable entre 50 y 900 pb las cuales se tuvieron en cuenta para el análisis estadístico. El dendrograma generado a partir de esas señales mostró un porcentaje de desacuerdo de cerca del 40% entre las cepas de interés (136 y137) y permitió ubicarlas en uno de dos grupos con el aislamiento 82 (Fig. 4).
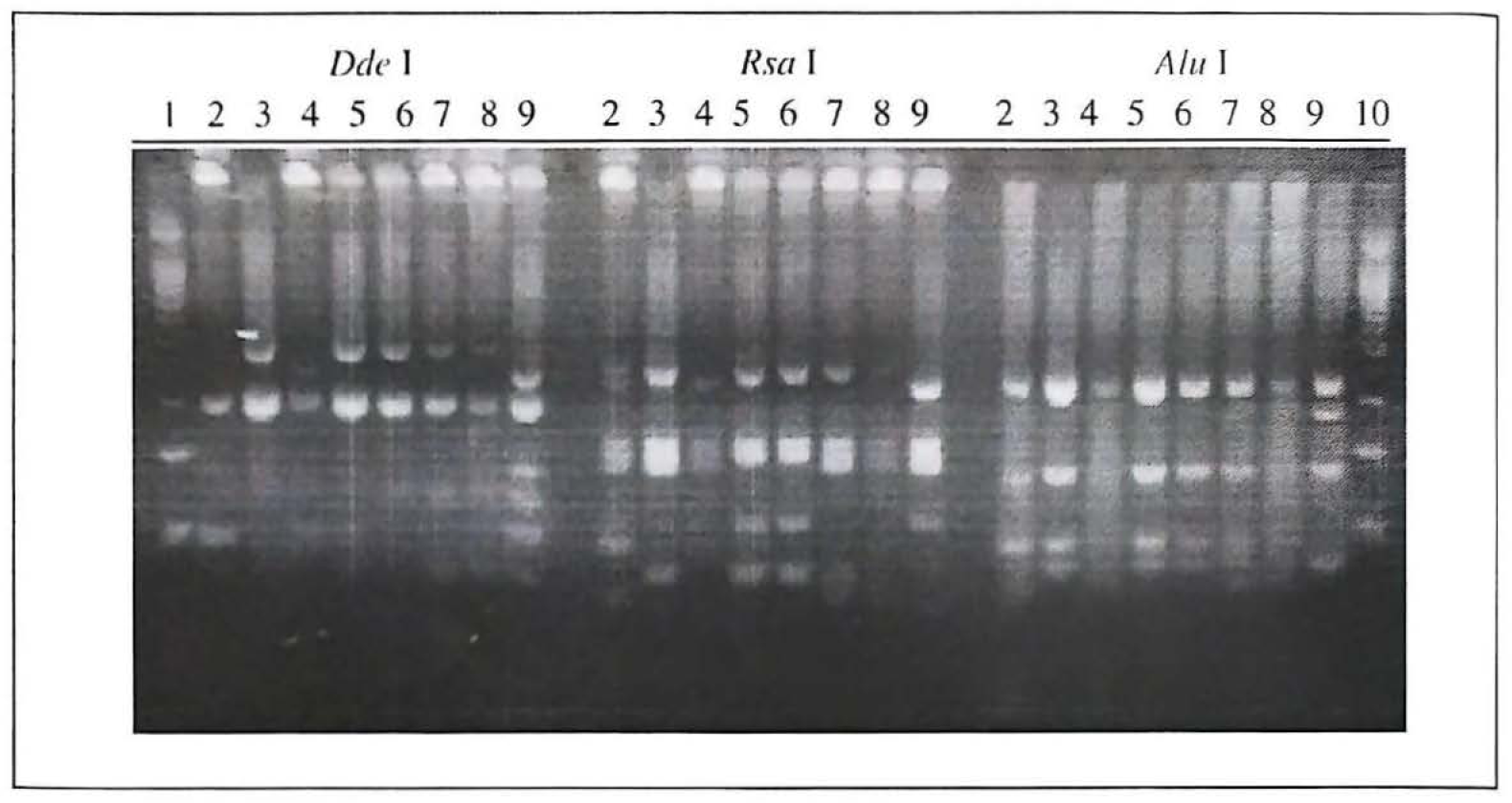
Perfiles de los productos de PCR del gen Prl de Metarhizium anisopliae generado con enzimas de restriccion. lineas 1 y 10, marcador de peso molecular (ladder 100 bp). linea 2, cepa 72: linea 3. cepa 82: linea 4. cepa 95: linea 5. cepa 136: linea 6, cepa 137: linea 7. cepa 77: linea 8, cepa 81: linea 9. cepa 92.
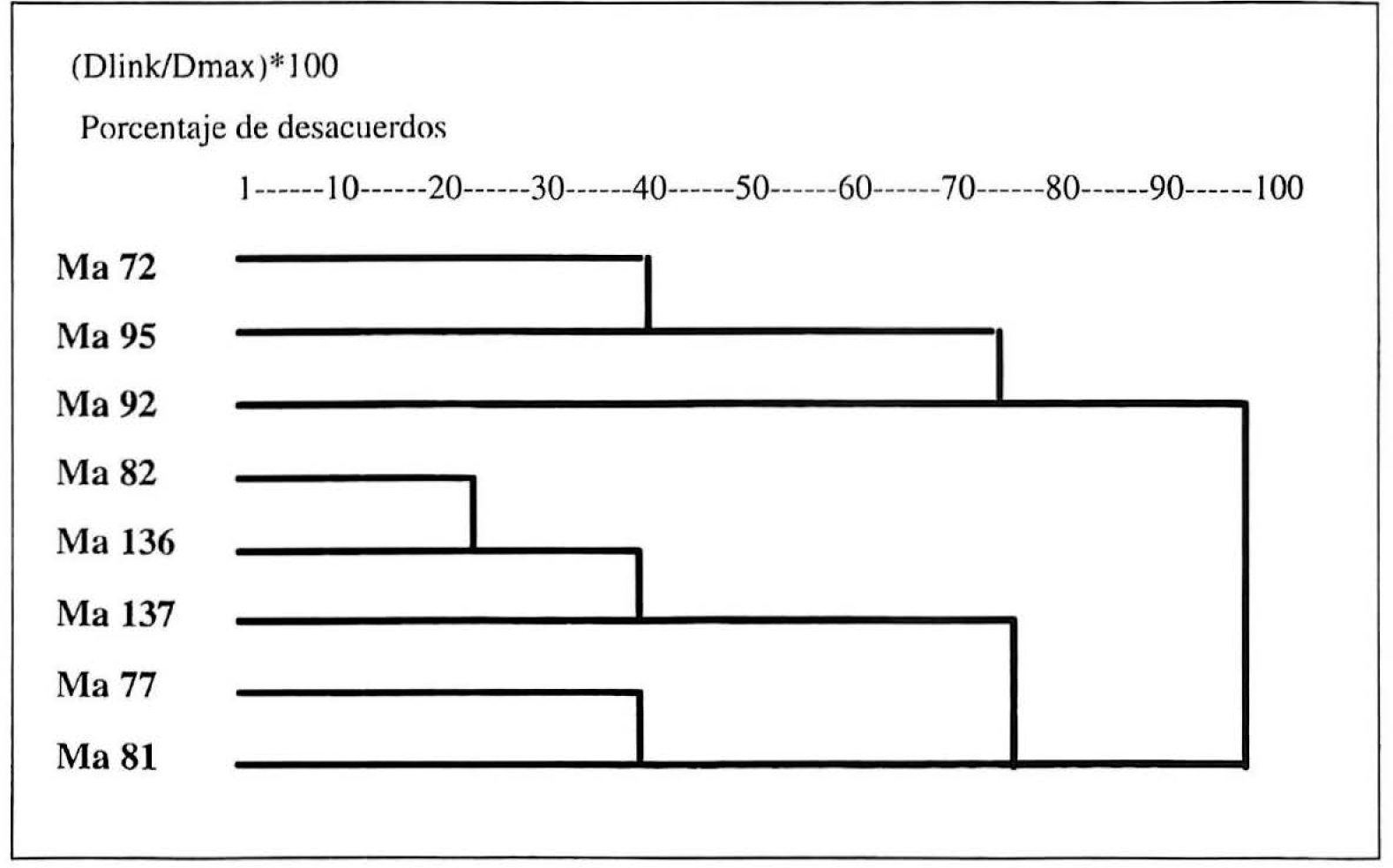
Dendrograma indicando la relación de ocho cepas de Metarhizium anisopliae aisladas en Colombia, generado por coeficientes de similaridad genética por la presencia o ausencia de 38 bandas de PCR-RFLP DNA basado en UPGMA. (Statistica. Cluster analysis).
Análisis por RAPD
Los ensayos por RAPD usando 20 iniciadores de 10 nucleótidos de longitud muestran que seis de estos cebadores (OPM 01, OPM 03, OPM 05, OPM 12, OPM 13 y OPM 20) produjeron los patrones de amplificación que fueron útiles para establecer las diferencias entre las cepas empleadas en este trabajo. En la evaluación del ADN genómico por medio de RAPD se tuvieron en cuenta un total de 60 bandas de ADN entre 300 y 2100 pb (Fig. 5). De acuerdo con el análisis realizado, los aislamientos se clasificaron en dos grupos (Fig. 6); un grupo que contiene los aislamientos de M. anisopliae realizados a partir de hormigas con un grado de desacuerdo entre ellos de 71%, a pesar de tener el mismo origen geográfico; mientras que el segundo grupo contiene los 6 aislamientos que se encontraron parasitando especies diferentes a hormigas.
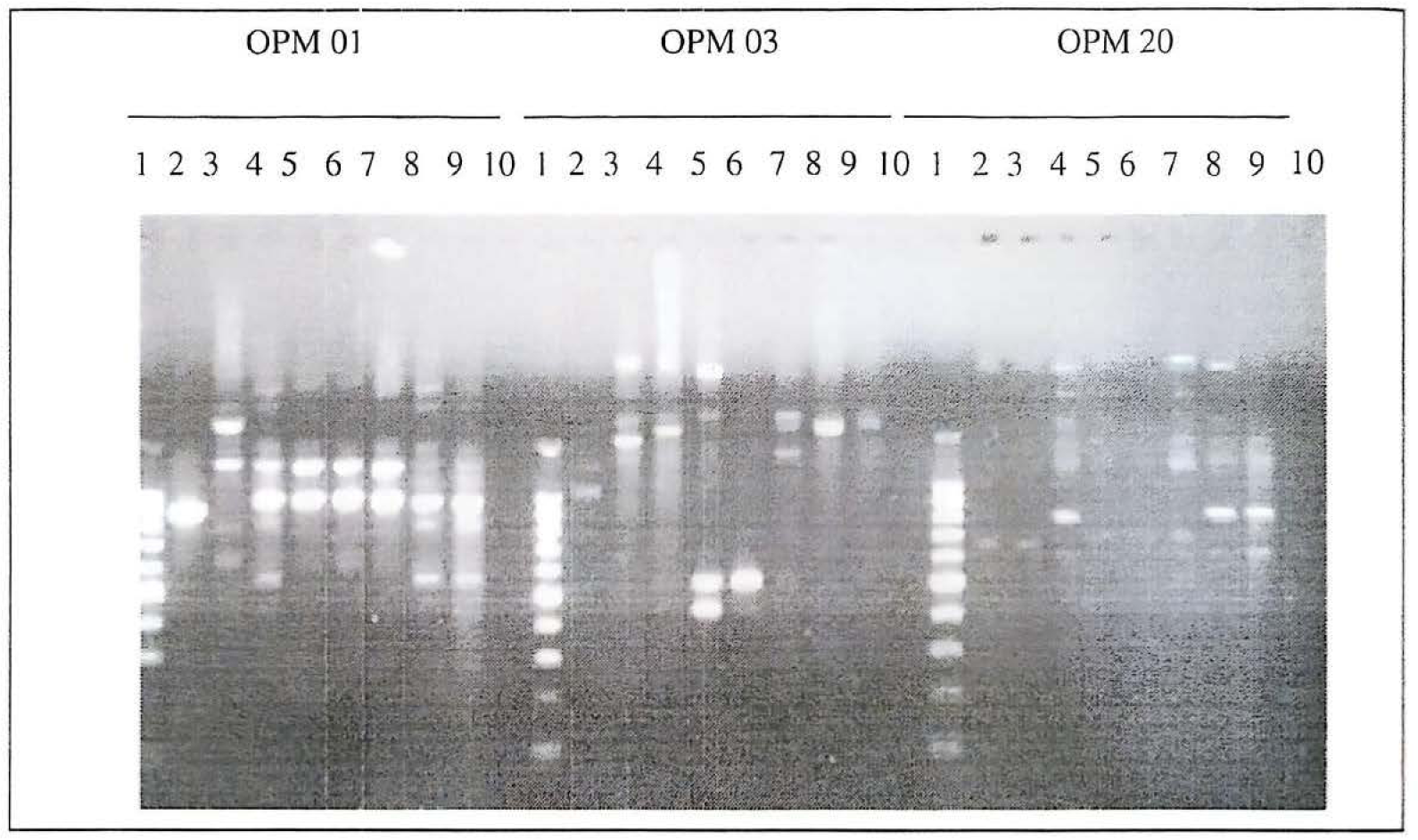
Perfiles de productos de PCR por RAPD de Metarhizium anisopliae con los iniciadores OPM 01, OPM 03 and OPM 20. linea 1. marcador de peso molecular (ladder 100 bp). linea 2, cepa 136; linea 3, cepa 137; linea 4, cepa 72; linea 5. cepa 77; linea 6, cepa 81; linea 7. cepa 82; linea 8. cepa 92: linea 9. cepa 95: linea 10: control negativo.
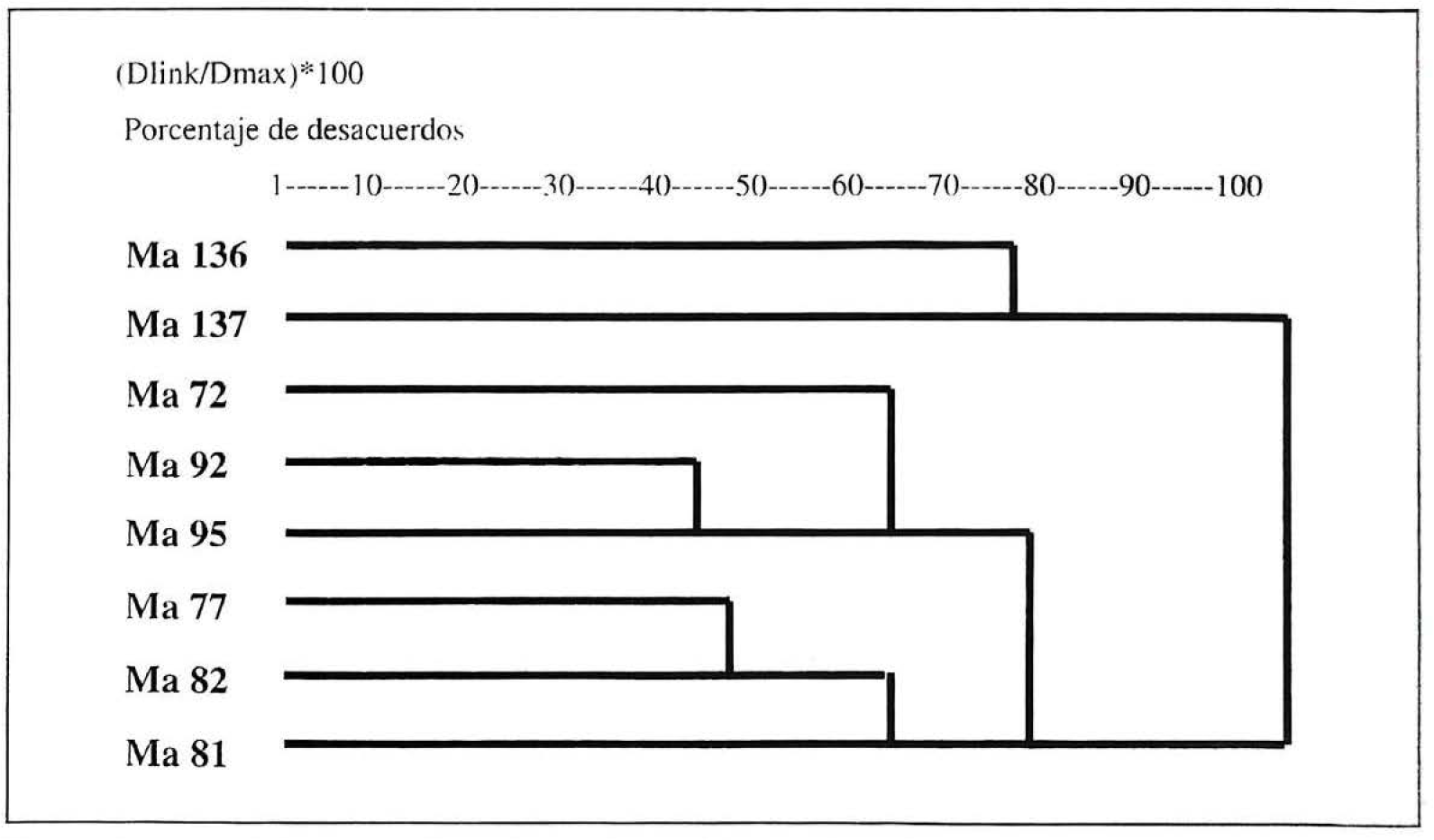
Dendrograma indicando la relación de ocho cepas de Metarhizium anisopliae de Colombia, generado por un coeficiente de similaridad genética por la presencia o ausencia de 60 bandas de ADN generados por RAPD. basado en UPGMA. (Statistica, Cluster analysis)
Discusión
La finalidad de un programa de control microbiológico está basado en la búsqueda de cepas de microorganismos con acción específica sobre un grupo de insectos, condiciones apropiadas de microclimas y técnicas de aplicación adecuadas a la agricultura y región geográfica (Dielht-Fleigh et al. 1992b). El control microbiológico de la hormiga cortadora de hojas ha sido realizado mediante la utilización de patógenos como Cordyceps sp., M. anisopliae y B. bassiana; sin embargo se ha encontrado que tanto la saliva como las secreciones anales y metapleurales de las hormigas tienen una fuerte actividad bacteriostática y bactericida pero baja actividad fungicida. Las glándulas metapleurales segregan ácido hidroxidecanoico que opera como un inhibidor de la germinación de esporas y semillas dentro del nido y además tiene funciones bactericidas (Aragua 1984; Cortés 1986), aunque estas secreciones tienen una muy baja acción antifúngica (Brough 1983), de tal suerte que es factible el uso de hongos entomopatógenos para controlar las hormigas.
La alta mortalidad encontrada en las hormigas utilizadas como control, en los bioensayos sugiere que las hormigas están en condiciones desfavorables, posiblemente por la falta de comunicación con la reina. la ausencia de alimento y por factores intrínsecos propios del bioensayo, tales como humedad y condiciones de temperatura y luz diferentes a las que ofrece el nido. Estos problemas de mortalidad fueron señalados por Da Silva y Diehl-Fleig (1988) cuando realizaron bioensayos sobre obreras de A. sexdens piriventris mostrando una pequeña diferencia en el tiempo letal medio, con 3.3 días para la cepa L87 de M. anisopliae y 4.4 días para las hormigas control.
La generación de una epizootia en poblaciones de insectos depende de muchos factores entre los que podemos contar las condiciones de tiempo, las condiciones fisiológicas del hospedero, la habilidad del hongo para infectar el insecto y por lo tanto la obtención de un producto microbiológico selectivo (Alves et al. 1988). Como lo informó Diehl-Fleig et al. (1992a) la cepa Bsa de B. bassiana aislada a partir de una obrera de A. sexdens piriventris, presentó mayor especificidad para controlar hormigas cortadoras que otros aislamientos de B. bassiana y M. anisopliae colectados de otros insectos, esto confirma la importancia de los aislamientos 136 y 137 que mostraron estar adaptados a algunas condiciones bióticas y abióticas que favorecieron la epizootia natural y que podría considerarse como un cierto grado de especificidad del entomopatógeno por el insecto blanco.
Para el control de insectos sociales es muy importante el tiempo de mortalidad y la capacidad de esporulación de hongos sobre los cadáveres de las hormigas. Un corto tiempo de mortalidad y rápida esporulación acompañada de una baja concentración de conidias necesaria para la infección, tal y como la muestran los aislamientos 136 y 137, podrían representar una ventaja en el momento de hacer una aplicación en el campo (Stimac et al. 1987) ya que el hongo estaría menos expuesto a factores ambientales que puedan reducir su virulencia, tendría una mayor oportunidad de introducir un inóculo suficientemente alto dentro del nido y además podría conducir al desarrollo de un micoinsecticida específico, efectivo y económico.
El gen Prl que codifica para subtilisina, la mayor proteasa secretada por M. anisopliae, (Leal et al. 1997) amplificado por PCR generó un fragmento de 1.2 kpb que digerido con enzimas de restricción produjo un patrón de bandas que permitio la diferenciación y la formación de dos grupos con los aislamientos utilizados. La similitud establecida entre los aislamientos hechos a partir de los hormigas de acuerdo con los análisis estadísticos realizados a partir de PCR-RFLP y RAPD, fue de 60% y 30%, respectivamente, indicando que aunque estos fueron encontrados infectando insectos de la misma especie, en la misma región geográfica y con un corto periodo de tiempo de diferencia entre ellos, se pudieron observar variaciones genéticas, Además la similitud establecida entre los aislamientos de hormigas y los realizados de otros insectos fue muy baja de acuerdo con el sistema estadístico utilizado. Esta situación contrasta con las observaciones realizadas por Tigano-Milani et al. (1995) usando la técnica de RAPD y con cebadores OPC (Operon Technologies) en M. anisopliae proveniente de Brasil, donde las cepas CG58 y CG54 aisladas el mismo año y de igual especie de insecto tuvieron muy poca diferencia genética.
El dendrograma generado con los datos de RAPDs también indica diferencias entre los aislamientos, aún entre aquellos que se colectaron simultáneamente en la misma localidad: sin embargo, los aislamientos obtenidos de reinas naturalmente infectadas son agrupados juntos indicando que estas diferencias se derivan probablemente de la adaptación del hongo al hospedero. Por lo tanto el análisis realizado en este trabajo por RFLP-PCR y RAPD podría ser usado para evaluar la eficacia de un hongo como agente de control biológico, (usado para encontrar marcadores genéticos de patogenicidad) especificidad de insecto blanco, supervivencia y distribución espacial y temporal de aislamientos de M. anisopliae utilizado en el campo (Leal et al. 1997; St. Leger et al. 1992; Tigano-Milani et al. 1995).
Según Braga et al. (1994) las exoenzimas producidas por el hongo M. anisopliae como la proteasa (PR1) con actividad elastolítica es particularmente importante durante la etapa de degradación enzimática de la cutícula del insecto huésped. Desde luego, la modificación en la producción de esta enzima puede ser uno los factores responsables de la variación en la virulencia presentada por los diferentes aislamientos estudiados.
Conclusiones
Los aislamientos de M. anisopliae obtenidos de reinas de A. cephalotes naturalmente infectadas en su nido (136 y 137) son el primer registro mundial en esta especie de hormigas y también fueron los más potentes en las evaluaciones de patogenicidad.
Queda establecido el gran potencial existente en la utilización de las cepas de M. anisopliae (136 y 137) como agentes de control de las hormigas cortadoras A. cephalotes, debido a que han demostrado ser altamente específicas, además de poseer características como esporulación rápida y concentración baja de conidias requeridas en su CI₅₀ lo que es de gran importancia en la evaluación de un microorganismo propuesto para ser utilizado como agente de control biológico.
La caracterización de los aislamientos utilizados en el estudio por medio de las técnicas PCR-RFLP y RAPD demostró ser de gran utilidad en la diferenciación de las cepas de M. anisopliae, debido a que con los dos métodos se evidenció la presencia de variabilidad genética y además permitió ubicar a los aislamientos 136 y 137 siempre en el mismo grupo.
Footnotes
Agradecimientos
Este trabajo se realizó en la Unidad de Biotecnología y Control Biológico de la Corporación para Investigaciones Biológicas - CIB, y fue cofinancindo por COLCIENCIAS. Agradecemos la colaboración del profesor Kenneth Roy por su asesoría en el manejo estadístico de este estudio.
