Abstract
For commercialization of entomopathogenic fungal formulations the control of biological, physical and chemical properties are necessary to assure the consumer a product of maximum field efficacy. This study summarizes the results of the analysis of quality variables such as spore concentration per gram, germination percentage (24 h), mortality percentage and average mortality time (days) of the coffee berry borer, of different Beauveria bassiana formulations evaluated between 1993-1998. Averages values were determined based upon the total number of samples of each product evaluated during the six years period. The highest spore concentration of B. bassiana was found in Conidia WG® (4,4x1010e/g), followed by freeze-dry Brocaril® (4.3x1010e/g). The latter also presented the highest germination (95±5,4) followed by the Cenicafé strain (86±5,6). The greater percentage of mortality caused to freeze-dry Brocaril® (92±10) in a time average of 4,5±0,8 days, and the Cenicafé strain (81±13) in 4,7±0,8 days. The Bb9205 isolation reactivated in berry borer, multiplied in rice with 30 days of development was used as reference, presented the following averages: concentration of 1,9x1010e/g, germination 90±8.1%, mortality 90±8.6% in 4,7±1,0 days. The results showed a high variability throughout the time especially in spore concentration; this variable this related to factors involved to the process of production like substrate, storage, temperature and humidity. The improvement of these limiting conditions has led to higher formulations quality in recent years.
Introducción
La protección de los cultivos está basada en el uso de pesticidas químicos. Es así como en 1988 el mercado de los pesticidas en el mundo fue estimado en más de 6 billones de dólares, de los cuales sólo el 1,6% fue de origen biológico y la mayoría derivados de Bacillus thuringiensis (Richards y Rogers 1990). Sin embargo más de 700 especies de hongos generalmente Deuteromycetos y Entomophthorales de cerca de 90 géneros son patógenos a insectos (Charnley 1989). Dentro de éstos los géneros más investigados incluyen Beauveria, Metarhizium, Verticillium, Hirsutella, Erynia (=Zoophtora), Nomuraea, Aspergillus, Aschersonia, Paecilomyces y Toliypocladium entre otros. Los dos primeros géneros han sido usados a gran escala por cierto número de años (Brady 1981).
Los intentos para usar hongos en forma extensiva en el control biológico fueron considerados inicialmente por Samson et al. (1988) y Gillespie (1988). B. bassiana se ha empleado a gran escala en China y en Rusia (Ferrón 1981, Khloptseva 1992), trabajos posteriores incluyen su utilización sobre Hypothenemus hampei (Murphy y Moore 1990, Bridge et al. 1990). En Irlanda Beauveria brongniartii ha sido usado para el control de Melolontha melolontha (Linnaeus) (Keller 1992). Metarhizium anisopliae ha sido desarrollado en Brasil (Metaquino) para control de Mahanarva posticata (Stal) plaga en caña de azúcar (Mendonca 1992, Ferrón 1981, Goettel et al. 1990) y en Australia contra plagas de pastos y caña de azúcar (Pinnock 1990); industrialmente Bayer formuló una preparación granular de micelio BIO 1020 (Reinecke et al. 1990) y cooperativas y compañías particulares lo han producido con niveles aceptables de control (Gillespie 1988). De las formulaciones más utilizadas, pero con éxito limitado, cabe destacarse Verticillium lecanii utilizado como un micoinsecticida contra áfidos y mosca blanca Trialeurodes vaporariorum (Westwood). Otro hongo, Hirsutella thompsonii, desarrollado como Mycar para control de Phyllocoptruta oleivora (Ashmead) (McCoy 1986), ha tenido inconvenientes entre los cuales se incluyen la necesidad de almacenamiento en frío, falta de un bioensayo útil, dificultad de producir conidias infectivas y la inconsistencia de los resultados observados en campo, probablemente debido a las condiciones ambientales adversas como largos períodos de humedad (McCoy y Tigano-Milani 1992).
La velocidad de acción de los productos biológicos es más lenta que un tratamiento químico y puede demorarse varios días o aún semanas; sin embargo, la diferencia entre los micoinsecticidas y los químicos en el tiempo de mortalidad no es tan grande como se sugiere (Bateman 1992). Además, los efectos debilitantes de la infección pueden reducir la capacidad del insecto para dañar los cultivos muchos días antes de la muerte (Moore et al. 1992). En aspectos como la seguridad humana y ambiental, los micoinsecticidas son potencialmente muy superiores, pero se requiere la educación de los agricultores, para poder entender sus limitaciones y si es necesario cambiar algunas prácticas agronómicas.
El mayor inconveniente en la producción masiva y eficiente de algunos micoinsecticidas es el costo alto de producción, ya que la comercialización no ha sido exitosa. Las condiciones medio ambientales adversas, incluyendo los efectos de bajos niveles de humedad, radiación U.V., temperaturas altas y prácticas agrícolas como la aplicación de fungicidas, van en contra del éxito de éstos (Moore y Prior 1993). Se adicionan además inadecuadas condiciones de almacenamiento, poca estabilidad en campo, falsas expectativas y malas interpretaciones de los resultados prácticos. Muchas de las fallas provienen de investigación básica inadecuada en la mayoría de los aspectos, desde la selección del patógeno hasta la aplicación en campo (Moore y Prior 1993). La optimización de las formulaciones basadas en la prevención de la desecación del hongo, mejoramiento genético y modificaciones en las prácticas de aplicación pueden disminuir la influencia de las condiciones ambientales adversas (Clarkson 1992, Keller 1992).
Afortunadamente, los productos biológicos se están mejorando continuamente, mientras las dificultades asociadas con el manejo convencional de productos químicos se están incrementando. Las compañías de agroquímicos están actualmente interesadas en la producción de pesticidas biológicos y su intervención puede acelerar el proceso de desarrollo. Para avanzar en el control de plagas con hongos entomopatógenos se requieren formulaciones que conserven en campo las características biológicas. La mayoría de los Deuteromycetos tienen requerimientos no específicos para la germinación, pero algunos inhibidores de germinación pueden estar presentes en el hospedero (Brownlee et al. 1990).
En la literatura es escasa la información acerca de protocolos o procedimientos para establecer un control de calidad a hongos entomopatógenos. Existe bastante información sobre Bacillus thuringiensis (Maas et al. 1967, Burges 1967) y algunas publicaciones sobre pruebas de seguridad a entomopatógenos (Burges 1981). En cuanto a hongos la información se limita a indicar las pruebas que se deben realizar (Müller-Kögler 1967, Habib 1986) y los requerimientos sobre la legislación de hongos entomopatógenos para su comercialización (Hall et al. 1983).
En Colombia el Instituto Colombiano Agropecuario (ICA) en 1991 expidió una reglamentación sobre la producción de entomopatógenos y los requerimientos para obtener licencias de producción y venta. Sin embargo, esta reglamentación adolece de una información detallada sobre el control de calidad de estos productos. Es así como, ante la sentida necesidad de tener normas claras y metodologías estandarizadas, Cenicafé emprendió desde 1992 la búsqueda de parámetros necesarios para el análisis de los hongos entomopatógenos, desarrollando pruebas de control de calidad con el fin de estandarizar y optimizar metodologías que permitan la evaluación de la calidad biológica y fisicoquímica de los hongos producidos comercialmente. Como resultado de estas investigaciones se han ofrecido técnicas para el control de calidad de formulaciones de hongos entomopatógenos las cuales permiten analizar periódicamente los productos presentados en sustratos naturales o formulados en seco con materiales inertes (Vélez et al. 1997).
En el laboratorio de control de calidad de hongos entomopatogenos de Cenicafé se han procesado hasta la fecha un total de 600 muestras, de las cuales el 33% corresponde a productos industriales formulados en inertes, 59% producciones en arroz en forma artesanal y el 8% restante producciones en SDA (Sabouraud Dextrosa Agar). Dichas formulaciones han sido recibidas y evaluadas entre los años de 1993 y 1998. Dentro de los productores de entomopatógenos están las casas comerciales que se interesaron desde un comienzo en formular esporas de estos hongos con productos inertes tales como: polvo estéril, microtalco estéril, tierra de diatomáceas, tierra filtrante, lactosa peptona, entre otros, con el objeto de conservar la viabilidad y capacidad infectiva después de largos períodos de almacenamiento y resistencia a factores medio ambientales en condiciones de campo. Estas compañías son: Laverlam, Biocontrol, Agrevo, y otras empresas que están incursionando en la formulación industrial como: Vecol, Onatec y Biogarden. La producción artesanal en sustrato arroz la realizan empresas como: centro de biotecnología Mariano Ospina Pérez, Centro de Investigaciones Biológicas (CIB), Cenicafé, cooperativas de caficultores a nivel nacional y agricultores asesorados a través de cursos de capacitación dictados por Cenicafé y por el Servicio de Extensión. Las producciones en SDA y en arroz (patrón de referencia) son realizadas en el laboratorio de Entomología de Cenicafé con el propósito de facilitar cepa reactivada a los laboratorios para sus producciones y para efectos de investigación, tanto de Cenicafé como de otras instituciones.
En el presente estudio se consolidan los resultados de calidad de las formulaciones existentes en el mercado nacional, para el control de la broca del café. Estos resultados han servido como parámetros y mecanismos de retroalimentación con los caficultores y productores con miras a mejorar los procesos de producción.
Materiales y Métodos
Para el análisis de los resultados de las pruebas de calidad, las diferentes formulaciones de B. bassiana se agruparon por producto (nombre comercial) y tipo de formulación (Tabla 1).
Las variables objeto de análisis para la discusión de resultados fueron: concentración de esporas/gramo, porcentaje de germinación a las 24 horas, porcentaje de mortalidad y tiempo promedio de mortalidad (días), las cuales determinan la aceptabilidad del hongo para aplicación en el campo.
Formulaciones de B. bassiana sometidas a pruebas de calidad en Cenicafé. (1993-1998)
Patrón de Comparación
Las pruebas de calidad se comparan con un patrón del hongo seleccionado producido con la tecnología de finca (Antía et al. 1992). El cultivo fue desarrollado a una temperatura promedio de 25±2°C y un tiempo de incubación de 25 días para obtener la máxima esporulación. El aislamiento utilizado fue Bb9205, este aislamiento ha presentado los mayores porcentajes de mortalidad y el menor tiempo promedio de mortalidad hacia la broca del café (González et al. 1993); motivo por el cual Cenicafé lo seleccionó para producirlo tanto a nivel artesanal como industrial.
Pruebas Microbiológicas
Concentración de esporas
La concentración de esporas determina el número de unidades infectivas por unidad de peso o volumen existente en la formulación, ésta sirve de base para establecer la dosificación de un producto. Para estimar la concentración de esporas del patrón de comparación de B. bassiana (Bb9205) se tomaron 4 submuestras procedentes de una misma botella escogida al azar de un cultivo con 25 días de desarrollo, a la cual se le removieron las esporas con la ayuda de una espátula, adicionando agua con Tween 80 al 0,1% hasta un volumen conocido (500 ó 1000 ml). De esta forma quedó preparada la suspensión madre de la cual se tomaron las submuestras de 1 ml; a partir de ésta se prepararon diluciones hasta 10−4 ó una dilución que permitiera el conteo en la cámara de Neubauer (Vélez et al. 1997). Para las formulaciones en polvo se tomó una muestra representativa del lote a examinar, por regla general, se toman 10g de cuatro recipientes y se prepara una mezcla de la cual se extraen cuatro sub-muestras de 1g, con estas submuestras, se prepararon las diluciones hasta 10−4 ó la dilución que permitiera el conteo (Vélez et al. 1997).
Germinación de esporas
Esta prueba, en combinación con el estimativo del número de esporas, calcula la cantidad de esporas viables de una formulación por unidad de peso o volumen. Este estimativo se hace con cada una de las submuestras preparadas para la concentración de esporas. La metodología empleada es la descrita por Vélez et al. (1997). Una formulación comercial debe tener una germinación superior al 85% en un tiempo de incubación de 24 horas. Lo anterior, debido a que cuando el hongo se asperja en el campo debe tener un rápido efecto sobre la población de la broca con miras a interrumpir el proceso reproductivo de ésta y a la vez sobreponerse a las condiciones ambientales adversas.
Prueba de patogenicidad
Corresponde al bioensayo más importante en el análisis de calidad de una formulación, determina si el patógeno realmente ataca o no a la broca. Sin embargo, no asegura que bajo condiciones de campo su eficacia sea igual a la registrada en laboratorio. Requiere la cría de los insectos en el laboratorio. Para el desarrollo de la prueba se utilizó la metodología descrita por González et al. (1993). Los productos deben causar porcentajes de mortalidad superiores al 80% en el menor tiempo posible (3,8 días).
Las pruebas de calidad de las formulaciones se deben realizar en las etapas de producción, distribución y almacenamiento de los hongos, para obtener información que permita corregir los factores que hacen que la calidad del producto se deteriore o pierda y de esta forma mantener los estándares de calidad.
Resultados y Discusión
Para la discusión e interpretación de los resultados se realizó un análisis de varianza (ANAVA) donde se incluyeron todos los tratamientos y se compararon mediante una prueba de Tukey a un nivel de significancia del 5%, a través de los 6 años de evaluación.
Los valores promedios para el producto Bassianil (T1) para los tres años (1993, 1994 y 1996) fueron los siguientes: Concentración de esporas/gramo 1,05x109; germinación 47,4%; porcentaje de mortalidad 25,26% en un tiempo de mortalidad de 5,39 días. Se presentaron diferencias significativas en la concentración de esporas a favor del año 1996 (Fig. 1).
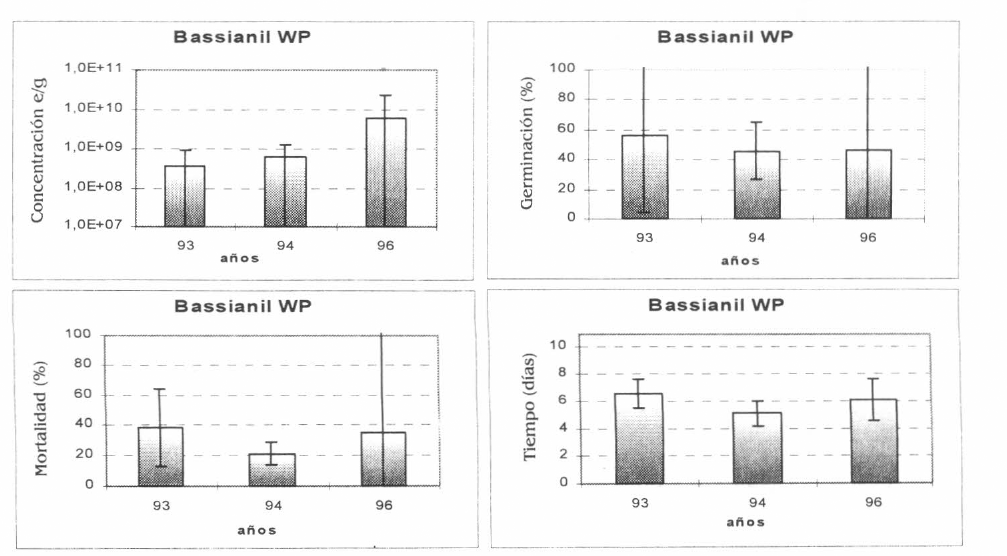
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) del producto Bassianil WP.
El T2 (Brocaril WP) se evaluó por cuatro años (1993, 1994, 1995 y 1996). Los promedios encontrados fueron: Concentración de esporas/gramo 3,9x109; germinación 71,8%, porcentaje de mortalidad 32,78 y tiempo de 6,5 días. No se encontraron diferencias para las variables concentración, mortalidad y tiempo, pero si para la variable germinación (Tukey 5%) (Fig. 2).
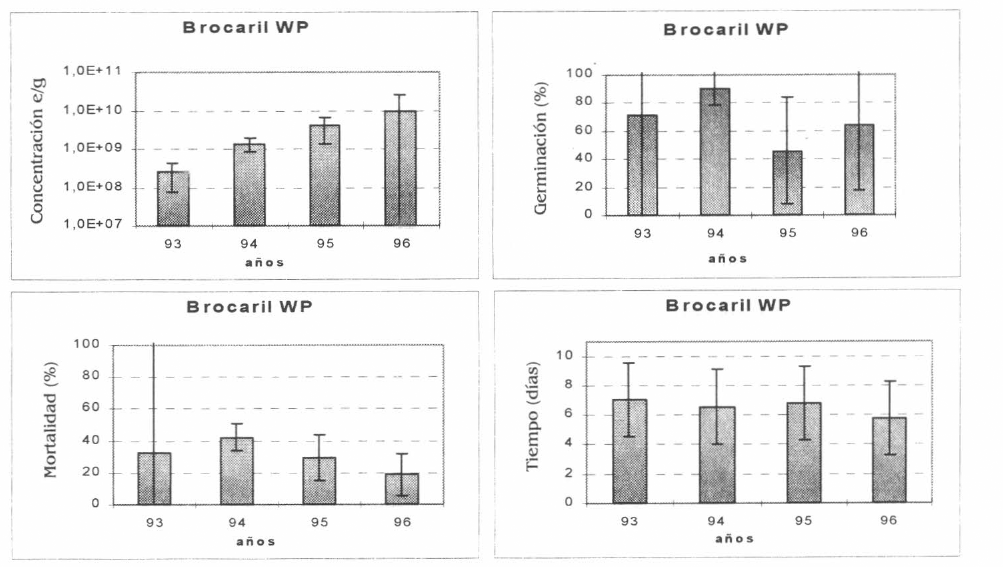
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) del producto Brocaril WP.
El producto Brocaril liofilizado (T3) fue recibido por dos años (1994, 1995), destacándose como el mejor producto formulado. Los promedios obtenidos a través del tiempo fueron: Concentración 4,3x1010e/g; germinación 95,8%; mortalidad del 91,56% en un tiempo de 4,5 días. Se presentaron diferencias significativas para las variables germinación, mortalidad y tiempo, a favor del año 1994 (Fig. 3). No obstante, las buenas características biológicas, presentó taponamiento de boquillas (aspersora presión previa retenida con boquilla HC-3) por el tamaño de partícula del inerte.
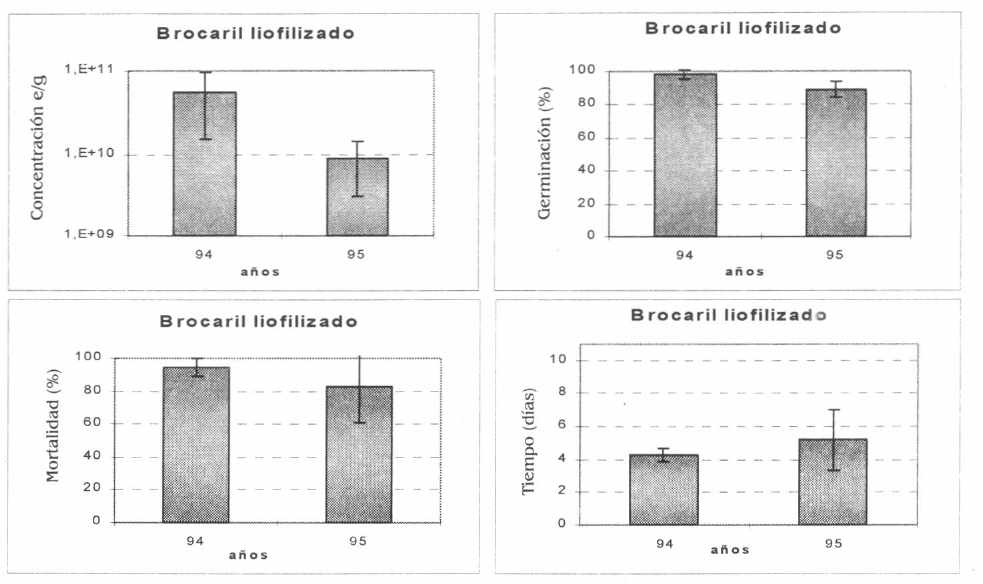
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) del producto Brocaril liofilizado.
A pesar de que la concentración del producto Conidia WP (T4) presentó en los dos años de evaluación (1993, 1994) muy buen promedio de esporas (1,1x1010), los promedios de germinación, mortalidad y tiempo estuvieron por debajo de los parámetros establecidos. No se presentaron diferencias significativas en las variables en los dos años de evaluación (Fig. 4).
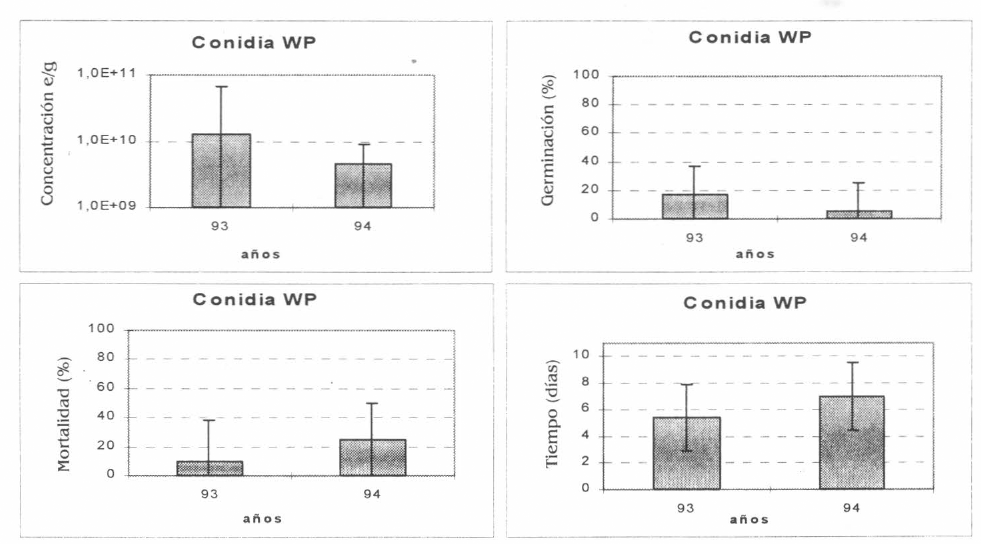
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) del producto Conidia WP.
Es de anotar que los tratamientos 1, 2 y 4 fueron formulaciones en polvo mojable que no cumplieron con los estándares de calidad, probablemente debido al tipo de inerte, el cual favoreció la presencia de contaminantes y causó pérdida de humedad de las conidias, retardando los procesos de germinación y patogenicidad.
El tratamiento Conidia WG (T5), elaborado en gránulos dispersables, inició su producción en 1994 hasta la fecha. Los promedios para las cuatro variables fueron: Concentración 4,4x1010 e/g; germinación del 49%, mortalidad del 35% y tiempo de 4,9 días. Se presentaron diferencias significativas (Tukey 5%) en la germinación a favor de los años 1997 y 1998 respecto a los años anteriores. Igual ocurrió con la patogenicidad la cual fue mayor para los años 97 y 98 (Fig. 5).
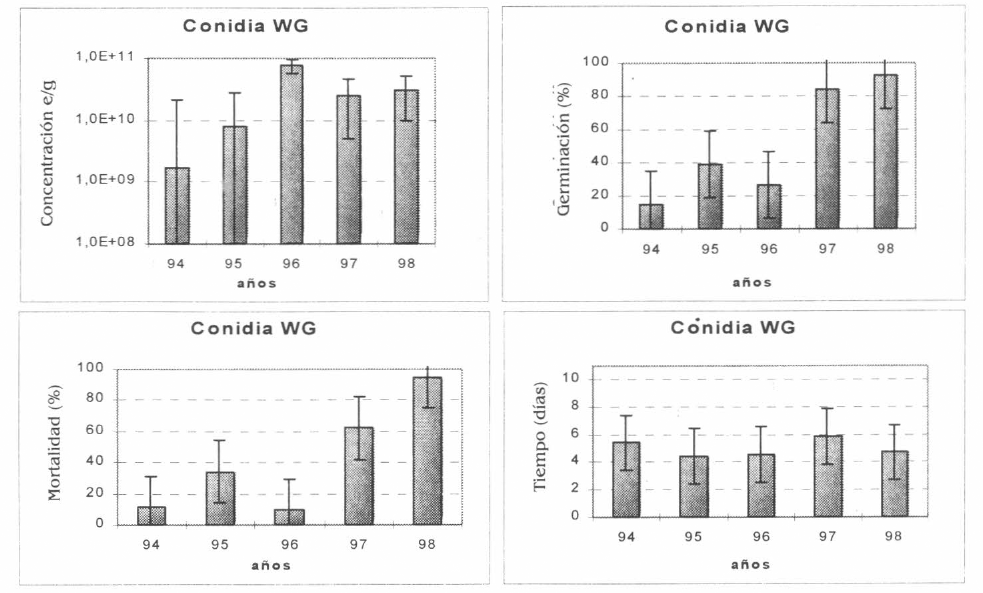
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) del producto Conidia WG.
La Cepa Cenicafé (T6) fue producida artesanalmente en botella, siguiendo la metodología de Antía et al. (1992), elaborado por un laboratorio particular ubicado en las instalaciones de Cenicafé-granja. Los promedios en los seis años de evaluación han sido los siguientes: concentración de esporas/gramo 3,7x109; germinación 84,8%; mortalidad 80,75% en un tiempo de 4,7 días. En todo el tiempo de seguimiento de la calidad de las formulaciones de B. bassiana, conservó las cualidades biológicas y físicas y mejoró la concentración significativamente en 1997 y 1998 con respecto a los años anteriores (Fig. 6).
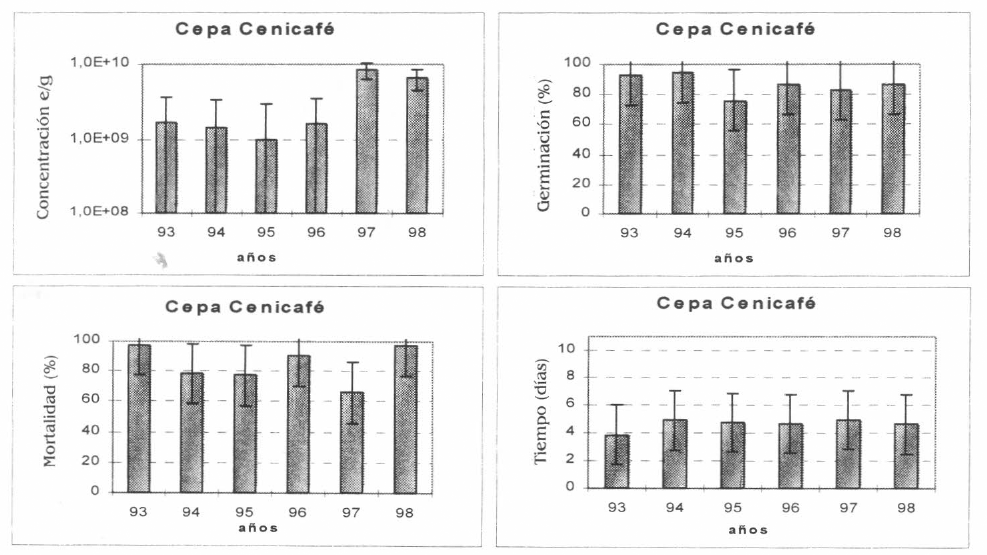
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) de la Cepa Cenicafé.
En la producción artesanal (T7) se incluyeron las producciones en arroz recibidas de las Cooperativas de Caficultores, agricultores y personas particulares que han incursionado en el proceso de comercialización. En general los resultados mostraron promedios aceptables para las cuatro variables, así: Concentración 3,9 x109e/g, germinación 86%, mortalidad de 79% en 4,9 días. El análisis estadístico no mostró diferencias significativas en los cinco años de evaluación para ninguna de las variables (Fig. 7).
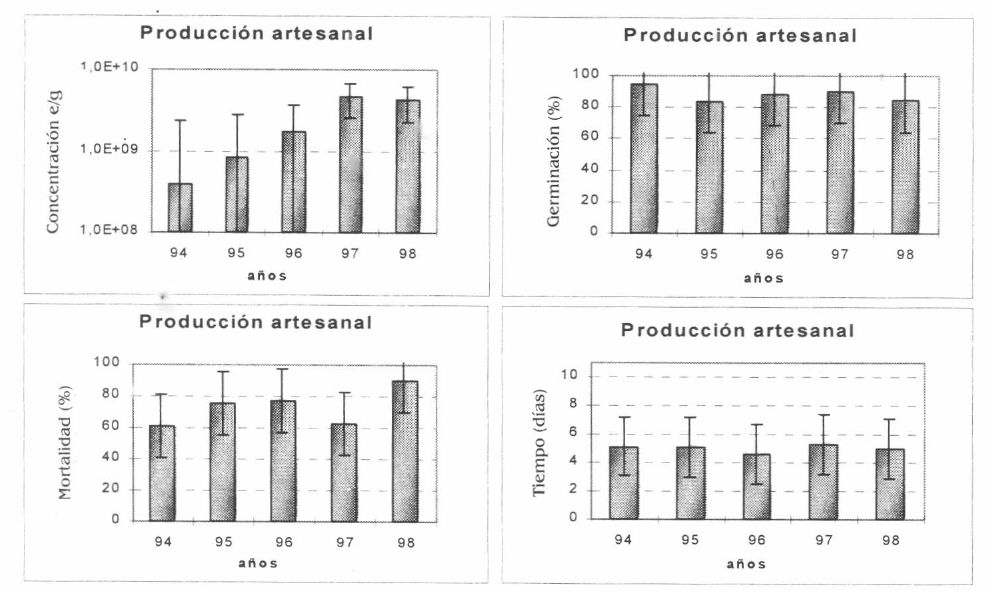
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) de la producción artesanal.
El tratamiento 8 correspondió a la formulación del hongo en arroz inicialmente denominada "Matabroca" el cual era empacado en bolsa plástica de polipropileno (1993, 1994, 1995) y posteriormente denominado Cebiopest cambiando su presentación de empaque a bolsas metalizadas. Los resultados han mostrado en general altos promedios de concentración y germinación de esporas, sin embargo, el promedio de mortalidad en los cinco años evaluados fue de 68,8%. Se presentaron diferencias significativas (Tukey 5%) en el año 98 para las variables concentración y mortalidad con respecto a los años 94, 95 y 97 (Fig. 8).
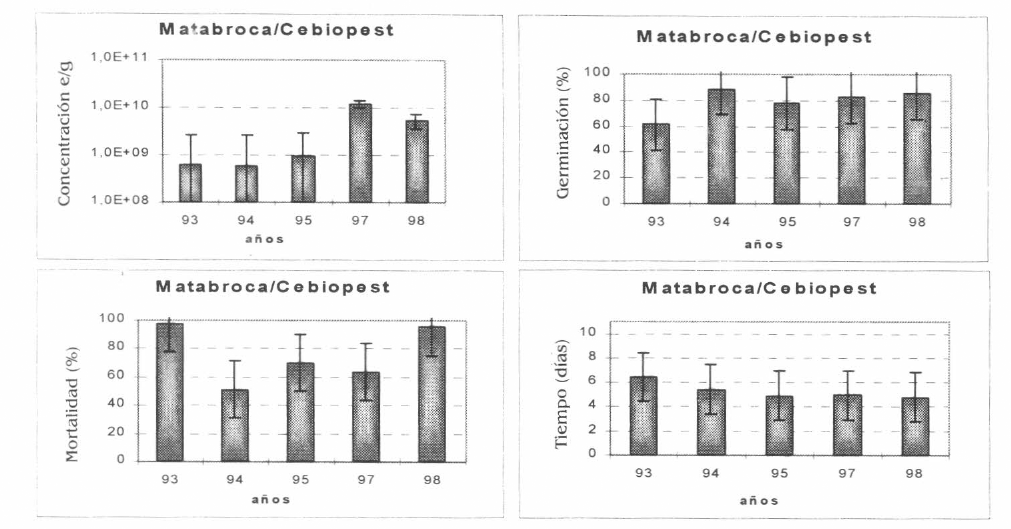
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) de la producción Matabroca/Cebiopest.
El tratamiento 9 (T9) o patrón de referencia ha sido el más estable y el mejor producto en arroz en todo el tiempo de evaluación, presentando promedios de concentración de 1,9x1010 e/g, germinación de 89%, mortalidad del 90% y tiempo promedio de 4,7 días. No se presentaron diferencias significativas a través del tiempo para las cuatro variables. Es de anotar que estas producciones corresponden a lotes pequeños utilizados como patrón de referencia en el proceso de calidad, evaluación de aislamientos de la colección de entomopatógenos de Cenicafé, distribución de cepa madre a las diferentes casas comerciales y ensayos de laboratorio y campo tanto de Cenicafé como de otras instituciones (Fig. 9).
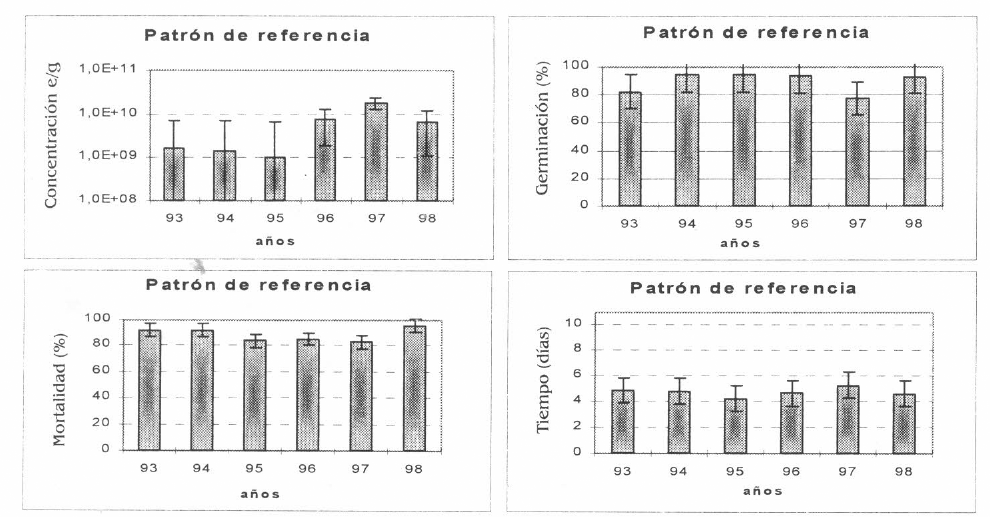
Promedio de las variables: Concentración de esporas/gramo, Germinación (%), Mortalidad (%) y Tiempo de mortalidad (días) del patrón de referencia.
Los resultados anteriores muestran que el aislamiento Bb9205 producido en arroz, pese a que presenta variaciones inherentes a su fisiología y condiciones medioambientales, ha sido el más estable a través del tiempo, lo que deja al descubierto la necesidad de continuar desarrollando investigación en el área de formulaciones, dado que hasta el momento cuando se adiciona al hongo cualquier insumo o inerte (talco, bentonita, tierra de diatomáceas, entre otros) los hongos no logran conservar las cualidades biológicas y alteran las propiedades físicas del mismo. Igualmente, se pone de manifiesto los esfuerzos realizados por Cenicafé para desarrollar investigaciones que conduzcan al conocimiento integral de los hongos tales como: efecto de la luz ultravioleta en laboratorio y campo (Vélez 1993), pH, tiempo y condiciones óptimas de almacenamiento (González 1994), evaluaciones en campo (Bustillo et al. 1991, Benavides y Posada 1995), tecnologías de aplicación en campo (Villalba et al. 1998), técnicas para el análisis de calidad (Vélez et al. 1997), selección de aislamientos y mejoramiento de cepas (Vélez 1996). En cuanto a la adopción en finca del hongo B. bassiana, Duque y Chaves (1997) registran un 13% en nueve departamentos cafeteros de Colombia, pero anotan que el caficultor piensa que el hongo es muy lento en su acción; sin embargo, en la medida en que se mejore la calidad biológica y fisicoquímica de las formulaciones, la posibilidad de que los agricultores adopten el hongo Beauveria bassiana, como otro componente en el Manejo Integrado de la Broca, es mayor.
Conclusiones Y Recomendaciones
• El conocimiento adquirido permite realizar retroalimentación con los caficultores y productores acerca de los requerimientos específicos del hongo para el desarrollo de una formulación óptima.
• Se deben realizar estudios donde se evalúen los factores que influyen en los procesos de germinación (tipos de inerte, tiempo de secado, procesos de deshidratación), requerimientos nutricionales específicos para cada hongo y condiciones adecuadas de almacenamiento necesarias para garantizar la estabilidad del producto final a través del tiempo.
Footnotes
Agradecimientos
Los autores expresan sus agradecimientos a los señores Eduardo Osorio, Myriam Giraldo, Carlos A. Quintero y Sergio Sánchez por su gran colaboración en el desarrollo de la investigación.
