Abstract
Six isolates of the entomopatogenous fungus Beauveria bassiana were selected from the culture collection of the Laboratorio de Investigaciones sobre la Química del Café y sus productos naturales (LIQC). The purpose of this study was to examine some of the macroscopic, microscopic, physiological y biochemical characteristics of these isolates, in order to establish which ones of these could be used for differentiation of isolates. Moreover, these characters were analyzed for their relation with virulence of isolates against Hypothenemus hampei. The macroscopic characteristics of the colonies such a color, type, aspect, sinemmata and oosporein production, could not be used for isolates differentation, because they are so variable. The microscopic characteristics evaluated, neither the size and form of the conidia, nor the relative abundance of blastoconidia, could be utilized for diferentiate the isolates. The conidial resistance to high temperatures and conidial resistance to their exposition to ultraviolet light, and the lipase production were the only characters that differentiated isolates. However, these physiological features only classified the islotes in groups and they do not allowed their differentiation individually. The banding patterns of a- y ẞ-esterases were clearly distinctive for each isolate, with unique bands, except the 8906 isolate (origin from Cuba). It was not find the existence of any type of relationship between the characteristics evaluated in this study, nor between these characters and the virulence of isolates against the coffee berry borer. However, based in the results of this study it can be suggested that the isolates 8505 and 8905, may be in a mixture, could be used in biological control programs. The reason for this suggestion is that these isolates have a group of important biological features. Any case, before to use these isolates, its behaviour under field conditions might be evaluated.
Introducción
El hongo entomopatógeno Beauveria bassiana Bálsamo (Vuillemin) ha sido ampliamente usado para el control de muchas plagas de importancia económica en varios cultivos en todo el mundo y ha sido probado en diferentes insectos plaga (Trefi 1984; Campbell et al. 1985; Rombach et al. 1986; Aguda et al. 1987; Hajek et al. 1987; Anderson et al. 1988; Ming-Guang y Johnson 1990; Leathers y Gupta 1993).
La broca del café, Hypothenemus hampei (Coleoptera: Scolytidae), es considerada como una de las plagas más importantes del. café (Bustillo et al. 1993). Este insecto pasa la mayor parte de su ciclo de vida dentro de la cereza de café, puesto que la copulación y todas las etapas de desarrollo del insecto se presentan allí. Solamente la hembra, que perfora el grano de café puede volar fuera de éste, mientras que el macho, que no posee alas, muere dentro del grano (Cárdenas 1993). Debido a esto es necesario realizar un control de la plaga que involucre un agente de amplia diseminación. Como el ciclo de vida de la broca se desarrolla principalmente dentro del grano, los agentes de control biológico que pueden transmitirse de un individuo a otro, podrían ser, en teoría, más efectivos que el control químico.
Además, la aplicación a gran escala de plaguicidas químicos, para controlar una plaga particular en áreas de cultivo altamente infestadas, favorecen la generación de resistencia por parte de la plaga, la resurgencia de la misma, la aparición de plagas secundarias, reducen las poblaciones de enemigos naturales y causan efectos adversos en los agricultores y el ambiente (Pedigo 1996). Todos estos problemas han renovado el interés por la utilización de métodos alternativos de control, entre los cuales los microorganismos que son capaces de atacar plagas constituyen una promesa alentadora (Charnley 1989).
Debido a que los hongos son los entomopatógenos potencialmente más versátiles, tienen un amplio rango de hospederos, infectan distintas edades y estados de desarrollo de sus hospederos y a menudo causan epizootias naturales (Ferron 1978) se seleccionó el hongo Beauveria bassiana para ser usado como agente de control biológico contra la broca del café H. hampei, dentro del marco de un programa para el control de esta plaga por parte de la Federación Nacional de Cafeteros de Colombia. La escogencia de esta especie se debió a que es un patógeno natural de este insecto y a que se ha encontrado como saprófito en zona cafetera.
Se puede lograr un control mejor de esta plaga utilizando los mejores patotipos que posean características adaptativas que favorezcan su supervivencia en campo y su efectividad como micoinsecticida.
Algunos estudios previos han investigado la posible relación existente entre ciertas características particulares de Beauveria bassiana y su relación con la virulencia del mismo, como ciertas características fisiológicas (Paris y Ferron 1979; Paris et al. 1985; Ming-Guang y Jonnson 1990) y la producción de enzimas (Bidochka y Kachatourians 1990; Sosa-Gómez et al. 1994). Sin embargo, es importante identificar un amplio rango de características morfológicas, fisiológicas y bioquímicas que favorezcan la supervivencia del hongo en campo y su efectividad como micoinsecticida contra H. hampei.
En este estudio, llevado a cabo a nivel de laboratorio, se reporta la variabilidad de seis aislamientos de B. bassiana, con base en características de morfología microscópica y macroscópica y características fisiológicas, y se prueba el significado de estas variables en relación con la virulencia frente a H. hampei.
Materiales y Métodos
Aislamientos
Se seleccionaron seis aislamientos de Beauveria bassiana de la colección con que cuenta el Laboratorio de Investigaciones sobre la Química del Café y sus Productos Naturales (LIQC), los cuales diferían en su origen geográfico y de hospedero (Tabla 1). Cultivos de reserva de cada aislamiento fueron conservados mediante liofilización y cada vez que era necesario, el cultivo liofilizado fue reconstituido en Sabouraud líquido y luego, sembrado en Agar Sabouraud Dextrosa con 0,2% de extracto de levadura (ASDY) e incubado durante siete días a 27°C en oscuridad.
Aislamientos de Beauveria bassiana utilizados en el presente estudio.
Para obtener el inóculo para todos los experimentos, el hongo crecido a partir de los cultivos anteriormente mencionados, fue recogido y suspendido en Tween 20 0,05%. Esta suspensión fue filtrada por un filtro Millipore #4, el cual tiene un tamaño de poro de 5-15 µm. La suspensión conidial obtenida fue ajustada a una concentración de 1x10º conidios/ml.
Se realizaron tres repeticiones para todos los experimentos.
Evaluación de la viabilidad de las conidios
Para la determinación de la viabilidad de las conidios en la mayoría de los experimentos, se utilizaron láminas portaobjetos impregnadas con una delgada capa de ASD, el cual es una variación del método utilizado por Samuels et al. (1989). La capa de agar fue dividida en tres secciones iguales con ayuda de un bisturí estéril y cada sección fue inoculada con 0,6 ml de una alícuota de la suspensión de conidios preparada. Las láminas fueron incubadas por separado en cámara húmeda, utilizando cajas de Petri (HR>90%), a 27°C, en oscuridad, por 24 horas, y al final de esťe período de incubación se determinó el porcentaje de germinación.
Morfología macroscópica de colonias
Se inoculó 0,1 ml de una alícuota de la suspensión de conidios preparada a una concentración de 1x10º conidios/ml en cada una de tres cajas de Petri que contenían ASD. Las cajas fueron incubadas a 27°C, en la oscuridad. Después de 10 días de incubación, se registró el color, tipo, aspecto, formación de sinemas y de oosporeína. El color se determinó de acuerdo con la tabla de colores de Küppers (1978).
Características de los conidios
300 conidios provenientes de cultivos de 10 días de edad, crecidos en ASD e incubados a 27°C, en la oscuridad, fueron examinados para determinar su forma y para medir su tamaño, mediante un microscopio al que se le adaptó un micrómetro.
Adicionalmente, la producción de conidios secundarios, con forma que varía de elipsoidal a cilíndrica (Mac Leod 1954), llamados por Thomas et al. (1987) blastosporas, fueron detectadas 24 horas después de la incubación, de una suspensión conidial de concentración 1x10 conidios/ml que había sido inoculada en ASD, a 27°C, en la oscuridad. Como este evento es bastante inusual, se registró su presencia y abundancia relativa de manera semicuantitativa (de + a +++).
Esporulación
Con el fin de cuantificar la esporulación de los diferentes aislamientos, se colocó 0,1 ml de una suspensión de concentración 1x10º conidios/ml (concentración final: 1x10 conidios/caja), en cajas de Petri que contenían ASD y una película de celofán sobre el medio de cultivo, método usado por Ritz y Crawford (1990), para evitar que las hifas penetraran en el agar. Después de un período de incubación de 10 días a 27°C y en oscuridad, todas los conidios fueron cosechados de la película de celofán y suspendidos en un erlenmeyer que contenía Tween 20 0,05%. Luego, la suspensión de conidios fue homogenizada con un homogenizador de aspas cortantes a 1200 rpm por dos minutos, para liberar todas los conidios en el agua.
A partir de esta suspensión, se realizó una dilución 1/100 y los conidios se contaron directamente en un hemocitómetro. Para determinar la producción de conidios, se realizaron tres conteos para cada erlenmeyer y se calculó la cantidad de conidios obtenido por cmβ.
Tasa de crecimiento de la colonia
A seis cajas de Petri de 90 mm de diámetro que contenían ASD, se les practicó un orificio de 2 mm de diámetro en el centro del agar. En cada orificio, se inoculó 0,1 ml de una suspensión de conidios de 1 x 10º conidios/ml. Las cajas se incubaron a 27°C en oscuridad. El diámetro de crecimiento de las colonias se midió diariamente durante 10 días, siempre sobre una línea previamente demarcada sobre la colonia, en el fondo de la caja.
Tasa de crecimiento hifal
Se realizaron mediciones del crecimiento de hifas individuales siguiendo el método descrito por Robinson (1978), pero introduciendo la variante de medir a intervalos de 10 minutos cada una, durante un período de una hora. Para la medición, se seleccionaron tres hifas de la periferia del crecimiento del hongo.
Germinación de las conidias
Se impregnaron láminas portaobjetos con una delgada capa de ASD. Cada una de tres láminas fue inoculada con 0,6 ml de una suspensión de conidios de 1 x 106 conidios/ml. Las láminas se incubaron en cámara húmeda (RH 90%) a 27°C, en oscuridad. A partir de las 12 horas de incubación y hasta las 24 horas, cada lámina fue examinada a intervalos de una hora, para cuantificar el porcentaje de germinación y, luego, determinar el tiempo requerido para la germinación del 50% de las conidias, el cual se calculó mediante un análisis probit.
Sensibilidad de las conidias a la temperatura
Este parámetro fue determinado por la inoculación de 1 ul de la suspensión de conidias en cada uno de tres tubos que contenían 10 ml de agua estéril (concentración final de 1 x 106 conidias/ml). Cada tubo fue colocado en un baño de agua a una de tres temperaturas: 45°, 50° y 55°C. Después de 10 minutos de exposición a cada temperatura, 0,6 ml de la suspensión de cada tubo fue sembrada en láminas portaobjetos impregnadas con una delgada capa de ASD. Las láminas fueron incubadas en cámara húmeda a 27°C y en oscuridad. El porcentaje de germinación fue registrado a las 24 horas, por el conteo de 600 conidias usando el microscopio. Se realizaron tres conteos de 200 conidias para cada tubo.
Susceptibilidad de las conidias a la radiación ultravioleta
Se tomaron tres alícuotas de 185 µl cada una, a partir de una suspensión conidial de 1x106 conidias/ml y cada una se colocó en un pozo de 1,5 cm de diámetro, de una placa de poliestireno de 24 pozos, de fondo plano. La placa fue ubicada a 25 cm de una lámpara germicida standard de onda corta (GE 30T8, de 15 W, con una emisión de longitud de onda de 240-260 nm). La radiación incidente a esta distancia fue de 2.4x10° erg/cmβ. La exposición de las conidias a la radiación ultravioleta se realizó en la oscuridad, a 25°C durante 30, 60, 90, 120, 150 y 180 segundos. Las conidias utilizadas como control, fueron protegidas de la radiación. 60 µl de cada alícuota irradiada con cada una de las dosis, fue inoculada en una lámina portaobjetos impregnada con ASD e incubada en cámara húmeda a 27°C y en oscuridad, durante 24 horas. Al final de este tiempo, el porcentaje de germinación fue determinado por el conteo de 600 conidias en el microscopio.
Producción de lipasa
El micelio usado para la extracción de las proteínas fue obtenido del crecimiento del hongo en ASD, usando el método de la película de celofán. El hongo fue incubado a 27°C, en oscuridad, durante diferentes períodos de tiempo (3, 4, 5, 6, y 7 días). Después de cada período de tiempo, el micelio fue recolectado de la película de celofán y se obtuvieron extractos de éste por maceración del micelio a 4°C en buffer Tris-maleato 0.1 M, pH 6.0. La actividad lipasa en los extractos de micelio fue visualizada usando la técnica de agar en placa descrita por Hankin y Anagnostakis (1975). Ensayos semicuantitativos se realizaron después de 24 horas de incubación a 27°C, para determinar el diámetro del halo de precipitación alrededor de orificios practicados en el agar, que contenían 10 µl de extracto de micelio. Se realizaron tres réplicas por placa para cada aislamiento.
Electroforesis
Las proteínas del micelio fueron separadas por electroforesis vertical en condiciones no denaturantes, en geles de poliacrilamida, los cuales fueron preparados para obtener un gradiente del 5-25%. Muestras de 40 µl de extracto de micelio, cada una con un contenido de proteína de 90 µg, determinada por el método de Bradford (Bradford 1976) fueron colocadas en cada carril. Los geles se corrieron usando buffer Tris-glicina 1,5 M pH 8,8, durante 12 horas a 4°C con un poder constante de 200 volt y una intensidad inicial máxima de 11 mA. Las proteínas totales fueron teñidas con azul de Coomassie (Sigma) y las bandas de a- y ẞ-esterasas con una coloración específica reportada por Shaw y Prasad (1970). Los geles fueron lavados con agua destilada y preservados en glicerol al 5%.
Extractos de los aislamientos de 3, 4,5, 6 y 7 días de crecimiento fueron corridos en los geles. Las muestras que mostraron un número mayor de bandas fueron seleccionadas para la comparación entre aislamientos.
Pruebas de virulencia
Para probar la virulencia relativa de todos los aislamientos contra H. hampei, se inocularon insectos adultos con el hongo, poniéndolos en contacto con una suspensión de conidias de concentración 1x106 conidias/ml durante dos minutos. Los insectos inoculados y los controles (no inoculados) se mantuvieron individualmente en frascos estériles de vidrio de 10 ml de capacidad, taponados con algodón. En el fondo de cada frasco, se colocó papel de filtro humedecido con agua estéril, con el fin de mantener la humedad interna. Para simular el microhábitat del insecto, se introdujo un grano de café en cada frasco. Los frascos que contenían los insectos inoculados y los no inoculados se mantuvieron a 25°C, con un fotoperíodo de luz: oscuridad de 10:14 horas, durante 10 días.
Las brocas se observaron diariamente para determinar el tiempo letal medio (LT50). Los insectos muertos se dejaron en cámara húmeda sin esterilización superficial para permitir el desarrollo saprofitico del hongo sobre la superficie del insecto. Para estas pruebas se usaron 10 insectos por réplica y cuatro réplicas para cada aislamiento. El experimento se repitió tres veces.
Análisis Estadísticos
Los análisis estadísticos para los datos de tamaño de conidias se realizaron mediante una prueba de Chi-cuadrado. Los datos de tasa de crecimiento de la colonia e hifal, la germinación de las conidias, la sensibilidad de las conidias a la temperatura, la susceptibilidad de las conidias a la radiación ultravioleta y la producción de lipasa se analizaron usando la prueba de Kruskal-Wallis y un análisis a posteriori tipo Tukey. Los análisis de regresión probit se realizaron para obtener los valores del tiempo de germinación medio (TG50 y LT50). El test de rangos de Spearman fue usado para establecer la correlación entre todas las variables. El nivel a de confidencia utilizado fue del 95%.
Resultados
En la Tabla 2 se presentan los resultados de la morfología macroscópica. El color de la colonia de los diferentes aislamientos presentó una amplia variación entre blanco y amarillo. El tipo y el aspecto de la colonia también fueron características que variaron, aún, para cada aislamiento. El aspecto está determinado por la proporción de micelio con respecto a la de conidios (MacLeod 1954). La producción de oosporeína y la formación de sinemas solamente se presentaron en dos aislamientos: 8911 y 9006.
Características de la morfología macroscópica de los aislamientos de Beauveria bassiana. Condiciones de cultivo: Medio ASD, 27±1°C, 10 días y en oscuridad.
Con respecto a la morfología macroscópica, se encontraron tres rangos de tamaño y dos tipos de forma de las conidias: <= 2,5 μm (redondos), 2,6-3,5 μm (redondos) y 4,0-5,0 x 2,5-3,0 μm (subglobosos). La Tabla 2 muestra que los aislamientos 8505 y 8905 tienen conidias elipsoidales, que difieren de las conidias redondas típicas de esta especie. Estos mismos aislamientos fueron los únicos que tuvieron una cantidad abundante de blastoconidios.
El tamaño de las conidias varió entre 2,5 y 5,0 µm. Algunos aislamientos tuvieron una alta proporción de conidios de 2,5 µm y otros de 3,75 µm de diámetro. Sólo dos aislamientos mostraron una proporción baja de conidios de 5,0 µm de diámetro (Tabla 3).
Tamaño y forma de los conidios de los aislamientos originales y de los monospóricos de B. bassiana.
Los datos de tamaño de conidios están expresados como porcentaje promedio ± desviación estándar, para cada aislamiento.
Para descartar la posibilidad de contaminación de los aislamientos 8505 y 8905 con Beauveria brongniartii, que se caracteriza por presentar este tipo de conidias (Domsch et al. 1980), se realizaron cultivos monospóricos de todos los aislamientos y los resultados se muestran en la Tabla 4. La proporción de los diferentes tamaños de conidios encontrados en los cultivos monospóricos fue similar a la de los aislamientos originales.
Morfología microscópica de los aislamientos de B. bassiana analizados.
Abundancia de blastoconidios en cultivo sólido: -=Ninguno, +=Pocos, +++= Abundantes. Datos de esporulación son los promedios + desviación estándar de nueve datos para cada aislamiento.
Promedios con la misma letra no son significativamente diferentes (P>0,05).
La mayoría de los aislamientos mostró una producción total de conidios similar, a excepción de los aislamientos 8904 y 8911, los cuales produjeron una mayor cantidad y una menor cantidad (Tabla 4), respectivamente (P=0,040).
Los resultados de los parámetros fisiológicos analizados, se muestran en la Tabla 5. La tasa de crecimiento de la colonia es muy similar entre los aislamientos, pero la tasa de crecimiento hifal mostró que los aislamientos 8505 y 8905 tenían una tasa de crecimiento mayor y que el 9006 tenía la menor (P=0,001).
Comparación de los aislamientos de B. bassiana con respecto a algunas características fisiológicas evaluadas.
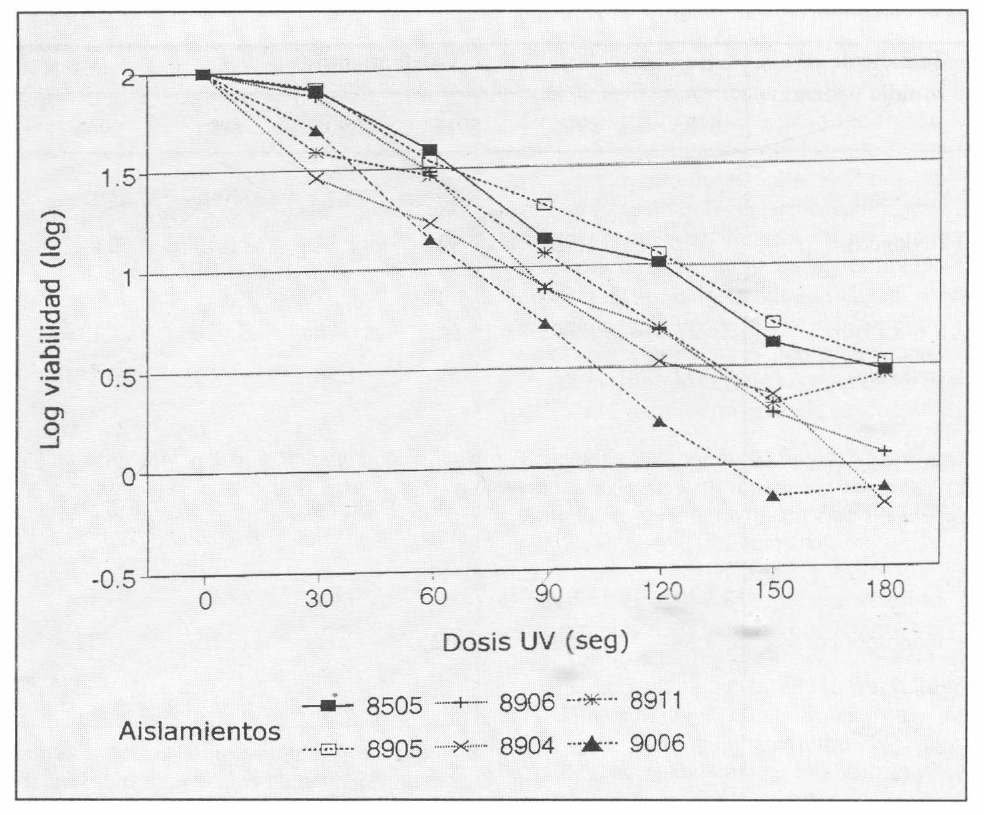
(1) Datos de tasa de crecimiento de colonia están expresados como promedio ± desviación standard. (2) Los datos de tasa de crecimiento hifal están expresados como el promedio ± desviación standard. (3) Los datos de tiempo de germinación (TG50) están expresados como promedios. (4) Los datos de sensibilidad a la temperatura son porcentajes promedio de viabilidad de los conidios a 50°C. (5) Los datos de susceptibilidad de los conidios a radiación ultravioleta son promedios de la viabilidad de las conidios expuestas 180 segundos a 2.4x106 erg/cmβ x sec. (n=90 para todas las variables).
Los datos con la misma letra (a,b,c,d) conforman grupos en los cuales los promedios no son significativamente diferentes uno de otro, por un análisis a posteriori tipo Tukey.
Comparación de los aislamientos con respecto a la detección de la actividad lipasa.
Los datos son los promedios de las mediciones realizadas + la desviación estándar e incluyen el área del orificio practicado en el agar para adicionar el extracto micelial (n=9/día para cada aislamiento).
Comparación del porcentaje de mortalidad de H. hampei provocada por una suspensión de conidios de B. bassiana los aislamientos sobre H. hampei¹.
Insectos adultos de H. hampei inoculados por contacto con una suspensión que contenía 1x107 conidios/ml.
Los datos de porcentaje de mortalidad son promedios después de 10 días + desviación estándar de 12 datos.
Promedios con la misma letra no son significativamente diferentes (P>0,05).
Los aislamientos 8505, 8906 y 8905 tuvieron un tiempo de geminación más corto. Los aislamientos que presentaron tiempos de germinación largos poseen tasas de crecimiento bajas, con excepción del 8906.
El tiempo de germinación medio (TG50) en ASD varió entre 14 y 19 horas para todos los aislamientos evaluados.
La viabilidad de los conidios disminuyó entre 45° y 50°C, con una mortalidad total a los 55°C para todos los aislamientos. Se encontró diferencia estadística entre los aislamientos de acuerdo con su respuesta a la temperatura (P=0.019). Una temperatura de 45°C no tuvo un efecto pronunciado en la viabilidad de los conidios. Esta sólo redujo en 10% a 20% la viabilidad para todos los aislamientos (datos no mostrados). Sin embargo, hay una alta mortalidad a 50°C, que varió entre el 82 y el 90%.
Los aislamientos 8906 y 8905 fueron los más resistentes a esta temperatura (Tabla 5).
Mayores dosis de radiación ultravioleta provocan una disminución en la sobrevivencia de los conidios. Este efecto se ve representado en las curvas dosis/mortalidad de los conidios de los diferentes aislamientos irradiados con ultravioleta (Fig. 1). A pesar que exhiben diferencias significativas en sensibilidad (P=0,001), solamente tres grupos pueden distinguirse basados en el efecto de este tipo de radiación.
Datos Figura 1
El diámetro del halo de producción de lipasa varió entre 5,66 mm (baja producción) a 14,44 mm (alta producción), entre el tercero y séptimo día de crecimiento de los distintos aislamientos (P=0,001) (Tabla 6). Una comparación entre los aislamientos para cada uno de los días de producción de lipasa examinados, mostró que se presentan diferencias significativas entre éstos (P=0,0001) para todos los aislamientos. La cantidad de enzima producida por los aislamientos 8906, 8905 y 9006 es estadísticamente diferente del día 3º al 7° (P=0,00021, P=0,0009 y P=0,0383, respectivamente). Se presentan dos grupos de aislamientos con una diferencia significativa de acuerdo con la producción de lipasa (P<0,05): 1) Tres aislamientos con una alta producción: 8505, 8906 y 890;. 2) Tres aislamientos con una baja producción: 8911, 8904 y 9006. Sólo dos aislamientos, 8906 y 9006 mostraron máxima producción al quinto día de crecimiento, el cual es significativamente diferente de los demís días. Los otros aislamientos no mostraron diferencias para la producción diaria de lipasa.
La comparación de las bandas de esterasas de los aislamientos se realizó con base en el día de crecimiento en que se presentó mayor número de bandas. Se encontraron seis patrones electroforéticos, uno para cada aislamiento analizado (Fig. 2). Sin embargo, el 75% de las bandas son compartidas por dos o más aislamientos. Todos los aislamientos mostraron de una a cuatro bandas exclusivas de cada uno (bandas A a K), excepto el aislamiento 8905 que no presentó ninguna. El mayor número de bandas lo presentó el aislamiento 8906. Además, los aislamientos 8505, 8904 у 9006, con origen a partir de insectos, comparten un número apreciable de bandas.
Aislamientos.
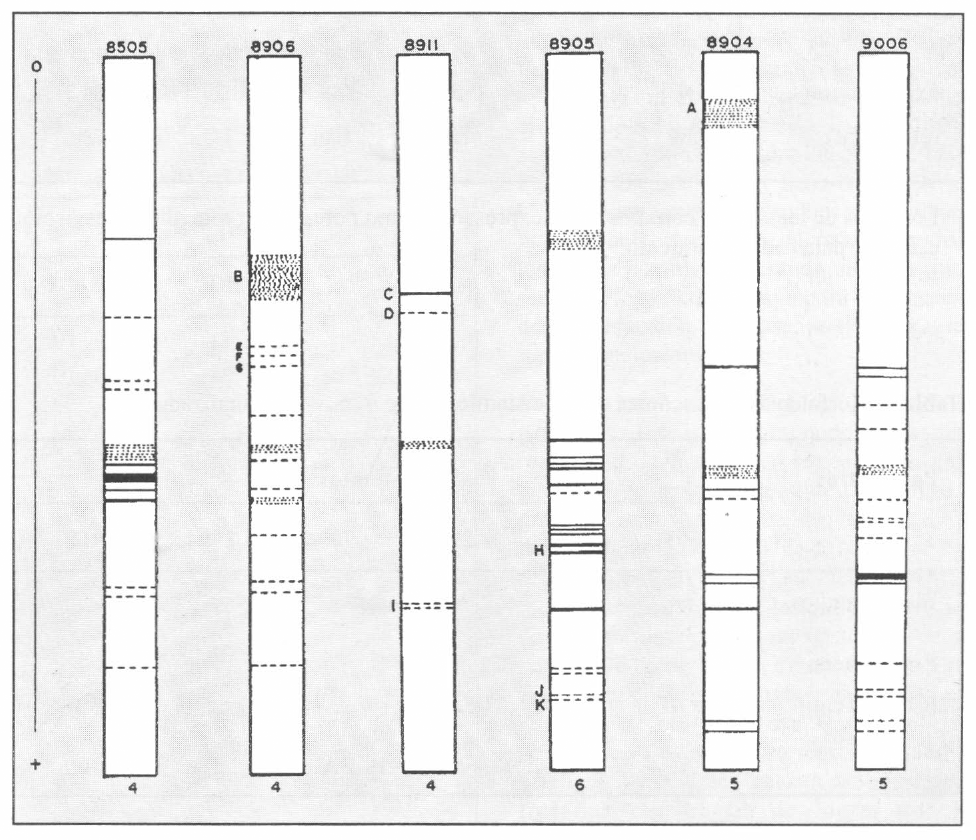
Comparación de los patrones electroforéticos de a- y ẞ- esterasas de cada uno de los aislamientos. El número en la parte inferior de cada patrón corresponde al día de mayor producción de esterasas. Las letras indican las bandas exclusivas de cada aislamiento.
Las pruebas de virulencia frente a H. hampei revelaron que todos los aislamientos son patógenos para la broca, pero en distinto grado. La mortalidad en todos los ensayos fue significativamente diferente de la del control (P=0,0001), con mortalidades que variaron entre 12,5 y 82,5% (Tabla 7). El aislamiento más virulento fue 8906, el cual difirió significativamente de los otros (Tabla 7). Este aislamiento mató el 75% de los insectos.
Los valores de LT50 no pudieron ser calculados para los aislamientos, puesto que menos del 25% de los insectos murieron, excepto para el aislamiento 8906, el cual mostró un LT50 de 6.25 días.
Discusión
Las características macroscópicas de colonia de los aislamientos examinados mostraron una amplia variabilidad, de tal manera que no pueden ser consideradas como criterios que ayuden a su caracterización y selección. Los aislamientos que produjeron oosporeína (pigmento rojo en el medio) mostraron una baja virulencia frente a H. hampei, lo cual significa que probablemente este pigmento no está directamente relacionado con la virulencia. Sin embargo, sería necesario examinar más aislamientos y cuantificar la producción de oosporeína.
El polimorfismo de los conidios encontrados en algunos aislamientos puede ser debido a la variabilidad genética inherente al aislamiento o a la contaminación con B. brongniartii. Los cultivos monospóricos realizados mostraron que no había aislamientos contaminados con esta especie de Beauveria, ya que la proporción de los diferentes tamaños de conidios fueron similares a los del aislamiento original.
La presencia de blastoconidios es una característica importante, ya que son una forma de conidios parasítica dentro del insecto y, por tanto, pueden estar relacionados con la virulencia de un aislamiento particular, aunque los resultados no son concluyentes porque no fueron evaluados cuantitativamente. Además, los estudios realizados al respecto, tampoco son concluyentes (Paris et al. 1985; Paris y Ferron 1979).
Los aislamientos con alta producción de conidios, como 8911 y 8904, tienen una clara ventaja sobre los que mostraron bajos niveles de esporulación, porque producirían epizootias en campo en un tiempo más corto lo que reduciría la cantidad de inóculo necesario para cultivar el hongo en su producción comercial.
La tasa de crecimiento hifal es un método mejor para evaluar las diferencias en las tasas de crecimiento entre aislamientos por ser una medida más precisa y que permite obtener datos en menor tiempo (24 h). De acuerdo con esto, los aislamientos que presentaron una tasa de crecimiento mayor, pueden tener una ventaja como agentes de control, porque esto permite una reducción del tiempo necesario para la producción del hongo como bioinsecticida, mejoraría la posibilidad de competir con otros microorganismos durante su vida saprofítica y posiblemente aceleraría el nivel de control de la plaga debido a una infección más rápida del insecto.
Un tiempo corto requerido para la geminación es una característica importante pues los conidios están expuestos en el campo a desecación, antibiosis, inhibición por lípidos epicuticulares o a ser removidos por la muda del insecto antes de su germinación y penetración en la cutícula del mismo y, por tanto, una rápida geminación aumenta la eficacia del hongo como micoinsecticida, reduciendo su dependencia de niveles relativamente altos de humedad relativa (Fuxa 1987).
Domsch et al. (1980) registraron el punto térmico de muerte para B. bassiana como 50°C. Sin embargo, en este estudio, la total mortalidad de los conidios se registró por encima de esta temperatura (55°C). Esta temperatura mayor encontrada puede deberse al método usado para exponer los conidios (calor húmedo) o a una mayor resistencia de estos conidios a la temperatura. Tal resistencia podría aumentar el tiempo de viabilidad del hongo en condiciones de campo, donde está expuesto al sol.
Para determinar con exactitud el punto de muerte térmica para estos aislamientos sería necesario evaluar la viabilidad de las conidios entre 50° y 55°C.
El nivel de supervivencia de las conidios, después de la irradiación con ultravioleta, fue diferente entre los aislamientos y fue registrado como el porcentaje de conidios que germinaron después del tratamiento. Este porcentaje refleja tanto la severidad del daño inicial de la célula, como la eficiencia en los sistemas enzimáticos que reparan los daños del DNA. A pesar de que la intensidad de esta radiación es menor en el campo que en el laboratorio, el tiempo de exposición es más prolongado que en campo, donde los efectos pueden ser equivalentes a los experimentados en laboratorio.
La lipasa es una de las enzimas utilizadas por este hongo para hidrolizar los componentes cuticulares y penetrar la cutícula del insecto (Smith et al. 1981; Samsinakova et al. 1971; St. Leger et al. 1987) y hay evidencia que muestra que juega un papel importante en la degradación de la barrera cuticular lipídica de algunos insectos para la penetración del hongo (Samsinakova et al. 1971, Smith et al. 1981). Por lo tanto, los aislamientos con una mayor producción entre el tercero y séptimo día de crecimiento tienen una ventaja sobre los que producen bajas cantidades. A pesar de que la relación que existe entre la producción de esta enzima y la virulencia no se ha establecido aún, una actividad mayor de lipasa hace que la infección del insecto por parte del hongo sea más fácil (Paris et al. 1985; Paris y Ferron 1979). En este estudio, parece que no se presenta una clara relación entre la producción de lipasa y la virulencia. Este resultado está de acuerdo con Champlin et al. (1981), Pekrul y Grula (1979) y Sosa-Gomez et al. (1994) e indica que la producción de lipasa no es el único factor involucrado en la virulencia. Es posible que usando métodos diferentes de los señalados aquí para la detección de la producción de lipasa, se llegue a diferentes conclusiones.
De acuerdo con la comparación de bandas de isoesterasa, los aislamientos podrían estar más relacionados con el origen de hospedero (particularmente insectos), que con su origen geográfico. Los aislamientos 8505, 8905 у 8904 tienen un número apreciable de bandas en común. Sin embargo, corridas electroforéticas repetidas mostraron que los patrones de bandeo de esterasas pueden ser inestables, como también lo ha registrado Tigano (1990). Esto puede ser debido a la variación en ciertas condiciones de cultivo y/o a la variabilidad genotípica de los aislamientos (Zhang y Changie 1991). Estos factores deben ser controlados con el fin de lograr que la electrotoresis de esterasas sea una herramienta útil para la caracterización de aislamientos.
Los resultados de las pruebas de virulencia con insectos demostraron que todos los aislamientos pueden atacar el estado adulto de la broca del café, debido a que causaron la muerte de un porcentaje de insectos mayor con respecto al control no inoculado. Sin embargo, el aislamiento 8906 es el único que podría ser considerado para ser usado como micoinsecticida porque tiene la capacidad de matar una proporción relativamente alta de insectos dentro de un período de tiempo no muy largo (seis días).
Es interesante que los aislamientos derivados de Coleoptera 8911, 8904 у 9006 mostraron menor virulencia frente a H. hampei que el originado de materia orgánica en descomposición, 8906. Esto puede sugerir que el origen de hospedero no necesariamente es un buen indicador de la probable virulencia de un aislamiento específico de B. bassiana frente a un hospedero. Como la mayoría de los aislamientos provocaron la muerte a menos del 25% de los insectos después de 10 días, este bajo porcentaje puede indicar una pérdida de virulencia y la necesidad de aumentarla por pases a través de un hospedero susceptible a la misma o de otra especie del mismo género. Este aumento en la virulencia probablemente es un reflejo de respuestas fenotípicas que llevan a una habilidad aumentada de los conidios para germinar rápidamente, y puede aumentar la capacidad invasiva del hongo, implicando mecanismos enzimáticos inducibles (Daoust y Roberts 1982; Fargues y Robert 1983).
Conclusiones
Las características macroscópicas y microscópicas de la colonia de los aislamientos examinados mostraron una amplia variación, que puede ser debida a la variabilidad genética inherente a los aislamientos, de tal manera que no pueden ser consideradas como criterios que ayuden a su caracterización y selección. Este polimorfismo resulta de los procesos que generan variabilidad en los hongos con reproducción asexual, tales como: mutaciones, hibridización y parasexualidad, y de procesos selectivos relacionados con factores bióticos y abióticos, como selección de los insectos hospederos, autólisis y heterólisis (Propawski et al. 1988).
En cuanto a las características fisiológicas evaluadas, sólo algunas como la tasa de crecimiento hifal y la viabilidad de los conidios frente a la temperatura permiten diferenciar entre aislamientos; mientras que otras permiten únicamente distinguir entre grupos de aislamientos, que se agrupan de acuerdo a su respuesta a la exposición a la radiación ultravioleta y en cuanto a la producción de lipasa.
De acuerdo con la comparación de bandas de isoesterasa, los aislamientos pueden distinguirse todos entre sí, ya que a pesar de compartir algunas bandas comunes, casi todos poseen bandas características, excepto el aislamiento 8905, originario de Cuba. En este sentido, esta técnica sería una herramienta útil para la diferenciación de aislamientos, si se logra hacer que arroje resultados estables.
A pesar de que los análisis de correlación no mostraron ninguna relación entre las características examinadas, ni entre éstas con la virulencia de los aislamientos, es posible seleccionar el aislamiento 8906 por su mayor virulencia y los aislamientos 8505 y 8905 porque reúnen una serie de características adaptativas (blastoconidios abundantes, alta producción de conidios, tasa de crecimiento alta, corto tiempo de geminación, relativa resistencia a radiación ultravioleta y producción de lipasa alta), que favorecerían su supervivencia en campo y su efectividad como micoinsecticidas.
Estos aislamientos podrían ser usados para posteriores estudios de mejoramiento genético, si fuera posible combinar estas características o para aumentar la virulencia (en el caso de los aislamientos 8505 y 8905, por pases a través del insecto). Sin embargo, es recomendable examinar más aislamientos para éstas y otras características, y con respecto a su virulencia contra la broca del café, con el fin de lograr un mejor control de la plaga.
Finalmente, no se recomienda la utilización de un sólo aislamiento como base de un micoinsecticida comercial, puesto que esto reduce la variabilidad genética del hongo y por tanto sus posibilidades de enfrentarse con éxito a la plaga.
