Abstract
One of the most important aspects in the search of improved strains of entomopathogens to control the coffee berry borer H. hampei (Ferrari), is related to its enzymatic activity and its capacity to take the substrates of the ecosystem, factors that determine the process of virulence of the fungus to the insect and its survival in natural conditions. The collection of entomopathogenic fungi of the Insect Pathology Laboratory at Cenicafé has 93 isolates of the fungus B. bassiana (Bb) from different hosts and geographic regions of the country and outside of it. Those isolates from their original host (HO) and passed through the coffee berry borer (cbb) (RB) are the basis for characterization and selection studies of these biological agents to use in the control of cbb. This work had as the main objective to conduct an enzymatic cualitative evaluation of some isolates of the fungus Bb, HO and RB by using the commercial system api-zym and the solid substrate system, in order to evaluate the effect of the transfer through the cbb on the enzymatic response of the fungus. As a result, 10 isolates of Bb, HO and RB were taken and celular suspension of known concentration were prepared in 10% glycerol and kept at -15°C for the enzymatic tests.
In general, it was observed that the RB isolates showed a better response in a shorter time of reaction. Consequently, the isolates HO presented some level of activity for 7 of 19 evaluated enzymes in the api-zym commercial system and once passed through the cbb (RB) enzyme activity of 10 of 19 probed enzymes was observed. In the enzymatic evaluation with the solid substrate method it was found that some isolates showed variable response to the chitinase and lipase production. However, after passing these isolates through the cbb, they presented a positive response in the above mentioned tests.
The results confirm the importance of carry out characterization studies of the isolates once passed through the insect to which the control is directed. This is a criterium of great utility for entities or research centers in which collections of biological agents from different host and geographic localities are mantained to be characterized and selected in the control of insect pest of crops of economic importance.
Introducción
La broca del fruto del café, Hypothenemus hampei (Ferrari), se encuentra ampliamente distribuida en el país infestando más de 650.000 hectáreas (Herrón 1997, Comunicación personal). El manejo integrado de este insecto plaga se ha basado en el uso de agentes de control biológico, manejo cultural del cultivo y uso de insecticidas químicos. Dentro de los agentes biológicos, el hongo B. bassiana ha mostrado ser eficaz en el control de la broca en las condiciones del ecosistema cafetero Colombiano (Bustillo y Posada 1996). El mecanismo de infección del hongo se inicia cuando la espora se adhiere a la cutícula del hospedero susceptible. El proceso de penetración es mediado por acción mecánica de forma que la espora germina en la superficie del insecto e inicia la penetración del integumento a través del tubo germinativo. Además, produce enzimas extracelulares relacionadas con la patogénesis al insecto tales como: proteasas, lipasas, ureasas, quitinasas y otras, las cuales hidrolizan sus componentes cuticulares (Smith y Grula 1981).
Las proteasas y las lipasas son enzimas constitutivas del hongo B. bassiana, que actúan degradando la cutícula del hospedero (Roberts y Yendol 1971). La quitinasa puede actuar como una enzima constitutiva o adaptativa, dependiendo de la especificidad de la cepa al insecto hospedero (Leopold y Samsinakova 1970). El integumento del insecto está compuesto de proteínas y quitinas con lípidos asociados y compuestos fenólicos, los cuales actúan como una barrera contra microorganismos invasores. A través de la acción combinada de enzimas hidrolíticas como quitinasas, proteasas y lipasas, los hongos filamentosos son capaces de penetrar esta barrera. La presencia de enzimas hidrolíticas suele facilitar cada etapa de infección del hongo y adicionalmente, pueden ser importantes en la invasión del hemocele del insecto (Hegedus y Khachatourians 1988).
El metabolismo primario de los hongos se relaciona con los procesos de crecimiento y desarrollo, tales como la utilización de fuentes de carbono y nitrógeno y la producción de enzimas. Las enzimas liberadas al medio externo por parte de los hongos, determinan los nutrientes que éstos puedan utilizar y por tanto, su hábitat de crecimiento (Garray y Evans 1984). La asimilación de fuentes de carbono y nitrógeno es realizada comúnmente mediante el empleo de medios básicos definidos químicamente, incorporando la fuente de interés (Paterson y Bridge 1994). La producción de enzimas es evaluada comúnmente en el sistema comercial Api-zym, el cual permite la determinación de 19 actividades enzimáticas extracelulares diferentes (Barth y Bridge 1989).
El Laboratorio de Patología de Insectos de Cenicafé cuenta con 93 aislamientos del hongo B. bassiana los cuales han sido objeto de caracterización morfológica, bioquímica y molecular; sin embargo, la caracterización bioquímica cualitativa se ha realizado a partir de aislamientos previamente inoculados en medios de cultivo sintéticos, pero aún no se ha evaluado su actividad enzimática cuando se cultivan previamente en sustratos que incluyen macerados de broca del café, en cuyo caso, se esperaría un incremento de dicha actividad, por cuanto corresponde a la situación natural en la cual el hongo expresa su acción de control sobre H. hampei. Por tal razón, el presente estudio tuvo como objetivo fundamental realizar una evaluación enzimática de algunos de los aislamientos de Bb, procedentes del hospedero original (HO) y reactivados sobre la broca del café (RB), mediante la utilización del sistema comercial Api-zym y el uso de sustratos sólidos, con el fin de comparar la respuesta enzimática de estos aislamientos en función del hospedero y establecer criterios para evaluaciones enzimáticas posteriores, teniendo en cuenta las condiciones en las cuales estos agentes biológicos desarrollan un mejor potencial para el control de la broca del café.
Materiales y Métodos
Para la realización del estudio, se tomaron 10 aislamientos de Bb, HO, preservados en liofilización y en nitrógeno líquido (Tabla 1), se inocularon en tubos de agar agua al 1,2% con la finalidad de evitar la transferencia de nutrientes a los sustratos prueba que pudieran inducir a resultados falsamente positivos y se llevaron a incubar a una temperatura de 25°C, hasta obtener una esporulación evidente del hongo en dicho medio, lo cual se logró aproximadamente a los 8 a 10 días de incubación. Posteriormente y con el propósito de proveer suficiente material y asegurar un inóculo homogéneo para cada una de las pruebas, se prepararon suspensiones celulares de concentración conocida en glicerol al 10% (2 x 10⁹ esporas/ml), las cuales se almacenaron a 25°C hasta el momento de la realización de las pruebas enzimáticas (Fig. 1).
Estos mismos aislamientos reactivados a través de la broca del café (RB), mediante siembra del aislamiento original en tubos con agar agua más macerado de broca adulta recién emergida (0,96%), fueron sometidos al procedimiento citado, con el fin de evaluar el efecto de la transferencia a través de la broca en su comportamiento enzimático.
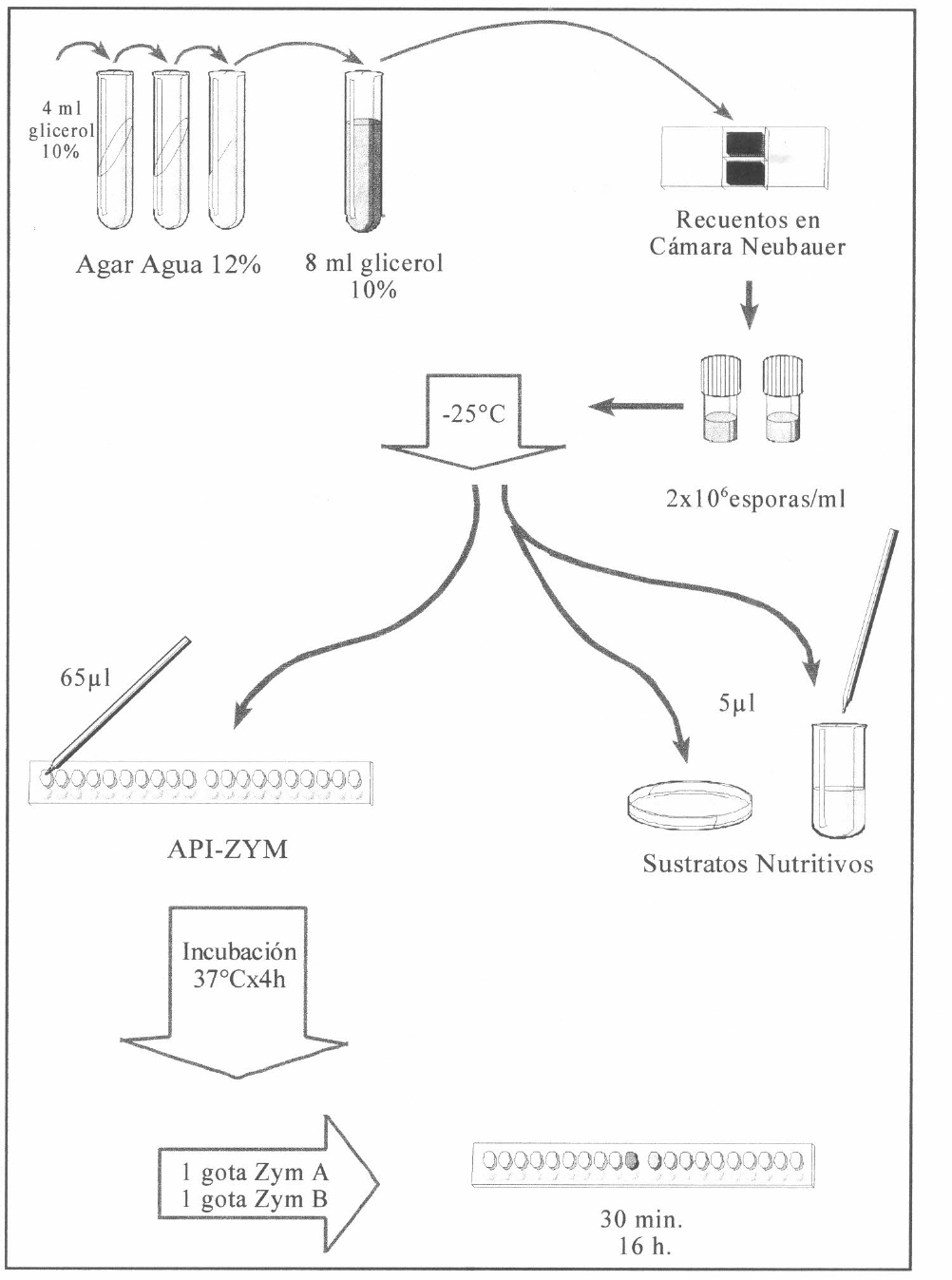
Método de conservación de aislamientos para la siembra en sustratos nutritivos y en el sistema comercial Api-zym.
Aislamientos del hongo B. bassiana utilizados en el estudio, hospedantes y procedencia geográfica
Enzimas detectadas en cada uno de los sustratos que provee el sistema comercial Api-zym
Para la realización de las pruebas enzimáticas se utilizó el sistema comercial Api-zym, el cual corresponde a una prueba semicuantitativa que incluye 19 sustratos deshidratados de enzimas (Tabla 2) y permite evidenciar la utilización del sustrato por parte del hongo, mediante una reacción colorimétrica semicuantitativa, en una escala que va desde 0 hasta 5, considerándose 0 = reacción negativa, 1 = reacción débil, 2 a 4 = reacción moderada y 5 = reacción fuertemente positiva. Las lecturas de la actividad enzimática se realizaron a los 30 minutos y a las 16 horas de iniciada la reacción, teniendo en cuenta que trabajos previos realizados en Cenicafé mostraron que algunas enzimas extracelulares de este hongo se expresan inicialmente al cabo de 30 minutos, pero otras se evidencian sólo al cabo de 16 horas. Adicionalmente, se utilizó el sistema a base de sustratos sólidos definidos químicamente en el cual se adiciona la fuente de interés.
La inoculación de cada uno de los aislamientos del hongo en el sistema comercial se realizó de acuerdo con el método recomendado por el fabricante, de modo que se realizó una agitación de la suspensión de esporas en vortex durante un minuto y se depositaron 65 µl de esta suspensión de concentración conocida de cada uno de los aislamientos a evaluar, en cada uno de los pozos que trae el sistema. Se llevó a incubación a 37°C durante 4 horas, tiempo al cabo del cual se realizó la lectura, teniendo como punto de referencia una cartilla de color que posee el sistema.
En el método de los sustratos sólidos se evaluó la actividad enzimática cualitativa de los diferentes aislamientos HO y RB, según metodología empleada por Paterson y Bridge (1994) y modificada por Valdés (1996). La utilización de las fuentes de carbono: citrato de sodio, N-acetil glucosamina, quitina, almidón, lactosa, lanolina y glucosamina, se evaluó mediante el cambio de color (amarillo a púrpura) del indicador de pH, púrpura de bromocresol, como resultado de la utilización del sustrato por parte del aislamiento. La única fuente de nitrógeno evaluada fue la urea, cuya hidrólisis se evidenció igualmente mediante el cambio de coloración del indicador de pH. La producción de proteasas se determinó en dos sustratos: gelatina y caseína, la reacción positiva se evidenció por licuefacción del medio y formación de halo al rededor de la colonia, respectivamente. La producción de lipasa se evaluó en un sustrato a base de tributirina, mediante la formación de un halo transparente alrededor de la colonia de crecimiento del hongo y la producción de esterasa se evaluó en un sustrato a base de tween 80, mediante cambio del indicador de pH.
La inoculación se realizó mediante el depósito de 5 ul de una suspensión de concentración conocida de esporas en el centro de las cajas y tubos empleados para las determinaciones. Los tiempos de evaluación de las diferentes reacciones (positiva, negativa o variable) fluctuaron entre 2 y 30 días, excepto para la determinación de proteasas en medio a base de gelatina, para la cual se estableció un tiempo de lectura de 10 días, en el que se presentaba un buen crecimiento del hongo en el medio, para poder proceder a la refrigeración de éste y evidenciar la licuefacción causada por la enzima producida.
Para evaluar la respuesta de cada uno de los aislamientos en las diferentes pruebas enzimáticas realizadas en medios químicamente definidos que incluían el sustrato de interés, se tomaron las unidades experimentales conformadas por dos unidades de observación (caja de petri), para un total de 3 repeticiones por tratamiento. Se evaluó la respuesta de los aislamientos de HO y RB en todos los sustratos enzimáticos. Posteriormente, se realizó un análisis de varianza y una prueba de Tukey al nivel del 5%, para comparar el promedio del tiempo medio de reacción de las pruebas en las diferentes condiciones (HO y RB).
La evaluación de la respuesta de los diferentes aislamientos en el sistema comercial Api zym se realizó teniendo en cuenta el número de reacciones positivas y el grado de intensidad de la reacción por aislamiento, en el total de sustratos evaluados.
Resultados y Discusión
Las tablas 3 y 4 ilustran la respuesta enzimática de los aislamientos HO y RB evaluados en el sistema comercial Api-zyrn. En el caso de los aislamientos de B. bassiana, HO, no se presentó ninguna actividad de las enzimas fosfatasa alcalina, lipasa C14, cistina arilamidasa, tripsina, alfa quimotripsina, alfa y beta galactosidasa, beta glucoronidasa, alfa glucosidasa, N-acetil beta glucosarninidasa, alfa manosidasa y alfa fucosidasa, por lo cual no se relacionan estos sustratos en las tablas que muestran la respuesta de los aislamientos en el sistema comercial Api zyrn, Dicho comportamiento se presentó también en los aislamientos RB, a excepción de las enzimas fosfatasa alcalina, beta galactosidasa y N-acetil beta glucosaminidasa en las cuales se evidenció actividad para algunos de estos aislamientos. En general, se observó que los aislamientos RB mostraron una mejor respuesta enzimática; fue así como los aislamientos procedentes del HO presentaron algún nivel de actividad para 7 de las 19 enzimas evaluadas y una vez fueron reactivados sobre la broca, se observó actividad enzimática en 10 de las 19 enzimas probadas.
Caracterización enzimática de los aislamientos del hongo B. bassiana procedentes del hospedero original mediante el sistema comercial Api-zyrn
O= Reacción negativa 2 a 4 = Reacción moderada
1 = Reacción débil 5 = Reacción fuertemente positiva
30' y 16 h = Tiempos en los cuales se realizó la lectura de la prueba enzimática
Caracterización enzimática de los aislamientos del hongo B. bassiana reactivados sobre la broca del café mediante el sistema comercial Api-zyrn
0= Reacción negativa
2 a 4 = Reacción moderada
1 = Reacción debil
5 = Reacción fuertemente positiva
30' y 16 h = Tiempos en los cuales se realizó la lectura de la prueba enzirnática
= glucosaminidasa
Caracterización enzimática de los aislamientos del hongo B. bassiana procedentes del hospedero original en sustratos sólidos
Cit = Citrato Est = Esterasa
Quit = Quitina ProC = Proteasa (Caseína)
N-a gl = N-acetil glucosmina ProG = Proteasa (Gelatina)
Lip = Lipasa
+' = Respuesta positiva en todas las repeticiones'
-' = Respuesta negativa en todas las repeticiones
v = Respuesta variable
Caracterización enzimática de los aislamientos del hongo B. bassiana reactivados sobre la broca del café en sustratos sólidos
Cit = Citrato Est = Esterasa
Quit = Quitina ProC = Proteasa (Caseína)
N-a gl = N-acetil glucosmina ProG = Proteasa (Gelatina)
Lip = Lipasa
+' = Respuesta positiva en todas las repeticiones
-' = Respuesta negativa en todas las repeticiones
v = Respuesta variable
En cuanto a la evaluación enzimática utilizando sustratos sólidos, se encontró que los aislamientos de HO Bb 9022, 9023 y 9213 presentaron respuesta variable a la producción de quitinasa, así mismo el aislamiento Bb 9213 mostró respuesta variable en la producción de lipasa. Sin embargo, luego de su reactivación estos aislamientos presentaron una respuesta positiva en las dos pruebas y en las tres repeticiones. El aislamiento Bb 9114 de hospedero original presentó respuesta negativa a la producción de lipasa y proteasa en el sustrato a base de gelatina, sin embargo, luego de su reactivación mostró una respuesta positiva (Tablas 5 y 6). Se han registrado pequeñas cantidades de esta enzima producida por el hongo B. bassiana en sustratos sintéticos, en este caso particular es posible que la reactivación a través de la broca haya potenciado su producción. Lo anterior, permite afirmar que en terminos generales no se observó una respuesta diferente de los aislamientos en las condiciones evaluadas (HO y RB), sin embargo si hubo una mayor expresión de la actividad enzimática de los aislamientos, una vez se realizó la reactivación a través de la broca.
El analisis estadístico de la variable tiempo de reacción de los aislamientos mostró diferencias significativas entre éstos, según prueba de Tukey al 5%, a favor de la condición reactivado sobre la broca del café, con un menor tiempo de reacción en todos los sustratos evaluados para estos aislamientos, excepto para la prueba de utilización de citrato como única fuente de carbono en la cual no se presentó una tendencia definida (Tabla 7). La producción de proteasa en el sustrato de gelatina no se considero en el análisis debido a que el único tiempo de lectura fue 10 días.
Los resultados obtenidos están de acuerdo con los hallazgos de otros autores, en cuanto a la capacidad que desarrollan estos agentes de control, para especializarse en su acción patogénica hacia el insecto sobre el cual se dirige el control, una vez se han reactivado, mediante pases sucesivos, a través de éste (González et al. 1993). Lo anterior, se explica porque el hongo desarrolla un mecanismo de penetración enzimática dirigido a la composición de la cutícula del insecto, de forma que expresa una gran cantidad de enzimas constitutivas e inducidas, de acuerdo al tipo de compuestos presentes.
López (1994) registró una mayor acción patogénica de aislamientos del hongo Beauveria bassiana, procedentes de Lepidoptera, sobre Bombix mori, lo que confirma la especificidad desarrollada por el hongo, como producto de su interacción con el insecto. Sin embargo, Prior (1991) afirma que tanto aislamientos procedentes del orden del insecto, sobre el cual se dirige el control, como de otros ordenes insectiles pueden expresar un buen potencial patogénico.
Para concluír, los resultados obtenidos permiten recomendar estas metodologías de evaluación enzimática para una selección inicial de aislamientos, posterior a su reactivación sobre el insecto de interés, teniendo en cuenta que las condiciones cuticulares del insecto inducen la respuesta de estos agentes biológicos, en términos de una mayor acción de las enzimas directamente involucradas en la virulencia y una mayor especificidad sobre el hospedero a través del cual se ha ejercido la presión de selección. El método de sustratos sólidos con un indicador de pH, aun cuando es más dispendioso y requiere un mayor tiempo de evaluación, permite la determinación de enzimas directamente responsables de la virulencia del hongo sobre diversos insectos; el sistema Apizym muestra en un período corto la respuesta enzimática en una amplia gama de sustratos predeterminados. Por tal razón, se sugiere el uso de ambas metodologías en forma complementaria, como un criterio de gran utilidad para entidades o centros de investigación, en los cuales se tienen colecciones de agentes biológicos procedentes de diferentes hospedantes y regiones geográficas, para ser caracterizados y seleccionados en el control de plagas en cultivos de importancia económica.
Comparación tiempos medios de reacción
Letras diferentes en la misma columna (enzima) para cada aislamiento, corresponden a tratamientos diferentes estadísticamente, según prueba de Tukey al 5%
Condi = Condición RB = Reactivado sobre la broca HO = Procedente de hospedero original
= Respuesta negativa o variable
Footnotes
Agradecimientos
Los autores expresan su agradecimiento a la Dra. Esther Cecilia Montoya R. por su asesoría en el análisis estadístico de la información y a los auxiliares Silvio Marín M. y Jairo Hernán Henao D. por su colaboración en el desarrollo del estudio.
