Abstract
In Mexico, Chloridea virescens is a pest of chickpea, tomato and other vegetables causing significant economic losses. To control this pest, three different strains (M1, M2 and M3) of Metarhizium robertsii (previously Metarhizium anisopliae) and three strains of Beauveria bassiana (B1, B3 and B9) were evaluated under laboratory conditions, based on radial growth parameters, and conidia production and germination. The pathogenicity of the best strains was assessed at concentration of 1×108 conidia/mL, against second and third instar larvae of C. virescens, at 28 ± 1 °C, 70 ± 5 % of relative humidity and a photoperiod of 12 hours light. The six strains caused larvae mortality of C. virescens, ranging from 57% to 97%, with statistically significant differences compared with the control (P < 0.02). The M1 strain of M. robertsii exhibited the highest radial growth of 4.79 ± 0.02 cm, a growth rate of 3.33 mm/day, and a production of 6×109 conidia/mL at 14 days, with 96% of germination at 24 hours. In terms of pathogenicity M1 caused 97% of total larvae mortality at 7 days with TL50 of 4 days. The M2 and M3 strains caused mortality of 83% and 77% with a TL50 of 4 days. Strains B1, B3 and B9 have mortalities of 63%, 57% and 70% with a TL50 of 4.3 days. (M1) M. robertsii had the best performance across all evaluated parameters, and it is therefore recommended for field testing to control of C. virescens.
Introducción
En el Estado de Sinaloa, México, el gusano del fruto Chloridea virescens (Fabricius) (Lepidoptera: Noctuidae) es una plaga que ataca los cultivos de garbanzo Cicer arietinum (L.) y tomate Solanum lycopersicum (L.), en los que se ha observado que las larvas del primer estadio se alimentan de las porciones tiernas de las hojas u otras partes vegetativas. Sin embargo, a partir del segundo y tercer instar tienen mayor movilidad y se alimentan de flores y frutos (García-Gutiérrez et al., 2019). Estudios de Manzanarez-Jiménez et al. (2021a) indican que el desarrollo de estos estadios sobre hojas de tomate dura 8,3 días a 23,5 °C ± 5,5 °C y humedad relativa 70% ± 10%, en esta etapa las larvas se encuentran alimentándose de manera voraz, el daño a las hojas terminales retrasa el crecimiento de las plantas y puede provocar un crecimiento de frutos de mala calidad, el cuarto y quinto estadio se alimentan activamente del fruto y el sexto reduce su movilidad dejando de alimentarse. Con relación a los daños que causan en el tomate, Manzanarez-Jiménez et al. (2021a) informaron que una sola larva de este insecto puede consumir el fruto en 25 % de su totalidad. Lo anterior causa grandes pérdidas económicas en este cultivo, las cuales se han estimado en 8,5% de la producción (García-Gutiérrez et al., 2019).
Por esta razón, el control de C. virescens y otras plagas en tomate y garbanzo se ha realizado con mezclas de dos o más insecticidas químicos (7 a 8 mil t/año) a base de organoclorados, organofosforados, carbamatos y piretroides, aplicados mediante aspersiones vía aérea o manual (SIAP, 2021). El empleo de estos productos causa efectos perjudiciales a la salud humana y los ecosistemas terrestres y acuáticos (Martínez-Valenzuela et al., 2019). En programas de manejo integrado de plagas en cultivos de chile y tomate se realizan aplicaciones de Bacillus thuringiensis (Berliner), algunos parasitoides como Trichogramma spp. y depredadores como Chrysoperla spp., así como como Metarhizium robertsii (Metchnikoff) Sorokin, Beauveria bassiana (Balsamo-Crivelli) Vuillemin, Isaria fumosorosea (Wize) (anteriormente Paecilomyces fumosoroseus) Brown & Smith y P. lilacinus (Thom) (García-Gutiérrez et al., 2019).
En esta región los hongos entomopatógenos B. bassiana y M. robertsii causan mortalidad en el adulto del picudo del chile Anthonomus eugenii Cano (Coleoptera: Curculionidae) y larvas del primer y tercer estadio de gusano cogollero Spodoptera frugiperda (J.E. Smith) (Lepidoptera: Noctuidae), gusano soldado Spodoptera exigua (Hübner) (Lepidoptera: Noctuidae), gusanos barrenadores de la caña Diatraea spp. (Lepidoptera: Crambidae) y gusano del fruto C. virescens (García-Gutiérrez et al., 2019). Sin embargo, es necesario seleccionar cepas que sean altamente infectivas para los estadios referidos a las condiciones climáticas y el cultivo en el que se desarrolla la plaga. Por esta razón, se realizó la selección de cepas de M. robertsii y B. bassiana y se evaluó su patogenicidad contra larvas del segundo a tercer estadio de C. virescens en condiciones de laboratorio.
Materiales y métodos
Origen de las cepas de los hongos entomopatógenos.
Se evaluaron seis cepas nativas aisladas en el norte de Sinaloa de los hongos M. robertsii y B. bassiana del laboratorio de Bioinsecticidas del Centro Interdisciplinario de Investigación para el Desarrollo Integral Regional Unidad Sinaloa (Tabla 1).
Origen de las cepas de Metarhizium robertsii y Beauveria bassiana en el norte de Sinaloa y número de acceso al GenBank.
Las cepas se cultivaron en una cámara climática (CBRFPLC-20, Prendo) a 28 °C ± 1 °C y 70% ± 5 % de humedad relativa (HR) y fotoperiodo de 12 h luz:12 h oscuridad, en medio nutritivo de agar papa-dextrosa (PDA) durante 14 días. Los conidios se recuperaron agregando 2 mL de agua destilada estéril al cultivo y con una espátula de acero inoxidable (18/10 BochemTM) se raspó el área de crecimiento. La suspensión de conidios se vertió en un tubo cónico (50mL) de polipropileno con 10 de Tween 80 al 0,05 % y se homogenizó durante 3 min en un agitador Vortex (MX-S5, Thermo scientific). Se cuantificó la concentración de conidios mediante una cámara Neubauer (0,1 mm, Marienfeld). La viabilidad de los conidios en las suspensiones se determinó en medio PDA siguiendo el protocolo de Inglis et al., (2012). Los cultivos se mantuvieron a 4 °C.
Crecimiento radial de las cepas.
En el día 14 del crecimiento de los hongos se tomó un fragmento de micelio de 4 mm del borde del cultivo utilizando un sacabocado (MOD.0629890, Cole-Parmer®), se sembró en el centro de cajas de Petri (90 mm) en posición invertida y se incubaron a 28 °C ± 1 °C y 70% ± 5% de humedad relativa y fotoperiodo de 12 horas luz. La medida de crecimiento radial de las cepas se midió con un vernier (Pie de rey) (UltraTech®, Mod. H-7352) en mm/día cada 24 h durante 14 días; midiendo el diámetro a partir del punto “0” del eje cartesiano (Cuadrante I, II, III y IV) previamente trazado en la base inferior de cada caja de Petri.
Esporulación y viabilidad de las cepas.
La esporulación de conidios se evaluó siguiendo el protocolo de Sun et al., (2002), los conidios de cada caja de cultivo de 14 días de crecimiento se suspendieron en 10 de Tween 80% al 0,05 % en agua destilada estéril, y después se obtuvo el promedio de conidios/mL de cada cepa. En cada muestra se observaron cinco campos de la cámara de Neubahuer. Las suspensiones se ajustaron a 1×108 conidios/mL, de donde se tomaron 100 µL y se sembraron por extensión con ayuda de un asa de Drigalsky triangular en medio PDA. La germinación se cuantificó cada 4 horas a partir de las 8 horas hasta las 24 horas, siguiendo los criterios de tamaño de tubo germinativo, el doble del tamaño del conidio y el porcentaje de germinación (Inglis et al., 2012).
Los datos de crecimiento radial de las cepas por día, crecimiento total de la cepa, esporulación y germinación se analizaron con el programa estadístico Minitab versión 21 (2021).
Bioensayo de patogenicidad.
La cría de C. virescens se inició con la colecta de larvas en cultivos de garbanzo en el valle agrícola de la ciudad de Juan José Ríos, Sinaloa. Las larvas se alimentaron con la dieta ICRISAT Diet 3 (Arévalo & Zenner de Polanía, 2010) modificada con 5% de aceite de soya como fagoestimulante, 10% de germen de trigo y 20 % de harina de maíz, para proporcionar consistencia a la dieta. Los adultos obtenidos de las pupas se colocaron a temperatura ambiente (~25 °C ± 2 °C) en un cilindro de PVC revestido con hojas de papel, allí se alimentaron las palomillas con una solución de sacarosa puesta en algodón humedecido en una caja Petri dentro del cilindro con tapa hasta obtener la oviposición en el papel.
La patogenicidad y el Tiempo letal medio (TL50) de las cepas de B. bassiana y M. robertsii se determinó en grupos formados al azar con 30 larvas de segundo y tercer estadio de C. virescens, por ser estos los de mayor movilidad en las plantas (Manzanarez-Jiménez et al., 2021b) y por tener mayor posibilidad de entrar en contacto con los hongos. Las cepas se prepararon en suspensión a una concentración de 1×108 conidios/mL en 10 mL de Tween® 80 al 0,05%. El control se hizo con agua destilada estéril. Las larvas de C. virescens se seleccionaron al azar de una colonia proveniente del laboratorio, y se individualizaron en caja Petri + papel filtro humedecido + alimento artificial, sin metilparabeno, y se inocularon con 50 µL de la suspensión de conidios sobre su exoesqueleto con ayuda de una micro-pipeta automática (LM-200, LabMate®). Las cajas se sellaron con papel parafilm y se incubaron a 27 °C ± 1 °C; humedad relativa de 70% ± 5% y fotoperiodo de 10 horas luz. La mortalidad se registró cada 24 horas durante 8 días.
Diseño experimental y análisis estadístico.
El experimento se realizó bajo un diseño completamente al azar. Los datos de mortalidad de larvas se ajustaron mediante la fórmula de Abbott (1925). Las diferencias entre los tratamientos se determinaron con el estadístico ANOVA y las diferencias entre las medias de los tratamientos se compararon mediante la prueba de Tukey (P < 0,05) en el programa SAS®, versión 9.00 (SAS, STAT®, 2009). El Tiempo letal medio de los tratamientos (TL50) se obtuvo a través del modelo de regresión Probit (Finney, 1978).
Resultados y discusión
Crecimiento radial, esporulación y germinación de cepas.
La cepa M1 de M. robertsii presentó los valores más altos del parámetro de crecimiento, comparados con las cepas M2 y M3 y con las cepas B1, B3 y B9 de B. bassiana (F = 6149,03; gl = 5,14; P < 0,00) (Tabla 2).
Tasa de crecimiento por día, crecimiento radial, esporulación y germinación de cepas de Beauveria bassiana y de Metarhizium robertsii a las 24 horas en medio Papa-Dextrosa-Agar (PDA).
Medias con la misma letra, en cada columna, no son significativamente diferentes (α < 0,05). Los resultados son medias ± de la desviación estándar, obtenidos de datos de los experimentos realizados por triplicado.
Desarrollo de micelio en larvas de Chloridea virescens.
Las larvas de segundo y tercer estadio de C. virescens infectadas por M. robertsii y B. bassiana tuvieron diferente desarrollo de micelio y esporulación con 4 ± 0,5 días, 8 ± 1 días y 7 y 10 días, respectively (Figura 1).
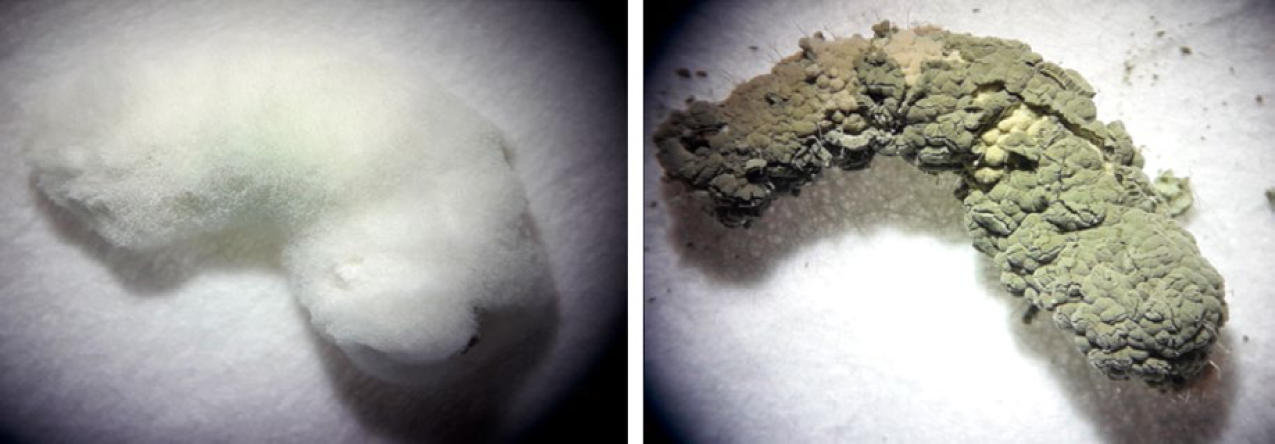
Larvas de Chloridea virescens infectadas con Beauveria bassiana y Metarhizium robertsii. a) micelio de aspecto algodonoso en cepa B9 a los 19 días. b) micelio en forma de tabiques de M. robertsii cepa M1 a los 14 días. Fotografías tomadas con un microscopio estereoscópico (Zeiss Stemi DV4, Oberkochen, Alemania).
Sun et al., (2002), encontraron presencia de micelio de estos dos hongos en tiempo de uno y dos días en cadáveres de larvas de termitas subterráneas de Formosa Coptotermes formosanus Shiraki, 1909 (Blattodea: Isoptera: Rhinotermitidae). La esporulación en este estudio fue similar a la observada en el cuerpo de las termitas, donde M. robertsii tuvo crecimiento micelial sobre C. virescens, dos días después de morir. Por su parte, Cheng et al. (2016) al realizar el estudio con B. bassiana y M. robertsii encontraron diferencias en el crecimiento del micelio, M. robertsii tuvo crecimiento rápido y alta esporulación, mientras que B. bassiana tuvo menor crecimiento y baja esporulación. Estos hallazgos son congruentes con el tiempo de desarrollo de las cepas evaluadas en este estudio, donde las cepas B1 y B3 de B. bassiana tuvieron baja esporulación, destacando la cepa B9 con alta tasa de esporulación, mientras que en todas las otras cepas de M. robertsii también fueron altas y el valor más alto lo tuvo la cepa M1 (Tabla 2). Estos resultados tienen que ver con la disponibilidad de conidios y la velocidad de colonización fúngica sobre las larvas de C. virescens.
Estudios recientes de crecimiento y propagación de M. robertsii en medios de cultivo a base de agar dextrosa y papa (PDA) como fuente de carbono y nitrógeno, mezclados con extracto acuso de alga parda gigante Macrocystis pyrifera (L.) C. Agardh (Laminariales: Phaeophyta), indicaron mayor viabilidad y producción de conidios de esta especie (Manzanarez-Jiménez & García-Gutiérrez, 2020; Manzanarez-Jiménez et al., 2021b).
El rápido crecimiento y alta producción de conidios de M. robertsii comparada con B. bassiana, podría deberse a su capacidad para crecer a temperatura > 35 °C (Bugeme et al., 2008; Chandra-Teja & Rahman, 2016). Por otro lado, Manzanarez-Jiménez et al. (2021b) reportaron persistencia de conidios de estas dos especies de hongos después de 14 días de haber sido asperjados en plantas de tomate en invernadero contra larvas C. virescens. No obstante, para seleccionar a una cepa además de los parámetros encontrados, es necesario realizar estudios de crecimiento de M1 a diferentes temperaturas y determinar su persistencia en campo.
Bioensayo de patogenicidad.
En el bioensayo de patogenicidad las seis cepas causaron mortalidad de larvas de segundo y tercer estadio de C. virescens, con diferencia significativa entre estas y con respecto al control (F = 1,81; gl = 6,49; P<0,02) (Tabla 3).
Mortalidad de larvas de Chloridea virescens causadas por cepas de Beauveria bassiana y Metarhizium robertsii.
Medias con la misma letra no son significativamente diferentes (α < 0,05). Los resultados son medias ± desviación estándar, obtenidos de datos de los experimentos realizados por triplicado.
En todas las cepas la mortalidad promedio varió de 57 % a 97%. La mayor mortalidad de larvas se obtuvo con la ceра nativa M1 de M. robertsii con 97% a los 7 días, las otras cepas causaron de 63% a 83%. Estos resultados de mortalidad son mayores a los encontrados por Acuña-Jiménez et al., (2015) sobre larvas de C. virescens usando formulados microencapsulados. Por su parte, Manzanarez-Jiménez et al. (2021b) usaron formulaciones en aceites sobre larvas de primer a tercer estadio de C. virescens, encontrando mortalidad superior al 50% a partir de los 4 días con M. robertsii y 4,5 días con B. bassiana.
Lo anterior nos indica que la patogenicidad de los hongos entomopatógenos es una característica importante para la selección de cepas con potencial para controlar plagas de insectos. De acuerdo con esto, la evaluación y selección de las cepas que se realizó en este trabajo permite aumentar la efectividad de estos agentes en el control de las plagas que afectan a estos cultivos, como lo han considerado otros autores (Faria & Wraight, 2007; Inglis et al., 2012; Vega et al., 2012).
El mejor tiempo letal medio de mortalidad de larvas de segundo a tercer estadio fue de tres días con M. robertsii (M1) y B. bassiana (B9). Este resultado es importante para el control biológico de C. virescens, ya que la mayor voracidad de las larvas fue del primero al tercer estadio (Manzanarez-Jiménez et al., 2021a). En este estudio se encontró que los hongos M. robertsii (M1) y B. bassiana (B9) se pueden utilizar para controlar larvas en estadios de desarrollo temprano para evitar que sus poblaciones alcancen umbrales económicos que causen pérdidas económicas en el rendimiento del cultivo, tal como lo sugieren García-Gutiérrez et al. (2019). No obstante, para evitar que las larvas se desarrollen es importante realizar estudios de la patogenicidad de cepas a utilizar en su control, y considerar el comportamiento de la plaga sobre las plantas, ya que se observó que el movimiento de las larvas sobre el follaje evita el contacto con los hongos (Manzanarez-Jiménez et al., 2021b).
Conclusiones
Las cepas de M. robertsii y B. bassiana fueron patógenas contra larvas del gusano del fruto a partir del tercer día de haber sido inoculadas con estos hongos en condiciones de laboratorio. La cepa M1 de M. robertsii y B9 de B. bassiana tuvieron tiempos letales cortos, destacando la cepa M1 con el mayor crecimiento, esporulación, germinación de conidios y patogenicidad. Estos parámetros determinaron el potencial de esta cepa para evaluarla en el control de larvas de C. virescens en condiciones de campo.
Contribución de los autores
Cipriano García Gutiérrez participó en la planeación y realización del trabajo, diseño del experimento, análisis de resultados, discusión, conclusiones y escritura del manuscrito.
Lucía Araceli Manzanarez Jiménez participó en la realización del trabajo, en el proceso de toma de datos experimentales, búsqueda de referencias, análisis estadístico de datos, resultados, discusión y escritura del manuscrito.
Antonio Luna González participó en realizar sugerencias y comentarios sobre la información general del manuscrito y revisión de las referencias.
Ninfa M. Rosas García participó en hacer sugerencias al trabajo experimental, comentarios sobre la información en el manuscrito y revisión de las referencias.
Conflicto de intereses
Los autores declaramos no tener conflicto de intereses.
Footnotes
Agradecimientos
Agradecemos a CONACYT por la beca otorgada para estudio de doctorado a Lucía Araceli Manzanarez Jiménez. Así como al IPN por el financiamiento al proyecto SIP-IPN 20210094.
