Abstract
The natural occurrence of specific pathogens and biopesticides applied in an inundative fashion can contribute significantly to control of the potato tuber moth, Phthorimaea operculella. Most of the research conducted and practices used for control of P. operculella use one species of granulovirus and the bacterium Bacillus thuringiensis (Bt). The P. operculella granulovirus (PhopGV) has the potential to play a significant role in the integrated management of the pest in stored tubers as well as in field crops. At the same time, Bt has been used successfully against P. operculella infestations in the field and in stored tubers. PhopGV and Bt are safe for application personnel and for the food products; in addition, they do not affect beneficial insects and other nontarget organisms. Other natural insecticides are the biofumigant fungus Muscodor albus, botanicals, sex pheromones and physical measures for P. operculella control in stored tubers. The implementation of biopesticides will ultimately depend on an increased awareness of their attributes by growers and the public, who will be the main drivers for their use and commercialization.
Introducción
La palomilla de la papa, Phthorimaea operculella (Zeller, 1873), es originaria de las regiones productoras de papa de la Cordillera Andina en América del Sur, pero se ha propagado a áreas más tropicales y subtropicales productoras de papa (Sporleder et al. 2004; Sporleder y Kroschel 2008). La palomilla está establecida en el Noroeste del Pacífico de los Estados Unidos y ha provocado serias inquietudes por el daño que causa al cultivo de la papa (Rondon et al. 2008; De Bano et al. 2010). Alternativas para su control antes de la cosecha incluyen el uso de varios insecticidas de amplio espectro (Mansour 1984; Bennett et al. 1999; Schreiber y Jensen 2005). Sin embargo, el intervalo de seguridad precosecha de muchos insecticidas químicos no permite el tratamiento de la papa justo antes de la cosecha y consumo.
Se han reportado varios enemigos naturales de P. operculella, incluyendo insectos parasitoides y predadores (Briese 1981; Horne 1990; Kroschel y Koch 1994; Kroschel 1995; Herman 2008a, 2008b; Horne y Page 2008) y patógenos (Kroschel y Lacey 2008; Lacey y Kroschel 2009). La ocurrencia natural y aplicaciones inundativas de entomopatógenos (biopesticidas) pueden contribuir significativamente al control de P. operculella como una estrategia de manejo integrado de plagas (MIP).
Se han desarrollado diversos plaguicidas microbiales (Lacey et. al. 2001a) y algunos de ellos se utilizan para el control de algunos insectos plaga de la papa, incluyendo P. operculella (Radcliffe 1982; von Arx et al. 1987; Hamilton y Macdonald 1990; Zehnder et al. 1994; Cloutier et al. 1995; Kroschel et al. 1996a, b; Zeddam et al. 2003; Wraight y Ramos 2005; Kroschel y Lacey 2008; Lacey et al. 2009; Wraight et al. 2009). Los insecticidas microbiales no requieren intervalos de seguridad precosecha, son inocuos para los agricultores y consumidores, y no afectan a organismos no específicos como los insectos benéficos.
En varios países alrededor del mundo se han hecho esfuerzos sustanciales para desarrollar agentes microbiales para el control de P. operculella. En contraste, muy poco se ha hecho a este respecto en los Estados Unidos. En esta revisión se presenta información acerca del desarrollo y potencial de virus, bacterias y nematodos para el control de P. operculella, con énfasis en las investigaciones desarrolladas en el estado de Washington.
Virus
En muchos de los países en donde se ha establecido la palomilla de la papa se ha encontrado al virus de la granulosis que ataca a P. operculella (PoGV). Su presencia se ha confirmado en la región Andina de América del Sur (Alcazar et al. 1991, 1992a; Sporleder 2003), África (Broodryk y Pretorius 1974; Laarif et al. 2003), el Medio Oriente (Kroschel y Koch 1994), Asia (Zeddam et al. 1999; Setiawati et al. 1999), Australia (Reed 1969; Briese y Mende 1981) y América del Norte (Hunter et al. 1975). El nombre del virus se deriva de su apariencia granular bajo microscopia electrónica (Fig. 1A). Cada gránulo o partícula del virus (OB) contiene una sola barra viral (Fig. 1B). Cuando las partículas (OBs) son consumidas por la larva de P. operculella éstas se disuelven en el medio alcalino del tracto digestivo, liberando a las barras virales que se unen y atraviesan las células epiteliales del intestino medio. De ahí, invaden una variedad de células del huésped y producen cientos de millones de partículas virales (OBs) por larva. Las células del cuerpo graso de la larva son el sitio predominante de producción del virus. Por último, la larva infectada muere y se convierte en una fuente de inóculo para otras larvas. Reed (1971) y (Sporleder et al. 2007, 2008), reportaron los efectos de la concentración del virus, la temperatura y la edad de la larva en la progresión de la enfermedad en P. operculella. La mayoría de las larvas mueren después de 10 - 14 días de ingerir el virus y dosis muy altas del virus PhopGV pueden causar la muerte por toxicosis en 48 horas.
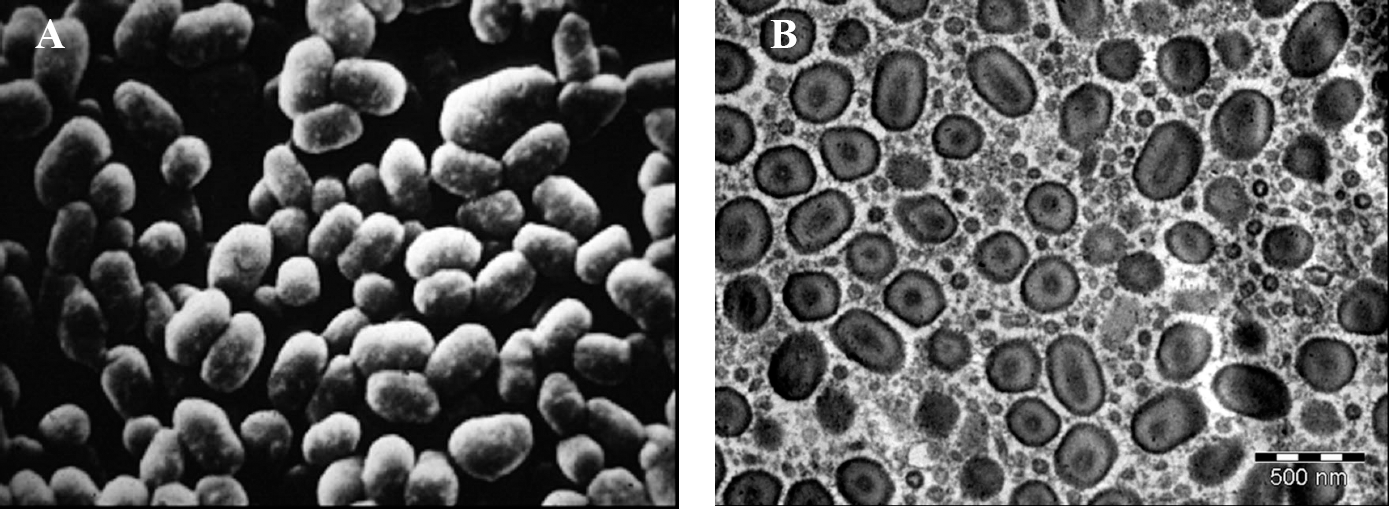
Gránulos del virus PoGV de la palomilla de la papa.
Sporleder (2003) evaluó la actividad de 14 asilamientos geográficos del PhopGV y encontró un rango de actividad que cubre varios órdenes de magnitud. Vickers et al. (1991) analizaron patrones de restricción de ADN y demostraron diferencias genéticas menores entre ocho aislamientos de PhopGV de diverso origen geográfico. Ellos descubrieron tres genotipos que están estrechamente relacionados y el aislado peruano pudo distinguirse fácilmente de otros cinco provenientes de otros insectos hospederos. Bioensayos de tres aislados de virus de la granulosis PhopGV de Indonesia revelaron propiedades biológicas similares (Zeddam et al. 1999). Kroschel et al. (1996a) reportaron semejanza entre un aislado de Yemen y uno de Perú. En contraste, Léry et al. (1998) demostró considerables diferencias genéticas entre un aislado de Túnez y aislados de virus granular PhopGV de otras regiones.
Como muchos virus granulares, PhopGV tiene un reducido rango de hospederos. Solamente infecta a P. operculella y algunas otras especies de la misma familia (Gelechiidae). Por ejemplo, la palomilla de la papa de Guatemala, Tecia solanivora, (Povolny 1930), es susceptible a PhopGV, pero menos que P. operculella (Zeddam et al. 2003; Villamizar et al. 2005). Aunque se ha aislado al PhopGV de Symmetrischema tangolias (Gyen 1913) (Ángeles y Alcázar 1996), éste no parece afectar a dicha especie (J. Kroschel, com. pers.). Pokharkar y Kurhade (1999) reportaron falta de infectividad para otras once especies de lepidópteros.
En Australia y Yemen se ha documentado la incidencia natural de PhopGV en poblaciones de P. operculella (Briese 1981; Kroschel y Koch 1994; Kroschel 1995) donde las larvas estaban infectadas en bajos niveles. Kroschel y Koch (1994) observaron que la mayoría de la mortalidad de P. operculella en Yemen fue causada por parasitoides ichneumónidos y bracónidos. Kroschel et al. (1996b) sugieren que los parasitoides resultaron ligeramente inhibidos por la aplicación de 5 × 1013 cuerpos de inclusión del virus PhopGV/ha, pero no por la aplicación del virus en una concentración diez veces menor. Las larvas de los parasitoides aparentemente continuaron desarrollándose en las larvas infectadas de P. operculella. El hecho de que PhopGV normalmente infecte larvas recién nacidas mientras que muchos parasitoides de P. operculella atacan huevos y larvas mayores, sugiere que puede emplearse un control combinado. Los registros sobre la incidencia natural del virus granular PhopGV en poblaciones de P. operculella indican que los niveles del virus son muy bajos para reducir el daño de la palomilla de la papa y que se requieren aplicaciones inundativas (fumigar o asperjar) para proveer un control efectivo. Las evaluaciones en campo del virus granular PhopGV para el control de P. operculella son limitadas y los resultados variables. Reed (1971) y Reed y Springett (1971) condujeron los primeros ensayos de campo del virus de la granulosis PhopGV en Australia y encontraron que una aplicación temprana del virus (6275 larvas/ha) puede lograr un control efectivo. Además, ellos observaron que el virus de la granulosis PhopGV se propaga fácilmente en áreas no tratadas.
Reed (1971) concluyó que el virus alcanzó a las larvas que minaban las hojas a través de las estomas, y que el viento y los pájaros fueron responsables de diseminar el virus. Salah y Aalbu (1992) probaron el virus en suspensión y en polvo bajo condiciones de campo en Túnez. La infestación de la papa se redujo hasta en un 73% cuando se aplicó el virus en la superficie del suelo en los cultivos de papa. Kurhade y Pokharkar (1997) reportaron que dosis de PhopGV de 5,5 × 1011 cuerpos de inclusión/ha y Endosulfan al 0,035% proporcionaron un control efectivo de P. operculella que resulta en una infestación de la papa 6,9% más baja comparada con otros tratamientos de insecticidas.
Salah et al. (1994) pusieron a prueba una combinación de Bacillus thuringiensis Berliner, 1911, PhopGV y una doble irrigación para el control integrado de P. operculella en pruebas de campo en Túnez. En algunos casos, el control integrado resultó ser más eficiente que los insecticidas convencionales. Kroschel (1995) y Kroschel et al. (1996b) obtuvieron un control significativo de P. operculella en papa con aplicaciones de 5 × 1013 cuerpos de oclusión/ha. Once días después del tratamiento se observaron los síntomas típicos como coloración blanca lechosa y vitalidad reducida de las larvas, y una mortalidad del 70% a los 19 días del tratamiento. Finalmente el tratamiento viral causó hasta un 82,5% de mortalidad de P. operculella.
Estudios en el estado de Washington revelaron el potencial de PhopGV en el Noroeste de Estados Unidos. El Laboratorio de Investigación Agrícola de Yakima del Departamento de Agricultura de Estados Unidos desarrolló y optimizó métodos de producción de la palomilla P. operculella y del virus PhopGV. Actualmente se producen alrededor de 10,000 huevecillos y más de 1,500 pupas de P. operculella por semana. El virus se produce en larvas de P. operculella recién emergidas y expuestas en papas previamente tratadas con suspensiones virales de aproximadamente 1.5 × 108 cuerpos de inclusión/ ml. Los huevecillos se inoculan con suspensiones con 1,5 × 1010 cuerpos de inclusión/ml. El virus se recolecta de las larvas infectadas que salen de las papas, aproximadamente 14 días después.
En pruebas de campo, aplicaciones semanales de PhopGVde 9,9 × 1012 cuerpos de inclusión/ha no redujeron el daño inicial (porcentaje de hojas minadas) en la primera generación de P. operculella, a pesar de que más del 90% de larvas tratadas estaban infectadas con virus y no puparon. Sin embargo, aplicaciones semanales de 9,9 × 1012/ha resultaron en una reducción de 76,3% de hojas minadas y una reducción de 96,3% de larvas de P. operculella en la segunda generación que es una dosis alta del virus. Una rotación semanal del PhopGV y Bacillus thuringiensis fue más efectiva que las aplicaciones semanales de sólo Bt 1,12 kg/ha con una reducción de larvas de la segunda generación del 97,1%. Una dosis menor del virus de la granulosis PhopGV de 9,9 × 1011 cuerpos de inclusión/ha fue significativamente menos efectiva que las tasas más altas.
Las aplicaciones de dosis de PhopGV que causaron más del 95% de mortalidad en condiciones de campo, no son económicamente factibles. Por ejemplo, Arthurs et al. (2008b) reportaron un buen control por mayor tiempo de altas poblaciones de P. operculella después de varias aplicaciones de PhopGVa la concentración de 1013 CO/ha. Las poblaciones fueron reducidas entre 86-96% cuando se aplicaron sobre follajes y 90 a 97% cuando se hicieron aplicaciones sobre los tubérculos depositados en cajas inmediatamente después de cosechados.
La eficacia de la aplicación no sólo depende de la cepa del virus, dosis y método de aplicación, sino que su efecto puede verse reducido por la inactivación del virus por los rayos ultravioletas (UV) (Kroschel et al. 1996a; Sporleder et al. 2001; Sporleder 2003; Arthurs et al. 2008b). Kroschel et al. (1996a) investigaron la eficacia y persistencia en campo de diferentes preparaciones del virus de la granulosis PhopGV. Ellos calcularon una vida media del virus en papas expuestas al sol de 1,3 días. Mortalidades de larvas en primer estadio variaron de 43 - 49% cuando se alimentaron de vegetación colectada dos días después del tratamiento. Solamente del 19,4 al 25,8% de larvas murieron cuando se alimentaron del follaje recogido a los ocho días después de la aplicación del virus. Una variedad de coadyuvantes que ha sido usado para proteger otros baculovirus de la inactivación de los rayos ultravioleta (UV) fueron revisados por Burges y Jones (1998).
Sporleder (2003) investigó el uso de colorantes, abrillantadores ópticos, antioxidantes, materiales derivados de insectos hospederos y tipos de formulación para protección del virus de la granulosis PhopGV de la inactivación de los rayos ultravioleta. El notó que el abrillantador óptico Tinopal y ciertos antioxidantes protegieron la infectividad de virus irradiados. Sin embargo, se logró mayor protección contra luz UV en las preparaciones de larvas infectadas molidas en agua comparado con otras preparaciones (Kroschel y Koch 1996; Sporleder 2003; Chaparro et al. 2010).
El virus de la granulosis PhopGV ha sido reportado por varios investigadores como una muy buena protección a papas tratadas, especialmente en almacenes sin refrigeración. Éxitos en el control de la palomilla de la papa usando el virus de la granulosis PhopGV han sido demostrados en países andinos como Perú, Ecuador, Bolivia y Colombia, de donde P. operculella y la papa se cree que son originarios (Alcazar et al. 1992b; CIP 1992; Zeddam et al. 2003). El virus, además ha sido evaluado en papas almacenadas en varios países en el Medio Oriente, Norte de África y Asia (Amonkar et al. 1979; Hamilton y MacDonald 1990; Islam et al. 1990; Das et al. 1992; Setiawati et al. 1999; Chandel y Chanla 2005; Chandel et al. 2008). Dado que el virus no está expuesto a los rayos ultravioleta en almacenamiento, la protección de las papas puede durar varios meses.
Se estudió la efectividad de una formulación en polvo seco del granulovirus, preparado mezclando 1 kg de talco en un litro de agua con 20 larvas infectadas con el granulovirus, más Triton al 0.2% como agente dispersante (Alcázar y Raman 1992). Esta formulación se utilizó para la proporción de 5 kg/ton de papa para el almacenamiento. En esta investigación se demostró que los tubérculos tratados con el granulovirus presentaron 7, 8, 13 y 31% de tubérculos dañados a los 30, 60, 90 y 120 días de almacenamiento respectivamente; mientras que los tubérculos sin protección presentaron 64, 96, 100 y 100% de daño respectivamente. Estos resultados indican una reducción del daño en 89, 91, 87 y 69% a los 30, 60, 90 y 120 días de almacenamiento.
Pruebas realizadas a 25°C por Arthurs et al. (2008a) indicaron que las suspensiones de PhopGV en agua o mezclado con diluentes (talco, arena, tierra de diatomeas y arcilla caolín), fueron efectivas para controlar larvas neonatas en tubérculos almacenados. Las suspensiones acuosas de PhopGV y virus formulado con talco provocaron 100% de mortalidad de larvas neonatas en tubérculos pre-infestados a concentraciones bajas como 0,00625 EL (equivalentes larvales) de PhopGV/kg tubérculos. Sin embargo, el tratamiento de tubérculos post-infestados con 0,4 EL de PhopGV/kg de tubérculos provocó solamente 92% de mortalidad. El efecto del PhopGV sobre la mortalidad y dispersión en condiciones de almacén refrigerado fue reportado por Lacey et al. (2010). El virus ocasionó un control efectivo de P. operculella en papas infestadas y también redujo la dispersión de las larvas que salieron de los tubérculos infestados a los tubérculos no infestados.
El potencial para el desarrollo de resistencia al virus de la granulosis PhopGV en larvas de P. operculella ha sido estudiado por Briese y Mende (1981, 1983) y Sporleder (2003). Briese y Mende (1981) notaron diferencias en susceptibilidad al virus PhopGV entre poblaciones de P. operculella en campos de Australia. Usando un bioensayo en laboratorio ellos compararon la susceptibilidad de 16 poblaciones en campo y observaron una diferencia de 11,6 veces entre las poblaciones más y menos susceptibles. Después de exposiciones seriadas de larvas susceptibles de P. operculella al virus PhopGV durante seis generaciones, Briese y Mende (1983) observaron un incremento de 140 veces la dosis letal media (LD50). Observaciones similares fueron hechas por Sporleder (2003). Larvas de P. operculella que sobrevivieron a la exposición de concentraciones de virus que produjeron 50, 75 y 90% de mortalidad de las poblaciones progenitoras susceptibles fueron altamente resistentes al virus después de 12 generaciones. Una retrocruza sencilla con la población susceptible no redujo el nivel de resistencia. Basado en los reportes anteriores, los manejos de resistencia deben ser incorporados en los programas de control que regularmente usan el virus PhopGV.
Métodos para la producción in vivo de PhopGV son presentados en Reed y Springett (1971), CIP (1992), Kroschel et al. (1996b), Sporleder (2003), Zeddam et al. (2003), y Villamizar et al. (2005). Básicamente los métodos empleados para la producción masiva de P. operculella se basan en la infección de larvas recién nacidas expuestas a las papas que han sido tratadas por inmersión en una suspensión acuosa de larvas trituradas e infectadas con PhopGV. Alternativamente, los huevos de P. operculella pueden sumergirse en suspensiones de PhopGV (Sporleder et al. 2005). Las larvas consumen el virus directamente cuando salen del huevo y son colocadas en papas en las cuales se desarrollan. Otro método de producción involucra la aspersión de suspensiones del virus en plantas de papa infestadas en el campo, la colección del follaje infestado después de que la larva muere, y la separación de la larva infectada del follaje exponiéndolo al calor (Matthiessen et al. 1978). Sporleder (2003) presentó información sobre los efectos de la temperatura, concentración inicial del virus, estadio larvario y densidad por gramo de papa en los rendimientos de los cuerpos de oclusión del virus. El número de larvas infectadas con el virus aumentó al aumentar la concentración del virus con una concentración óptima de 109 cuerpos de inclusión/ml de suspensión. La temperatura óptima y la densidad larvaria para la producción del virus fueron de 25°C y dos gramos de papa/larva respectivamente. Pokharkar y Kurhade (1999) reportaron además 25°C como óptima para la producción del virus. Léry et al. (1997) y Sudeep et al. (2005) reportaron el establecimiento de líneas de células de P. operculella y demostraron su utilidad para la producción de virus in vitro. El virus se ha producido comercialmente en Perú, Bolivia, Egipto y Túnez. Aunque el virus PhopGV no está disponible comercialmente en los Estados Unidos, su desarrollo y registro está garantizado basado en la necesidad del control de P. operculella, el potencial del virus PhopGV para retardar el desarrollo de resistencia a insecticidas convencionales. La seguridad del virus PhopGV le permitirá ser usado en los sistemas de manejo integrado de plagas (MIP) con un mínimo impacto sobre los organismos benéficos no específicos (Lacey y Arthurs 2008; Lacey y Kroschel 2009).
Bacterias
Bacillus thuringiensis Berliner, 1915 (Bt) es la única bacteria que ha sido evaluada para el control de P. operculella. Esta bacteria produce en forma natural toxinas cristalinas (venenos estomacales) que causan intoxicación en los insectos por la ruptura de las células epiteliales del intestino medio del tracto digestivo (Beegle y Yamamoto 1992; Garczynski y Siegel 2007). Los insecticidas basados en las toxinas de Bt son los más usados mundialmente como plaguicidas microbiales y se producen comercialmente para su uso contra un amplio rango de plagas incluyendo coleópteros (escarabajos), dípteros (moscas y mosquitos) y lepidópteros (mariposas y polillas) incluidas especies que atacan a la papa (Krieg et al. 1983; Hamilton y Macdonald 1990; Kroschel y Koch 1996; Lacey et al. 1999, 2001b; Wraight y Ramos 2005; Wraight et al. 2007; Arthurs et al. 2008a, 2008b). Bt es considerado ideal para el manejo de plagas porque es específico para plagas e inocuo para humanos y enemigos naturales de muchas plagas de cultivos. Formulaciones agrícolas típicas de Bt incluyen polvos humectables, concentrados líquidos, polvos, cebos y otros, y se comercializan con nombres como Acrobe, Bactospeine, Certan, Dipel, Javelin, Leptox, Novabac, Thuricide y Victory (Navon 2000; Garczynski y Siegel 2007) Para ser efectivos, los cristales de Bt tienen que ser ingeridos por la larva, siendo inefectivo contra insectos adultos. La muerte puede ocurrir dentro de pocas horas o en pocas semanas de la aplicación de Bt, dependiendo de la especie de insecto, edad y de la cantidad de Bt ingerido. Aunque hay muchas razas de Bt, cada una con una toxicidad específica a ciertos tipos de insectos, Bt subespecie kurstaki es la más comúnmente usada contra lepidópteros (Navon 2000). En Bolivia se detectaron incidencias naturales de Bt en poblaciones nativas de P. operculella (Hernández et al. 2005). Se aislaron muchas razas de suelos agrícolas, bodegas y papas infestadas con P. operculella. Aun más, algunas de las cepas mostraron tener igual o incluso mayor toxicidad comparadas con una cepa comercial normal (HD -1), lo que sugiere que se pueden desarrollar cepas nativas más efectivas.
Bt ha sido ampliamente probada para controlar infestaciones de P. operculella en laboratorio, campo y en condiciones de almacenamiento. La concentración letal media (LC50) requerida aumenta con la edad de la larva (Salama et al. 1995a). Bt subespecie kurstaki (Turicide HP) aplicada a 200mg/ kg de papa redujo sustancialmente la sobrevivencia de P. operculella del huevo a la emergencia del adulto (0,4%), comparado con PhopGV (0,8-34,7%, dependiendo de la dosis) o el testigo (32,5%) (von Arx y Gebhardt 1990). En otros estudios de laboratorio, formulaciones con polvo de Bt (5000 unidades internacionales/mg) junto con permetrina (0,1%), protiofos (1%) y rotenona (2,4%) dieron buena protección a las papas contra infestaciones de P. operculella y fueron más efectivas controlando infestaciones comparadas con 1% clorpirifos (Hamilton y Macdonald 1990). En estudios de laboratorio e invernadero la potencia de Bt se mantuvo por más de 60 días cuando se aplicó al suelo para proteger semillas o papas en maceta (Amonkar et al. 1979).
Bt controla exitosamente las infestaciones de P. operculella en condiciones de campo, sin embargo, es necesario hacer varias aplicaciones porque Bt se degrada con los rayos ultravioleta (UV) del sol, y se pierde del suelo con la lluvia (Salama et al. 1995b; Arthurs et al. 2008b). Se necesitaron tres aplicaciones consecutivas de Bt (B10-T) en intervalos de ocho días para controlar a P. operculella en un cultivo de tomate en Israel (Broza y Sneh 1994). Se utilizaron aplicaciones de alto volumen (500 l/ha) para hacer llegar el ingrediente activo a los túneles de las hojas donde las larvas jóvenes estaban minándolas. En pruebas de campo en la India, aplicaciones foliares de Bt (Thuricide a 2-5 Kg/ha) en intervalos de 15 días iniciados 60 días después de la plantación, resultaron casi tan efectivas para controlar las infestaciones de P. operculella como el Paratión y el Carbaril aplicados a la superficie del suelo, resultando en un rendimiento promedio de papas de 9,3 - 10,7 ton/ha, comparado con 6,7 toneladas sin insecticidas (Awate y Naik 1979). En la República de Yemen las infestaciones de Polilla de la papa son muy altas, Kroschel (1995) ensayó Bt (‘Dipel') por dos estaciones, en dos concentraciones (0,2% y 0,3%) con tres y cuatro aplicaciones por estación de papa. En el tratamiento testigo la infestación en hojas alcanzó 26 y 25 minas por planta. La aplicación de Bt hasta la fase de amarillamiento de la planta, redujo la infestación de hojas por la polilla en 41% y 54% y al final la infestación de los tubérculos a la cosecha en 23% y 10% respectivamente, comparado con el tratamiento testigo. En comparación, los mejores resultados se lograron con el piretroide Fenvalerato (0,1%) el cual redujo la infestación de hojas en 100% y la infestación de tubérculos en 70%.
En muchas partes del mundo, también se ha evaluado a Bt y otros métodos no químicos para el control de P. operculella después de la cosecha en almacenes de papa tradicionales (no refrigerados). En Yemen, Kroschel y Koch (1996) evaluaron varios plaguicidas de bajo riesgo para proteger las papas de P. operculella en el almacén. Aplicaciones sobre las papas de Bt mezclado con arena fina y polvo resultó completamente efectivo contra los huevecillos recién depositados, y controló además al 96% de larvas que ya estaban dentro de la papa. En Egipto, otra preparación de Bt (Dipel 2X 0.3%) resultó ser muy efectiva en almacén, eliminando la infestación de P. operculella frente a una infestación del 100% en los testigos no tratados 60 días después del tratamiento (Farrag 1998). En Túnez, el manejo integrado de Bt aplicado en el comienzo del periodo de almacenaje en combinación con el control cultural (cosecha temprana) eliminó la dependencia de fumigaciones con paration (von Ark et al. 1987). En los casos en que la papa tenía una infestación inicial alta (mayor a 20%), se reemplazó a Bt con un piretroide sintético (Permetrina). En Indonesia, tratamientos con Bt subespecie kurstaki (Thuricide en 2 g/l) causó 79% de mortalidad en larvas después de cuatro meses de almacenaje comparado con 58% de mortalidad de larvas sobre el follaje en invernadero (Setiawaiti et al. 1999). En Perú, Raman et al. (1987) encontraron que Bt subespecie kurstaki (Dipel) fue efectiva reduciendo el daño de alimentación en el almacenamiento cuando se aplicó como formulación en polvo. El aceite vegetal (1-2%) además redujo la eclosión de huevos pero fue fitotóxico, resultando en niveles altos de pudrición de papas. Sin embargo, en otros estudios, Bt subespecie thuringiensis (0,2% Bactospeine WP 16000 IU/mg) fue inefectivo en la protección de las papas en el almacenamiento, resultando tantas papas dañadas como los controles no tratados (Das et al. 1992).
Otra investigación sugiere que la efectividad de Bt puede mejorarse mediante formulaciones con extractos vegetales con propiedades insecticidas. Por ejemplo, extractos de Atropa belladona L., 1753, Hyoscyamus niger L., 1753 y Solanum nigrum L., 1753 (Solanaceae) redujeron la concentración letal media (LC50) de Bt contra P. operculella de 82 a 43, 31 y 40 μg/ml, respectivamente (Sabbour y Ismail 2002).
Nemátodos Entomopatógenos
Los nemátodos entomopatógenos (NEPs) son parásitos específicos de insectos de los géneros Steinernema (Steinernematide) y Heterorhabditis (Heterorhabditidae) que están asociados obligadamente con bacterias simbióticas (Xenorhabdis spp. y Photorhabdis spp., respectivamente). Estas últimas son responsables de matar rápidamente a los insectos hospederos. Después de entrar a un insecto hospedante, los nemátodos en su etapa juvenil infectiva liberan una bacteria simbiótica. Además de matar al hospedante, la bacteria digiere los tejidos del insecto y produce antibióticos que protegen el cadáver de organismos saprófitos y carroñeros (Kaya y Gaugler 1993). Después de dos o tres ciclos reproductivos, cuando se reducen los nutrientes del hospedante, los estadios juveniles infecciosos se reproducen y abandonan al insecto hospedante. Este estado es capaz de infectar a los nuevos hospedantes o persistir por meses sin ellos (Kaya y Gaugler 1993; Glazer 2002). En las últimas cinco décadas se ha demostrado el potencial de los NEPs como agentes de control biológico de una gran variedad de insectos plaga (Georgis et al. 2006). Actualmente se producen comercialmente varias especies de NEPs para el control de diversas especies de insectos plaga de importancia económica (Grewal et al. 2005; Koppenhöfer 2007). Sin embargo, su uso para el control de P. operculella se ha investigado sólo recientemente. Investigaciones sobre el efecto de nematodos entomopatógenos en P. operculella en el Laboratorio de Investigación Agrícola de Yakima, en Wapato, Washington, revelaron un buen potencial para el control de estadios de la palomilla que entran y salen del suelo. Se considera que estos nematodos tienen potencial para el control de P. operculella en pilas de desecho de papas. Se demostró que la L4 de todas las especies del complejo de P. operculella son altamente susceptibles a las cepas de Heterorhabditis sp. procedentes de los altos de los Andes de Ecuador y Perú (J. Alcázar datos no publicados).
Hongos Entomopatógenos
Numerosas especies de hongos entomopatógenos son agentes efectivos para el control microbiano de varias especies de insectos plaga (Goettel et al. 2005; Ekesi y Maniania 2007), incluyendo algunas plagas claves de la papa (Lacey et al. 1999, 2009; Wraight y Ramos 2005, Wraight et al. 2007, 2009). Sin embargo, las investigaciones sobre el uso de hongos para el control de P. operculella aún son limitadas. Estudios de laboratorio con dos Hypocreales comunes, Metarhizium anisopliae (Metschnikoff) Sorok y Beauveria bassiana (Balsamo) Vuillmen, indican que tienen potencial para el control de larvas de P. operculella, particularmente larvas jóvenes (Hafez et al. 1997; Sewify et al. 2000). Hafez et al. (1997) también demostraron la actividad de B. bassiana contra prepupas, pupas y adultos de P. operculella. Sewify et al. (2000) reportaron que la combinación de M. anisopliae y PhopGV tuvo un efecto sinérgico para el control de larvas cuando utilizó una concentración alta del hongo con una concentración baja del virus.
El hongo endofítico, Muscodor albus, Worapong et al. 2001, produce varios compuestos volátiles como alcohol, ésteres, cetonas, ácidos y lípidos, que son biocidas para un amplio rango de organismos incluyendo bacterias y hongos fipatogenos, nemátodos e insectos (Strobel et al. 2001; Worapong et al. 2001; Riga et al. 2008; Lacey et al. 2008). La actividad contra adultos y larvas de M. albus fue reportada contra P. operculella por Lacey y Neven (2006) y Lacey et al. (2008). Los adultos y larvas neonatas de P. operculella fueron expuestos a los volátiles de M. albus por 72 horas en cámaras herméticamente cerradas. Los porcentajes promedio de mortalidad de adultos de P. operculella en las cámaras con 15 y 30 g de micelio formulado fueron de 84,65 y 90,6%, respectivamente. El desarrollo del estado de pupa de P. operculella que fueron tratadas como larvas neonatas en tubérculos infestados, con 15 y 30 g de micelio formulado de M. albus se redujo a 61,8% y 72,8%, respectivamente. Lacey et al. (2008) observaron que el tiempo de exposición al hongo M. albus afectó significativamente la mortalidad de larvas cuando están infectando los tubérculos y su desarrollo hacia el estado de adulto. La duración del tiempo de exposición de 3,7 ó 14 días a 24°C seguido por un periodo de incubación a 27°C hasta la emergencia de adultos provocó una mortalidad de 84,2%, 95,5% y de 99,6%, respectivamente. A 10°C y 15°C, la mortalidad de larvas se redujo significativamente.
Conclusiones
Los enemigos naturales como parásitos, depredadores y patógenos pueden ejercer un control substancial de las poblaciones de P. operculella, especialmente cuando se utilizan pocos insecticidas adicionales (Matthiessen y Springett 1973; Briese 1981; Kroschel y Koch 1994; Coll et al. 2000; Kroschel y Lacey 2008; Lacey y Kroschel 2009). Es probable que ninguna especie de enemigo natural provea por si sola un control adecuado, pero juntas pueden complementarse y regular a P. operculella durante toda la temporada de crecimiento, en las diferentes etapas de su ciclo de vida y en varias densidades de poblaciones de la palomilla. Además de su utilidad para controlar P. operculella y otros insectos plaga, los patógenos específicos ofrecen otros beneficios incluyendo seguridad para los aplicadores y consumidores, e inocuidad sobre enemigos naturales y el ambiente (Laird et al. 1990; Hokkanen y Hajek 2003). La integración de patógenos y nemátodos contra insectos específicos en el agroecosistema de la papa dependerá de su compatibilidad con otros agentes de control, incluyendo plaguicidas, así como efecto de las condiciones del ambiente en su infectividad y persistencia. Su utilización adecuada requerirá de la selección de cepas de patógenos efectivas, del desarrollo de formulaciones para mejorar el su vida útil en almacenamiento, aplicación y persistencia, de la selección cuidadosa de la etapa de aplicación óptima, así como del mejor entendimiento de “cómo” se integran a los sistemas de producción de la papa. En última instancia, su implementación dependerá del mejor conocimiento de sus atributos por parte de los productores y el público (Lacey et al. 2001a).
Footnotes
Agradecimientos
Nina Bárcenas, Jorge Toledo, Don Hostetter y a Jaime Molina, por sus comentarios constructivos a este manuscrito.
