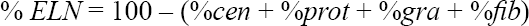Abstract
The use of insect cuticle is a viable option to induce the growth of entomopathogenic fungi. Spodoptera frugiperda (Sf) and Heliothis virescens (Hv). Pupal powder was obtained, which was added to enrich the Potato Dextrose Agar (PDA) culture medium at concentrations of 0.25, 0.5 and 1 %. The powder was used to induce the radial growth of Beauveria bassiana and Metarhizium robertsii. The lethal time (TL) of M. robertsii induced at a concentration of 108 spores/mL and a PDA control. Larval mortality was analyzed by ANOVA and a Tukey test (α = 0.05). The fat content of Sf was 49.9 % and that of Hv 41.9 %; the extract free of nitrogen (ELN) 21.3 and 32.0 %; proteins 15.7 and 13.5 %, and energy 517.87 and 493.73 (Kcal/g), respectively. Nutrients and energy had inducer effect on the growth of M. robertsii with 1 % Sf and Hv pupal powder, reaching 75.5 and 74.2 mm of radial growth and 60 mm in the PDA control. B. bassiana with Hv 0.5 % 55 mm and with Sf 0.25 %, 50 mm and in the PDA control 32.5 mm (α = 0.05). M. robertsii induced with Sf causing 91.6 % mortality of Sf larvae and 66.6 % in PDA, at seven days (α = 0.05). The supplementation of the insects increased the growth of the fungi in PDA medium, this contributed to the pathogenicity of the induced strain of M. robertsii on S. frugiperda.
Introducción
El gusano cogollero del maíz Spodoptera frugiperda (J. E. Smith, 1797) (Lepidoptera: Noctuidae) y el gusano del fruto del tomate Heliothis virescens Fabricius, 1777 (Lepidoptera: Noctuidae) son insectos plaga que atacan cultivos de importancia económica en México (Blanco et al. 2007; Suris Campos et al. 2013; Nunes-Lemes et al. 2014). El método más utilizado para combatir a las plagas agrícolas es el control químico, aún con los daños que ocasiona en el ambiente (Mahmood et al. 2016), por lo que es necesario contar con métodos alternativos de control biológico como los hongos entomopatógenos. Las especies más utilizadas en el control de insectos son Metarhizium robertsii (Metschnikoff) Sorokin, 1883 (antes M. anisopliae) (Hypocreales: Clavicipitaceae) y Beauveria bassiana (Balsamo-Crivelli) Vuillemin, 1912 (Hypocreales: Clavicipitaceae) (Alatorre-Rosas 2007; Yehia et al. 2022). Sin embargo, se sabe que la capacidad patogénica de estos hongos disminuye cuando se mantienen por tiempos prolongados en el mismo medio de cultivo (González-García et al. 2001; Polovinko 2013; Keyhani 2018), por lo que es necesario contar con el medio de cultivo óptimo que contenga las sustancias nutritivas que requiere el hongo para su crecimiento y le confiera virulencia a las cepas durante la infección a insectos (González García et al. 2001; Cañedo & Ames 2004; Ishak et al. 2020; Rajula et al. 2021).
Los medios de cultivo de hongos entomopatógenos deben contener nitrógeno, carbono y vitaminas, para un desarrollo óptimo y reproducción, un pH de 6 a 6,3, así como antibióticos para evitar el crecimiento de bacterias saprofitas (Cañedo & Ames, 2004). De estos, los más comunes son PDA, Agar Agua (AA), Sabouraud Dextrosa Agar (SDA), Sabouraud Dextrosa Agar con extracto de levadura (SDAY) y Agar Melaza levadura (AML). Al respecto, se han llevado a cabo estudios para determinar el crecimiento radial de los hongos M. robertsii y B. bassiana bajo diferentes condiciones de crecimiento (García-Gutiérrez et al. 2020), y otros con la finalidad de inducir su patogenicidad al usar suplementos de integumento de algunos insectos diana (González García et al. 2001; Sharapova 2019; Sapna Bai et al. 2020), así como para conocer su potencial en la inducción de la actividad enzimática dinámica y caracterización bioquímica de B. bassiana (Peteira et al. 2011). Los hongos tienen diferentes atributos que determinan su virulencia frente a sus hospedantes, tales como la producción de enzimas hidrolíticas como proteasas, lipasas y quitinasas (Zibaee & Bandani, 2009; Batool et al. 2020). Este mecanismo enzimático puede lograr una alta mortalidad de insectos plaga ocasionada por los hongos, si a éstos se les provee el sustrato necesario para su desarrollo y se promueve la inducción de las enzimas involucradas en la patogenicidad (González García et al. 2001). Debido a esto, la virulencia de un hongo es considerada una característica importante en el control de las plagas.
El objetivo fue evaluar el crecimiento radial de cepas de B. bassiana y M. robertsii en medio suplementado con polvo de S. frugiperda y H. virescens y determinar la patogenicidad que M. robertsii induce sobre larvas de S. frugiperda.
Materiales y métodos
Producción del suplemento a base de los insectos Spodoptera frugiperda y Heliothis virescens
Obtención del suplemento de insectos
Se siguió el procedimiento descrito por García-Gutiérrez et al. (2020). Se usaron pupas de la generación F3 de la cría axénica; se secaron en horno (Riossa®) a 50 °C durante tres días, se molieron en un mortero manual de porcelana hasta obtener un polvo, el cual se llevó a peso constante. Se almacenó en frascos de vidrio con boca ancha con capacidad de 118 mL a temperatura ambiente hasta su utilización.
Análisis proximal del suplemento
Al polvo se le realizó un análisis proximal por los métodos respaldados por la Asociación de químicos analíticos oficiales (A.O.A.C., por sus siglas en inglés) (Ramos Elorduy et al. 2002), para conocer el contenido de humedad por diferencia de peso a 105 °C/4 h y determinación de la energía, mediante factores de conversión propuestos por Heras et al. (1998), las proteínas por el método de Kjeldahl (1883), grasas por el método de Soxhlet (1879), cenizas por diferencia de peso: calcinación 600 °C/5 h, fibra cruda por hidrólisis sucesiva: ácido/base) y extracto libre de nitrógeno (ELN) con la ecuación:
En la ecuación ELN es el % de extracto libre de nitrógeno, cen de ceniza, prot de proteína, gra de grasa y fib de fibra.
Evaluación del crecimiento radial de B. bassiana y M. robertsii en medios suplementados
Evaluación de la patogenicidad de M. robertsii inducido sobre S. frugiperda
Resultados
Composición del suplemento de Spodoptera frugiperda y Heliothis virescens
El análisis proximal realizado al integumento en polvo de los dos insectos se presentan en la tabla 1.
Crecimiento radial de M. robertsii y B. bassiana en medio PDA suplementado con H. virescens y S. frugiperda
El crecimiento radial de M. robertsii suplementado con S. frugiperda al 1% fue de 75,5 mm y con H. virescens de 74,2 mm, con diferencias estadísticas respecto al control (60 mm). El crecimiento de B. bassiana suplementado con H. virescens al 0,5% fue 55 mm y con S. frugiperda al 0,25%, 50 mm, con diferencias estadísticas con el control 33,25 mm (a = 0,05) (figura 1).
Análisis proximal del polvo de H. virescens y S. frugiperda
Extracto libre de nitrógeno
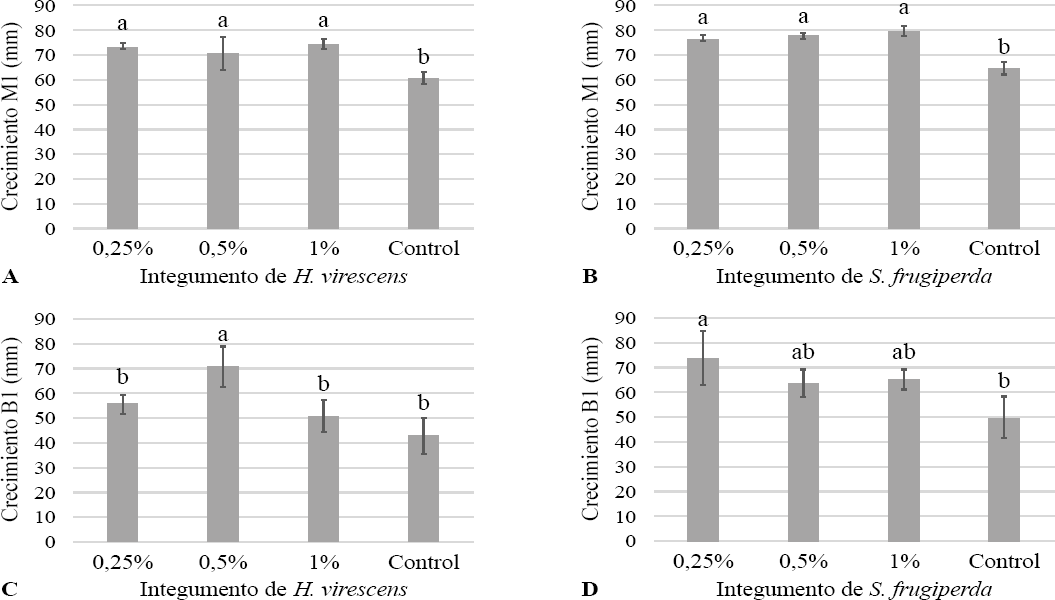
Crecimiento radial de los hongos en PDA: M. robertsii: A) Suplementado con H. virescens, B) Suplementado con S. frugiperda; B. bassiana, C) Suplementado con H. virescens, D) Suplementado con S. frugiperda.
En la figura 2 se puede observar el mayor halo de crecimiento de la cepa M1 suplementados con Hv y Sf al 1%, la colonia es de una coloración verde oliva característica de este hongo, y en la cepa B1 suplementada con Hv al 0,5 % y Sf al 0,25% aparece un halo de menor diámetro de color blanco típica en B. bassiana. En ambos casos la cepa en el medio control tuvo menor diámetro en mm, que los hongos crecidos en medios suplementados con polvo de pupas durante 15 días.

Crecimiento radial de M. robertsii (cepa M1) y B. bassiana (cepa B1) a los 15 días de desarrollo.
Patogenicidad de M. robertsii inducido sobre larvas de S. frugiperda
La viabilidad de las conidias de la cepa M1 de M. robertsii utilizada en este estudio fue superior al 90% de esporas germinadas a las 16 h.
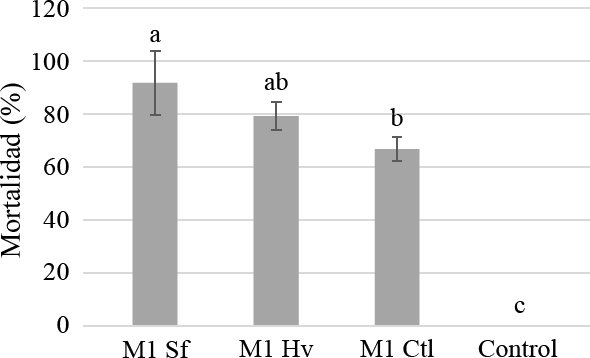
Mortalidad de larvas de S. frugiperda causada por la cepa M1 a las 168 h. Tratamientos: M1 Sf = Hongo desarrollado en medio con S. frugiperda, M1 Hv = hongo desarrollado en medio con H. virescens, M1 Ctl = hongo desarrollado en medio sin insecto, Control = agua y Tween 80 como control negativo.
Discusión
El análisis proximal del polvo indicó que el mayor nutrimento en S. frugiperda y H. virescens son las grasas, valores superiores a los de Rodríguez-Ortega et al. (2016) en pupas del gusano de seda Bombyx mori Linnaeus, 1758 (Lepidoptera: Bombycidae) (20,63 %). El contenido de ELN de H. virescens fue 10 veces mayor a la reportado en B. mori (3,92 %) por Rodríguez-Ortega et al. (2016) y similar a lo reportado por Ramos-Elorduy et al. (1998) en Heliothis zea (Boddie, 1850) (Lepidoptera: Noctuidae) con 21%. Con relación a las proteínas, los resultados fueron inferiores a los obtenidos por Rodríguez-Ortega et al. (2016) en B. mori (64,31%) y por Ramos Elorduy et al. (1998) en H. zea (41,98 %). Lo anterior es importante, al considerar que los hongos requieren fuente de carbono y de nitrógeno para su crecimiento y desarrollo, los cuales son aportados como suplemento al medio de cultivo PDA, además de la fuente de energía libre disponible para la realización de los procesos metabólicos de estos hongos.
El crecimiento radial de las cepas de M. robertsii y B. bassiana durante 15 días fue mayor en el medio suplementado con H. virescens y S. frugiperda, y estos fueron superiores a lo reportado por García-Gutiérrez et al. (2020) con los dos hongos (2,46 y 2,63 mm/día) respectivamente, inducido con cutícula de S. frugiperda, mientras que Vejar-Cota et al. (2017) reportaron crecimiento de 2,05-2,62 mm/d con B. bassiana en medio PDA y con M. robertsii 2,70-3,03 mm/d. Las diferencias en el crecimiento de estos hongos se deben a la adición de nutrientes del suplemento en las concentraciones aplicadas.
La patogenicidad de M. robertsii en medio suplementado con S. frugiperda alcanzó 91,6% de mortalidad de larvas. En otros estudios donde el hongo se aisló de cadáveres de este insecto, la mortalidad máxima fue 88% (Ullah et al. 2022) en larvas de S. friguperda y del 100% en huevos y larvas neonatas del mismo insecto con M. robertsii (Cruz-Avalos et al. 2019). Por otro lado, se reportó patogenicidad de B. bassiana con eficiencia del 96,6% (García-Gutiérrez et al. 2011). Otros estudios consignan patogenicidad de M. robertsii y B. bassiana del 33%-100% (Gutiérrez-Cárdenas et al. 2019).
Los resultados sugieren que M. robertsii alcanzó una mayor patogenicidad en larvas de S. frugiperda, debido a que el hongo se cultivó en medio suplementado con polvo del insecto diana. Lo anterior coincide con lo reportado por González-García et al. (2001) quienes observaron una mayor mortalidad de Hypothenemus hampei (Ferrari, 1867) (Coleoptera: Curculionidae) por acción de B. bassiana después de cultivarlo en medio con integumento del insecto hospedero. Se sugiere también que los componentes del polvo favorecieron la producción de enzimas que el hongo necesita para infectar al insecto, lo cual coincide con Gato-Cárdenas et al. (2017) quienes relacionan la rápida mortalidad con altos niveles de enzimas. En relación con la virulencia de M. robertsii, se sabe que está asociada a la actividad de enzimas extracelulares como quitinasa, lipasa y proteasa (Gebremariam et al. 2022), a su vez relacionada a los genes mad1, mad2 y gmact presentes en M. robertsii (Cruz-Avalos et al. 2019). De esta forma, la virulencia y efectividad de M. robertsii en el control de S. frugiperda es evidenciada, por lo que este hongo y B. bassiana pueden ser usados como alternativa a los insecticidas químicos tradicionales (Montecalvo et al. 2021).
Conclusiones
Los resultados demostraron que los medios de cultivo suplementados con polvo de pupas de los insectos S. frugiperda y H. virescens, inducen el crecimiento de los hongos entomopatógenos B. bassiana y M. robertsii. También se incrementó la patogenicidad de M robertsii sobre larvas de S. frugiperda. El uso del suplemento a base de estos insectos podría mejorar la producción masiva de hongos entomopatógenos en laboratorio.
Origen y financiación
Esta investigación se realizó en el laboratorio de Bioinsecticidas del Departamento de Biotecnología Agrícola del Centro Interdisciplinario de Investigación para el Desarrollo Integral Regional (CIIDIR) Unidad Sinaloa del Instituto Politécnico Nacional (IPN), El trabajo se derivó de la tesis de maestría de Adara Graciano Obeso y fue financiado por el proyecto: Estu-dio de efectividad y persistencia de formulaciones de hongos entomopatógenos para el control de plagas del tomate” Clave SIP: 20200535.
Contribución de los autores
Adara Graciano-Obeso fue responsable de la realización del trabajo experimental, procesamiento de datos e imágenes y redacción del artículo. Cipriano García-Gutiérrez se encargó de la dirección, diseño y supervisión del trabajo experimental, revisión de resultados y redacción del artículo, es además el autor de correspondencia. María Nancy Herrera-Moreno apoyó en el diseñó y supervisión del trabajo experimental, revisión de resultados y redacción del artículo. Hervey Rodríguez-González contribuyó con la realización de los análisis bromatológicos de las pupas de insectos estudiados. Juan Carlos Sainz Hernández participó en la supervisión del trabajo experimental, sugerencias y revisión del artículo. Gabriela Lizbeth Flores Zamora proporcionó apoyo técnico en el desarrollo del trabajo experimental.
Conflictos de interés
Los autores declaramos no tener conflictos de intereses.
Footnotes
Agradecimientos
Agradecimientos. Al Consejo Nacional de Ciencia y Tecnología CONACYT, México y al Programa BEIFI-IPN. Por las becas recibida en los estudios de maestría de la primera autora.