Abstract
Random Amplified Polimorphic DNA (RAPD) markers were used to examine the genetic variability among Beauveria bassiana isolates from several insect hosts, geographic origin, and different pathogenicity percentages on the coffee berry borer, Hypothenemus hampei (Ferrari). For this purpose the DNA was isolated from ten B. bassiana isolates, one from B. brongniartii and one from Paecilomyces lilacinus, the DNA was amplified randomly with 36 decamers. Amplification products were resolved in agarose gels and 445 reproducible bands ranging in size between 0.36-2.0 kb were scored. For the analysis, the similarity coeficient from Jaccard and the genetic distance from Nei &Li were calculated and a dendrogram was constructed using the UPGMA method. The dendrogram was divided in two principal groups, in the first group were placed 90% of B. bassiana isolates that exhibited certain correlation with the geographic origin. In contrast, there were no correlations between the clusters, the insect host and the coffee berry borer pathogenicity. The B. brongniartii isolate clusted together with B. bassiana, perhaps because this isolate is more closely related to the last species. In the second group it was found B. bassiana Bb 9023. That isolate is different from the other group of Beauveria spp. due to different genetic patterns. The P. lilacinus isolate was completely separated from the group of Beauveria spp. It was possible to recognize RAPD markers useful for the intraespecific differentiation of the entomopathogenic fungi B. bassiana.
Introducción
La broca, Hypothenemus hampei (Ferrari) (Coleoptera: Scolitydae), es considerada el insecto plaga de mayor importancia del café en Colombia y otros países productores del grano (Bustillo 1993). Con el fin de disminuir daños económicos y defender el sistema agroecológico se ha utilizado el control biológico de la plaga el cual se fundamenta principalmente en el uso de parasitoides de origen africano y hongos entomopatógenos. Cenicafé desarrolla en la actualidad un programa de investigación con hongos entomopatógenos dirigidos al control de la broca del café que comprende: el aislamiento, colección y caracterización de cepas; realización de pruebas de patogenicidad, selección y evaluación de métodos de producción, evaluación de los métodos de aplicación, compatibilidad con plaguicidas y seguridad para la fauna benéfica, con el fin de producir un bioinsecticida eficaz (Posada 1993).
En la micoteca de Entomología de Cenicafé existen 95 aislamientos de B. bassiana, de los cuales 67 han sido colectados en Colombia, 23 han sido obtenidos de diferentes colecciones internacionales y 5 son de procedencia desconocida. Con relación al rango de hospederos, el hongo se ha aislado de 32 especies de insectos, con un mayor número de aislamientos (39) procedentes de la broca del café (Posada y Vélez 1997).
La diferenciación de aislamientos por técnicas bioquímicas o morfológicas es afectada por condiciones medioambientales, que pueden llevar a producir resultados muy variables (St Leger et al. 1992b). El uso de técnicas moleculares como la amplificación aleatoria de ADN polimórfico (RAPD) permite detectar polimorfismos en el ADN, los cuales pueden ser usados como marcadores genéticos (Williams et al. 1990). Estos marcadores han sido especialmente empleados en la diferenciación de hongos que se reproducen asexualmente, se obtienen de manera rápida y no se requiere conocer una secuencia de ADN para su detección (McDonald 1997).
En estudios realizados por Rivera et al. (1997) se observó un alto grado de homogeneidad entre aislamientos de B. bassiana procedentes de Colombia y otros países y no se encontró una relación entre la agrupación genética, el tipo de hospedero y su localización geográfica. En otros estudios moleculares de B. bassiana utilizando RAPD, se han encontrado genotipos asociados a hospederos específicos (Maurer et al. 1997; Urtz y Rice 1997), sugiriéndose cierta selección natural dada por el tipo de hospedero.
Teniendo en cuenta que con la técnica RAPD se puede estimar el polimorfismo del ADN de varios microorganismos a nivel inter e intraespecífico y con la diversidad de aislamientos de B. bassiana existentes en la micoteca de Entomología, este trabajo tuvo como objetivo principal analizar la variabilidad genética de B. bassiana como herramienta para la selección de cepas potenciales para el control de la broca del café.
Materiales y Métodos
Obtención de micelio
Se seleccionaron 10 aislamientos de B. bassiana de la colección de la disciplina de Entomología del Centro Nacional de Investigaciones de Café (Cenicafé), teniendo en cuenta su diversidad con respecto al sitio geográfico, tipo de hospedero y porcentaje de patogenicidad sobre la broca del café. Como organismos de comparación se analizó un aislamiento de B. brongniartii y uno de Paecilomyces lilacinus, que de igual forma a B. bassiana, son utilizados como agentes biocontroladores de insectos plaga (Tabla 1). De cada uno de los aislamientos, sembrados en Agar Sabouraud, se obtuvo micelio en medio líquido GYM (medio glucosa-extracto de levadura) incubando en agitación orbital (150 r.p.m.) a 25 °C durante 6 días. El micelio se recuperó por filtración al vacío utilizando papel filtro (Whatman No 1), lavando dos veces el micelio filtrado con agua ultrafiltrada estéril. Este se liofilizó y almacenó a -20°C hasta la extracción de ADN.
Hospederos, origen geográfico y patogenicidad sobre la broca del café de aislamientos de B. bassiana, B. brongniartti y P. lilacinus
% Patogenicidad = Porcentaje de patogenicidad sobre Hypothenemus hampei (González, M.T. 1995. Informe Anual de Labores de Cenicafé. Chinchiná)
N.D. = No determinado
Extracción de ADN
Se utilizó una modificación del método de extracción de ADN con bromuro de cetil-trimetil-bromuro de amonio (CTAB), dado por Zolan y Pukkila (1986). Se pesaron entre 50 y 100 mg del micelio liofilizado y se homogenizó adicionando nitrógeno líquido hasta obtener micelio pulverizado. A éste se le agregaron 5 ml del buffer de extracción (700 mM NaCl; 50 mM Tris-HCl pH 8.0; 10mM EDTA; 2% (p/ v) CTAB; 1% mercaptoetanol). Después de incubar 1 hora a 60°C, se realizaron dos extracciones consecutivas con 5 ml de cloroformo isoamilalcohol (24:1). Después de centrifugar a 3.500 r.p.m. (15 min) se recuperó el sobrenadante, se adicionaron 0.54 V de isopropanol y se colectó el precipitado por centrifugación a 14.000 r.p.m. (15 min a 4°C). Este fue disuelto en 500 µl de buffer TE (10 mM Tris-HCl pH 8.0; 1 mM EDTA PH 8.0), se adicionaron 5 µl de ARNasa A (10 mg.ml−1) e incubó por 1 hora a 37°C. Después de la digestión del ARN se adicionaron 500 µl de cloroformo: isoamilalcohol (24:1) y se recuperó el sobrenadante después de centrifugar a 3.500 r.p.m. por 15 minutos. El ADN se precipitó con 2V de etanol absoluto, se colectó por centrifugación a 3.000 r.p.m. (2-3 min a 4°C) y se disolvió en 100 µl de buffer TE. Las extracciones se almacenaron a -20°C hasta su uso. Se realizaron, como mínimo, dos extracciones de ADN por aislamiento, que fueron utilizadas independientemente en las reacciones de amplificación (RAPD). Para determinar la pureza del ADN extraído se hizo por espectrofotometría un barrido entre A220-320 nm determinando la absorbancia a A260 nm con la que se halló la concentración de ADN y se calculó la relación A260/A280 para detectar la contaminación con proteínas (Sambrook et al. 1989). La integridad del ADN se analizó por medio de electroforesis en gel de agarosa al 0.8%, se coloreó con bromuro de etidio (0.5 µg.ml−1) y se observó con luz ultravioleta (Sambrook et al. 1989).
Iniciadores y condiciones de la amplificación
Se evaluaron 36 iniciadores aleatorios, de 10 bases de longitud (Gibco-BRL, Life Technologies) (Tabla 2). Las reacciones de amplificación se llevaron a cabo en 25 ml que contenían: 1.25 U Taq ADN polimerasa (Gibco-BRL); 200 mM de cada uno de los desoxiribonucleótidos (dCTP, dATP, DGTP, dTTP); 20 mM Tris-HCl pH 8.4; 50 mM KCI; 1.75 mM MgCl2; 0.6 mM iniciador; aproximadamente 50 ng de ADN y agua ultrafiltrada. La amplificación se realizó en un termociclador MJ-Research PTC-200 con el siguiente programa: una desnaturalización inicial a 94°C por 5 minutos; seguido por 40 ciclos de 1 minuto a 94°C, 1 minuto a 36°C, 2 minutos a 72°C; y un último ciclo de extensión a 72°C por 5 minutos. Se hizo un control negativo para las reacciones de amplificación, que contenía todos los componentes, excepto el ADN que fue sustituido por agua. Todas las reacciones de amplificación se realizaron mínimo dos veces utilizando como plantilla el ADN obtenido en dos extracciones independientes, con el objetivo de ver la reproducibilidad en los patrones de bandeo electroforético.
Secuencias de los iniciadores (5' → 3') utilizados en este estudio
Electroforesis
Los productos de la amplificación se analizaron por medio de electroforesis en gel de agarosa al 1.5% usando 1X del buffer Tris-Borato-EDTA (TBE) y fue corrida durante 2 horas a 60V. Los geles fueron teñidos con bromuro de etidio y visualizados con luz UV.
Análisis de datos
Con las fotografías de los geles de electroforesis se verificó la reproducibilidad de las bandas y sólo se tomaron en cuenta bandas reproducibles y de intensidad fuerte. El polimorfismo del ADN fue identificado cuando estuviera una banda presente en un aislamiento pero ausente en otro. Se elaboró una matriz de datos asignando el valor de 1 cuando estuviera la banda presente y 0 cuando estuviera ausente. Con esta matriz se calculó el coeficiente de similitud de Jaccard (Sij) expresado como: Sij = a / a+b+c. Donde Sij es la similitud entre 2 aislamientos, i y j; a es el número de bandas presentes en los dos aislamientos i y j; b es el número de bandas presentes en i y ausentes en j; y c es el número de bandas presentes en j y ausentes en i. Este coeficiente de similitud excluye bandas ausentes en dos aislamientos, ya que la mutua ausencia no puede ser atribuida a una causa común y por consiguiente a similitud. Con este coeficiente se calculó la distancia genética D con la siguiente ecuación: Dij = 1- Sij (Nei y Li 1979). Con base en la matriz de distancia genética se elaboró un dendrograma, usando el método de agrupamiento no ponderado para grupos pares UPGMA (Sneath y Sokal 1973). Los cálculos de coeficientes de similitud, distancia genética y dendrogramas fueron realizados con el programa Similit (SAS versión 6.12.)
Resultados y Discusión
Extracción de ADN
Se obtuvieron en promedio 866 µg de ADN.gr-¹ de micelio liofilizado de B. bassiana; el grado de pureza fue óptimo ya que la relación A260/A280 fue en promedio para todas las extracciones realizadas 2.05 (DE = 0.56), valor característico de ácidos nucleicos puros (Sambroock et al. 1989). En la electroforesis del ADN total se verificó la integridad del ADN como una banda de alto peso molecular (23 kilobases) con baja degradación. El análisis del ADN extraído permitió determinar la pureza de las extracciones realizadas e identificar muestras que requerían otra extracción.
Amplificación
En las reacciones de amplificación para Beauveria spp. con los 36 iniciadores evaluados se amplificaron 445 bandas con un peso molecular entre 369 y 2091 pares de bases, de las cuales 289 fueron polimórficas. Los polimorfismos observados con el análisis de RAPD pueden ser causados por varios eventos tales como la sustitución de pares de bases, inversión o deleción en los sitios de apareamiento del iniciador. El porcentaje de sitios polimórficos (65%) refleja de manera general la diversidad genotípica de los aislamientos analizados de Beauveria spp., destacándose el aislamiento B.b 9023 con patrones de bandeo electroforético muy diferentes al resto del grupo de Beauveria spp. (Figs 1-2. Carril 3). Este aislamiento fue una donación del Instituto Micológico Internacional (IMI) clasificado como B. bassiana y se comprobó microscópicamente que no estuviera contaminado con otro microorganismo. Adicionalmente se hicieron tres extracciones de ADN por separado, que sirvieron como ADN plantilla para las reacciones de amplificación. Independientemente de la reacción se observaron patrones reproducibles que se caracterizaron por ser notoriamente diferentes en comparación con los otros aislamientos de Beauveria spp.
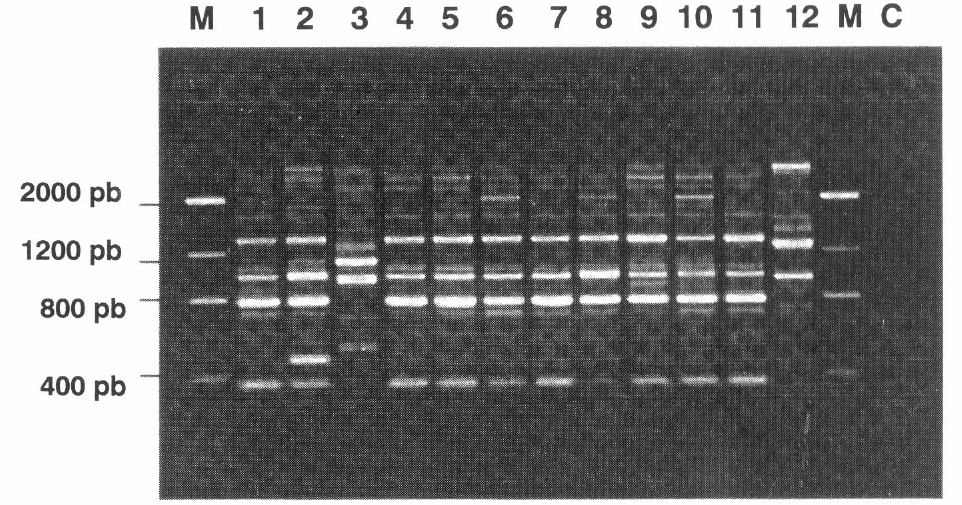
Electroforesis de la amplificación obtenida con el iniciador 55. Carril M. Marcador de peso molecular "low DNA mass ladder"; 1. B.b 9018; 2. B.b 9021; 3. B.b 9023; 4. B.b 9027; 5. B.b 9101; 6. B.b 9112; 7. B.b 9205; 8. B.b 9218; 9. B.b 9315; 10. B.b 9506; 11. B.br 9301; 12. P.1 9601; M. Marcador de peso molecular; C. Control negativo. (B.b = B. bassiana; B.br = B. brongniartii; P.l = P. lilacinus; pb = pares de bases).
Con algunos iniciadores se puede observar en general un patrón de bandeo electroforético muy similar entre los aislamientos de Beauveria spp. distinguiéndose algunas bandas polimórficas (Fig.1 Carril 2 y 9), con los iniciadores 55, 58 48, 42 y 40 se observó un patrón de bandeo muy similar. En contraste con los iniciadores 14, 23, 36, 50 y 57 se evidencian de mejor manera bandas polimórficas (Fig. 2). Se obtuvo reproducibilidad en las bandas más intensas, la mayoría de las bandas débiles no fueron reproducibles y otras se observaron sólo una vez al comparar el duplicado de la reacción de amplificación.
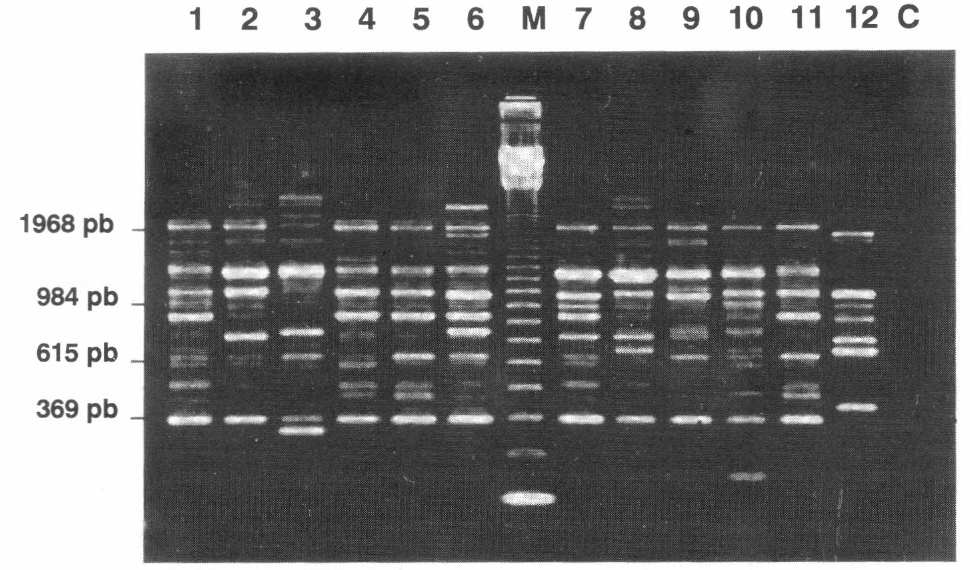
Electroforesis de la amplificación obtenida con el iniciador 50. Carril 1. B.b 9018; 2. B.b 9021; 3. B.b 9023; 4. B.b 9027; 5. B.b 9101; 6. B.b 9112; M. Marcador de peso molecular "123 bp ladder"; 7. B.b 9205; 8. B.b 9218; 9. B.b 9315; 10. B.b 9506; 11. B.br 9301; 12. P.l 9601; C. Control negativo.
En la figura 3 se presenta el dendrograma generado de la matriz de distancias con los 36 iniciadores evaluados, donde se agrupan los aislamientos de acuerdo con su relación genética y se describe el origen geográfico, tipo de hospedero y porcentaje de patogenicidad sobre la broca del café de cada uno de los aislamientos. Se puede observar un grupo principal donde están el 90% de los aislamientos de B. bassiana junto con el de B. brongniartii. Este aislamiento no se logró diferenciar de los de B. bassiana, resultado que se ha obtenido en otros trabajos (Glare e Inwood 1998), donde con la técnica RAPD se agruparon genéticamente estas dos especies. La diferenciación morfológica de estas dos especies ha sido materia de controversia, ya que comparando la forma de los conidios, B. brongniartii produce sólo elipsoidales o cilíndricos y B. bassiana produce globosos y elipsoidales (Mugnai et al. 1989). Aunque el objetivo de este trabajo no era identificar genéticamente especies, el aislamiento de B. brongniartii parece estar más relacionado con la especie B. bassiana. Sin embargo, con otras técnicas moleculares como el análisis de restricción de las regiones ITS se han encontrado claras diferencias entre estas dos especies, y posiblemente, el uso de otras técnicas moleculares diferentes de RAPD permita distinguirlas (Neuvéglise et al. 1994).
Al comparar la distribución de los grupos dentro del dendrograma se observa cierta asociación de los aislamientos con respecto a su origen geográfico, puesto que los aislamientos colombianos se condensaron en una misma rama (Fig. 3). Aunque allí mismo se encuentra un aislamiento de diferente localidad Bb 9027, se evidencia la persistencia de ciertos genotipos en regiones específicas; esta correlación se ha establecido en otros estudios de B. bassiana usando la técnica RAPD y perfiles isoenzimáticos (Glare e Inwood 1998; Poprawski et al. 1988). Los aislamientos colombianos tienen un porcentaje de divergencia genética del 23,6%; esta baja variación intraregional puede ser debida a la ausencia de la fase sexual, ya que la recombinación sexual es la principal fuente de variación intraespecífica en hongos. El origen de la variación genética en hongos Deuteromycetes no es clara y aunque existen registros de eventos de parasexualidad en condiciones de laboratorio en B. bassiana (Paccola-Meirelles y Azevedo 1991), ésta no ha sido demostrada en condiciones naturales y por tanto sus implicaciones en la variabilidad genética son por ahora desconocidas (St. Leger et al. 1992a).
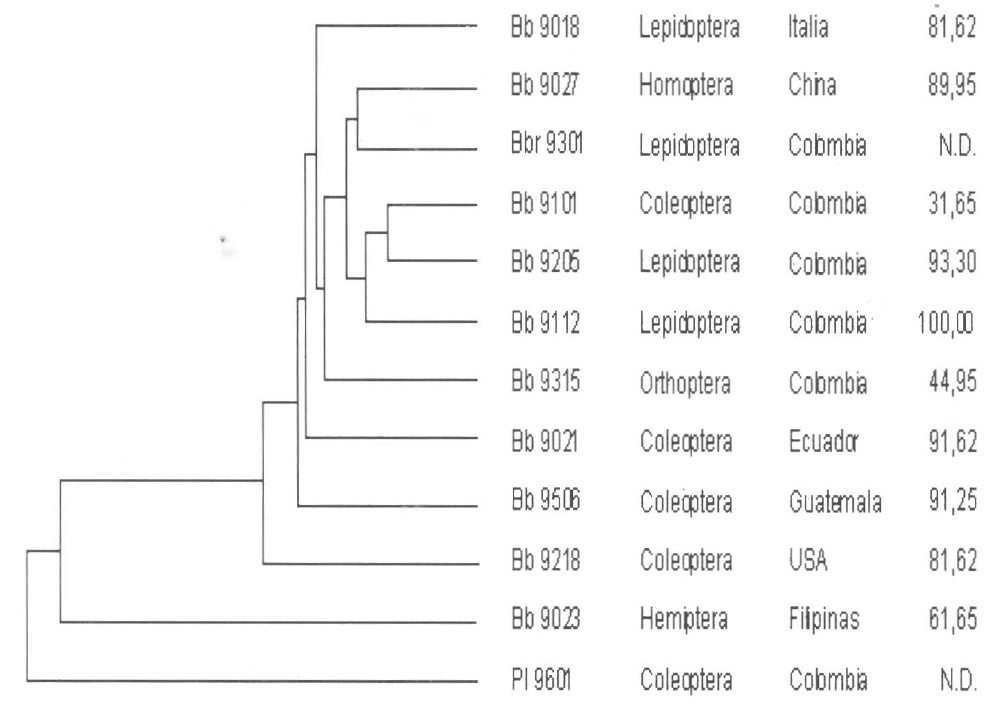
Dendrograma de los aislamientos evaluados y su relación con el tipo de hospedero, origen geográfico y porcentaje de patogenicidad sobre la broca del café.
Al comparar la agrupación genética de los aislamientos con el tipo de hospedero, no se encuentra una relación puesto que en un mismo grupo se reúnen aislamientos provenientes de diversos órdenes de insectos (Fig. 3); la falta de asociación ha sido explicada por el bajo grado de especialización de este hongo hacia un hospedero particular (Bidochka et al. 1994), aunque en otros estudios se han encontrado genotipos específicos a ciertos hospederos (Maurer et al. 1997; Urtz y Rice 1997). Igualmente, al comparar la agrupación genética de los aislamientos con el porcentaje de patogenicidad a la broca del café, se encuentran en un mismo grupo aislamientos con alta y baja patogenicidad. Esta asociación no se logró establecer posiblemente porque la virulencia y patogenicidad son características gobernadas por muchos genes, lo que hace difícil encontrar marcadores ligados a ellos.
Como reflejo de la variabilidad genotípica el aislamiento B.b 9023 se ubicó en una rama diferente al grupo principal (Fig. 3); dicha variabilidad podría atribuirse a su origen geográfico (Filipinas), pero es necesario evaluar un mayor número de aislamientos de esta procedencia para sustentar esta hipótesis. Igualmente el aislamiento de P. lilacinus se situó en una rama diferente del grupo de Beauveria spp.; demostrando la utilidad de la técnica RAPD para la diferenciación de estos dos géneros de hongos entomopatógenos.
Este estudio permitió identificar marcadores RAPD que mostraron polimorfismo genético entre los aislamientos de B. bassiana y con éstos se está analizando una población mayor de aislamientos con el objetivo de establecer relaciones entre el polimorfismo y otras características biológicas (porcentaje de germinación, producción enzimática, resistencia a la luz UV), importantes en la selección de cepas con potencial biológico para el control de la broca del café.
Conclusiones
La técnica de amplificación de ADN polimórfico al azar (RAPD) permitió evaluar la variabilidad genética de aislamientos de B. bassiana, estableciendo diferencias a partir de características estables (ADN) que no están influenciados por factores medioambientales.
El análisis de agrupamiento permitió establecer cierta relación genética con el origen geográfico del aislamiento pero no con el tipo de hospedero o el porcentaje de patogenicidad a la broca del café.
Se identificaron ciertos marcadores RAPD útiles en la diferenciación de B. bassiana que permitieron reconocer patrones de bandas polimórficas.
Footnotes
Agradecimientos
Esta investigación fue financiada por un convenio Colciencias-Federacafe. Agradecimientos al Centro Nacional de Investigaciones del Café especialmente a la Bacterióloga Patricia E. Vélez A., al Microbiólogo Armando Rivera Malo por su apoyo técnico y logístico y al Sr. Hernando García por su ayuda en el proceso de datos.
