Abstract
In an attempt to evaluate in the laboratory the effect of different times of exposure to the UV light at the sunlight simulator on the germination of conidia of Beauveria bassiana 191 650, oil and water suspensions of B. bassiana I91 650 were prepared. Germination tests carried out in Nutrient Gelatin showed protection of the standard mixture of oils to the conidia exposed 90 minutes to the simulator as compared to conidia in water suspension. No direct germination of conidia of B. bassiana I91 650 in oil and water suspensions, sprayed on coffee leaf discs and exposed 0 - 60 minutes to the simulator, was observed. However, B. bassiana 191 650 sprayed to coffee leaf discs in the standard mixture of oils showed viability after 60 minutes of exposure to the sunlight simulator, as evaluated by the unity forming colonies (UFC) in nutrient medium. The spraying of different formulations of B. bassiana 9002 to coffee berries in Colombian coffee plantations showed defined trends in some treatments. It was observed that the longer the exposure time to the sunlight radiation, the less viability of the propagules of this fungus. The variables temperature and relative humidity were relatively constant during the field study. Consequently, the variable global radiation played an important role in the response of the treatments.
Introducción
La importancia de los hongos entomopatógenos como reguladores naturales de poblaciones de insectos ha sido reconocida por muchos años (Gillespie y Moorhouse 1989). Factores tales como el aumento de la resistencia de los insectos a los insecticidas y los efectos adversos del uso generalizado de químicos en el control de plagas, han fomentado el uso de hongos entomopatógenos como sustitutos potenciales de los insecticidas químicos (Samsinakova et al. 1981).
Existen productos biológicos disponibles comercialmente para el control de insectos en países como Rusia, China y Brasil (Ferron 1978; Gillespie y Moorhouse 1989). Entre ellos, Beauveria bassiana (Bals.) Vuill. y Metarhizium anisopliae (Metsch.) Sorokin (Hyphomycetos) son los hongos más comúnmente usados en programas de control microbiano de insectos (Deacon 1983).
El rango de huéspedes de algunos géneros de hongos entomopatógenos es variable (Gillespie y Moorhouse 1989), y tienden a ser más comunes en áreas tropicales, en las cuales factores tales como la temperatura y la humedad relativa favorecen su crecimiento. Sin embargo, pueden encontrarse también en áreas templadas (Doberski y Tribe 1980).
B. bassiana y M. anisopliae tienen en forma individual un rango de huéspedes de más de 200 especies de insectos (Doberski 1981). Sin embargo, se consideran patógenos no especializados de insectos, cuya actividad puede localizarse en algunas especies en particular, cuando se presentan condiciones ambientales favorables (Doberski y Tribe 1980).
La infección causada en insectos por los hongos entomopatógenos ocurre en forma primaria a través de la cutícula. Por esta razón, está muy influenciada por las condiciones ambientales (Deacon 1983).
Factores de tipo abiótico como la luz solar, la temperatura, el agua o la humedad y las sustancias químicas determinan el éxito o fracaso de un agente de control biológico en el campo (Couch e Ignoffo 1981).
La radiación solar, especialmente la de tipo ultravioleta, desempeña un papel importante en la mortalidad de esporas de hongos (Rotem y Aust 1991). La vida media de los diferentes tipos de inóculo de hongos expuestos a la luz solar se estima en un tiempo aproximado de una hora para el hongo entomopatógeno más susceptible y de 96 horas para el más resistente. La luz solar puede inactivar a los hongos entomopatógenos en forma directa por medio de delecciones, uniones cruzadas, ruptura de bandas y formación de sitios lábiles en la molécula de DNA; y en forma indirecta debido a la formación de radicales altamente reactivos, los cuales a su vez inactivan a los hongos entomopatógenos, reduciendo su persistencia en el campo (Ignoffo 1992).
El uso de los hongos entomopatógenos B. bassiana y M. anisopliae como agentes de control microbiano ha tenido un éxito limitado, debido a dos factores fundamentales: la necesidad de selección y mantenimiento de aislamientos altamente virulentos para una plaga en particular y la importancia relevante del microambiente en el desarrollo de epizootias (Campbell et al. 1983).
El suelo constituye un ambiente favorable para el control de insectos con hongos entomopatógenos (Gardner y Storey 1985). Sin embargo, el control de plagas foliares con estos agentes biológicos ha mostrado eficiencia en forma esporádica (Gardner et al. 1977; Campbell et al. 1983). Lo anterior se explica por la mayor supervivencia del hongo en las condiciones de humedad del suelo, y la protección suministrada por el suelo a la acción directa de la luz ultravioleta sobre estos agentes biológicos (Gardner et al. 1977).
La capacidad que muestran las conidias de los hongos entomopatógenos para permanecer estables en el campo, es la más importante restricción para el uso efectivo de estos agentes en el control de plagas (Daoust y Pereira 1986).
Experiencias previas con algunas formulaciones de B. bassiana (Bb) en campos experimentales y comerciales de CENICAFE, han mostrado eficiencia en el control de la broca del café, Hypothenemus hampei (Ferrari) (Coleoptera: Scolytidae) (Bustillo y Castillo 1992).
Los principales objetivos de este estudio fueron: evaluar, en el laboratorio, el efecto de diferentes tiempos de exposición a la luz ultravioleta en un simulador de luz solar, sobre la germinación de conidias del aislamiento de B. bassiana Bb 191 650 suspendidas en agua y en aceite; evaluar la germinación de estas preparaciones asperjadas sobre discos de hojas de café y expuestas a la luz ultravioleta en el simulador de luz solar; y evaluar, en condiciones de campo, el efecto de la radiación solar global en la viabilidad de diferentes formulaciones del aislamiento del hongo Bb 9002.
Materiales y Métodos
El trabajo se llevó a cabo en dos etapas: La de laboratorio, la cual se realizó en el laboratorio de Patología de Insectos del Instituto Internacional de Control Biológico, IIBC, con sede en Silwood Park, Ascot, Inglaterra, y otra de campo, la cual se llevó a cabo en Chinchiná (Caldas), en un lote experimental de la Estación «Naranjal» del Centro Nacional de Investigaciones de Café, y en el laboratorio de Patología de Insectos de dicho Centro.
Como hipótesis de trabajo se estableció que a mayor tiempo de exposición de las conidias de B. bassiana a la luz ultravioleta, en el equipo simulador de luz solar en condiciones de laboratorio y a la radiación solar global en condiciones de campo, mayor reducción de la viabilidad de las conidias del hongo.
Etapa de Laboratorio
El aislamiento probado fue el Bb 191 650, aislado de frutos de café afectados por H. hampei, en la zona de Ansermanuevo (Valle). Este aislamiento fue suministrado por el Dr. Prior del IIBC, y fue cultivado en Agar Molischs (Speare 1920).
En prueba de germinación directa se evaluó el efecto de la radiación de tipo ultravioleta sobre la germinación de las conidias del hongo, expuestas al simulador de luz solar por períodos de 15 a 120 minutos. Con tal propósito se prepararon suspensiones del hongo en la mezcla de aceites y agua. El proceso usado para formular el hongo en la mezcla de aceites, ondina (aceite de nuez, Sigma) y queroseno sin olor (aceite mineral liviano, Shellsol) (50/50 v/v), fue llevado a cabo según la metodología de formulación del hongo M. anisopliae para el control de la langosta en Africa, según el programa desarrollado en el IIBC (Lomer y Prior 1992). Se tomaron dos aislamientos esporulados del hongo, cultivado en agar Molischs, y se adicionó la mezcla de aceites a cada uno de ellos, hasta cubrir totalmente el área de crecimiento del hongo. Posteriormente se hizo una remoción de conidias de cada uno de los tubos, mediante agitación con espátula. El total de conidias en la suspensión fue transferido a erlenmeyers, se realizó agitación en el equipo de ultrasonido durante 2 minutos y filtración a través de un filtro de 53 um, con el fin de obtener conidias en forma pura. La concentración final de conidias en la suspensión fue de 5,76 x 108 conidias/ml.
Para la suspensión de Bb 191 650 en agua, se utilizó la misma metodología empleada para la suspensión en aceite. La concentración final de conidias en la suspensión fue de 4,05 x 108 conidias/ml.
Alícuotas provenientes de las suspensiones de Bb 191 650, en aceite y agua, se depositaron en el centro de cajas de petri con Gelatina Nutritiva. Posteriormente se dispersó el inóculo alrededor de las cajas, y éstas se llevaron a incubación durante 24 horas a 25°C, con un fotoperíodo de 12 horas, con el fin de promover la germinación de las conidias. Después de la incubación, se tomaron cuadrados de 1 cmβ del medio contenido en cada caja de petri, y se llevaron a láminas de vidrio, se adicionó una gota de azul de lactofenol y posteriormente una laminilla. La germinación se evaluó con la ayuda de un microscopio marca Nikon (40x), contando las conidias germinadas y no germinadas por campo, para un total de 25 campos evaluados por caja, después de estar expuestas las suspensiones de conidias al simulador de luz solar. Se incluyeron controles para cada prueba, mediante la utilización de cajas de petri con Gelatina Nutritiva, en las cuales se hizo depósito de la suspensión de conidias, pero no se hizo exposición de éstas a la luz ultravioleta en el simulador de luz solar.
La germinación de las suspensiones de Bb 191 650 en aceite y agua, también fue evaluada mediante la aspersión del hongo (2 ml de la suspensión) sobre discos de hojas de café colocados en cajas de petri estériles (5 discos de 1,1 cm de diámetro). Para la aspersión se utilizó la torre de Potter, a 5 l/pulgβ. Posteriormente los discos de hojas de café se expusieron al equipo simulador con tiempos de exposición de 15 a 60 minutos para la preparación en aceite, y de 30 y 60 minutos para la preparación en agua. Una vez realizada la exposición y con el fin de liberar las conidias adheridas a las hojas, los discos de hojas se lavaron en agua o aceite, dependiendo del medio usado para preparar las suspensiones, y se realizaron pruebas de germinación, tomando alícuotas de las suspensiones en agua (0,1 ml de la suspensión), y en aceite (cantidad tomada con la espátula), según la metodología descrita previamente.
Posteriormente se evaluó la viabilidad de los propágulos del hongo (o unidades formadoras de colonia - UFC) mediante el método de siembra en superficie, tomando 0,1 ml de una dilución de la suspensión original, para inocular cajas de petri de 8,7 cm de diámetro con Agar Papa Dextrosa más 0,5% de Acido Láctico (Solución al 20% en agua). El inóculo se diseminó mediante el empleo de un rastrillo, y se llevaron las cajas a incubación a 25°C con el fin de proporcionar condiciones adecuadas para el desarrollo de propágulos del hongo. De esta manera se evaluó la respuesta de viabilidad de los propágulos del hongo (conidias) a través del tiempo de exposición a la radiación ultravioleta en el equipo simulador, teniendo en cuenta la concentración inicial de UFC en cada una de las preparaciones. Como testigo se emplearon discos de hojas de café asperjados con las diferentes preparaciones y sin ser expuestos al simulador.
El equipo simulador de luz solar utilizado consta de una lámpara de Xenón de alta presión, la cual produce un rayo uniforme que simula el espectro solar terrestre. La lámpara emite esencialmente rayos de luz ultravioleta tipo A, tipo B y menos de un 20% del espectro visible e infrarojo. La configuración usada en el equipo produjo luz ultravioleta en el rango de 280 a 400 nm, bloqueando la luz ultravioleta de tipo C.
Para el análisis estadístico, por caja se determinó el porcentaje de germinación, por medio de un estimador de razón (Número de conidias germinadas/Número total de conidias), y con dicha estimación se obtuvo el promedio de 25 repeticiones, para el porcentaje medio de germinación por lectura.
Trabajo de Campo
Para evaluar la viabilidad del hongo Bb 9002 (Vélez y Benavides 1990) en campo, se selecccionó el medio selectivo Sabouraud dextrosa agar (SDA) más 0,06 g de oxicloruro de cobre por 150 ml de medio y 4 microlitros del producto comercial «Alto 100 SL», fungicida cyproconazol, por 150 ml de medio (Rivera y López 1992). Así mismo, se utilizó el equipo de aspersión «Calimax Leo Cafetera» con boquilla HC-3 y un flujo aproximado de 200 ml/minuto, a 40 l/pulgβ, y se realizó una aspersión dirigida a la parte superior e inferior de la rama seleccionada.
Los tratamientos se asignaron aleatoriamente a las 14 parcelas seleccionadas. Los tratamientos o formulaciones se evaluaron en dos condiciones de luminosidad: plena exposición solar y 53% de luminosidad (condición adoptada mediante el uso de la tela «Polisombra», la cual fue instalada en siete parcelas sorteadas aleatoriamente, con sombra). Los tratamientos fueron:
Bb 9002 en talco.
Bb 9002 en talco más «Carrier»
Bb 9002 en bentonita.
Bb 9002 en bentonita más «Carrier».
Bb 9002 en aceite de soya «Correo».
Bb 9002, formulación Danesa.
Suspensión en agua de Bb 9002 (preparada con glicerol al 10% en agua destilada).
Para el registro de las variables exógenas, como radiación global, temperatura y humedad relativa, se instaló una estación meteorológica automática en el lote experimental. En los tratamientos evaluados bajo condiciones de 53% de luminosidad, la tela "sombra" cubría la parte superior y lateral de la parcela, permitiendo una buena circulación de aire dentro de ella e impidiendo el desarrollo de condiciones microclimáticas. Las formulaciones de Bb 9002 en talco y bentonita se prepararon en el laboratorio de Patología de Insectos de CENICAFE, según metodología de Samsinakova et al. (1981) y la formulación en aceite, según la metodología usada en el IIBC para formular el hongo M. anisopliae, en la mezcla estándar de aceites. La concentración final de cada formulación fué de 1x105 conidias/ml. Se realizaron pruebas de control de calidad a las formulaciones, con valores de germinación superiores al 85% para las formulaciones en talco y bentonita, y 44,5% para la formulación Danesa. Así mismo, se confirmó la pureza de las formulaciones mediante el cultivo de ellas en el medio SDA.
Una vez asperjada la formulación a cada tratamiento, en las cuatro ramas de cada árbol (5 árboles por parcela de 50 árboles, por tratamiento), se registró el tiempo 0, y empezaron a tomarse 5 frutos verdes al azar de la parte superior de las 4 ramas seleccionadas. Dicho proceso se realizó con pinzas, para evitar el contacto de la piel con el inóculo depositado sobre el fruto, y, de esta forma, obviar los procesos de remoción manual de conidias y contaminación.
Los frutos recolectados se almacenaron en cámaras humedas, las cuales se depositaron en neveras de icopor, para su transporte al laboratorio. El mismo proceso de muestreo se utilizó a los 30, 60, 90, 120 y 1.440 minutos después de la aplicación del tratamiento a cada uno de los árboles. Se registró el tiempo exacto de cada muestreo, con el propósito de hacer el registro de las variables, según los datos suministrados por la estación automática y los termohigrógrafos ubicados dentro de la parcela experimental.
Para la prueba de germinación por conteo de UFC, los cinco frutos seleccionados por árbol y depositados en las cámaras húmedas (420 en total) se llevaron al laboratorio y se transfirieron a recipientes plásticos estériles, con 5 ml de glicerol al 10% en agua destilada. Posteriormente se almacenaron a -5°C durante 48 horas, y luego a -25°C hasta el momento de hacer el conteo de propágulos del hongo en los frutos. Se realizaron diluciones sucesivas de la suspensión inicial (-1 a -4), y se hizo siembra en la superficie del medio selectivo, según la metodología descrita previamente.
Para el análisis estadístico de los tratamientos de campo se tomaron los valores promedios (UFC/ml) para cada tiempo (0 a 1.440 minutos), y se evaluó la viabilidad de las preparaciones conidiales de 1 hongo (UFC/ml), a través del tiempo, mediante un modelo de regresión lineal simple.
Resultados y Discusión
Etapa de Laboratorio
La estimación del porcentaje de germinación de conidias en los medios aceite y agua, para la lectura a los 90 minutos, fue de 38% y 11%, respectivamente. Los coeficientes de variación para el porcentaje de germinación, a través de las lecturas, fluctuaron entre 0,7 y 6,3% (Tabla 1). El límite para el error de estimación estuvo entre 1,5 y 4,7%, con una probabilidad mayor o igual al 75%. Con la estimación del porcentaje de germinación del hongo B. bassiana se evaluó la tendencia de dicho parámetro a través del tiempo, y se corroboró que a mayor tiempo de exposición de las conidias del hongo a la radiación UV en el simulador de luz solar, menor porcentaje de germinación, tanto en aceite como en agua.
Al comparar, mediante la prueba de «t», los promedios de germinación en agua y aceite, para la lectura realizada a los 90 minutos, se encontraron diferencias significativas al 5%, a favor del medio con aceite, el cual mostró niveles de germinación mayores (Tabla 1). Esto evidencia el efecto protector del aceite a las conidias expuestas por un período de 90 minutos a la radiación de tipo ultravioleta.
Con relación a los tiempos evaluados, en el intervalo de 15 a 75 minutos se registraron porcentajes de germinación menores, estadísticamente, para el aceite. La respuesta de germinación en tiempos inferiores a 90 minutos para los medios agua y aceite, puede explicarse como un mecanismo de adaptación inicial del hongo al efecto de la radiación ultravioleta, de modo que se observa retardo en el proceso de germinación del hongo a las 24 horas de evaluación de esta variable. Es probable que la respuesta a las 48 horas de evaluación muestre porcentajes mayores de germinación, tal como se ha registrado para el hongo M. anisopliae (Zimmermann 1982). De otra parte, las conidias suspendidas en aceite están expuestas a condiciones de oxígeno un poco limitantes, y teniendo en cuenta que se trata de un organismo que sólo puede expresarse en condiciones óptimas de aerobiosis, la conidia suspendida en aceite y sometida al efecto de la luz UV podría requerir un tiempo mayor a las 24 horas para desarrollar completamente su proceso germinativo, y sólo hasta los 90 minutos de exposición al efecto de la luz UV logra desarrollar un proceso germinativo superior al observado en agua.
Los resultados obtenidos fueron similares a aquellos registrados para otros hongos entomopatógenos expuestos a la luz solar, en formulaciones en aceite y agua. Se ha observado muerte de conidias y retraso en la germinación de conidias viables para M. anisopliae. Asi mismo se ha observado una reducción de la germinación de conidias en formulaciones en aceite, después de la exposición de éstas al simulador de luz solar, a longitudes de onda entre 280 y 320 nm (Lomer y Prior 1992).
La respuesta observada en este estudio se muestra promisoria en la selección de aislamientos de B. bassiana a formular, para aplicaciones en el campo. Esto, debido a que la germinación mostró valores mayores del 38% a los 90 minutos, para la suspensión en aceite, y 11% a los 90 minutos para la suspensión en agua, mientras que Lomer y Prior (1992) registraron una pérdida completa de la germinación de conidias de hongos entomopatógenos suspendidas en agua, después de una hora de exposición al espectro UV de la luz. Los resultados obtenidos en esta etapa del trabajo confirmaron el efecto letal de la luz UV sobre la germinación de conidias del aislamiento Bb 191 650, en suspensiones en aceite y agua. Sin embargo, se plantea un mecanismo protector del aceite, lo que puede reducir el efecto directo de la luz UV sobre las conidias.
Con relación a las pruebas de germinación directa en discos de hojas de café, no se observó germinación de conidias de Bb 191 650 en suspensiones en aceite y en agua, aun a las 24 y 48 horas de realizada la prueba. Tampoco se observó germinación en los controles no expuestos a la luz UV en el simulador. Esta respuesta puede atribuírse a la presencia de compuestos fenólicos con actividades fungitóxicas, liberados por las hojas de café jóvenes sometidas a daño mecánico (Rodríguez et al. 1975).
Con relación a la prueba de germinación por conteo de UFC, de las diferentes preparaciones del hongo, se observó respuesta para la formulación del hongo en aceite (Tabla 2), lo que demuestra la presencia de compuestos de tipo fungistático que actuan sobre la germinación directa del hongo. Sin embargo, las suspensiones en agua del Bb 191 650 no mostraron viabilidad despúes de 30 y 60 minutos de exposición a la luz UV en el simulador (Tabla 2), lo que confirma de nuevo el efecto protector del aceite a las conidias sometidas a la radiación UV.
Estimación del porcentaje de germinación de conidias de B. bassiana 191 650 en dos medios, después de exposición a diferentes tiempos de luz ultravioleta..
Porcentaje medio de germinación CV: Coeficiente de variación tc: 53,79
Prueba de viabilidad de suspensiones de B. bassiana 191 650 en agua y en aceite, asperjadas sobre discos de hojas de café
Etapa de campo
En el lote experimental se asume la presencia de un inóculo natural del hongo B. bassiana, debido al registro de éste atacando a la broca y a otros insectos hospedantes en el área.
Con relación al análisis descriptivo de los tratamientos, la variación observada fue alta, aún con valores transformados. Esto es debido al número reducido de unidades experimentales y a la metodología de manejo de las unidades de observación en el campo (frutos de café). Con el propósito de minimizar variaciones en el método de laboratorio para la recuperación de propágulos del hongo, sólo se seleccionó la información obtenida de la dilución 10−1, y de esta forma se observaron las tendencias de cada uno de los tratamientos.
Los tratamientos de B. bassiana en suspensión en glicerol al 10% en agua destilada (53% de luminosidad), Bb en talco (plena exposición solar), Bb en bentonita (53% de luminosidad), Bb en talco más «Carrier» (53% de luminosidad) y Bb en aceite de soya «Correo» (plena exposición solar) mostraron una tendencia lineal definida a los 60, 90, 90, 120 y 120 minutos, respectivamente, de la variable UFC a través del tiempo. La evaluación de los coeficientes de correlación fue significativa al 10%, según la prueba de «t» (Tabla 3).
El comportamiento observado en tiempos posteriores a aquellos en los cuales se registraron tendencias lineales definidas (120 minutos y 1.440 minutos) (Fig. 1 y 2), puede explicarse por la capacidad de supervivencia del hongo en el inerte de la formulación, como respuesta al efecto de la radiación solar global, y a la posible expresión del inóculo del hongo presente en forma natural.
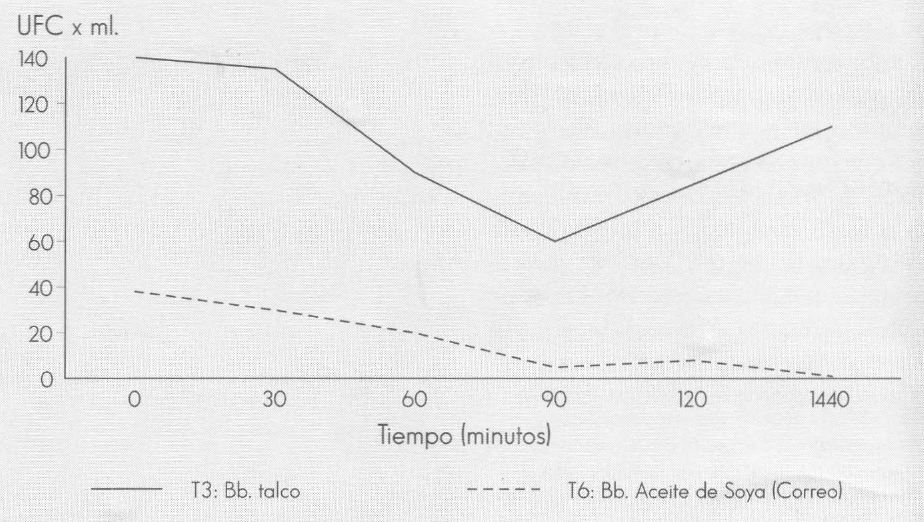
Viabilidad de B. bassiana 069 a plena exposición solar
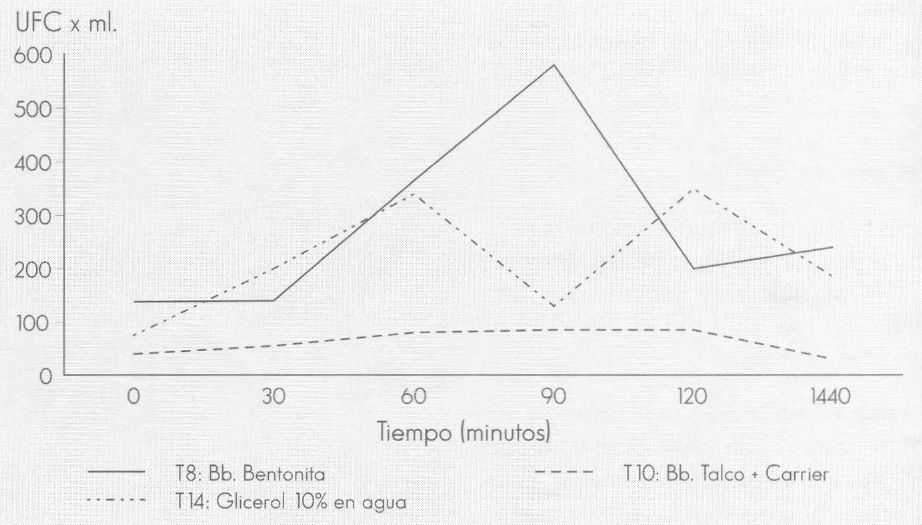
Viabilidad de B. bassiana 069 a la sombra (53% de luminosidad)
Los tratamientos Bb en talco (plena exposición solar) y Bb en aceite de soya «Correo» (plena exposición solar) mostraron tendencias lineales negativas, lo que implica que a mayor tiempo de exposición a la radiación solar menor viabilidad de los propágulos del hongo (Tabla 3, Fig. 1). No se observó ninguna protección por parte del aceite a la conidia del hongo, tal como era de esperarse teniendo en cuenta la respuesta obtenida en la etapa de laboratorio, para la formulación de Bb 191 650 en aceite de ondina y queroseno. Es posible que factores tales como la naturaleza del aislamiento de B. basiana, el tipo de aceite usado para formular el hongo, el manejo de las unidades de observación en el campo (frutos de café) y la tecnología de aspersión de la formulación en aceite a los frutos de café, hayan influenciado la respuesta de este tratamiento. Los tratamientos Bb en suspensión en glicerol al 10% en agua destilada (53% de luminosidad), Bb en bentonita (53% de luminosidad) y Bb en talco más «Carrier» (53% de luminosidad) mostraron tendencias lineales positivas hasta los 60,90 y 120 minutos, respectivamente, como respuesta al tiempo de exposición a la radiación solar global. A su vez, el número de propágulos en los diferentes tiempos de exposición para cada uno de estos tratamientos, muestra una relación lineal con la radiación acumulada, según estadístico de prueba de «t», para la significancia del coeficiente de correlación lineal, evaluado al 5% (Tabla 4, Fig. 2). Esta respuesta puede atribuirse a los niveles de radiación global registrados para estos tratamientos durante el estudio. Dichos valores fluctuaron entre 196,14 y 2.834,71 Wh/m2 (tiempos de 30 minutos a 1.440 minutos) para la condición sombra, y entre 385,00 y 5.456,86 Wh/mβ (tiempos de 30 minutos a 1.440 minutos) para la condición sol (Fig. 3 y 4).
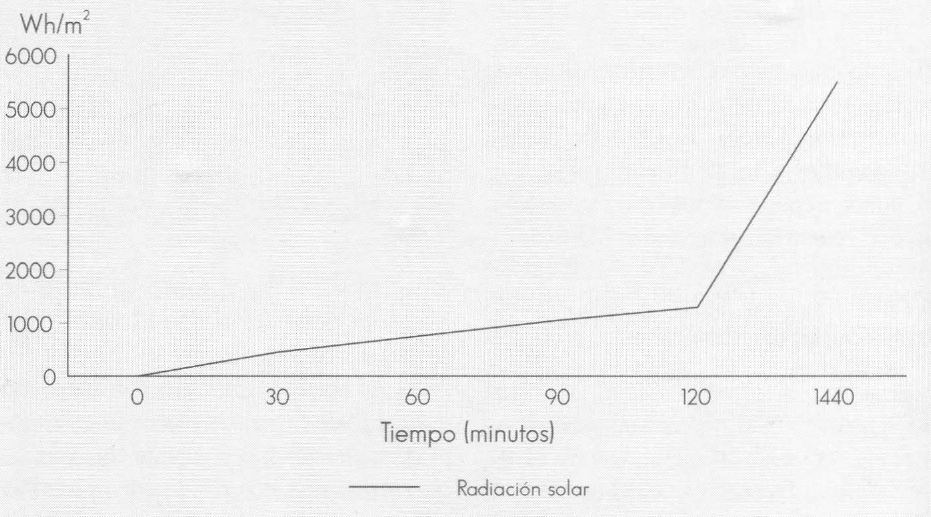
Variable radiación solar global a plena exposición solar
Variable radiación solar global a 53% de luminosidad
El aumento en la viabilidad de los propágulos a través del tiempo pudo además estar relacionado con la pérdida de propágulos asperjados a los frutos durante los primeros tiempos de evaluación. Lo anterior se aplica a los propágulos presentes en frutos tomados entre 0 y 30 minutos, debido a preparaciones húmedas, en las cuales el proceso de selección y depósito de frutos en la cámara húmeda pudo haber contribuído a la pérdida de propágulos del hongo. Una vez seco el inóculo aplicado a los frutos (tiempos de evaluación 60, 90, 120 minutos y 1.440 minutos), los propágulos adheridos al fruto se expresaron en el medio selectivo.
Las variables exógenas temperatura y humedad relativa fueron constantes a través del tiempo, para ambas condiciones evaluadas (plena exposición solar y 53% de luminosidad) (Fig. 5 y 6). Consecuentemente, aun cuando se presentaron problemas con la recuperación de las UFC durante los primeros tiempos de evaluación (0 a 30 minutos), e incluso en tiempos posteriores, para el caso de las formulaciones en aceite, la radiación solar desempeñó un papel decisivo en la respuesta de los tratamientos.
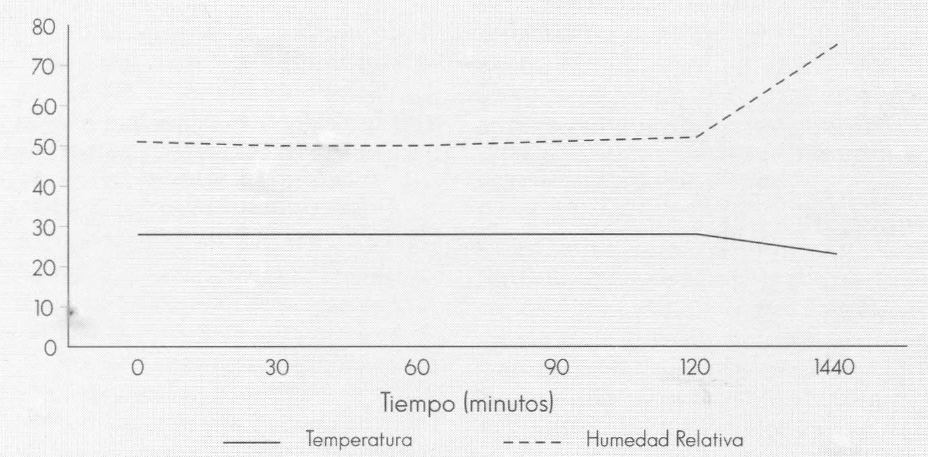
Variables temperatura y humedad relativa a plena exposición solar
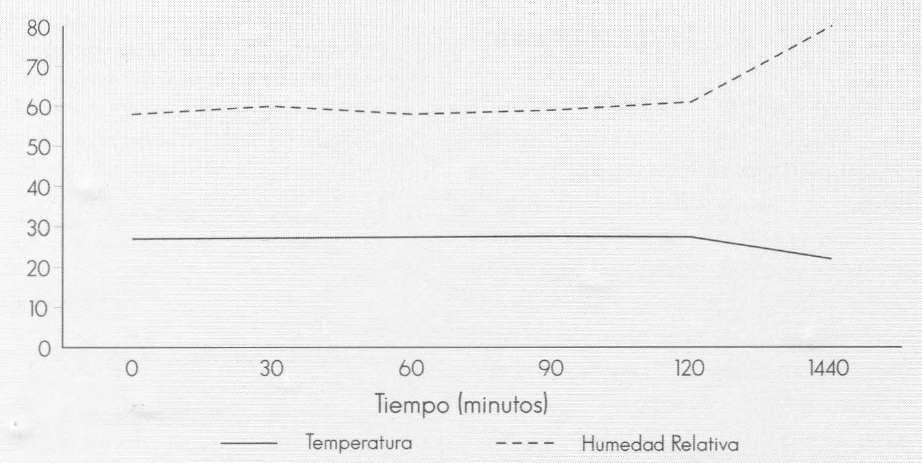
Variables temperatura y humedad relativa a 53% de luminosidad
El efecto del adherente «Carrier», medido por el aumento en la persistencia de la preparación, no fue consistente en las condiciones de sol y sombra.
La tecnología de aspersión usada en este trabajo incluyó volúmenes considerables de plaguicida biológico. Por tanto, el inóculo inicial asperjado a los frutos de café, mediante esta tecnología, pudo haberse perdido. La aplicación con gotas controladas a ultrabajo volumen ha mostrado ser un método más eficiente de aplicación de plaguicidas que los métodos convencionales de atomización. Esta tecnología de aplicación a ultrabajo volumen desarrollada para el control de la langosta con formulaciones en aceite de los hongos Metarhizium y Beauveria, ha mostrado eficiencia en el control de esta plaga, debido a que no ocurre una evaporación rápida de las pequeñas gotas (Prior et al. 1988; Abraham et al. 1991; Lomer y Prior 1992)
El uso de diferentes formulaciones del hongo B. bassiana se muestra promisorio en el control de la broca del café, H. hampei, en condiciones climáticas colombianas, y esto lo confirma la supervivencia de los propágulos del hongo en el estudio bajo condiciones de sombra.
Respuesta de los tratamientos a diferentes tiempos de exposición a la radiación solar global.
a Significativo al 10%
1 = Tasa de unidades formadoras de colonias/minuto.
2 = Coeficiente de correlación.
3 = Estadístico de prueba «t» para la significación de r.
4 = Grados de libertad para la evaluación del estadístico de prueba.
Relación entre la radiación acumulada y el número de propágulos (UFC/ml) del hongo B. bassiana 9002 en diferentes formulaciones
(1) = Tiempo (min)
(2) = UFC/ml
* = Significativo al 5%
r = Coeficiente de correlación
tc = t estimado
