Abstract
Place in therapy of olmesartan
Olmesartan has been de-reimbursed in France since January 2017 following a negative evaluation of its benefit/risk profile compared with other sartans. However, olmesartan is one of the antihypertensive blockbusters in Italy in terms of usage and expenditure. This article illustrates the pathway leading to a critical appraisal issued by the Lazio Regional Committee for Medicines with the aim of promoting the rational use of olmesartan and its place in therapy. Moreover, this short communication offers potential scenarios to combine the use of evidence-based information about a widely prescribed antihypertensive drug with cost considerations related to the entire class of sartans.
Keywords
Il farmaco olmesartan è un principio attivo della classe dei sartani, utilizzato per il trattamento dell'ipertensione arteriosa, e dal 2 gennaio 2017 non è più rimborsato in Francia (1). L'Autorità nazionale francese per la Salute (HAS) ha infatti stabilito che i farmaci a base di olmesartan (in monoterapia o in combinazione con idroclorotiazide o amlodipina) hanno un'efficacia dimostrata solo in termini di riduzione della pressione sanguigna (esito surrogato) ma, a differenza di altri sartani, non su esiti clinici robusti quali morbilità (riduzione di eventi cardiovascolari quali infarto miocardico e ictus) e mortalità. Inoltre, in confronto con altri sartani, olmesartan presenta un aumento del rischio specifico, seppur raro, di patologie enteriche. Sulla base di tali dati la stessa HAS dichiara che prescrivere olmesartan al posto di un altro sartano può rappresentare oltre che un rischio una mancata opportunità terapeutica per il paziente iperteso.
La decisione dell'Agenzia francese, come prevedibile, non è stata ben accolta dalle aziende interessate (Daiichi Sankyo e Menarini) e ha determinato una serie di contenziosi legali risolti molti mesi dopo (a giugno 2016) di fronte al Consiglio di Stato francese che ha però confermato la posizione dell'HAS (2, 3).
Nonostante anche nel nostro Paese si tratti di un farmaco molto ben conosciuto e prescritto, la notizia è passata pressoché inosservata. Infatti, cercando su Google le pagine in italiano contenenti le parole chiave “olmesartan” e “Francia” o “rimborsabilità” dal 1° aprile 2015 al 15 febbraio 2017 non si ritrova alcun riferimento specifico a tale avvenimento.
La decisione ha comunque sollecitato alcune rivalutazioni a livello locale. Ad esempio, nell'ambito delle attività rivolte all'aggiornamento del prontuario regionale del Lazio, la Commissione Regionale del Farmaco (CoReFa) ha deciso di rivalutare i medicinali contenenti olmesartan per favorirne l'uso appropriato e un'analisi critica delle evidenze disponibili attraverso l'adozione di un metodo di lavoro condiviso. Si è quindi proceduto a un approfondimento che ha visto l'analisi dei consumi a livello regionale e nazionale e una rilettura dei dati di efficacia e sicurezza fino ad oggi pubblicati.
A fronte di ciò, in Italia il rapporto Osmed del 2015 fotografa una situazione che mette l'olmesartan tra i blockbuster dei farmaci cardiovascolari (4). Infatti, il trend temporale dei consumi è in continua ascesa: olmesartan (monoterapia) passa dalle 3,6 DDD/1000 ab. die nel 2007 a 7,7 DDD/1000 ab. die nel 2015, con un aumento dei consumi del 5,8% rispetto al 2014; anche l'associazione olmesartan/idroclorotiazide registra un ampio consumo passando da 0,7 DDD/1000 ab. die nel 2008 a 6,9 nel 2015, con un aumento del 4,8% rispetto al 2014. Tra tutte le possibilità prescrittive del principio attivo, il “campione” è stato l'associazione di olmesartan/amlodipina che con 3,6 DDD/1000 ab. die nel 2015 registra un aumento dei consumi del 31,6% rispetto al 2014. In realtà, questo fenomeno era atteso e, infatti, se si sfoglia il rapporto del 2013 dell'azienda Daiichi Sankyo, è riportato chiaramente che le strategie sul mercato europeo prevedevano uno spostamento dalle monoterapie alle associazioni fisse (5). Negli stessi documenti l'azienda dichiara che accelererà il passaggio (switch) alle associazioni fisse in quanto “also have extended market life and revenue opportunity”.
Per quanto riguarda i principi attivi appartenenti alla stessa categoria dei sartani i consumi di valsartan, irbesartan, telmisartan (monoterapia o in associazione al diuretico) sono tutti stabili o in diminuzione, in qualche caso di oltre tre punti percentuali rispetto al 2014. I motivi di tale fenomeno possono essere spiegati da diverse ragioni. Tra queste il fatto che nel 2015 l'olmesartan era ancora sotto brevetto (in scadenza nel 2017), mentre tutti gli altri sartani (irbesartan, valsartan, losartan, telmisartan, candesartan) erano a brevetto scaduto.
Se ragioniamo in termini di spesa, olmesartan è tra i primi trenta principi attivi per spesa da parte del SSN (convenzionata di classe A) in Italia (4). Secondo i dati OsMed, l'olmesartan (monoterapia o in associazione al diuretico) nel 2015 è stato associato a 273 milioni di euro di spesa convenzionata SSN (il 2,5% della spesa totale di classe A). Si stima inoltre che l'associazione olmesartan/amlodipina abbia comportato in Italia ulteriori 72 milioni di euro di spesa nel 2015 da parte del SSN (0,65% della spesa).
Il rapporto Osmed 2015 ci offre anche la possibilità di confrontare la spesa dell'olmesartan nei principali Paesi europei (4). In Italia l'olmesartan si classifica come secondo principio attivo mentre esso è al 33° e 62° posto in Francia e Germania e addirittura al 229° nel Regno Unito. Da notare che, oltre all'Italia, l'olmesartan è ai primi posti come spesa (sia pubblica che privata) anche in Grecia, Portogallo e Spagna, che non sono proprio tra i Paesi europei con elevato PIL/pro capite!
Nella rivalutazione del profilo beneficio/rischio di olmesartan è stata posta particolare attenzione agli aspetti di sicurezza riguardanti gravi eventi cardiovascolari e gastrointestinali. Per gli eventi cardiovascolari ci si è basati su valutazioni già disponibili (6, 7). In particolare sono stati esaminati quattro studi osservazionali comparativi dove gli utilizzatori incidenti di olmesartan venivano confrontati con altri sartani su esiti clinici robusti quali infarto e morte (Tab. I). In tutti questi studi (8–11) viene evidenziato un rischio più elevato di morte o infarto associato a olmesartan in alcuni sottogruppi di pazienti, specialmente quelli diabetici o trattati con alte dosi (40 mg).
Descrizione degli studi osservazionali comparativi di olmesartan vs altri sartani/ACE inibitori sul rischio di mortalità e di eventi avversi cardiovascolari
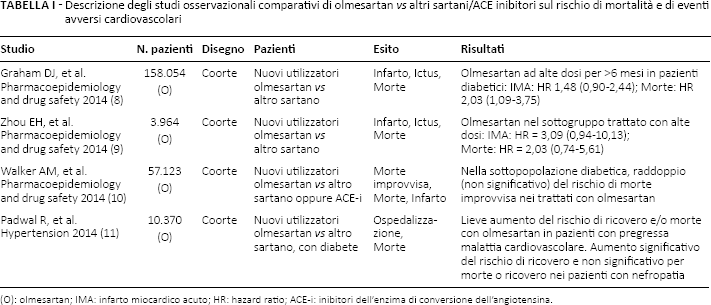
(O): olmesartan; IMA: infarto miocardico acuto; HR: hazard ratio; ACE-i: inibitori dell'enzima di conversione dell'angiotensina.
Per quanto riguarda gli eventi avversi gastrointestinali, il gruppo di lavoro si è basato sulle valutazioni già condotte dall'Agenzia statunitense FDA e dall'Agenzia francese HAS. In particolare, sulla base di segnalazioni spontanee, sono state evidenziate gravi enteropatie con olmesartan, confermate, in alcuni casi, anche dalla biopsia intestinale o dal dechallenge positivo (12–14). Tali reazioni non erano mai state rilevate con altri sartani. Inoltre, a ottobre 2016 è stato pubblicato uno studio osservazionale francese condotto su 4,5 milioni di pazienti con l'obiettivo di valutare il rischio di ospedalizzazione per malassorbimento intestinale e morbo celiaco associati a olmesartan o altri sartani rispetto agli ACE inibitori (15). Tale studio ha evidenziato un rischio di ospedalizzazione per malassorbimento intestinale (RR 2,49; IC 95% 1,73-3,57) e di ospedalizzazioni per morbo celiaco (RR 4,49; IC 95% 2,77-6,96) associato a olmesartan. Nel caso degli utilizzatori di altri sartani non viene osservato alcun rischio per entrambi gli eventi.
Analizzando anche i consumi nel Lazio (Tab. II) si osserva che la spesa (Classe A convenzionata) per la classe dei sartani (in monoterapia o in associazione) nel corso del 2015 ha superato i 70 milioni di euro con una stima analoga per il 2016. Nella stessa regione, l'olmesartan pur costituendo il 47% della spesa per sartani, rappresenta solo il 23% delle unità posologiche dell'intera classe. Il costo per utilizzatore di tutta la classe dei sartani usati in monoterapia è di circa 113 euro/anno e un costo per DDD di 0,30 euro; i costi sono simili per l'associazione sartano/idroclorotiazide (116 euro-paziente/anno e 0,43 euro per DDD), mentre l'associazione sartano/Ca-antagonista ha un costo per utilizzatore quasi doppio (225,96 euro/anno) e un costo per DDD triplo (0,93 euro). Se si analizza in dettaglio la spesa per la classe dei sartani nel Lazio, emerge che l'olmesartan (in monoterapia) ha un costo per DDD di 0,84 euro rispetto agli altri sartani disponibili in commercio la cui DDD ha un costo che varia tra 0,16 e 0,31 euro. Analogamente, l'associazione olmesartan/diuretico costa 0,85 euro per DDD, rispetto a 0,31-0,39 euro per DDD delle altre associazioni sartano/diuretico disponibili.
Descrizione dell'uso dei sartani nella regione Lazio (2015)
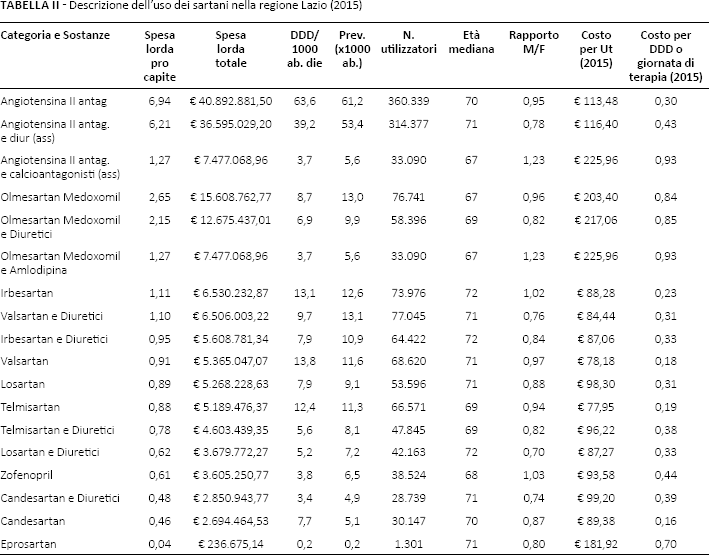
Quando si considerano i dosaggi utilizzati, emerge anche che nella stessa realtà regionale circa il 25% degli utilizzatori assume olmesartan (da solo o in associazione) ad alto dosaggio (40 mg) e un quarto di essi risultano anche in trattamento concomitante con antidiabetici.
La rivalutazione del profilo beneficio/rischio di olmesartan e l'analisi dei consumi regionali è stata inclusa nel documento di indirizzo per l'uso appropriato di olmesartan della CoReFa, che ha concordato sulla necessità di porre in atto iniziative volte a evitare l'uso di olmesartan ad alte dosi e/o nei pazienti con diabete (16).
In conclusione, gli elementi riguardanti il profilo di sicurezza di olmesartan andrebbero considerati attentamente dai prescrittori, anche considerando che nei pazienti per cui è indicato il farmaco, sono disponibili molteplici e valide alternative terapeutiche (anche all'interno della stessa classe dei sartani) che, tra l'altro, sono anche più vantaggiose da un punto di vista economico e contribuiscono a garantire la sostenibilità dei SSR.
Si poteva/potrebbe fare di più per il governo dei sartani? Probabilmente sì. Ad esempio dopo le pubblicazioni dei dati sui rischi più elevati di eventi cardiovascolari e gastrointestinali sarebbero auspicabili iniziative centrali volte alla rinegoziazione del prezzo dei farmaci a base di olmesartan. Anche a livello regionale, sarebbe forse possibile prospettare una maggiore analisi critica che tenga conto di tutti i principi attivi di questa categoria omogenea, discutendo i dati sopra riportati insieme agli specialisti e tenendo conto di opzioni terapeutiche con i migliori dati di efficacia e sicurezza. Ancora, si può agire sull'offerta promuovendo maggiormente la prescrizione dei sartani a brevetto scaduto (da soli o in associazione). Quando emergono condizioni che consigliano lo spostamento di una così ampia popolazione da un farmaco a un altro, per quanto all'interno della stessa categoria omogenea, occorre adottare alcune cautele. Infatti, la possibilità per i pazienti che sono in trattamento con olmesartan di passare a un altro sartano è stata valutata attentamente dalla stessa Autorità francese HAS prevedendo raccomandazioni specifiche al riguardo e una comunicazione mirata al paziente e al prescrittore (1). Ragioni e modi del cambio di terapia sono in questo caso spiegate dettagliatamente prevedendo fino a 6 alternative terapeutiche (di cui 5 prive di brevetto). In fondo, se in Francia è previsto che i pazienti cambino terapia (da olmesartan ad altro sartano o altro anti-ipertensivo) perché non possiamo farlo anche in Italia?
Footnotes
Financial support: The authors are public employees of the regional health authority. No financial support was received for this submission.
Conflict of interest: The authors declare that they have no conflict of interest.
