Abstract
Economic evaluation of lenalidomide (Revlimid®) for the treatment of mielodysplastic syndrome with 5q deletion at low/intermediate-1 risk
Background
Lenalidomide is an effective treatment for patients with lower risk myelodysplastic syndrome (MDS) del5q. It reduces disease-related transfusion requirements, inhibits the malignant clone and causes a delay in tumor growth. There are also benefits in terms of quality of life and use of other health care resources.
Objective
To perform an economic evaluation of lenalidomide for transfusion-dependent patients with Low/Intermediate-1-risk MDS del 5q from the perspective of the public health care sector in Mexico.
Material and methods
We developed a cost-effectiveness analysis using a Markov model of 5 stages: MDS transfusion-dependence, MDS transfusion-independence, complications from transfusion, acute myeloid leukemia, and death. The analyzed period was 5 years. Discount rate of 5% after year 1 was applied. Efficacy was elicited from a phase III clinical trial, MDS-004, which shows lenalidomide benefit in patients achieving transfusion-independence. There were also benefits with lenalidomide related to extended overall survival and decreased risk of acute myeloid leukemia. Unitary cost are from public price list of IMSS, and resources use was calculated from a Delphi panel methodology with clinical hematologists. A multivariate sensitivity analysis using a Monte Carlo technique was performed.
Results
Over a 5-year period, each patient on lenalidomide avoided 487 days of transfusion, on average. The incremental cost per life-year without transfusion dependence is USD$14,072 (Exchange Rate = 1USD = 17.55 MXN). According to the sensitivity analysis the model is robust. If all expected patients are treated, their cost would be wUSD$19.7 million, which represents 0.18% of the total budget in the public health sector.
Conclusions
Lenalidomide provides important clinical benefits in the treatment of patients with lower risk myelodysplastic syndromes with del5q, with a limited economic impact and with a cost per life living without blood transfusions is within 3 times of the Mexican GDP (Gross Domestic Product).
Keywords
Introducción
Los Síndromes Mielodisplásicos (SMD), comprenden un grupo heterogéneo de entidades nosológicas de origen clonal, caracterizados por diferentes grados de desajustes en la capacidad de proliferación y diferenciación de la célula progenitora hematopoyética, que se expresa con citopenias progresivas, alteraciones cualitativas en las 3 series hematopoyéticas y riesgo de transformación a leucemia mieloide aguda. En el pasado el SMD fue llamado pre-leucemia o leucemia quiescente. Los SMDs estuvieron anteriormente clasificados como una enfermedad de bajo potencial maligno, ahora que se conoce más de la enfermedad, se le considera una forma de cáncer (1, 2).
Se estima que la incidencia de SMD es de 4-12 casos por 100 mil individuos/año; la incidencia se incrementa significativamente con la edad avanzada donde puede llegar hasta los 30 a 60 casos × 100 mil individuos mayores de 70 años de edad. La aparición en la edad pediátrica y en el adulto joven es poco frecuente (1, 3).
Existen 2 tipos de SMD, el primario que es de etiología generalmente desconocida y el secundario que corresponde al 20% de los MDS, este último tipo se asocia al tratamiento previo con esquemas de quimioterapia que contienen agentes alquilantes, epipodofilotoxinas y antraciclinas. Otros factores causales relacionados son el contacto con productos químicos tales como los derivados del benceno; plaguicidas y la exposición a radiaciones ionizantes.
En México la información epidemiológica de ésta enfermedad es escasa debido a la carencia de estudios en ésta área, existe, sin embargo, el Registro Mexicano de Enfermedades Hematológicas (REMEDEH), el cual agrupa sedes hospitalarias del centro del país con mayor afluencia de enfermos con SMD, y en cual reportó 329 casos de pacientes adultos con SMD (4).
Las variedades de SMD están basadas en la clasificación publicada por la Organización Mundial de la Salud en el año 2008 (Tab. I).
Clasificación Síndromes Mielodisplásicos. WHO (2008)
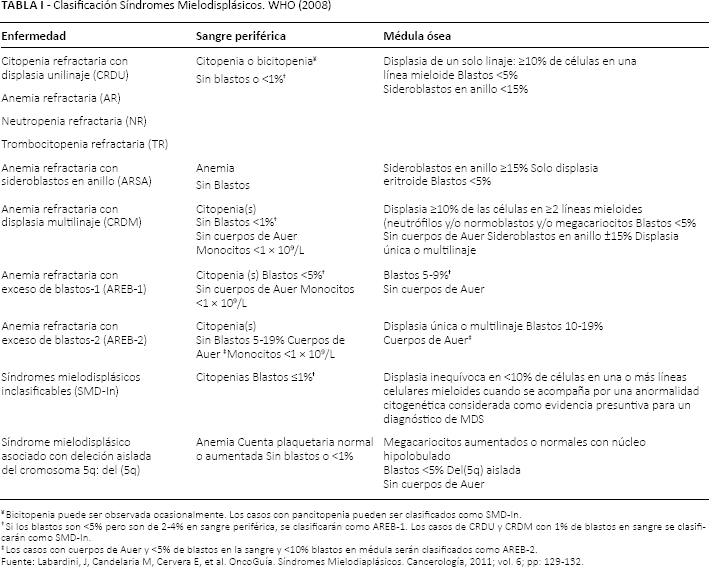
Fuente: Labardini, J, Candelaria M, Cervera E, et al. OncoGuía. Síndromes Mielodiaplásicos. Cancerología, 2011; vol. 6; pp: 129-132.
Bicitopenia puede ser observada ocasionalmente. Los casos con pancitopenia pueden ser clasificados como SMD-In.
Si los blastos son <5% pero son de 2-4% en sangre periférica, se clasificarán como AREB-1. Los casos de CRDU y CRDM con 1% de blastos en sangre se clasificarán como SMD-In.
Los casos con cuerpos de Auer y <5% de blastos en la sangre y <10% blastos en médula serán clasificados como AREB-2.
El diagnóstico puede sospecharse clínicamente en pacientes con anemia crónica o infecciones repetitivas, o como ocurre en la mayoría de las ocasiones, puede ser un hallazgo fortuito en un estudio de citometría hemática de rutina. Dentro de las causas más comunes de citopenias y las cuales deben descartarse en todo paciente con sospecha de SMD son: ingesta de medicamentos, infecciones virales (hepatitis, parvovirus B19, VIH, VEB), deficiencias de hematínicos (B12, hierro y ácido fólico), y en casos especiales la hemoglobinuria paroxística nocturna. En todos los casos el diagnóstico se fundamenta en la observación de cambios displásicos en las células hematopoyéticas en el aspirado de médula ósea. A fin de estadificar al enfermo y con esto elegir el tratamiento, debe realizarse estudio de cariotipo, tinciones para hierro (búsqueda de sideroblastos en anillo) en médula ósea, niveles séricos de eritropoyetina y en casos específicos citometría de flujo y prueba de FISH (síndrome 5q-) (2).
El tratamiento tiene como objetivo el control de los síntomas derivados de las citopenias, mejorar la calidad de vida del paciente minimizando los efectos adversos de los fármacos y aumentar la supervivencia global. Tradicionalmente el tratamiento se basa en la terapia de soporte, como transfusiones, aplicación de eritropoyetina (EPO) exógena, factores estimulantes de colonias de granulocitos e incluso esquemas de quimioterapia. Éste panorama ha tenido un cambio con la aprobación de nuevos fármacos surgidos en los últimos años, entre los cuales se cuentan los fármacos anti-angiógenicos, antitumorales e inmunomoduladores como la lenalidomida. El beneficio terapéutico obtenido con la lenalidomida en estos pacientes incluye un alto índice de respuestas citogenéticas (77%) e incluso remisiones completas (45%) (5, 6). La lenalidomida actúa en blancos moleculares específicos del microambiente medular mediante la inhibición de factores angiogénicos y proapoptóticos como el factor de crecimiento del endotelio vascular y el factor de necrosis tumoral alfa. Este fármaco también ejerce un efecto inmunomodulador, por lo que contribuye a la restauración de la inmunidad de los SMD con mejoría funcional de los linfocitos T. Cabe destacar que en las guías de tratamiento de la NCCN (National Comprehensive Cancer Network) contempla el uso de lenalidomida en pacientes con SMD de riesgo bajo o intermedio-1 con citopenias clínicamente significativas y anemia sintomática, que hayan recibido tratamiento de soporte y en aquellos con deleción en el brazo largo del cromosoma 5 asociado o no a otras anomalías citogenéticas (7). La evidencia creciente de la eficacia de lenalidomida en pacientes con SMD, especialmente en aquellos con el síndrome 5q-, sitúa al fármaco como una opción terapéutica estándar.
El objetivo del presente estudio es realizar una evaluación económica completa del tipo de costo-efectividad de lenalidomida (Revlimid®), para el tratamiento de pacientes con anemia dependientes de transfusiones debido a síndromes mielodisplásicos de riesgo bajo o intermedio 1 asociados a una anomalía por deleción 5q (del 5q) con o sin anomalías citogenéticas adicionales en comparación con las alternativas disponibles. Todo lo anterior desde la perspectiva de las instituciones públicas del sector salud en México.
Material y Método
Descripción del modelo
Se realizó una evaluación económica completa de tipo costo-efectividad, para lo cual se construyó un modelo de tipo Markov con 5 estados de salud. El esquema con lenalidomida utilizado, consta de ingesta del fármaco durante 21 días seguidos de 7 días de descanso, es decir ciclos de 28 días (Fig. 1) en donde los pacientes dependientes de transfusiones pueden transitar hacia el estado de independencia transfusional por el efecto de lenalidomida, y en el caso de aquellos que se encuentren con solo terapia de soporte, podrán también ser independientes de transfusiones, pero en una menor proporción. En los estados de independencia y dependencia transfusional los pacientes pueden progresar a leucemia mieloide aguda con mortalidad elevada. Por otro lado, el modelo también refleja la probabilidad de presentar complicaciones por dependencia transfusional a mediano y largo plazo como falla cardiaca e infecciones (8). Es conocido que estas complicaciones impactan directamente en la supervivencia global del enfermo, el modelo refleja que todo aquel paciente quien presente alguna de estas complicaciones, tendrá dos opciones, o continuar en ese estado o la muerte. Cabe agregar que desde cualquier estado de salud se puede transitar al estado absorbente “Muerte”.
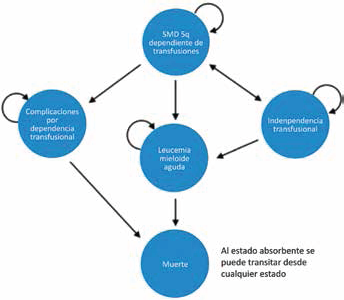
Modelo de Markov.
Alternativas a Comparar
Actualmente en México no existe ningún medicamento en el cuadro básico de medicamentos con la misma indicación de lenalidomida para el tratamiento del SMD del 5q, debido a esto se decidió tomar las recomendaciones de la Guía de Práctica Clínica para el Diagnóstico y Tratamiento del Síndrome Mielodisplásico del Centro Nacional de Excelencia Tecnológica en Salud (CENETEC) en México, con base a sus recomendaciones utilizo a el “mejor tratamiento de soporte” como alternativa comparadora, la cual consiste en transfusión de concentrados eritrocitarios y de plaquetas, eritropoyetina y factores estimulantes de colonias de granulocitos (9). Se recomienda el uso de quelantes de hierro en pacientes que han recibido más de 20-30 concentrados eritrocitarios. Se debe considerar la quelación diaria con deferoxamina subcutánea o deferasirox oral, particularmente en riesgo bajo o intermedio-1 y para potenciales receptores de trasplante. La eritropoyetina se utiliza para incrementar los niveles de hemoglobina y limitar la dependencia de transfusiones. El uso de filgrastim no está recomendado para profilaxis rutinaria de infección y solo debe considerar su uso en pacientes con infecciones recurrentes o asociado al uso de eritropoyetina. Aun cuando se conocen los componentes de la terapia de soporte en estos pacientes, la frecuencia y uso de estos recursos es variable dependiendo del especialista médico, los recursos con los que cuente, así como las características biológicas y clínicas del paciente. Por lo anterior, para incluir este comparador en el presente estudio, fue necesario consultar a un panel de expertos, mediante la metodología Delphi.
Perspectiva de análisis
La perspectiva del presente estudio es la de las instituciones públicas del Sistema Nacional de Salud.
Parámetros clínicos del modelo
En México al no contar con datos clínicos específicos ni del comportamiento de lenalidomida y ni del tratamiento de soporte se decidió utilizar para la matriz de transición los valores de los parámetros clínicos que fueron utilizados en el modelo de una evaluación económica previa que se desarrolló para la evaluación económica de lenalidomida por parte del National Institute for Clinical Excellence (NICE, por sus siglas en inglés) en el Reino Unido, siendo este hecho una limitación de nuestro estudio. En los Anexos 1A-1G (Ver el material adicional disponible en linea www.grhta.com) se puede revisar el detalle específico de cómo fueron construidas cada una de las matrices de transición, a partir de los datos abajo mencionados (Ver Tab. II). Las tasas de respuesta, tanto para lenalidomida como para el “mejor tratamiento de soporte” están ya expresadas a 28 días. El riesgo de complicaciones por dependencia transfusional (acumulado a 5 años) fue extraído del artículo de Malcovati et al, (8) donde el autor muestra la relación entre anemia grave y enfermedad cardiaca en pacientes dependientes de transfusiones, la cual se muestra enseguida.
Parámetros clínicos del modelo de decisión
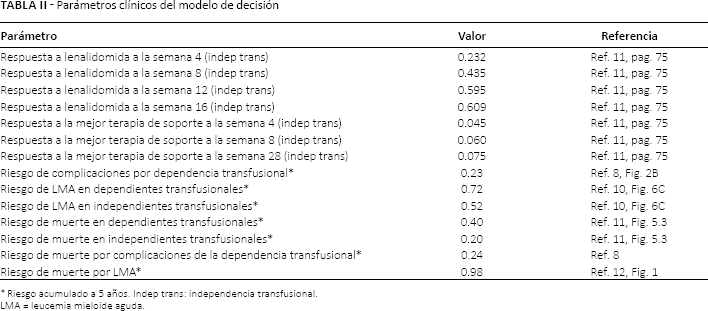
LMA = leucemia mieloide aguda.
Riesgo acumulado a 5 años. Indep trans: independencia transfusional.
Los riesgos acumulados a 5 años de desarrollar LMA, en ambos grupos de pacientes (dependientes e independientes transfusionales), fueron tomados del artículo de Fenaux et al, (10) que muestra el tiempo a la progresión mediante curvas de Kaplan-meier. El riesgo de muerte en pacientes con SMD (dependientes e independientes transfusionales) fue extraído del reporte técnico elaborado por Riemsma et al, (11) donde los autores estimaron la mortalidad mediante una distribución Weibull. Finalmente, el riesgo de muerte (acumulado a 5 años) en pacientes con LMA fue extraído del artículo de Wahlin et al, (12). Con base en la práctica clínica y lo observado en el ensayo clínico de lenalidomida, (10) los pacientes bajo tratamiento con lenalidomida pueden requerir reducciones de dosis e interrupciones del medicamento por eventos adversos (Ver Tab. III).
Interrupciones del tratamiento con lenalidomida

Fuente: Elaboración Propia con base en lo reportado por Riemsma R, Al M, Blommestein H, et al. Lenalidomide for the treatment of myelodysplastic syndromes associated with dele on 5q cyto- gene c abnormality: a Single Technology Appraisal. York: Kleijnen Systema c Reviews Ltd, 2013.
Segunda.
En nuestro estudio las interrupciones del tratamiento con lenalidomida se modelaron en el 2do y 3er ciclo respectivamente, donde los ajustes de dosis se ciñeron a la información del producto (Ver Tab. IV). Aquellos pacientes que sí responden a la terapia con lenalidomida después de 3 ciclos de tratamiento, continuarán recibiendo el medicamento a lo largo de todo el horizonte temporal del modelo (5 años). Los eventos adversos más comunes con lenalidomida (neutropenia y trombocitopenia), ameritan las interrupciones que se describieron previamente y los ajustes de dosis de lenalidomida descritos en la información para prescribir del producto.(Ver Tab. V).
Interrupciones del tratamiento con lenalidomida consideradas en el modelo de Markov
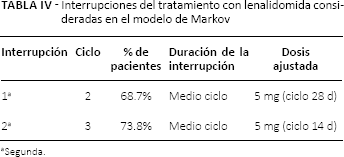
Segunda.
Reducción de dosis por eventos adversos
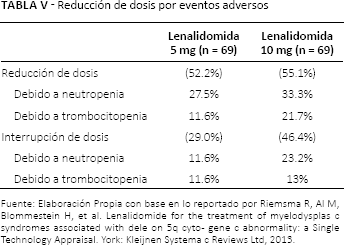
Fuente: Elaboración Propia con base en lo reportado por Riemsma R, Al M, Blommestein H, et al. Lenalidomide for the treatment of myelodysplas c syndromes associated with dele on 5q cyto- gene c abnormality: a Single Technology Appraisal. York: Kleijnen Systema c Reviews Ltd, 2013.
Medida de efectividad
La medida de efectividad utilizada en el modelo fueron los años de vida libres de transfusiones.
Uso de recursos y costos
Para conocer el uso y frecuencia de recursos en estos pacientes, se llevó a cabo un panel de expertos (5 especialistas Médicos Hematólogos de Instituciones Públicas en México como el IMSS, Secretaria de Salud e ISSSTE, así como 2 especialistas Médicos Hematólogos que trabajan tanto en Instituciones Públicas como Privadas, con un promedio de casos de atención de 2 a 36 pacientes por año) con la metodología Delphi. El precio de los recursos se obtuvo de aquellos publicados en el sector salud. Es importante aclarar que solamente se consideraron los costos directos. Con dicha información se realizó la estimación de costos. Para las estimaciones de estos costos se consultaron distintas fuentes de precios y costos unitarios oficiales del sector salud, siendo necesario tomar en cuenta la inflación para algunos valores, mediante factores de actualización que se calcularon a partir de los índices nacionales de precios al consumidor (INPC) que reporta el INEGI. Todos los costes están referenciados a 2015.
En la Tabla VI se muestra de forma resumida el costo anual por paciente dependiente de transfusiones, donde claramente se aprecia el porcentaje significativo que recae sobre el consumo de concentrados sanguíneos.
Costo del paciente dependiente de transfusiones
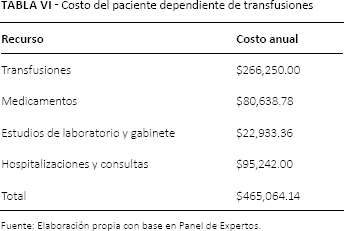
Fuente: Elaboración propia con base en Panel de Expertos.
En las Tablas VII y VIII se muestran los costos de la medicación con lenalidomida, así como el costo del monitoreo de los pacientes que se encuentran bajo tratamiento con dicho fármaco.
Costo del tratamiento con lenalidomida

Fuente: Elaboración propia con precios de lenalidomida proporcionados por Celgene.
Costo del monitoreo del paciente bajo tratamiento con lenalidomida

Fuente: Elaboración propia con base en Panel de Expertos.
Costo de complicaciones y progresión de la enfermedad
A partir de la opinión de los expertos, las complicaciones más frecuentemente observadas en los pacientes con dependencia transfusional son la insuficiencia cardiaca congestiva y la septicemia. Los costos de estas complicaciones fueron extraídos de las guías de diagnóstico médico (GRD's 2008) del IMSS, los cuales fueron promediados y a partir de los índices nacionales de precios al consumidor (INPC) que reporta el INEGI se actualizaron al año 2015. Por otro lado, para estimar el costo de la LMA, se consultó también a los expertos para conocer el patrón de recursos consumidos anualmente en los pacientes con dicho diagnóstico, y se realizó la estimación del costo anual por paciente con LMA (Ver Tab. IX).
Costo de las complicaciones y de la progresión del SMD-5q

Fuente: Elaboración Propia con base en Grupos Relacionados con el Diagnóstico (GRD). Instituto Mexicano del Seguro Social (IMSS). Dirección de Prestaciones Médicas. 2008.
Tasa de descuento.
En el caso de evaluaciones económicas en México (Guía de Evaluación de Insumos para el Sector Salud, GEISS. 2011) con horizontes temporales mayores a un año, tanto los costos como las ganancias en salud futuras deben ser descontadas a una tasa del 5% (13).
Análisis de Sensibilidad
Para comprobar la robustez del modelo se realizó un análisis de sensibilidad univariado de los parámetros de costos y efectividad, en + 10%. Se aplicó una tasa de descuento del 5% a los resultados del modelo a partir del segundo año. En ambos casos se analizaron las posibles variaciones tanto del precio de lenalidomida, como de aquellos parámetros que pueden generar incertidumbre en los resultados del modelo. Este último sirvió también para generar la curva de aceptabilidad de lenalidomida, mediante simulación de Monte Carlo.
Resultados
Los resultados muestran claramente que lenalidomida conlleva a la independencia transfusional del paciente. En el año 5, se puede observar que se tiene una ganancia de 17.41 ciclos en esta medida, es decir 487 días de independencia transfusional, que equivalen a $246,971 MXN por año de vida de independencia transfusional.
Caso Base
En las Tablas X a XII se muestran los resultados basales de costo-efectividad (con y sin descuento) para diferentes periodos de análisis: 1, 3 y 5 años. En todos los casos, se muestra una ganancia en los años de vida libres de transfusiones con lenalidomida. Como se ha comentado a lo largo del presente estudio, lenalidomida impacta directamente en la dependencia transfusional, lo cual definitivamente tendrá un impacto sustancial en la calidad de vida de los pacientes con esta enfermedad. Hacia el año 5 se puede observar que la ganancia equivale a 512 días de independencia transfusional, lo cual es aproximadamente año y medio. A cinco años, el costo por año de vida libre de transfusiones equivale a $249,972 MXN.
Resultados basales a un año del Modelo
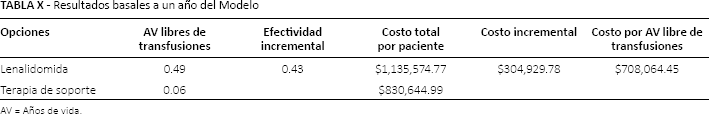
AV = Años de vida.
Resultados basales a tres años del Modelo (valores descontados)
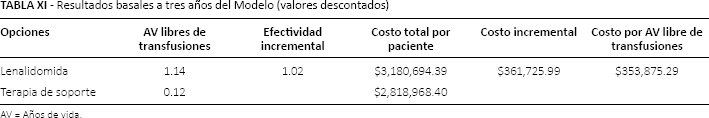
AV = Años de vida.
Resultados basales a cinco años del Modelo (valores descontados)
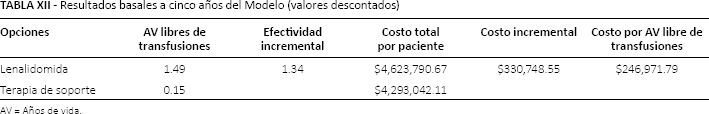
AV = Años de vida.
Resultados del análisis de sensibilidad
En el análisis de sensibilidad determinista univariado, en forma de diagrama de tornado (Ver Fig. 2), se aprecia que el riesgo de muerte por LMA es el parámetro que introduce la mayor cantidad de incertidumbre al modelo, seguido de los precios de ambas presentaciones de lenalidomida y en tercer lugar el costo de las complicaciones de la dependencia transfusional. Por otro lado, las tasas de respuesta terapéutica de lenalidomida resultaron ser los parámetros con el menor impacto sobre los resultados basales de costo-efectividad. En los resultados del análisis de sensibilidad probabilístico en el plano de costo-efectividad, donde la nube de puntos representa la distribución bivariada entre el costo incremental y la efectividad incremental (Ver Fig. 3), la cual queda ubicada casi en su totalidad en el primer cuadrante del plano, permitiendo reconocer el grado de incertidumbre asociado a la distribución de probabilidad de cada uno de los parámetros del modelo y cómo esto impacta en la variabilidad de los resultados de costo-efectividad.
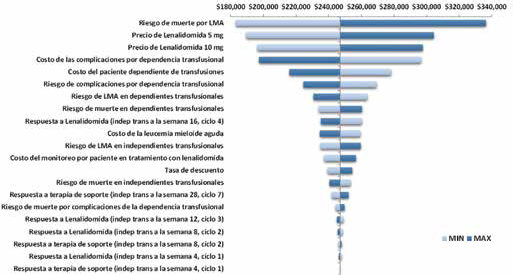
D iagrama d e t ornado g enerado a partir de los resultados del análisis de sensibilidad univariado.
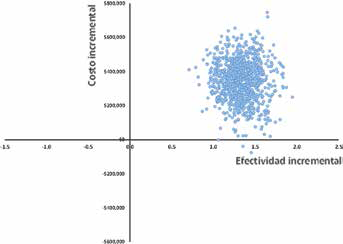
Resultados del análisis de sensibilidad probabilístico del Modelo en el plano de costo-efectividad.
A partir de los resultados de la simulación de Monte Carlo y utilizando el enfoque del beneficio monetario neto, se construyó la curva de aceptabilidad de lenalidomida que se muestra en la Figura 4, vemos que a mayor disponibilidad a pagar por parte de las instituciones públicas a cambio de obtener un año adicional de vida libre de transfusiones para los pacientes con SMD- del 5q, la probabilidad de que lenalidomida sea una opción terapéutica costo-efectiva se incrementa exponencialmente.
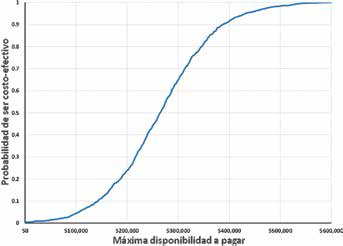
Curva de aceptabilidad. Resultado del Modelo para lenalidomida.
Discusión
El SMD es una alteración hematopoyética clonal caracterizada por citopenias, hematopoyesis inefectiva y alteraciones morfológicas de las células hemáticas, esta entidad nosológica puede estar ocasionado por alteraciones citogenéticas como la deleción del cromosoma 5q (del 5q) que ocurre en el 7 a 10% de los casos, a este grupo de pacientes hace referencia el presente estudio. La única opción terapéutica disponible hasta hace poco tiempo era la transfusión sanguínea con incremento considerable del riesgo de sobrecarga de hierro, falla cardiaca e infecciones entre otras. El uso de lenalidomida representa una opción terapéutica cuyo principal objetivo es la corrección de la alteración genética primaria que se refleja clínicamente en la independencia a transfusiones, esto mejora considerablemente la calidad de vida y disminuye la mortalidad (6, 14).
Basados en estos datos, se realizó una evaluación económica completa de tipo costo-efectividad del uso de lenalidomida (Revlimid®) en las instituciones públicas del sector salud en México, para el tratamiento de pacientes con anemia dependientes de transfusiones secundario a SMD de riesgo bajo o intermedio 1 asociados a una anomalía por del 5q en comparación con el mejor tratamiento de soporte utilizado en las instituciones públicas del sector salud en México. Se eligió este tipo de análisis debido a que la evidencia (estudio MDS-004,42) señala que el uso de lenalidomida en estos pacientes genera beneficios en salud versus la terapia de soporte. Los resultados de la evaluación económica mostraron que, en 5 años, se genera una ganancia de 17.41 ciclos, que equivalen a 487 días de independencia transfusional, lo cual es aproximadamente año y medio. A cinco años, el año de vida ganado de independencia transfusional equivale a $246,971.79 MXN. Se comprobó la robustez del modelo mediante análisis de sensibilidad univariado, con los que al variar en +10 el parámetro del modelo se observó que la RCEI no se modificaba en gran medida, a excepción del costo por ciclo de lenalidomida, lo que era de esperarse.
Conclusiones
Con base en los resultados encontrados en el presente estudio, es posible concluir que lenalidomida es una alternativa que genera beneficios a la salud en pacientes con anemia dependientes de transfusiones debido a SMD de riesgo bajo o intermedio 1 asociados a una anomalía por del 5q con o sin anomalías citogenéticas adicionales, al incrementar los años de vida con independencia transfusional, desde la perspectiva de las instituciones de salud del sector público, en un periodo de análisis de 5 años. Además de beneficios en el ahorro económico de las instituciones de salud a largo plazo, en definitiva, se gasta más en un paciente con transfusiones repetitivas comparados con aquellos quienes reciben lenalidomida como primera opción terapéutica.
Footnotes
Financial support: We acknowledge the unrestricted support provided to this project by Laboratorio Celgene, S. de R.L. de C.V.
Conflict of interest: There is no conflict of interest to declare.
