Abstract
In the Colombian Amazon termites attack bare root stumps of the rubber tree Hevea brasiliensis. The objective of the study was to evaluate the pathogenicity of the fungus Metarhizium anisopliae on Heterotermes tenuis termites under laboratory conditions. The concentrations used were 1x10¹, 1x10³, 3x10⁵, 1x10⁷ and 3x10⁸ conidia/ml and the control (distilled sterile water). The dead insects were cleared with KOH at 10% and mounted on glass slides. Mortality was compared using Kaplan-Meier survival curves and the CL₅₀ and TL₅₀ were determined. The concentration of 3x10⁸ conidia/ml was the most effective (100% of insects eliminated in six days). There were differences found among the six concentrations used in percent survival of H. tenuis (H₅,₈₁=19.4; p < 0.05) and in the time (days) of survival (H₄,₆₀=14.0; p < 0.05). The CL₅₀ was 9.64 x 10³ conidia/ml after a time of six days. The TL₅₀ was three days for the concentration of 3 x 10⁸ conidia/ml. Under laboratory conditions M. anisopliae is very effective on H. tenuis, and for this reason its use under natural conditions should be considered in the integrated management of the termites that affect the cultivation of rubber trees in the Amazonian region. This study is the first report on the in vitro biocontrol of H. tenuis in H. brasiliensis.
Introducción
Las termitas son insectos que se han especializado en una dieta a base de madera en descomposición, pasto seco, hon-gos, hojas muertas, cortezas, suelo rico en humus y estiércol de herbívoros entre otros materiales con lignocelulosa (Cancello y Myles 2000; Takuya y Masahiko 2001). Sin embargo, se les considera de importancia económica por las pérdidas que ocasionan en plantaciones forestales, huertos, árboles urbanos, frutales, cosechas, pastos y construcciones de madera (Wolff 2006).
La familia Rhinotermitidae (Isoptera) son termitas que nidifican bajo tierra excavando cámaras y túneles en relación con raíces próximas, troncos y piezas de madera (Constantino 2002). Esta familia comprende muchas especies consideradas plagas de cultivos, entre las cuales se encuentran: caña de azúcar y té. En Colombia se han registrado los géneros Heterotermes y Coptotermes que causan daño además en cultivos forestales (Madrigal 2003). Según Light (1946), los géneros Heterotermes, Coptotermes y Reticulitermes son considerados los responsables de las mayores pérdidas económicas por parte de las termitas alrededor del mundo.
Heterotermes tenuis (Hagen, 1858) es una de las especies con mayor importancia económica, son termitas de pequeño porte con soldados dimórficos (Constantino 1991). Esta especie consume diferentes sustratos ricos en celulosa (heces de bovinos, bagazos de tallos, papel, entre otros) (Campos et al. 1998) y ataca un amplio número de especies vegetales entre las que se destacan el maíz (Zea mays), la caña de azúcar (Saccharum officinarum) y el eucalipto (Eucalyptus sp.) (Mill 1991); además pueden defender intra e interspecíficamente su territorio (Camargo-Dietrich y Costa-Leonardo 2000). Los métodos de regulación de esta plaga han incluido el uso de insecticidas y hongos entomopatógenos (Moino et al. 2002; Almeida et al. 1998).
El uso de organismos benéficos como los hongos entomopatógenos es una opción ecológica y económicamente viable para la regulación de diferentes especies de termitas plaga (Butt et al. 2001; Moino y Alves 1998; Ferron 1978). Tanada y Kaya (1993) afirmaron que los primeros microorganismos que se encontraron causando enfermedades en estos insectos, fueron los hongos entomopatógenos, debido a su notable capacidad de invasión y su rápido crecimiento macroscópico sobre la superficie de sus hospederos.
Las enfermedades fungosas en insectos son comunes y en ocasiones lo suficientemente severas para causar epizootias que llegan a eliminar casi por completo una población en un hábitat determinado (Herrera y Ulloa 1990). Los hongos entomopatógenos poseen ciertas ventajas sobre otros agentes de control microbiano (bacterias, protozoarios y virus), debido a que son capaces de atacar todas las fases de desarrollo de los insectos, además pueden infectar a aquellos que normalmente no son susceptibles a la infección por bacterias y virus (Ferron 1978).
Metarhizium anisopliae (Metsch.) Sor., 1879 es uno de los hongos biocontroladores con mayor potencial entomopatógeno en el control de insectos plaga en diferentes cultivos agrícolas (Albuquerque et al. 2005; Shi y Feng 2004; Faria y Wraight 2001; Saldarriaga y Pineda 2001; Feng y Poprawski 1999). Este hongo Deuteromycota (anamorfo) se caracteriza por formar esporulación en capas, fialides sencillas, en pares o en ramilletes, con fialoconidias producidas en cadenas basipetalas, compactadas y en columnas (Samson et al. 2004; Kiffer y Morelet 2000; Domsch et al. 1980; Barnett y Hunter 1972). En diversos estudios se ha informado sobre la capacidad patogénica de M. anisopliae en diferentes especies de termitas en condiciones de laboratorio (Chouvenc et al. 2009a, 2009b; Chouvenc et al. 2008; Gutiérrez et al. 2005; Gutiérrez y Saldarriaga 2004; Sun et al. 2002; Milner et al. 1997; Milner 1992). También se ha informado sobre su patogenicidad en H. tenuis, que atacan cultivos de caña y plantaciones de eucalipto (Moino et al. 2002; Moino y Alves 1998).
En la Amazonía colombiana, y en particular en los polos de explotación cauchera del Departamento del Caquetá (Noroccidente y Suroccidente), las termitas atacan frecuentemente los tocones a raíz desnuda de caucho natural Hevea brasiliensis (Willd. ex Adr. de Juss.) Muell.-Arg. durante la fase de siembra y establecimiento en campo de finitivo del cultivo, lo que históricamente se ha reflejado en pérdidas que han oscilado entre el 10% y el 20% (ASOHEСА 2007).
El manejo de las termitas plaga en los cultivos recién establecidos de H. brasiliensis se ha realizado preventivamente con los insecticidas Furadan® y Malation® (Garzón 2000). El método consiste en preparar una solución de estos químicos, en la cual se sumergen los tocones a raíz desnuda por 24 horas y posteriormente se realiza la siembra. Este método no es efectivo y puede causar problemas a la salud humana y al ambiente; además puede generarse resistencia en las poblaciones (FAO 1970). Debido a los problemas que conlleva el uso de insecticidas, M. anisopliae constituye a una estrategia viable y efectiva que puede ser usada para el manejo de termitas plaga asociadas al cultivo del caucho natural.
El cultivo del caucho natural en el Departamento del Caquetá constituye uno de los renglones más significativos dentro de la actividad agrícola, económica y social de la región, dado que de la producción y explotación laticífera dependen cerca de 1700 familias campesinas en la región (ASOHECA 2007). En este sentido, el presente estudio tuvo como objetivo evaluar, en condiciones de laboratorio, la patogenicidad del hongo M. anisopliae sobre termitasplaga de la especie H. tenuis a partir de ejemplares colectados en tocones a raíz desnuda de plantaciones en crecimiento de H. brasiliensis establecidas en la zona noroccidental del Departamento del Caquetá.
Materiales y Métodos
Área de estudio
La fase de campo se realizó en el municipio de El Doncello, al noroccidente del Departamento del Caquetá (Colombia). Éste es el municipio más heveícola del Departamento con el 14,3% del total establecido en plantaciones de H. brasiliensis en etapa de crecimiento y en producción (ASOHECA 2009). La región presenta paisajes de lomerío, se encuentra ubicada a una altitud de 289 msnm, posee una temperatura promedio de 28°C, una pluviosidad promedio de 3500 mm/año y una humedad relativa media del 74% (IGAC 1993).
Se seleccionaron las veredas Maguaré y La Libertad, localizadas entre las coordenadas 1°38′21N, 75°09′32,7″W, 1°38′55,6″N 75°09′19,6"W, respectivamente, por presentar el mayor registro de termitas en tocones de caucho (>10% de infestación) (ASOHECA 2009). En tres plantaciones en crecimiento (2-6 meses), se coleccionaron ejemplares de H. tenuis de las castas obrera y soldado que son importantes para la identificación taxonómica; de cada plantación se escogieron y de forma aleatoria tres puntos de muestreo. Estas plantaciones se establecieron a partir de tocones a raíz desnuda en surcos dobles con un distanciamiento de 3 x 3 x 12 m.
La fase de laboratorio se desarrolló en el Laboratorio de Biología de la Universidad de la Amazonia en Florencia, Caquetá (Colombia), municipio localizado en las coordenadas 1°37′03″N 75° 37'03"W. Florencia está a una altitud de 242 msnm, posee una temperatura promedio anual de 25,5°C, una pluviosidad de 3793 mm/año y una humedad relativa promedio de 84,2% (IGAC 1993).
Recolección y mantenimiento de ejemplares de H. tenuis
Los tocones a raíz desnuda de H. brasiliensis infestados por las termitas H. tenuis se introdujeron en bolsas plásticas de color negro con el fin de emular condiciones de oscuridad y evitar así el estrés en los individuos coleccionados. Se utilizaron también frascos de 15 x 8 cm a los cuales se les agregó 500 g de sustrato (suelo y restos de tocones de donde se obtuvieron las termitas). Los recipientes se taparon con muselina sujetada por una banda de caucho sintético.
Bajo condiciones de laboratorio se establecieron las colonias. Las termitas se mantuvieron en los tocones de donde se coleccionaron y se colocaron luego en un recipiente rectangular con dimensiones de 21 x 56 x 30 cm, cubiertos con tela muselina y plástico negro para simular oscuridad, hábito críptico y subterráneo característico de la familia Rhinotermitidae (Márquez 2006; Sun et al. 2003). Se simularon las características climáticas básicas (74% de humedad relativa y 28°C de temperatura) y físicas del sitio de procedencia. Para prolongar el tiempo de vida de las termitas, se adicionó una mezcla de arena fina con suelo del sitio de origen en una relación 1:3.
Previo a las pruebas de patogenicidad con M. anisopliae se realizó un ensayo que consistió en introducir obreras de H. tenuis en cajas de Petri de 9 cm de diámetro con papel filtro estéril para registrar su supervivencia (Wang y Powell 2004) y garantizar así que en los bioensayos de patogenicidad los insectos morirían efectivamente por acción de M. anisopliae y no por falta de alimento u otro factor estresante. Se utilizaron 10 repeticiones y 20 termitas por repetición. El indicador de supervivencia fue el porcentaje de termitas que permanecieron vivas por un periodo mayor a 15 días alimentándose exclusivamente del papel filtro.
Reactivación y cultivo del hongo
Las pruebas de patogenicidad se realizaron con el hongo M. anisopliae (M3C5), aislado de un coleóptero de la familia Melolonthidae, suministrado por el Laboratorio de Micología de la Universidad de Antioquia, Medellín (Colombia). La reactivación de M. anisopliae se realizó en obreras de H. tenuis. Se utilizaron dos métodos de infección: El primero realizando una aspersión sobre las termitas con una suspensión concentrada de 3x10⁸ conidios/ml (Gutiérrez y Saldarriaga 2004) y un segundo método, exponiendo los insectos al ataque del hongo por invasión hifal en cajas de Petri de 9 cm de diámetro sobre medio de cultivo Saboroud Dextrosa Agar (SDA). Después de muertas las termitas por la invasión de M. anisopliae se transfirieron a cajas de Petri con papel filtro estéril humedecido, hasta que se lograba la invasión total del hongo potenciando así su patogenicidad. El hongo se reprodujo en los medios de cultivo: Papa Dextrosa Agar (PDA), y Saboroud Dextrosa Agar (SDA) y se incubó a una temperatura de 24°C entre 8 a 10 días.
Preparación de las suspensiones de inóculo
En un vaso de precipitado de 250 ml se vertieron 50 ml de agua destilada estéril, luego se le adicionaron las esporas del hongo con un asa estéril y se le agregaron dos gotas de Tween 80 al 0,05% para facilitar remoción del inóculo y obtener una solución homogénea. A partir de esta solución madre de esporas se prepararon las siguientes concentraciones (tratamientos): 1x10¹, 1x10³, 3x10⁵, 1x10⁷ y 3x10⁸ conidios/ml, realizando los conteos mediante la cámara de Neubauer (Goettel y Inglis 1997). Se utilizó agua destilada estéril como tratamiento testigo, totalizando así seis tratamientos.
Pruebas de patogenicidad
Cada concentración de M. anisopliae se agregó en un vaso de precipitado estéril de 250 ml, luego se sumergió una lona 100% de algodón durante 5 minutos y a partir de la lona humedecida se impregnaron los insectos experimentales (método de inoculación tópica indirecta) (Gutiérrez et al. 2005).
Los ensayos se realizaron en termitas obreras de H. tenuis adaptando la metodología de Gutiérrez et al. (2005). En este sentido, se colocaron 10 ejemplares de termitas obreras en frascos de vidrio de 9 x 8 cm. En cada frasco se agregaron aproximadamente 25 ml de agar-arena (Staples y Milner 2000) y luego se adicionó la lona impregnada con las esporas del hongo y papel filtro estéril. Con el fin de cubrir la boquilla de cada frasco se empleó muselina sujetada por una banda elástica. Se realizaron cuatro repeticiones por cada concentración, cada repetición con 10 termitas y un lote de testigos (lona tratada con agua destilada estéril). En total se utilizaron 240 termitas. Los ensayos se realizaron bajo condiciones de oscuridad utilizando una incubadora a una temperatura de 28°C y humedad relativa de 74%.
Las termitas se observaron cada día, registrando los porcentajes de mortalidad, las muertas se trasladaron a cajas de Petri con papel filtro estéril humedecido y se colocaron en cámara húmeda e incubaron a temperatura ambiente (28°C) durante 10 días. Los insectos muertos y colonizados por el hongo se aclararon con KOH al 10% (Gutiérrez y Saldarriaga 2004) y montados en placas microscópicas. Se realizaron también placas coloreadas con azul de lactofenol con el fin de observar las diferentes estructuras hifales y verificar así la presencia e identidad del hongo (Goettel y Inglis 1997).
Análisis estadístico
La mortalidad diaria y acumulada de las termitas para cada concentración, se comparó mediante las curvas de supervivencia de Kaplan-Meier siguiendo la prueba generalizada de Gehan. Utilizando estas curvas se calcularon también los TL₅₀ (tiempo letal mediano) para cada concentración con el programa Statistica 7.0. Se realizó una prueba no paramétrica de Kruskal-Wallis (H) con nivel de significancia del 5% para las variables supervivencia (%) y tiempo de supervivencia (días) con el fin de comparar los tratamientos. Se usó también la prueba a posteriori no paramétrica de comparaciones múltiples Student Newman Keuls al 5% de significancia. La CL₅₀ (concentración letal mediana) se estimó por medio de una regresión lineal de logaritmo dosismortalidad empleando el programa Statgraphics Centurion XV.
Resultados y Discusión
Supervivencia de termitas en condiciones de laboratorio
En el ensayo en cajas de Petri con papel filtro el 100% de las termitas permanecieron vivas por más de 15 días y se alimentaron durante todo el tiempo de la fuente de celulosa suministrada a través del papel filtro. Esta prueba permitió confirmar que las termitas durante los ensayos de patogenicidad murieron efectivamente por acción de M. anisopliae y no por inanición o estrés. Camargo-Dietrich y Costa-Leonardo (2000) dedujeron que los factores que influyen significativamente en la adaptación y el comportamiento de H. tenuis son muy complejos y parecen depender de características individuales como tamaño y edad de las castas escogidas y las condiciones ambientales. Por lo que la supervivencia de las termitas luego de 15 días en las condiciones antes señaladas reflejó un mínimo efecto de la condiciones de experimentación, atribuyendo por tanto sólo el efecto de las concentraciones patogénicas de M. anisopliae.
Patogenicidad de M. anisopliae sobre H. tenuis
Las termitas tratadas con una menor concentración sobrevivieron por más tiempo que aquellas infectadas con una concentración mayor (Fig. 1). Se encontró que en el primer día después de la inoculación de M. anisopliae las termitas empezaron a morir ante las concentraciones 3x10⁸ y 1x10⁷ conidios/ml con unas mortalidades promedio de 17,5% y 10% respectivamente. En sexto día post-inoculación todas las termitas expuestas a la concentración 3x10⁸ conidios/ml murieron. En el séptimo día murieron todas las termitas tratadas con la concentración 1x10⁷ conidios/ml.
Para el segundo día post-inoculación con la concentración 3x10⁵ conidios/ml se evidenció la muerte de termitas y el 100% de los individuos murieron al noveno día post-inoculación. Solo hasta el tercer día se observaron las primeras termitas muertas con el tratamiento 1x10³ conidios/ml y toda la población murió al día 13. Al día quinto se presentaron las primeras termitas muertas con la concentración 1x10¹ conidios/ml, y sólo hasta el día 20 se registró la muerte de todas las termitas tratadas con esta concentración.
Se encontró diferencia en la supervivencia (%) de H. tenuis (H₅,₈₁-19,4; p < 0,05) y en el tiempo de sobrevivencia (días) (H₄,₆₀-14,0; p < 0,05) entre los seis tratamientos. De acuerdo con la prueba a posteriori Student Newman Keuls, todas las concentraciones patogénicas presentaron diferencias significativas respecto al tratamiento testigo. En particular, la máxima diferencia en la supervivencia y en el tiempo de supervivencia de H. tenuis se presentó entre las concentraciones 3 x 10⁸ y 1 x 10¹ conidios/ml. El 100% de la muestra de termitas de H. tenuis fue eliminada a los seis días postinoculación.
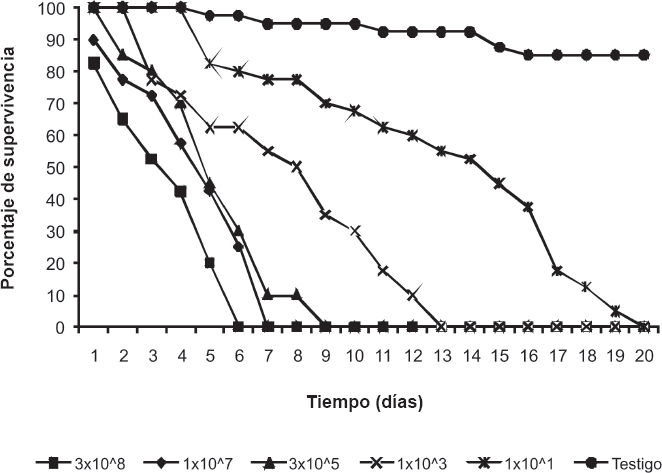
Evolución de la supervivencia de H. tenuis en presencia de M. anisopliae en función del tiempo y la concentración aplicada.
Resultados similares encontraron Gutiérrez et al. (2005), al evaluar en condiciones de laboratorio la patogenicidad de M. anisopliae sobre termitas Microcerotermes sp., concluyendo que la concentración 3x10⁸ conidios/ml fue la más efectiva (mayor mortalidad y menor tiempo de supervivencia). Dong et al. (2007), demostraron la misma eficacia en una nueva variedad de M. anisopliae (M. anisopliae var. dcjhyium, DQ288247), obtenida y evaluada sobre Odontotermes formosanus Shiraki en condiciones de laboratorio; el nuevo aislamiento resultó ser muy infeccioso y virulento contra las termitas, causando el 100% de mortalidad en tres días post-inoculación a una concentración de 3x10⁸ conidios/ml.
Moino y Alves (1998) evaluaron el efecto inhibitorio de algunos insecticidas como Imidacloprid y Fipronil sobre la capacidad patogénica de M. anisopliae en H. tenuis, lo que permitiría también explicar por qué una misma concentración patogénica posee mayor virulencia en un sitio y menor capacidad infecciosa en otro, toda vez que el efecto fue evaluado sobre la misma especie de termita.
Los individuos testigo que presentaron mortalidad, probablemente fueron resultado de la fragilidad natural de estos insectos que no permite someterlos a técnicas de asepsia previas a los ensayos (Tanada y Kaya 1993) ó a las condiciones propias de los ensayos que pueden causar estrés (Staples y Milner 2000). La técnica de aclaración con KOH al 10% permitió observar que las termitas testigo no mostraron invasión de sus tejidos por M. anisopliae ni por otros hongos contaminantes.
Capacidad de conidiación de M. anisopliae sobre cadá-veres de H. tenuis
La aparición de micelio en los insectos varió en días y en los diferentes tratamientos. En cuatro de cinco concentraciones patogénicas se observó conidiación por el hongo M. anisopliae (Fig. 2). En particular, 74 de 200 termitas presentaron invasión micelial por M. anisopliae (Figs. 3A-D). Con el tratamiento 3x10⁸ conidios/ml, M. anisopliae esporuló en el 100% de las termitas, al segundo día post-inoculación conidió el 12,5% de los insectos, al quinto día la mitad de la población y al octavo día el 100% de las termitas.
La germinación de M. anisopliae sobre las termitas sometidas a la concentración 1x10⁷ conidios/ml sólo se evidenció al quinto día post-muerte y al octavo sólo germinó el 57,5%. Para las concentraciones 3x10⁵ conidios/ml y 1x10³ conidios/ml la conidiación no fue mayor al 30% de la muestra tratada. Las termitas inoculadas con la concentración 1x10¹ conidios/ml no presentaron conidiación. Se observó que una disminución en la concentración de conidias, implicó una menor la probabilidad de esporulación y de invasión sobre las termitas evaluadas.
Moino et al. (2002) estudiaron la duración de las diferentes fases de infección de M. anisopliae sobre H. tenuis usando microscopio electrónico de barrido y una única concentración patogénica (1 x 10⁹ conidios/ml). Estos autores encontraron que la adhesión conidial de M. anisopliae al integumento del insecto ocurrió inmediatamente después de la inoculación y entre las 0 y 6 horas, mientras que la germinación ocurrió entre las 12 y 24 horas después de la inoculación. La colonización de M. anisopliae ocurrió entre las 48 y 72 horas después de la inoculación. M. anisopliae mató a los insectos a las 48 y 72 horas después de la inoculación, y el micelio extruyente apareció entre las 48 y 120 horas después de la inoculación. La conidiogénesis apareció entre las 96 у 144 horas post-inoculación. El cadáver fue cubierto por las conidias de M. anisopliae 120 horas después de la inoculación. En este estudio, M. anisopliae con una concentración inferior (3x10⁸ conidios/ml) a la utilizada por Moino et al. (2002), mató a los insectos en un rango de 24 a 144 horas después de la inoculación, es decir, que inició más rápido el proceso infeccioso pero tardó más tiempo el proceso invasivo de los insectos. El inicio del proceso de conidiación también fue más rápido (48 horas post-inoculación), sin embargo, una vez iniciado se prolongó más la aparición de conidias sobre los insectos infectados en un rango que osciló entre las 48 y las 192 horas post-inoculación.
Los resultados de Moino et al. (2002), muestran una mayor patogenicidad de la cepa evaluada (M. anisopliae E-9) luego de las 48 horas post-inoculación en relación con el aislamiento probado en este estudio, inicialmente atribuible a la concentración patogénica empleada. Lo anterior, consideraría también la posibilidad de que las termitas H. tenuis asociadas a H. brasiliensis tengan una mayor resistencia a M. anisopliae debido al mayor rango en el tiempo de supervivencia observado en las diferentes concentraciones patogénicas.
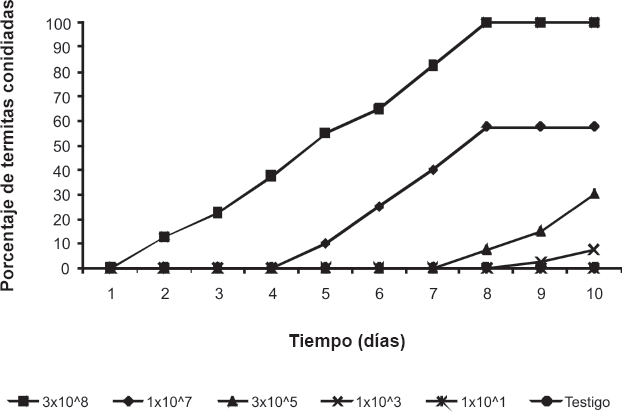
Evolución de la conidiación de M. anisopliae sobre termitas H. tenuis en función del tiempo y la concentración aplicada.
Considerando el origen alóctono de la cepa utilizada en este estudio, se podría afirmar que la ausencia de interacción hospedero-parásito asociada a sustratos provenientes de tocones de caucho natural bajo las condiciones de la Amazonia colombiana, ha generado mejores ventajas adaptativas en H. tenuis para contrarrestar la patogenicidad de aislamientos alóctonos de M. anisopliae. Esto confirmaría la necesidad de probar aislamientos nativos con un mayor grado de virulencia y mejor potencial para la región. Sun et al. (2002) y Hajek y Leger (1994) afirmaron que el grado de patogenicidad de los entomopatógenos puede variar de acuerdo con el sustrato de procedencia, su nicho ecológico y sus condiciones fisiológicas y metabólicas.
En relación con las condiciones de infección que favorecieron la conidiación sobre H. tenuis, todos los tratamientos ocurrieron a una humedad relativa del 72%, lo que pudo favorecer la patogenicidad de M. anisopliae matando el 100% de los individuos de H. tenuis al séptimo día cuando se empleó la concentración de 1x10⁷ conidios/ml. Ensayos realizados por Milner et al. (1997), donde se evaluó el efecto de la humedad en la germinación e infección de M. anisopliae sobre Coptotermes acinaciformis froggatt, permitieron apreciar que el hongo mató el 100% de termitas en seis días a una concentración 1x10⁷ conidios/ml y una humedad relativa de 93% y 97,5%. Aunque en ambos estudios se empleó la misma concentración, la mortalidad registrada en el tiempo difiere por el grado de susceptibilidad de la especie y por la variación en la humedad relativa considerada en las pruebas de patogenicidad. En particular, Milner et al. (1997), establecieron la necesidad de hacer pruebas con humedades relativas superiores al 86% para alcanzar mayores niveles de eficiencia en M. anisopliae.
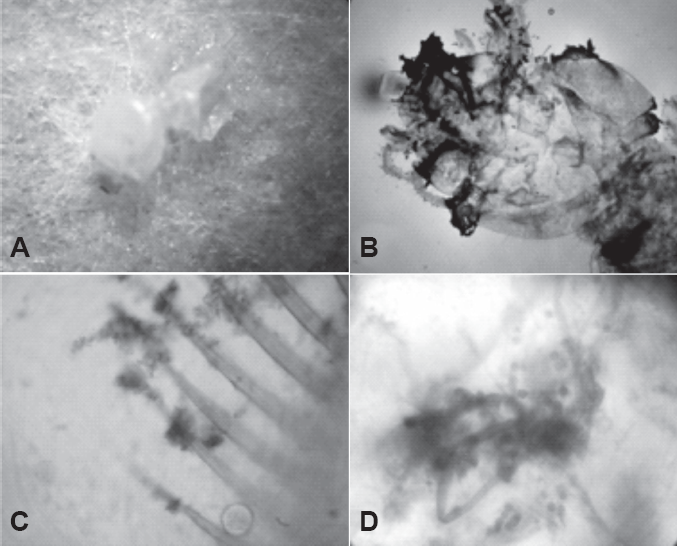
Presencia de M. anisopliae sobre H. tenuis. A. Integumento de una termita obrero con presencia de conidiación 10X. B. Conidios sobre la cabeza y las setas de la maxila 40X. C. Micelio invadiendo los tejidos de la región torácica 40X. D. Hifas y conidios diseminados en los tejidos del abdomen 100X.
Según Gutiérrez et al. (2005), el hecho que el hongo invada los cadáveres es trascendental ya que la posibilidad de la transmisión de la micosis a partir de termitas enfermas constituye una forma exitosa de acceder a partes de la colonia y al nido que no son accesibles por tratamiento directo. Ante esta aseveración debe considerarse que el éxito de las termitas (incluso las subterráneas) está dado por su comportamiento social, la limpieza que se hacen los individuos cuando son infectados por hongos, presencia de secreciones de defensa y el hábito de excluir a cadáveres e individuos enfermos de la colonia (Chouvenc et al. 2009a, 2009b; Torales et al. 2005; Myles 2002).
Mediante la técnica de aclaración y tinción del insecto, se verificó la presencia de M. anisopliae sobre H. tenuis. Los conidios se observaron sobre la cutícula, los palpos labiales, en las setas de la cabeza, setas maxilares y setas de las patas; las hifas se observaron invadiendo la cabeza y los tejidos del abdomen (Figs. 3B-D). Estas observaciones coinciden con los estudios realizados por Gutiérrez y Saldarriaga (2004) y Moino et al. (2002) quienes observaron la patogenicidad de M. anisopliae en Nasutitermes sp. y H. tenuis respectivamente. En ambos casos se encontró que el mecanismo de invasión y toxicidad del hongo es vía integumentaria, iniciándose con la adherencia de la espora a la cutícula y penetración al tejido graso, llevando a la muerte del insecto y posterior esporulación. Estos resultados también fueron confirmados por Chouvenc et al. (2009a) en termitas Reticulitermes flavipes (Kollar, 1837). St. Leger et al. (1988) informó que una enzima del grupo de las quimoelastasas (Pr1) se encuentra implicada en la degradación cuticular. Tanada y Kaya (1993) observaron que M. anisopliae produce metabolitos secundarios como: destruxinas A, B, C, D, E y una desmetildestruxina B, los cuales son tóxicos y actúan como micotoxinas.
Concentración letal mediana (CL₅₀) y tiempo letal media-no (TL₅₀) de M. anisopliae
La concentración letal mediana (CL₅₀) para M. anisopliae fue de 9,64 x 10³ conidios/ml en seis días con un intervalo de confianza del 95%. El tiempo de TL₅₀ fue de tres días para la concentración 3x10⁸ conidios/ml, cinco días para las concentraciones 1x10⁷ conidios/ml y 3x10⁵ conidios/ml, ocho días para la concentración 1x10³ conidios/ml y 14 días para la concentración 1x10¹ conidios/ml. Estos valores fueron inferiores a los registrados por Gutiérrez et al. (2005) quienes informaron un CL₅₀ fue de 0,69 x 10β conidios/ml en un tiempo de siete días y valores de TL₅₀ de cinco días para las concentraciones 1 x 10³ y 3 x 10⁵ conidios/ml y de tres días para la concentración 3 x 10⁸ conidios/ml en termitas de Microcerotermes sp.
En este estudio, se observó que las termitas de H. tenuis son susceptibles a M. anisopliae, quien debe considerarse como un agente potencial de control microbiológico de termitas plaga asociadas a tocones a raíz desnuda del caucho natural y que debe ser evaluado en condiciones de campo (considerando aspectos propios del ecosistema, el aislamiento y la etología de las termitas) para valorar implementación dentro de un programa de manejo integrado de plagas (Dong et al. 2007; Myles 2002).
Footnotes
Agradecimientos
Los autores agradecen al proyecto: Investigación en la cadena productiva del caucho natural entre la Universidad de la Amazonia y la Asociación de Reforestadores y Cultivadores de Caucho del Caquetá (ASOHECA) por el soporte económico a la presente investigación; al doctor Reginaldo Constantino por su colaboración en la verificación taxonómica de H. tenuis, al doctor Jaime Enrique Velásquez por sus comentarios en el desarrollo de la investigación, y al Grupo de Recursos Genéticos del Instituto Amazónico de Investigaciones Científicas SINCHI por la asesoría prestada en la fase de laboratorio.
