Abstract
The degree of resistance of a Tetranychus urticae population, from production greenhouse roses, was determined for five miticides from different toxicological groups in comparison to a laboratory line. The presence of enzymes related to that resistance was also evaluated. Several bioassays were conducted on the laboratory line to establish the slope of the concentration /mortality relationship. Afterwards, the value of LC90 was selected and doubled to obtain a diagnostic concentration, in such a way that applying it to the field line would determine the degree of resistance. Lastly, biochemical tests were conducted to detect enzymes related to the resistance. The highest levels of α and β-esterase and oxidases were presented in the field population. These results suggest that α and β-esterase and oxidases are involved in the resistance of the population studied.
Introducción
La arañita roja Tetranychus urticae Koch, 1836 (Acariformes: Tetranychidae) afecta a muchas especies de plantas en el mundo, incluyendo cultivos agrícolas y ornamentales. Se le ha reportado en 180 especies de plantas en invernadero y en condiciones de campo (Kim et al. 2004) causando marchitamiento, desecación del follaje y la muerte de las plantas (Gould 1987). Además son capaces de desarrollar resistencia a muchos acaricidas en un período relativamente corto (uno a cuatro años) e inducir un alto grado de resistencia cruzada (Saito et al. 1983). Por lo mismo, este ácaro ha desarrollado resistencia a la mayoría de los productos que se utilizan para su control (Devine et al. 2001). Esta habilidad de T. urticae para desarrollar resistencia, cuando se usan intensivamente acaricidas ha causado problemas resultando en una exigencia de acaricidas con nuevos modos de acción (Suh et al. 2006).
De acuerdo con Georghiou (1965) la resistencia fisiológica es la más importante en artrópodos, debido a la acción de mecanismos detoxificadores enzimáticos que provocan una mayor degradación o excreción del insecticida o acaricida (Lagunes Tejada y Villanueva-Jiménez 1994). Yang et al. (2001) mencionan que en artrópodos la detoxificación de los xenobióticos se debe principalmente a esterasas, citocromo P-450 dependiente de las monooxigenasas y glutation S-transferasas. La resistencia a organofosforados está asociada a varias enzimas. Hemingway y Karunaratne (1998) mencionan a las esterasas; Matsumura y Voss (1964) a las carboxiesterasas y fosfatasas y Yu (1982) menciona que las enzimas glutation S-transferasas intervienen en la detoxificación de compuestos organofosforados en Spodoptera frugiperda (J. E. Smith, 1797), alimentado en diferentes hospederos. La enzima acetilcolinesterasa insensible constituye el mecanismo principal de resistencia de T. urticae a los organofosforados (Voss y Matsumura 1964), las oxidasas intervienen en la detoxificación de los piretroides (Bisset et al. 1998). Lagunes-Tejada y Villanueva-Jiménez (1994) mencionan que las enzimas que degradan al DDT y sus derivados son las oxidasas y la DDT-asa.
Para establecer un programa de manejo efectivo contra T. urticae dado el uso intensivo de acaricidas de diferentes grupos toxicológicos para su control en cultivos de rosal de invernadero, es importante conocer la susceptibilidad y las causas de resistencia fisiológica hacia los acaricidas en esta especie. Por lo anterior, la presente investigación tuvo como objetivo detectar el grado de resistencia y los mecanismos fisiológicos de ésta en una población de T. urticae procedente de invernaderos productores de rosas del Estado de México.
Materiales y Métodos
Se utilizaron los reactivos: tampón fosfato de potasio a 0.05 M y pH 7.2 (Tfos), α ο β-naftil acetato (naf), dianisidina (did), albúmina sérica bovina (alb), homogeneizado de ácaros (hac), dihidrocloruro de 3, 3’, 5, 5’-tetrametil-bencidina (dtb), metanol (met), acetato de sodio (ace) a 0.25 M, pH 5, peróxido de hidrógeno an 3% (per), fitocromo c (citc), glutatión reducido (glr), 1-cloro-2, 4’ dinitrobenzeno (cdb), yoduro de acetilcolina (yac), 5, 5’-ditiobis-2-ácido nitrobenzoico (dan).
Resultados y Discusión
En la línea de laboratorio el menor valor de CL90 fue para el acaricida avermectina seguido por naled, óxido de fenbutatin, bifentrina y dicofol en su orden (Tabla 1). Con estos resultados se elaboraron las concentraciones diagnóstico con la línea de campo.
Concentración letal, límites fiduciales y chi cuadrada (Chi2) de acaricidas aplicados a la línea de laboratorio de hembras adultas de Tetranychus urticae (Chi2tablas=11.070, P ≥ 0.05). (N = 360 individuos evaluados en cada caso).
En la línea de campo el mayor porcentaje de mortalidad se obtuvo con el acaricida avermectina seguido por naled, bifentrina, óxido de fenbutatin y dicofol en su orden (Tabla 2). En relación con la avermectina, el resultado de mortalidad obtenido (82,4%) con 10,8 ppm, difirió del descrito por Grafton-Cardwell y Hoy (1983) quienes registraron un 95% de mortalidad con una concentración de 4 ppm, después de 24 h de exposición. Lo anterior indica que la población utilizada en este estudio es menos susceptible. Por otro lado, Landeros et al. (2002) reportan, 100% de mortalidad de T. urticae con una concentración de 10 ppm de avermectina después de 72 h de exposición. En estudios realizados con el dicofol Dennehy et al. (1983) realizaron comparaciones de mortalidad a 24 de h de exposición en varias poblaciones de T. urticae, utilizando 1000 ppm como concentración diagnóstico, se obtuvieron porcentajes de mortalidad entre 2,5 y 68,6%.
Respuesta de hembras adultas de Tetranychus urticae a concentraciones diagnóstico procedentes de invernaderos del Estado de México (N= 400 en cada caso).
Dennehy et al. (1987) indican que cualquier población es resistente si al exponer la población a una concentración diagnostico (el doble del valor de CL90 obtenido de una línea susceptible) el resultado de mortalidad es menor a 80%; en esta investigación podríamos indicar que la línea de campo utilizada en este estudio resultó susceptible para avermectina con un 82,4% de mortalidad y resistente para los demás productos. Este resultado probablemente es debido a que en los cultivos de rosal, donde se recolectó el material para los bioensayos, se realiza una rotación de acaricidas y los productores de estos cultivos indicaron que únicamente realizan dos aplicaciones de avermectina por año. Sobre este mismo acaricida Clark et al. (1994) no detectaron resistencia en poblaciones de T. urticae recolectadas en California, Florida e Islas Canarias después de seis aplicaciones de avermectina por año. Así mismo Hoy y Conley (1987) no encontraron diferencias en susceptibilidad en cinco poblaciones de T. urticae después de 6-8 aplicaciones con abamectina en condiciones de laboratorio.
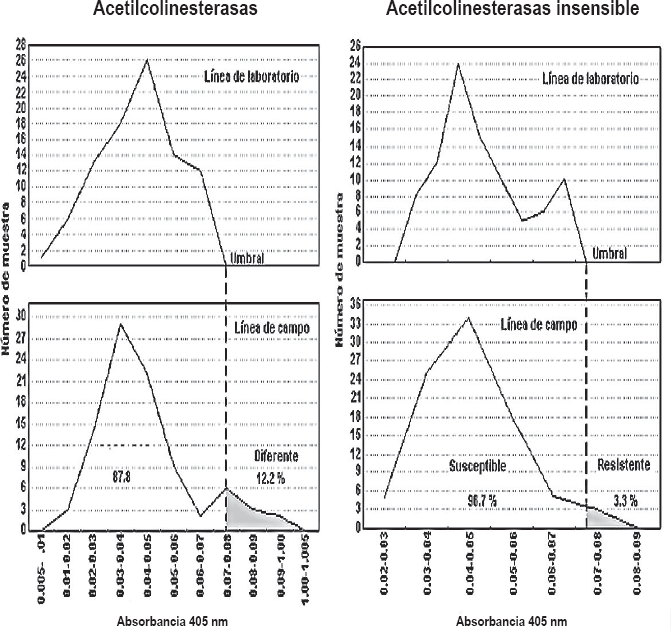
Distribución de frecuencia de los niveles de acetilcolinesterasa y acetilcolinesterasa insensible para dos líneas de Tetranychus urticae y discriminación con el umbral de tolerancia para cada enzima en la población de campo.
Niveles promedio de los máximos de absorbancia para cada enzima de las dos poblaciones de Tetranychus urticae y número de muestras que superan el umbral de tolerancia.
Número de muestras que superaron el umbral de tolerancia
Umbral de tolerancia para cada enzima,
Promedio de tres repeticiones
Desviación Estándar.
Al comparar los resultados con el acaricida organofosforado naled en el cual el 25% de la población sobrevivió con la exposición a la dosis diagnóstico y la detección de las enzimas α y β esterasas en la población estudiada (Figura 2) podemos determinar que estas enzimas fueron las directamente responsables de la resistencia al acaricida organofosforado. Al respecto Matsumura y Voss (1964) y Herne y Brown (1969) reportan resistencia de T. urticae a organofosforados por incremento de la actividad de las enzimas carboxiesterasas.
Para el caso de los insecticidas piretroides (bifentrina) también se presentó una alta relación entre el porcentaje de supervivencia de la población a la concentración diagnostico (Tabla 2) y las enzimas esterasas (Fig. 2), por lo que también se consideran responsables de la resistencia en esta investigación; al respecto Yang et al. (2002) registraron que el principal mecanismo de resistencia a bifentrina en T. urticae está relacionado con una alta actividad de esterasas. Los mismos autores (Yang et al. 2001) reportan a las enzimas esterasas y en menor grado a las glutation S-transferasas como los principales causantes de la resistencia a bifentrina y λ-cyhalotrina.
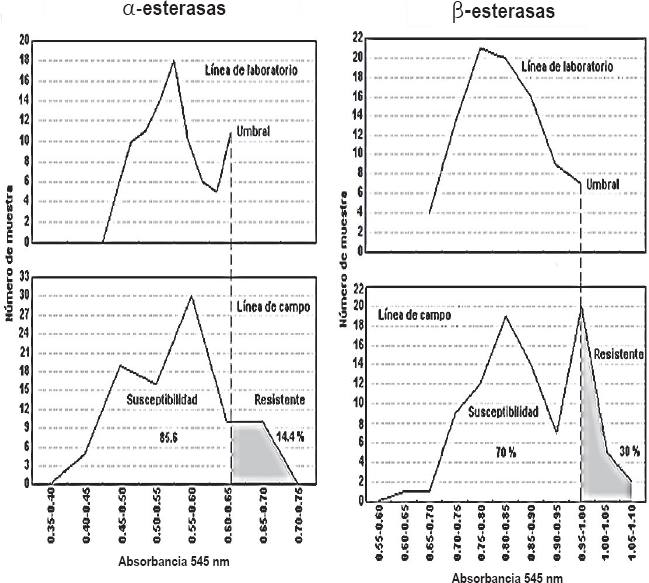
Distribución de frecuencia de los niveles de α-esterasa y β-esterasa para dos líneas de Tetranychus urticae y discriminación con el umbral de tolerancia para cada enzima en la población de campo.
Como ya se señaló en este estudio se observó que los niveles de glutation S-transferasas fueron inferiores a los de la línea de laboratorio lo que permite deducir que no intervienen en la resistencia a bifentrina, ya que la población de campo resultó susceptible para esta enzima (Fig. 3). Por otro lado, Riley et al. (2000) reportan a las α-esterasas como el principal mecanismo de resistencia a bifentrina en mosca blanca, aunque también involucran al sistema oxidativo, que como se muestra en la misma figura, es un factor importante como causa de resistencia.
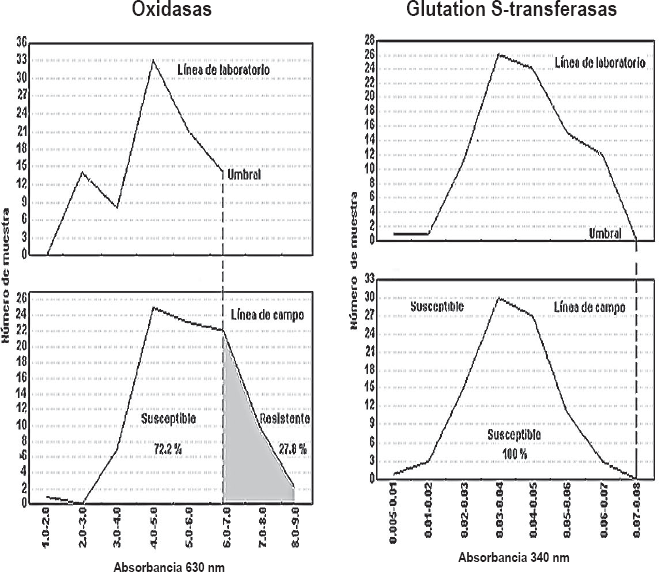
Distribución de frecuencia de los niveles de oxidasas y glutation S-transferasas, para dos líneas de T. urticae y discriminación con el umbral de tolerancia para cada enzima en la población de campo.
En relación con las enzimas oxidasas (presentes en el proceso de resistencia a dicofol), en esta investigación no se presentó una relación contundente ya que solo el 27,8% de la población de campo resultó con altos niveles de oxidasa (Fig. 3), mientras el 59,7% de la población, sobrevivió a la concentración diagnostico utilizada para el acaricida dicofol (Tabla 2). Motoyama y Dauterman (1980) y Clark y Shaman (1984) reportan a las enzimas glutation S-transferasas como causa de resistencia a organoclorados, sin embargo en el presente estudio este sistema no resultó relevante (Fig. 3), al respecto Narahashi (1983) menciona que la resistencia a clorados (DDT y sus análogos) se debe a insensibilidad en el sistema nervioso de los insectos.
Al relacionar el porcentaje de individuos vivos después de la aplicación de la concentración diagnóstico del acaricida óxido de fenbutatin con la presencia de esterasas (44,4%) y oxidasas (27,8%), se nota una marcada diferencia. Estos porcentajes nos sugieren que posiblemente otro mecanismo de resistencia está involucrado. Al respecto Carbonaro et al. (1986) indican que una de las enzimas encargada de la liberación de energía (ATPasa) puede cambiar de forma de tal manera que el acaricida no afecta su función, lo que hace resistente a su portador.
La presencia de individuos que sobrevivieron al exponerlos a la concentración diagnóstico del acaricida avermectina (17,6%) sugiere la acción de algunas de las enzimas estudiadas. Clark et al. (1994) precisan que las esterasas están involucradas en el mecanismo de resistencia a este acaricida. Por su parte Argentine y Clark (1992) mencionan que líneas de insectos resistentes a avermectina no presentan niveles significativos de resistencia cruzada para otros insecticidas.
