Abstract
In 1998 the eucalyptus weevil, Gonipterus scutellatus (Coleoptera: Curculionidae), a major defoliator of the genus Eucalyptus, which causes growth and economic losses, was detected in Chile. This has caused concern because more than 525,000 ha are planted with species of eucalypt. To understand the protein responses of development stages of G. scutellatus fed on the three species of eucalypt trees most important in the country, electrophoretic profiles were obtained and characterized on polyacrylamide gels under denaturizing conditions, and marker proteins were sought through gel densitometry. Proteins became more numerous with insect development. Protein bands were concentrated between 20 and 120 kDa, with the exception of eggs, which presented lower values. The appearance of distinct bands of proteins in the extracts from larvae and adults of G. scutellatus fed on different species of eucalypts reflected changes in their metabolism. These results are useful for integrated pest management, as the identification of marker proteins is possibly associated with metabolic patterns related to the consumption of host plants. Changes in insect diet may affect the marker proteins, indicating a differential ability of G. scutellatus to use host plants.
Introducción
El gorgojo del eucalipto, Gonipterus scutelallatus (Gyllenhal, 1833) (Coleoptera: Curculionidae), es un insecto australiano específico del género Eucalyptus (Withers 2001) y uno de los principales agentes de daño para estas especies. Se ha distribuido prácticamente por todos los continentes y se ha constituido en una plaga en la mayoría de las plantaciones de eucaliptos de África, Europa (Mansilla 1992; Rabasse y Perrin 1979; Richardson y Meakins 1986; Cordero et al. 1999), California (Cowles y Downer 1995; Hanks et al. 2000) y Nueva Zelanda (Cadahía 1980). En Sudamérica, se ha detectado en Argentina, Brasil, Uruguay y Chile (Rosado 1993; Beéche 1999; Zanuncio et al. 1998).
Tanto las larvas como los adultos de G. scutellatus se alimentan del follaje del eucalipto. El daño causado por este insecto es muy característico, dejando huellas en las hojas afectadas (Elliott y De Little 1984). Su población puede crecer mucho en pocos años, si abundan árboles hospedantes, existe un clima templado y no hay enemigos naturales (Tooke 1953). El alto potencial reproductivo del insecto, junto con su intensa capacidad de defoliación puede causar pérdidas de crecimiento o deformaciones del fuste (Santolamazza y Cordero 1998). Incluso, defoliaciones continuas pueden causar la muerte de los árboles (Elliott y De Little 1984).
En Chile central, G. scutellatus se detectó por primera vez en 1998 en las regiones 5ª y Metropolitana (Beéche 1999), y podría afectar el futuro de las 525.057 ha plantadas en el país con eucaliptos (INFOR 2006). En la actualidad esta plaga se ha desplazado hacia el norte (4ª Región) como hacia el sur (regiones 7ª y 8ª) (SAG 2005).
G. scutellatus ha tenido una marcada preferencia por varias especies de Eucalyptus (Cordero y Santolamazza 2000). En Chile, la especie principal es E. globulus ssp. globulus (Labill., 1800). Otras especies plantadas de cierta importancia son E. viminalis (Labill., 1806) y E. camaldulensis (Den., 1832), en zonas áridas, y E. nitens ((Deane y Maiden) Maiden, 1913) en áreas más frías (INFOR 2006). En la zona de San Felipe, 5ª Región, G. scutellatus presenta entre tres y cuatro generaciones (Estay et al. 2002). Según Klein y Waterhouse (2000), su importancia como plaga de los eucaliptos es superada sólo por el taladrador del eucalipto, Phoracantha semipunctata (Fabricius, 1775) (Coleoptera: Cerambycidae).
Las características morfológicas y bioquímicas de las plantas pueden causar alteraciones en el metabolismo de los insectos, y traducirse en cambios en la composición de sus proteínas (Metcalf y Luckmann 1992), de forma que el conocimiento de estas variaciones es importante cuando se desean utilizar estrategias de tipo genético en el Manejo Integrado de Plagas (MIP), pues puede revelar compuestos químicos que sirvan como instrumento para alterar su comportamiento.
Los genes permanecen básicamente sin cambio de un año a otro, pero las proteínas de las células varían según su tipo, edad, género, sanidad, y otras. La proteómica engloba tres actividades principales, la identificación de todas las proteínas sintetizadas por una célula, tejido u organismo, la deter-minación del modo en que interactúan, y el trazado de sus estructuras tridimensionales precisas (Ezzell 2002). Los resultados de las electroforesis de proteínas son caracteres fenotípicos que reflejan mucho mejor las diferencias genéticas entre especies o poblaciones que cuando se estudian los caracteres morfológicos. Por ello, la electroforesis en gel ha llegado a ser la herramienta más valiosa para los estudios taxonómicos, sistemáticos y evolutivos (Navas et al. 2002).
Esta investigación se desarrolló con el objetivo de abordar desde el punto de las proteínas la reacción de G. scutellatus frente a la alimentación con distintas especies de eucaliptos, mediante una caracterización de perfiles electroforéticos del insecto y la búsqueda posterior de proteínas marcadoras (PM) por densitometría de los geles, para indagar PM asociadas posiblemente a cambios fisiológicos del insecto, aportando con ello hacia su caracterización en el plano molecular y por ende hacia programas de MIP.
Materiales y Métodos
El material biológico se recolectó en árboles juveniles de E. globulus fuertemente infestados por G. scutellatus en el Sector El Tártaro, Comuna de Putaendo, Provincia de San Felipe (5ª Región de Chile) (32°32′30″S, 70°43′16″W). Las plantas se adquirieron en el Vivero Antumapu de la Facultad de Ciencias Forestales de la Universidad de Chile, y se trasplantaron a macetas de plástico de 18 cm de diámetro con un substrato compuesto de arena, tierra de hoja y turba, tratado con fungicida Captan 2g/L y fertilizado con urea.
Perfiles electroforéticos de G. scutellatus alimentados con E. globulus
En una fase inicial de campo se recolectaron en forma periódica a fines de verano ejemplares adultos, pupas, larvas y huevos de G. scutellatus. Los insectos se mantuvieron en laboratorio, alimentando a las larvas y adultos con hojas frescas de E. globulus, previamente lavadas con hipoclorito de sodio al 15% (Cordero y Santolamazza 2000). Los huevos y las pupas se ubicaron en placas Petri; las larvas y los adultos se mantuvieron en cajas plásticas cerradas de 20 x 15 cm. Las crianzas se hicieron en el Laboratorio de Entomología Forestal del Departamento de Silvicultura de la Facultad de Ciencias Forestales de la Universidad de Chile.
Se tomaron tres muestras de dos insectos por estado de desarrollo (huevo, larva, pupa y adulto) y se homogenizaron a 4°C en buffer (TRIS-HC1 50mM pH 8,5, EDTA 5 mM, SDS 0,07%) con un inhibidor de proteasa FMS 0,1 mM. Esta homogenización se hizo forzando los insectos a pasar por un espacio estrecho entre un émbolo de teflón y un recipiente de vidrio (Fleischer et al. 1979) y se centrifugaron 10 min a 1.250 G. Este material se refrigeró inmediatamente y se almacenó a -20°C. Luego estas muestras se maceraron y se les extrajeron las proteínas y determinó su concentración mediante el método de Bradford (1976). Los extractos de proteínas se utilizaron para determinar los perfiles electroforéticos mediante gel de poliacrilamida en condiciones desnaturalizantes (SDS-PAGE), utilizando la técnica de Laemmli (1970) y el protocolo de Bollag et al. (1996).
Perfiles electoforéticos de G. scutellatus alimentados con tres especies de eucalipto
En una segunda fase se caracterizaron electroforéticamente los perfiles de proteínas asociadas a G. scutellatus alimentados con tres especies de eucaliptos de importancia económica en Chile y que presentan algún grado de susceptibilidad a la plaga; estos son: E. globulus, E. robusta (Sm., 1793) y E. camaldulensis.
Para caracterizar electroforéticamente los perfiles de proteínas de los insectos alimentados con cada una de las especies de eucalipto, se hizo un ensayo en una jaula (1,8 x 1,5 x 1,8 m) instalada bajo condiciones naturales de clima Mediterráneo e irrigación periódica, donde se ubicaron plantas de un año (cerca de 1 m de altura) de cada especie, las que se infestaron con dos larvas por planta (5-8 mm de longitud). Las plantas se protegieron con una bolsa de tul, para evitar su escape, con una abertura longitudinal con velcro para facilitar las evaluaciones. Las larvas permanecieron en cada una de las plantas hasta que pasaron a pupa; las larvas que murieron por manipulación se reemplazaron por otras que se encontraran en la misma fase de desarrollo.
Al finalizar el ensayo con larvas se desarrolló una segunda etapa, en la que se pusieron durante un mes dos insectos adultos en las mismas plantas utilizadas en la primera parte del ensayo, para su alimentación sobre las mismas; los adultos que murieron antes del fin del ensayo se reemplazaron por otros en la misma fase de desarrollo.
Transcurrido un mes se tomaron muestras de larvas alimentadas con las diversas especies de eucalipto para hacer el análisis electroforético de proteínas. De igual forma se tomaron muestras de los adultos. Los insectos se mantuvieron 24 h en placas Petri sin alimentarse para vaciar su tubo digestivo y se homogenizaron, refrigeraron y almacenaron con los mismos procedimientos señalados anteriormente. Se maceraron varios insectos en cada muestra, cada uno de ellos alimentado con la misma especie de eucalipto. El diseño experimental para estos análisis electroforéticos tuvo dos factores de efecto fijo, el primero fue el nivel de desarrollo del insecto (larva o adulto) y el segundo, la especie de eucalipto; se realizaron tres repeticiones para cada nivel de desarrollo del insecto en cada una de las especies de plantas. A las muestras de insectos adultos y larvas se les extrajeron las proteínas y determinó su concentración mediante los mismos protocolos ya mencio-nados.
Posteriormente, se analizaron los perfiles electroforéticos de proteínas de los insectos alimentados con las especies de eucalipto, en busca de PM mediante la determinación de su posición y los cambios en su concentración y localización. La búsqueda de dichas PM se hizo mediante densitometría de geles, usando el Software BioCaptMW (versión 11.01, Microsoft, Redmond, EE.UU.) Para evaluar si existían diferencias significativas entre los resultados se hicieron pruebas de Chiβ y análisis de variación según diseño bifactorial. Además se hizo un análisis de similitud entre las PM de G. scutellatus, mediante el algoritmo de UPGMA (Sneath y Sokal 1973), usando el índice de similitud 1-Pearson r, basado en la presencia o ausencia de PM en las muestras. Se usó el programa Statistica (1993).
Resultados y Discusión
Perfiles electroforéticos de G. scutellatus alimentados con E. globulus
La composición proteica de los estados de desarrollo de G. scutellatus asociados a E. globulus se presenta en la Figura 1. Se observa una gran cantidad de bandas de proteínas en la zona comprendida entre 20 a 120 kDa, con excepción de los huevos, los que presentaron un número bajo y de pequeña intensidad de proteínas. Las proteínas se hicieron más numerosas a medida que los insectos se desarrollan. La composición proteica de las pupas fue similar a la de las larvas, probablemente porque se trató de pupas recién formadas. Sin embargo, los perfiles de las larvas y adultos tuvieron grandes diferencias.
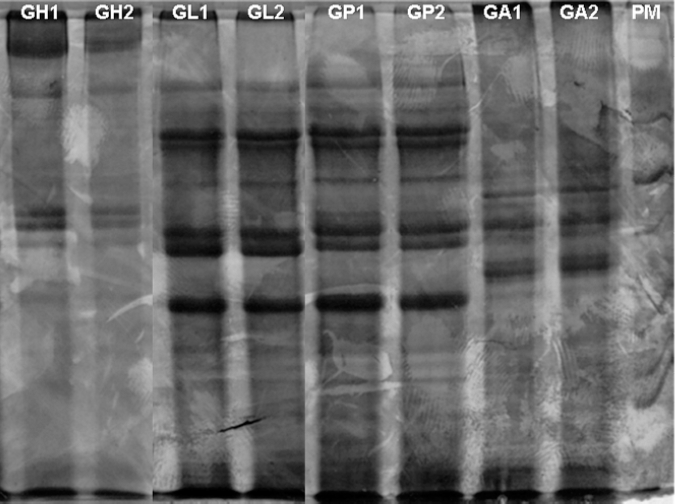
Extractos proteicos de los estados de desarrollo de G. scutellatus asociados a E. globulus. SDS-PAGE al 12,5%. GH=huevos, GL = larvas, GP = pupas y GA = adultos. Los números uno y dos son las repeticiones. PM = estándar de masa molar (kDa).
Perfiles electroforéticos de G. scutellatus alimentados con tres especies de eucalipto.
Las larvas de G scutellatus están compuestas por un número mayor de proteínas marcadoras que los adultos, independientemente de la alimentación recibida, lo que indica que la composición proteica de los insectos varía con su estado de desarrollo (Fig. 2). El mayor número de PM en las larvas puede estar relacionado con los cambios en el insecto debido a su metamorfosis; sin embargo, el número de proteínas de las larvas en E. globulus fue casi el mismo que el de los adultos, haciendo pensar que el aumento de las bandas en las larvas alimentadas con E. robusta y E. camaldulensis está más relacionado con la alimentación que recibieron los insectos que con su metamorfosis.
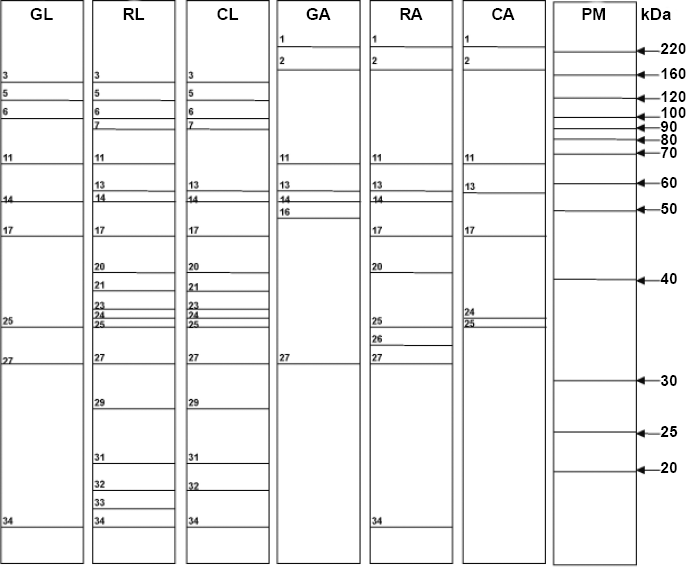
Representación idealizada de las proteínas marcadoras de acuerdo con el estado de desarrollo de G. scutellatus y la alimentación recibida. G = E. globulus, R = E. robusta, C = E. camaldulensis, L = larvas, A = adultos. PM = estándar de masa molar (kDa). Las líneas horizontales corresponden a bandas de proteínas, numeradas según su orden de aparición en el gel.
La composición proteica de las larvas alimentadas con E. globulus no difirió de la de los adultos alimentados con esta misma especie (Chiβ calculado = 0,24, g. l. = 1, P = 0,05). Por otra parte, la composición proteica de las larvas difirió de la de los adultos cuando los insectos se alimentaron con E. robusta y E. camaldulensis (Chiβ calculado = 6,72, g. 1. = 1, P = 0,05), dado el mayor número de proteínas exclusivas de las larvas frente al de los adultos (Figura 2). Esto parece indicar que las larvas de G. scutellatus son más susceptibles a los cambios en su alimentación, y modifican en mayor grado su composición proteica por este factor.
En la Figura 2 se presentan las bandas de las proteínas que tuvieron variaciones en función de la alimentación recibida, notándose que en los extractos de larvas hubo mayores cambios en proteínas que en los de adultos. Es importante resaltar que las bandas uno y dos se presentaron sólo en adultos y las bandas tres, cinco y seis sólo en larvas, independientemente de la alimentación, por lo que serían útiles tanto para identificar el estado de desarrollo de un insecto en función de su alimentación como para diseñar tácticas de tipo genético dentro del manejo integrado de plagas.
Como se mencionó, las larvas de G. scutellatus alimentadas con E. robusta y E. camaldulensis parecieron ser más susceptibles al cambio de alimentación que los adultos, ya que sólo en los extractos de larvas de estas dos especies se presentaron seis PM (proteínas siete, 21, 23, 29, 31 y 32) (Fig. 2), causando que la composición proteica de las larvas y adultos haya sido diferente. El análisis de conglomerados indicó que existen diferencias entre las PM de G. scutellatus. Las PM de las larvas alimentadas por E. camaldulensis y E. robusta son más cercanas y las más alejadas son las de E. globulus. Las PM de los adultos alimentados con las tres especies de eucalipto se agruparon en otro conglomerado (Fig. 3).
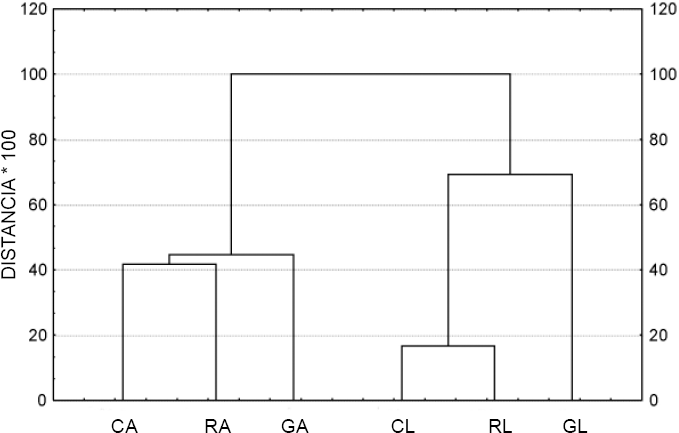
Análisis de conglomerados de las proteínas marcadoras de G. scutellatus alimentados con las tres especies de eucaliptos, construido con el método UPGMA. G = E. globulus, R = E. robusta, C = E. camaldulensis, L = larvas, A = adultos.
Por otra parte, según la cantidad de proteínas de las bandas se encontró que tanto el nivel de desarrollo del insecto (factor estado) como la alimentación recibida (factor especie) influyeron en el área de las PM (F = 8,599; g. 1. = 2; P < 0,05). Las PM de las larvas presentaron un área mayor que las correspondientes a los adultos, lo que se debe a que las larvas tuvieron más cambios en su composición proteica. Respecto a las especies, las larvas alimentadas con E. robusta presentaron la mayor cantidad de proteínas, con una media diferente a la de las alimentadas con las otras dos especies de eucalipto bajo estudio; las diferencias de las larvas alimentadas con E. robusta se relacionan con la cantidad de proteínas que varió en las alimentadas sobre esta especie, especialmente en los extractos asociados a larvas. Hubo diferencias en las PM, en función tanto del estado de desarrollo (larva o adulto) como de la alimentación recibida por los insectos, y las mayores modificaciones ocurrieron producto de la alimentación con E. robusta (Chiβ calculado = 5,23, g. l. = 1, P = 0,05; F = 8,0; g. 1. = 2; P < 0,05).
Como se observa en la Figura 2, los adultos alimentados con E. robusta tuvieron los mayores cambios en composición proteica, mientras que los alimentados con E. globulus y E. camaldulensis presentaron una variabilidad mucho menor. De las proteínas que variaron, tres se presentaron sólo en E. robusta (proteínas 20, 26 y 34), una apareció solamente en E. globulus (16), y una fue exclusiva de E. camaldulensis (24); estas proteínas serían útiles en la identificación de adultos a nivel proteico, permitiendo discriminar qué tipo de alimentación han recibido. Las proteínas 26 y 33, exclusivas de E. robusta, podrían usarse para inferir los cambios en la composición química de las larvas y adultos de G. scutellatus causados por su alimentación sobre las plantas de esta especie.
La ausencia de las proteínas 14 (E. camaldulensis), 17 (E. globulus), 25 (E. globulus) y 27 (E. camaldulensis) en adultos (Fig. 2) es también un indicador de los cambios bioquímicos del insecto a causa de su alimentación, y al igual que las proteínas que se presentan exclusivamente en un extracto, podrían usarse en su identificación.
La distribución proteica de los adultos en función de la alimentación recibida no fue diferente (Chiβ calculado = 5,23, g. l. = 2, P = 0,05), lo que se debe a que el 37,5% de las proteínas difirió entre los extractos. Cuando la prueba se aplicó sólo a las PM, se encontraron diferencias entre los extractos (Chiβ calculado = 14,24, g. l. = 2, P = 0,05), las que se relacionan con el número de proteínas que varió en los adultos alimentados con E. robusta, ya que los extractos provenientes de los insectos alimentados con las otras dos especies tuvieron la misma cantidad de PM.
Al observar la participación porcentual de las proteínas respecto al área relativa de los geles (Fig. 4), la proteína uno, proveniente de los extractos de larvas, presentó el área mayor (14,47%), seguida de las proteínas 23 (9,65%) y 30 (8,79%). Estas bandas se presentaron en todos los extractos, independientemente de la alimentación. Las bandas restantes tuvieron cantidades de proteínas inferiores a 5%. Otro hecho importante es que las PM de las larvas tuvieron áreas similares a las que no lo fueron, con porcentajes que oscilan desde 1,38% en la banda 11 hasta 4,19% en la 27. Esto indica que a pesar que no estuvieron presentes en todas las especies, la cantidad de proteínas en estas bandas no fue despreciable.
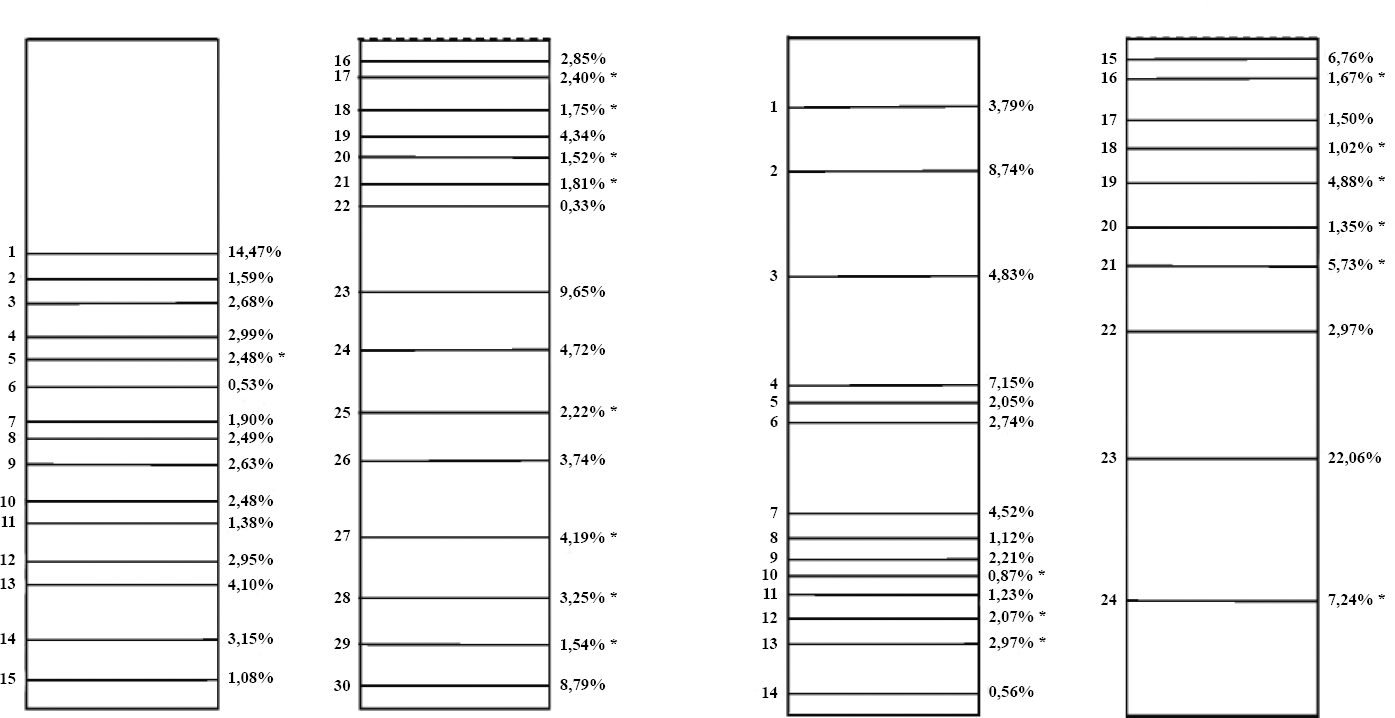
Participación porcentual de las proteínas asociadas a larvas y adultos de G. scutellatus en función del área relativa, considerando las tres especies de eucaliptos estudiadas. Las líneas horizontales corresponden a bandas de proteínas, numeradas según su orden de aparición en el gel. Las bandas con asteriscos son las proteínas marcadoras.
El área de las proteínas de las larvas difirió significa-tivamente y la interacción entre las proteínas y las especies también fue significativa; sin embargo, no hubo diferencias en el área cuando el factor evaluado fue la especie objeto de alimento de las larvas (F = 12,53; g. l. = 2; P < 0,05). En los adultos, la banda 23 tuvo la mayor cantidad de proteínas (22,06%), seguida de la banda dos (8,74%), la 24 (7,24%) y la cuatro (7,15%). Respecto de las PM de los adultos, la que obtuvo el porcentaje mayor fue la banda 21 (5,73%). Las PM restantes tuvieron valores similares a las que no presentaron variaciones, lo que indica que su participación en los geles no fue despreciable.
Según el análisis de variación para los extractos de adultos hubo una diferencia significativa entre las proteínas (F = 28,35; g. l. = 2; P<0,05), relacionada con su posición en el gel (masa molar), y una interacción entre las proteínas y las especies. Estos resultados son equivalentes a los obtenidos en los extractos proteicos de las larvas. Por otra parte, hubo diferencia en las PM de los adultos de G. scutellatus producto de su alimentación (F = 16,87; g. l. = 2; P < 0,05). Las diferencias en este factor se debieron a la mayor variación en la composición proteica de los adultos cuando se alimentaron con E. robusta, ya que las otras dos especies tuvieron el mismo número de PM.
La presencia o ausencia de bandas en los extractos proteicos de G. scutellatus puede deberse a la composición química de las hojas, lo que hace que el insecto reaccione ante la alimentación recibida (Dermott et al. 1996). En este sentido, la constitución de los aceites esenciales en las especies de Eucalyptus puede causar diferencias en la susceptibilidad al daño de un insecto en particular, las que pueden verse reflejadas en la composición química de los insectos (Floyd y Foley 2001). Kessler y Baldwin (2002) indican que la función de los metabolitos secundarios de las plantas es actuar específica-mente contra la infestación de insectos, haciendo que se reduzca su daño. Por lo tanto, estos elementos podrían estar influyendo también en la composición proteica encontrada en los extractos.
Conclusiones
Este estudio contribuye al Manejo Integrado de Plagas de este insecto, a través del conocimiento de la composición de las proteínas de G. scutellatus alimentados con diferentes especies de eucalipto, obteniendo proteínas marcadoras para las larvas y adultos. Estas proteínas están asociadas posiblemente con patrones metabólicos relacionados con el consumo de las plantas hospederas. Los cambios en la dieta del insecto podrían estar asociados con las proteínas marcadoras, indicando una habilidad diferente de G. scutellatus para poder usar las plantas hospederas.
Footnotes
Agradecimientos
Los autores agradecen al Proyecto DID I-02/6-2«Resistencia de distintas especies de Eucalyptus spp. frente al ataque del gorgojo del eucalipto (Gonipterus scutellatus, Coleoptera: Curculionidae)», financiado por la Dirección de Investigación de la Universidad de Chile.
