Abstract
Laboratory bioassays were performed to determine the susceptibility of the termite Microcerotermes sp. to the entomopathogenic fungus Paecilomyces lilacinus and Metarhizium anisopliae. The termites were collected from Eucalyptus plantations at the locality San Sebastián of Buenavista, Magdalena (Colombia). Termites were maintained in darkness at mean temperature, 25°C, and relative humidity, 59,5%. The bioassays consisted in putting worker termites in direct contact with 100% cotton canvas, impregnated with concentrations of the fungus at concentrations of 1x10¹, 1x10³, 3x101, 1x103, 3x105 conidia/ml. The agar-sand method was used to evaluate the effect of the fungus. Statistical analysis showed that there were no significant differences (X2=3,32, P=0,51) between the effects caused by P. lilacinus and the control. But, there was a significant difference in the mortality of the termites with the different concentrations, 3x108 conidia/ml being the dose that caused the highest percentages of mortality (X2=81,3, P<0,001). With M. anisopliae significant differences were observed in the mortality at the different concentrations and the control (Xβ = 320,7, P<0,001), except for 1x103 and 3x105 conidia/ml (Z = -0,97, P = 0,33). The conidiation of both fungi in the dead termites was higher at the concentration of 3x108 conidia/ml (P<0,001). The DL50 was 1,78x108 conidia/ml for P. lilacinus at two days and 0,69x10β conidia/ml for M. anisopliae at seven days.
Introducción
Las termitas son insectos que se alimentan de una gran variedad de sustratos entre ellos los lignocelulíticos, el caucho, plástico, entre otros, constituyéndose en organismos muy nocivos en los ecosistemas de zonas templadas y tropicales. (Garcés 1997; Harris 1971).
Las termitas atacan frecuentemente a Eucalyptus tereticornis, árbol utilizado ampliamente por las reforestadoras como fuente de madera, utilizando la parte seca de la corteza como fuente de alimentación y posteriormente accediendo al interior causando la muerte lenta del árbol (Berón 1983; Madrigal 1989; Garcés 1997).
Aunque en Colombia existen algunos registros sobre daños ocasionados por termitas en diversos cultivos y plantaciones de eucalipto, son muy pocos los trabajos realizados en control biológico para las termitas.
Entre las alternativas para el control biológico de estos insectos, se han realizado a nivel mundial estudios con virus (Hassan 1990), bacterias (Gavino 1984; Logan et al. 1990), nemátodos (Mix y Beal 1985; Coppel y Liang 1987) y hongos como Beauveria bassiana (Bals.)Vuill. y M. anisopliae (Metsch.) Sor. (Zoberi y Grace 1990; Fernandes y Alves 1991; Alves et al. 1995; Zoberi 1995; Milner et al. 1998a, 1998b; Shimizu y Yamaji 2002; Wright et al. 2002). Dichos estudios señalan que los hongos nativos son los agentes de control biológico más promisorios debido a que se encuentran en el mismo nicho ecológico y se replican por sí mismos, aumentando la población e infectando la colonia (Delate et al. 1995; Zoberi 1995; Madrigal 1999).
En países como Brasil, diversos grupos de investigadores han utilizado los hongos entomopatógenos contra termitas tanto en laboratorio como en campo, obteniendo porcentajes de mortalidad altos. No obstante, algunos de los resultados se han controvertido debido a que varían de acuerdo con las condiciones ambientales y con aislamientos fúngicos particulares.
Milner et al. (1998a), en Australia, realizaron pruebas in vitro y en campo con varios aislamientos de M. anisopliae sobre termitas Coptotermes spp. y Nasutitermes exitiosus encontrando que todos los aislamientos fueron patógenos siendo más susceptibles Coptotermes spp.
Los investigadores Csiro (1990), Fernándes y Alves (1991), Alves et al. (1995), Grace (1991), Grace y Zoberi (1992), Delate et al. (1995) y Zoberi (1995) observaron que las termitas Coptotermes spp., Reticulitermes flavipes y Cornitermes cumulans tratadas con M. anisopliae y B. bassiana en sus sitios de alimentación, sobre la colonia y aplicando suspensiones conidiales tópicas, murieron a causa de la invasión de los hongos. Es importante aclarar que M. anisopliae a concentraciones bajas produjo mayor mortalidad en menor tiempo que B. bassiana. Igualmente, Rosengaus (1997) demostró que la termita Zootermopsis angusticollis expuesta en papel de filtro impregnado con varias suspensiones de conidias de M. anisopliae son susceptibles a la infección por éste.
Sajap y Kaur (1990) observaron la histopatología y la ontogenia del hongo M. anisopliae sobre Coptotermes curvignathus encontrando que la mortalidad ocurrió 36-48 h postinoculación y la colonización completa de la termita no fue evidente hasta 72 h.
Estudios realizados por Khader Khan et al. (1990) y Khan et al. (1991) en termitas de cultivos agroforestales (Odontotermes brunneus, O. wallonensis y O. obesus) tratadas con los hongos: B. bassiana, M. anisopliae var. anisopliae, M. flavoviridae var. minus, Paecilomyces lilacinus y P. fumosoroseus señalaron que B. bassiana fue la más patógena.
El objetivo principal de este estudio fue evaluar la patogenicidad de dos aislamientos de los hongos entomopatógenos P. lilacinus (Thom) Samson y M. anisopliae sobre las termitas Microcerotermes sp. que atacan las plantaciones de eucalipto en la reforestadora San Sebastián de Buenavista, Magdalena.
Materiales y Métodos
Origen de los aislamientos
El estudio se realizó en el laboratorio de Micología del Instituto de Biología de la Universidad de Antioquia. Las termitas se colectaron en la reforestadora San Sebastián, ubicada en el municipio de San Sebastián de Buenavista en el departamento de Magdalena, con coordenadas latitudinales de 9°17′ norte y longitudinales de 74°32′ oeste, con un total de 7.000 hectáreas. El área se encuentra en la zona de vida Bosque Seco Tropical (bs - T) caracterizada por tener una temperatura promedio de 28,8°C, una precipitación media anual de 1,787 mm y una altitud de 25 m sobre el nivel del mar (Espinal 1990; Hernández 1993; Borreros 1996).
Colección de insectos
Las termitas se colectaron con sus respectivos sustratos (hojas, litera y suelo), fragmentos o termiteros completos. Se trasladaron al laboratorio en recipientes plásticos de 16 x 12 cm de diámetro tapados con muselina, sellados con vinilpel y envueltos en bolsas oscuras dándoles condiciones apropiadas.
En el laboratorio, las termitas se mantuvieron en recipientes plásticos dentro de una cámara climatizada (WTBbinder 78532 (Tuttlingen/Germany) con temperatura controlada de 25°C, humedad relativa de 59,5% y en oscuridad.
Origen de los hongos
El hongo P. lilacinus se aisló de muestras de suelo de las plantaciones de eucalipto de la reforestadora y se purificó realizando cultivos monospóricos, siguiendo la técnica descrita por Calle (2000). Su determinación taxonómica se realizó según criterios morfológicos y de cultivo, de acuerdo con las claves de Nelson et al. (1983), Samson et al. (1984), Domsch et al. (1993), Goettel e Inglis (1997), Papierok y Hajek (1997) y Barnett y Hunter (1998).
M. anisopliae (Ma 45), aislado de un coleóptero (de una subfamilia de la familia Melolonthidae) fue donado por CORPOICA (Corporación Colombiana de Investigación Agropecuaria Seccional Antioquia). Los hongos se cultivaron a temperatura ambiente en tubos y cajas con Agar Sabouraud Dextrosa (SDA) (Oxoid LTD., Basingstoke, Hampshire, England), durante 10-12 días antes de hacer la dilución. Además, después de las pruebas se multiplicaron en arroz acidificado (ácido láctico) y se conservaron en el laboratorio de Micología del Instituto de Biología de la Universidad de Antioquia.
Pruebas de Patogenicidad
Preparación de la suspensión de conidios
A partir de los cultivos en SDA se realizaron diluciones para obtener las concentraciones de 1x10¹, 1x10³, 3x105, 1x107, 3x108 conidios/ml según la metodología de Goettel e Inglis (1997) y Pérez (1997).
Bioensayo
Se utilizaron las concentraciones 1x10¹, 1x10³, 3x105, 1x107, 3x108 conidios/ml, que fueron vertidas en cajas de vidrio previamente esterilizadas donde se sumergieron las lonas (100% de algodón) durante 4 min. Los ensayos se realizaron con termitas obreros. Estos se introdujeron en frascos oscuros de vidrio de 9 x 8 cm preparados con las lonas y de acuerdo con la metodología de agar-arena de Staples y Milner (2000). Se realizaron cuatro repeticiones, cada una con 30 termitas obreros, por cada una de las concentraciones de los hongos y un lote de testigos (lona tratada con agua destilada estéril).
Las termitas tratadas se mantuvieron en condiciones de oscuridad en una cámara climatizada (WTBbinder 78532 (Tuttlingen/Germany), a una temperatura de 25°C y una humedad relativa de 59,5%.
La supervivencia de las termitas se verificó durante 10 días contando el número de individuos muertos y calculando el porcentaje de mortalidad diaria y acumulada. Los cadáveres se colocaron en cámara húmeda y se incubaron a temperatura ambiente (22°C) durante 10 días, para favorecer la conidiación del hongo y verificar la muerte por el mismo (mortalidad intrínseca). A todos los insectos muertos y colonizados por el hongo se les realizaron montajes en placa microscópica con azul de lactofenol, KOH y cultivos para observar las diferentes estructuras morfológicas y verificar la presencia e identidad del mismo (Goettel e Inglis 1997).
Análisis estadístico
Para cada concentración de los conidios de P. lilacinus y M. anisopliae, se analizó la patogenicidad de las termitas tomando como criterio el porcentaje de mortalidad. La mortalidad diaria de las termitas se comparó mediante las curvas de supervivencia de Kaplan-Meier y utilizando la prueba generalizada de Gehan. Mediante estas curvas se estimaron también los TL50 para cada concentración. La CL50 se estimó con el análisis Probit según Wardlaw (1987). Se consideró α=0,05 como el nivel de significancia estadística y se calculó la corrección de Bonferroni en la comparación de las curvas de supervivencia. La mortalidad corregida fue determinada según el método de Schneider - Orelli (CYBA GEIGY 1981).
Resultados y Discusión
Patogenicidad del aislamiento de P. lilacinus y M. anisopliae sobre obreros Microcerotermes sp.
En el aislamiento de P. lilacinus no se observaron diferencias significativas en la sobrevivencia de las termitas tratadas con dosis entre 1x10¹ y 1x107 conidios/ml. No obstante, al comparar la sobrevivencia de las termitas tratadas con la concentración de 3x108 conidios con las demás, se encontraron niveles de significancia (Xβ = 81,3; P<0,001). Con esta concentración se obtuvieron los valores más bajos de sobrevivencia: 2,5% a los cuatro días. Esto se evidencia en la gráfica de sobrevivencia acumulada (Fig. 1) en la cual los porcentajes similares se obtuvieron entre el 8º y 10 día con las demás dosis.
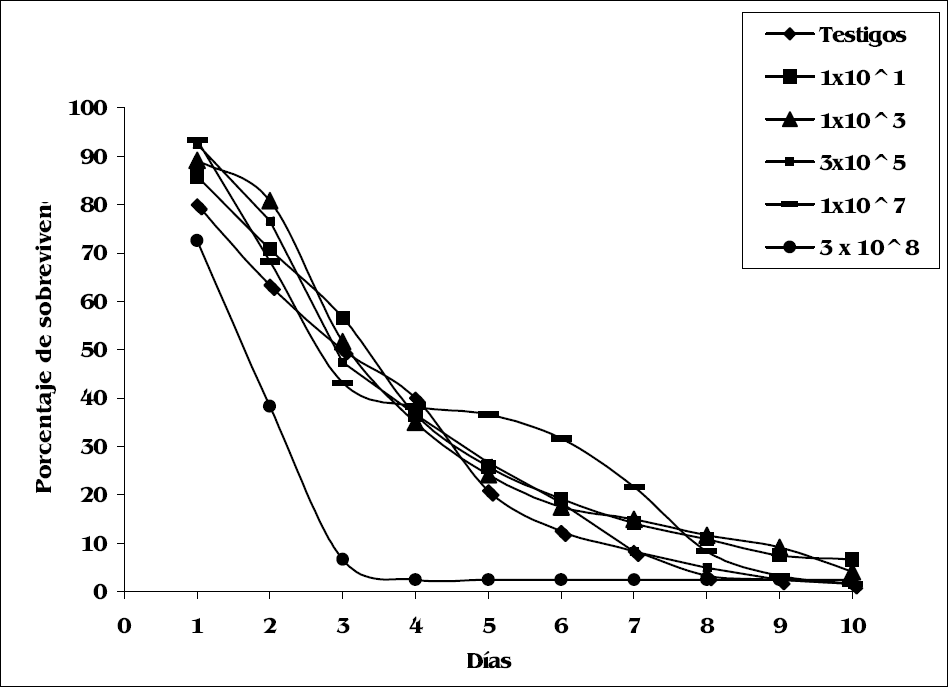
Evolución de la sobrevivencia de obreros Microcerotermes sp. en presencia de P. lilacinus en función del tiempo y la dosis aplicada.
Resultados similares se encontraron para el aislamiento de M. anisopliae, ya que la dosis de 3x108 conidios/ml originó los niveles más bajos de sobrevivencia en las termitas al quinto día después del tratamiento. Valores tan bajos de sobrevivencia sólo se observaron con las demás dosis entre 8 y 10 días después del tratamiento. Sin embargo, para las dosis 3x105 y 1x10¹ conidios/ml los períodos de sobrevivencia fueron mayores a los 10 días (Fig. 2).
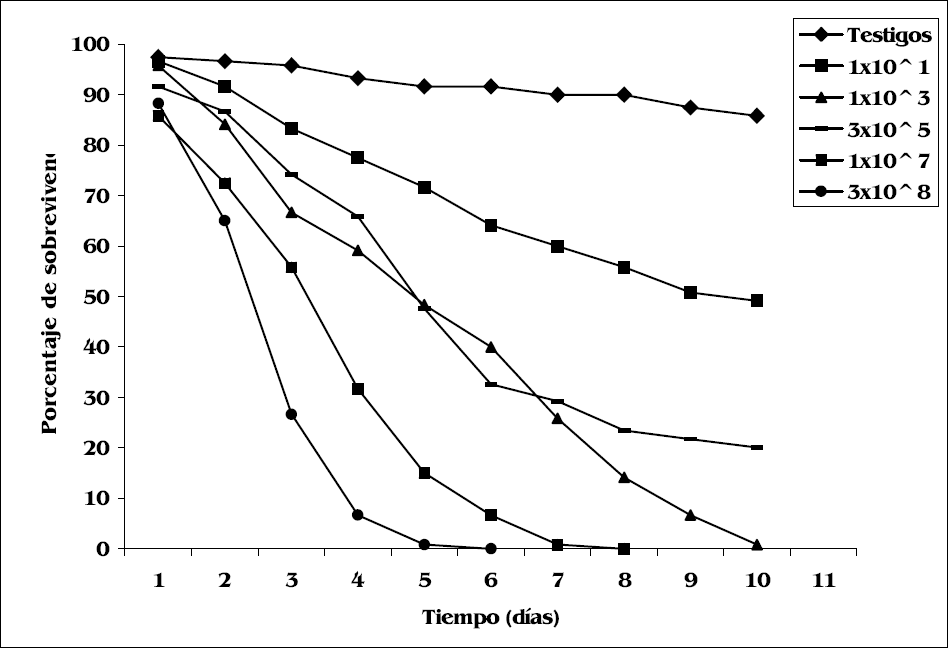
Evolución de la sobrevivencia de obreros Microcerotermes sp. en presencia de M. anisopliae en función del tiempo y la dosis aplicada.
Se observaron diferencias significativas en la sobrevivencia de las termitas tratadas con todas las dosis de M. anisopliae (Xβ=320,7; P<0,001) excepto entre 1x10³ y 3x105 conidios/ml. Con excepción de la dosis 3x105 conidios/ml hubo correspondencia entre la dosis y la mortalidad.
Las diferencias en tiempo de sobrevivencia relacionadas con la dosis de tratamiento son relevantes cuando se realizan bioensayos con entomopatógenos, ya que el tiempo es considerado como un factor real de respuesta al agente (Matthews 1997). Para el presente estudio, con base en la sobrevivencia en función de la dosis y el tiempo, la respuesta de las termitas al agente se observó en menor tiempo para el hongo Paecilomyces que para Metarhizium.
En estudios similares con M. anisopliae sobre Macrotermes subhyalinus los tiempos promedios de sobrevivencia de las termitas variaron entre dos y ocho días después del tratamiento (Abebe 2002). El tiempo promedio de sobrevivencia varió dependiendo del aislamiento. En la presente investigación los rangos de sobrevivencia variaron entre 4 y 10 días para Paecilomyces. Para M. anisopliae los rangos fueron mayores ya que en el día 10 se observaron altos porcentajes de sobrevivencia para las dosis 1x10¹ (52%) y 3x105 conidios/ml (21%).
Capacidad de conidiación de P. lilacinus y M. anisopliae sobre cadáveres de Microcerotermes sp.
En la figura 3 se observa el porcentaje de termitas conidiadas cuando se trataron con P. lilacinus. De las 600 termitas tratadas con P. lilacinus, 433 presentaron invasión por el hongo. En general, la conidiación sobre los cadáveres se observó desde el primer día después de la muerte. Para la dosis 3x108 conidios/ml, que causó los porcentajes más altos de mortalidad en el menor tiempo, se observó el mayor número de termitas colonizadas por el hongo encontrándose diferencias significativas con respecto a las demás dosis (Xβ= 89,6; P<0,001).
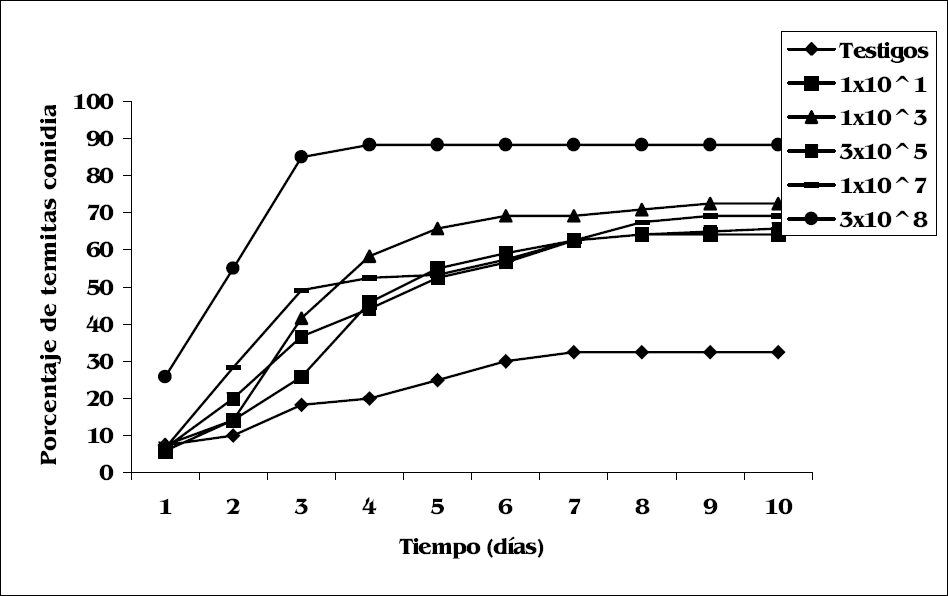
Evolución de la conidiación de P. lilacinus sobre termitas obreros Microcerotermes sp. en función del tiempo y la dosis aplicada.
Es de mencionar que el hongo P. lilacinus esporuló en un 30% de las termitas testigo, lo cual sugiere una probable contaminación mecánica o por manipulación con el hongo (Carvajal 2002). Este valor explica, en parte, los bajos porcentajes de sobrevivencia del testigo que se observaron en el bioensayo.
Para el caso de M. anisopliae, de 600 termitas tratadas, 199 fueron colonizadas por el hongo; el mayor porcentaje de termitas conidiadas se obtuvo con la dosis de 3x108 conidios/ml, pero la aparición del micelio sólo se observó a partir del quinto día (Fig. 4) y al segundo día en P. lilacinus con la misma dosis (Fig. 3). Patcharin (1996) observó que M. anisopliae en termitas Coptotermes sp. y Microcerotermes sp. murieron después de dos días de postinoculación y a los 7 días se desarrolló el micelio blanco y el verde alrededor de los cadáveres. Ambos aislamientos en este estudio causaron micosis a las termitas; sin embargo, P. lilacinus invadió los cadáveres en menor tiempo.
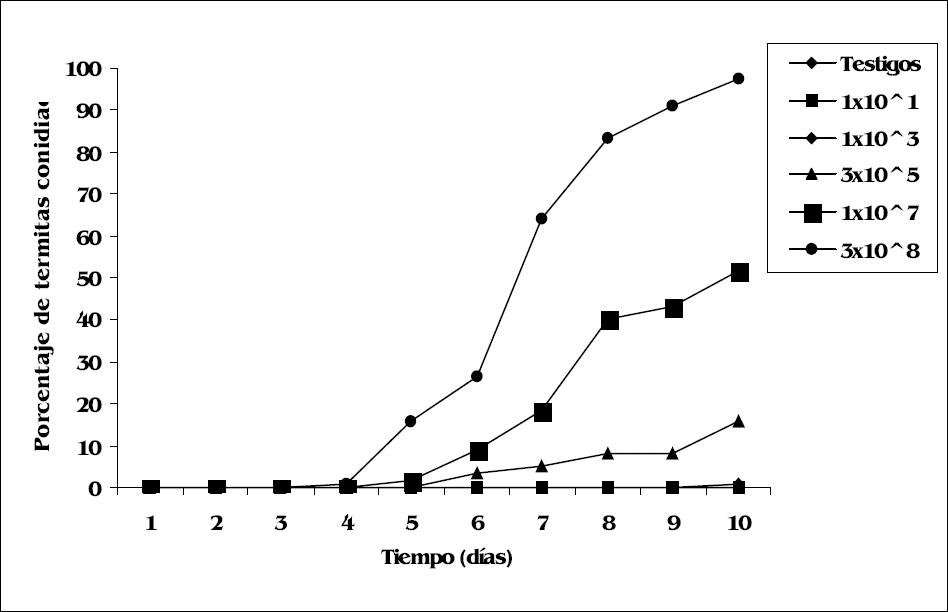
Evolución de la conidiación de M. anisopliae sobre termitas obreros Microcerotermes sp. en función del tiempo y la dosis aplicada.
El hecho de que el hongo invada los cadáveres es de gran importancia, ya que la posibilidad de la transmisión de la micosis a partir de termitas enfermas sería una forma exitosa de acceder a las partes de la colonia y el nido, que no son accesibles por tratamiento directo (Fig. 5). Adicionalmente, el tiempo de conidiación sobre los cadáveres puede influir sobre la diseminación y contagio de termitas sanas a partir de termitas infectadas (Rosengaus et al. 1998; Rath 2000).
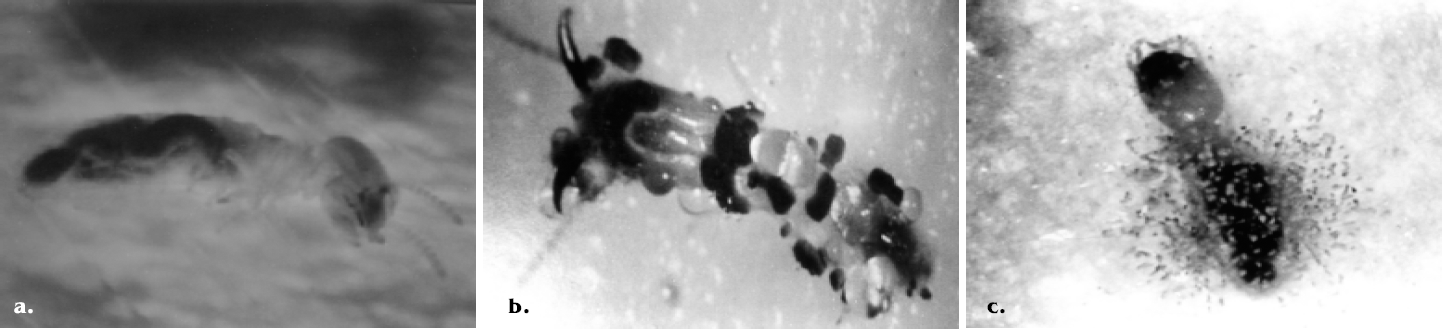
a. Microcerotermes sp. Obrero testigo, b. Microcerotermes sp. Soldado tratado con M. anisopliae, c. Microcerotermes sp. Obrero tratado con P. lilacinus.
Concentración letal mediana (CL50) del aislamiento de P. lilacinus y de M. anisopliae y tiempo letal medio (TL50) de las concentraciones utilizadas
La dosis letal 50 (DL50) para P. lilacinus fue de 1,78X108 conidios/ml en 2 días con un intervalo de confianza del 95%: (0,44; 3,59) x 108 conidios/ml. El tiempo de TL50 fue de 3 días para todas las concentraciones excepto para 3 x108 conidios/ml (dos días).
Para M. anisopliae la dosis letal 50 (DL50) fue de 0,69x10β conidios/ml pero en un tiempo de 7 días con un intervalo de confianza del 95%: (0,33; 1,44) x 10β conidios/ml. El tiempo letal 50 (TL50) fue de 5 días para las concentraciones 1x10³ y 3x105 conidios/ml y de 3 días para la concentración de 3x108 conidios/ml.
De acuerdo con los resultados, las termitas del género Microcerotermes son susceptibles a los aislamientos de P. lilacinus y M. anisopliae. Tomando como criterios la sobrevivencia, la conidiación del hongo en los cadáveres, el tiempo promedio de invasión y el TL50 y DL50, P. lilacinus aparece como mejor candidato que M. anisopliae como agente potencial de control microbiológico de termitas. Los tiempos de respuesta tanto en la mortalidad, como en la conidiación y en la efectividad para matar el 50% de la población tratada así lo confirman. Las diferencias podrían explicarse teniendo en cuenta aspectos como la procedencia de los aislamientos. P. lilacinus fue aislado directamente de la zona de hojas de eucalipto mientras que M. anisopliae se aisló de un coleóptero de una subfamilia de la familia Melolonthidae donado por CORPOICA. La patogenicidad varía de acuerdo con el sustrato de procedencia, su nicho ecológico y por lo tanto sus condiciones fisiológicas y metabólicas.
Aunque hongos entomopatógenos como M. anisopliae han sido utilizados con éxito para el control de termitas en Brasil, es necesario realizar pruebas en campo bajo las condiciones del país y considerar aspectos propios del ecosistema, el aislamiento fúngico y el comportamiento de las termitas, que podrían afectar los resultados (Shimizu y Yamaji 2003; Sun et al. 2003; Abebe 2002; Myles 2002; Traniello et al. 2002).
Conclusiones
Las termitas obreros Microcerotermes spp. presentaron una susceptibilidad similar para P. lilacinus y M. anisopliae, por lo cual podrían ser considerados como agentes potenciales de control biológico.
La mortalidad en las termitas obreros Microcerotermes spp. fue atribuida a la conidiación causada por ambos aislamientos debido a que éstos fueron recuperados de los cadáveres de los insectos.
Footnotes
Agradecimientos
Los autores agradecen al profesor Abel Díaz Cadavid y a Camilo Quintero por el análisis estadístico y elaboración de tablas y gráficos, respectivamente. A los compañeros del laboratorio de Micología de la Universidad de Antioquia por su aporte técnico y logístico en el desarrollo de esta investigación. Se agradece a la Corporación de Patologías Tropicales, al Instituto de Biología de la Facultad de Ciencias Exactas y Naturales, al CODI de la Universidad de Antioquia y al Posgrado de Entomología de la Universidad Nacional por su apoyo y financiación. Se agradece de manera muy especial al personal de la Reforestadora San Sebastián de Buenavista, Magdalena (Colombia) por su hospitalidad y ayuda en el trabajo de campo.
