Abstract
The communities of benthic macroinvertebrates (BMI) can be used as efficient biological indicators of the water quality in fresh aquatic ecosystems. Between October 2002 and September 2003, evaluations of MIB were developed in the Rímac River downstream from Atarjea, Lima-Callao, Peru. The objective was to analyze their faunistic composition, richness of families and water quality, based on the modified Biological Monitoring Working Party index (BMWP’ modified). The evaluation was conducted in six sampling stations located along the course of the Rimac river that crosses Lima and Callao. Thirty-five taxa of BMI were reported: Hexapoda (27), Annelida (2), Mollusca (2), Arachnidae (2), Plathyhelmintes (1) and Chilopoda (1). From 2,166 specimens collected, Oligochaeta (n = 597) had the higher absolute abundance, followed by Psychodidae (n = 521), Physidae (n = 442), Chironomidae (n = 300), and Dixidae (n = 168). The modified BMWP’ index scored the water of Rimac River downstream from Atarjea as critical quality or very polluted waters (29 points). Of all the physicochemical analyses evaluated, Biochemical Oxygen Demand indicated perturbance effects in this freshwater ecosystem. Finally, the potential of the BMI to evaluate the water quality of the rivers in Peru is analyzed.
Introducción
Las comunidades de macroinvertebrados bentónicos (MIB) empleados como bioindicadores acuáticos vienen aumentando en estos últimos años en lo que respecta a la protección y restauración de los ambientes acuáticos (Brown
Muchos representantes de estos grupos de invertebrados pueden distribuirse en distintos tipos de condiciones ambientales, así como ser muy susceptibles a la contaminación, motivo por el cual son recomendados en el establecimiento de sistemas de vigilancia y control de los ecosistemas hídricos (Leslie
Se han empleado los índices de diversidad y bióticos usando a los insectos acuáticos para caracterizar biológicamente los cuerpos de agua dulce (Iannacone
Materiales y Métodos
Zona de estudio
Incluyeron seis estaciones de muestreo establecidas en la trayectoria del río Rímac desde las inmediaciones del puente Graña (Estación 6), cercana a la sede de captación o bocatoma de la Atarjea de SEDAPAL en el distrito de El Agustino, Lima, Perú hasta las cercanías del puente Gambeta (Estación 1), en el Callao, próxima a la desembocadura al mar (Fig. 1) Este recorrido tiene aproximadamente 17,5 Km de longitud, con una pendiente aproximada de 1,1 % y disminuyendo desde los 195 a los 0 msnm (Fig. 1). Se determinó la ubicación geográfica de cada una de las estaciones de muestreo con un GPS 12 Garmin (Fig. 1). El río Rímac es considerado de cuarto orden según la clasificación de Strahler (Wetzel y Likens 2000).
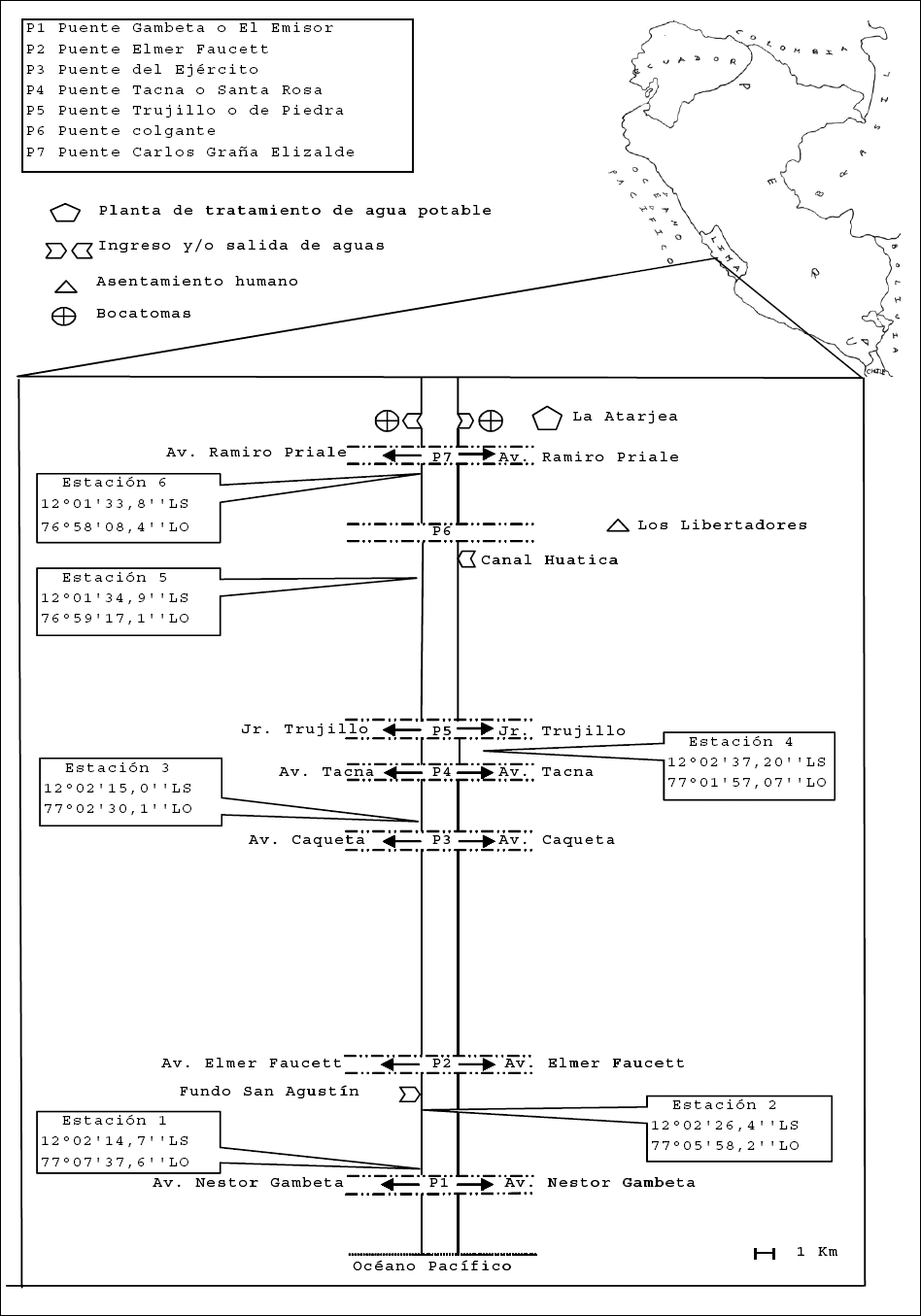
Estaciones de muestreo en el río Rímac, Lima, Perú.
Muestreos
Se realizaron muestreos mensuales entre Octubre 2002 y Setiembre 2003. Los análisis fisicoquímicos incluyeron mediciones de: pH y conductividad eléctrica (CE: ohm.cm-2) mediante instrumentales portátiles marca Hanna®, temperatura en °C mediante un termómetro de mercurio. Los datos de caudal (m³.s-1) y de velocidad superficial promedio (m.s−1) del río se obtuvieron siguiendo el método propuesto por Lind (1979). El Oxígeno Disuelto (OD) y la Demanda Bioquímica de Oxígeno (DBO5,20) en mg L siguieron el protocolo propuesto por Winkler (APHA 1995).
El procesamiento de las muestras se realizó en el laboratorio de Ecofisiología Animal, Facultad de Ciencias Naturales y Matemáticas, Universidad Nacional Federico Villarreal, Pueblo Libre, Lima, Perú. Para tomar las muestras biológicas en las estaciones de estudio se emplearon: el método manual y la técnica rápida de Hynes modificada, con un muestreador Surber modificado, una red estándar de 30 x 30 cmβ con abertura de 1 mm (Paredes
Análisis de datos
Se empleó el análisis de componentes principales (ACP) como un criterio de reducción y ordenación de los siete parámetros fisicoquímicos y de los catorce índices de diversidad alfa, obtenidos de cada una de las seis estaciones de muestreo, para producir variables compuestas no relacionadas. Se realizó la rotación varimax para facilitar la interpretación de los componentes del ACP (Zar 1996; Vivanco 1999). Se utilizó el coeficiente de correlación de Pearson entre los índices bióticos y algunos taxa más abundantes. Se aplicó el índice biótico BMWP´ modificado por Zúñiga de Cardoso
Puntuaciones asignadas a las diferentes familias de MIB para la obtención del índice BMWP’ modif.
Clase
Valoración de calidad de agua para la obtención del BMWP’ modif. (Domínguez y Fernández 1998)
Resultados y discusión
Los promedios de siete parámetros fisicoquímicos evaluados mensualmente de Octubre 2002 a Setiembre del 2003 son señalados en la Tabla 3. La DBO5,20, para las estaciones uno a la cinco, indicó perturbación e impacto en el río Rímac. El valor promedio anual obtenido en este estudio fue más alto que el valor permisible por la Ley General de Aguas (LGA) peruana vigente. El coeficiente de variación (CV) se vio incrementado expresamente para este parámetro (Tabla 3). La estación dos presentó niveles de degradación ambiental en términos de DBO5,20, OD y CE, aparentemente como consecuencia de los efluentes vertidos por las inmediaciones del fundo San Agustín (Callao). Tanto el OD y el pH se encontraron dentro del límite permisible por la LGA peruana vigente. Hay que resaltar que a pesar de la pendiente que presenta el río Rímac en la zona de estudio (1,1 %) y además de la presencia de pantallas, que logran incrementar la velocidad superficial del agua y los niveles de oxígeno, estos no son suficientes para oxidar la tremenda carga orgánica disuelta en sus aguas como lo demuestran los niveles de DBO5,20 (Tabla 3).
Parámetros fisicoquímicos por estaciones de muestreo en el río Rímac, Lima-Callao, Perú.
Prom.: Promedio, DE: Desviación estándar, CV: Coeficiente de Variación. CE: Conductividad específica, OD: Oxígeno disuelto, DBO5,20: Demanda bioquímica de oxígeno.
El ACP produjo tres componentes con Eigenvalues > 1 para los parámetros fisicoquímicos (Tabla 4). Los parámetros fisicoquímicos fueron ordenados en un espacio de dos dimensiones, de acuerdo con el ACP (Fig. 2). La velocidad, DBO, CE y OD del agua estuvieron correlacionados con el primer componente que explicó el 64,804 % de la variabilidad. El caudal y pH estuvieron correlacionados con el segundo componente que explicó el 18,245 % de la variabilidad (Tabla 4). El tercer componente describió la variación en la temperatura del agua (Tabla 4). El CP1 va en relación con el factor oxígeno. Muy correlacionado al OD se encuentra la DBO, esta última a su vez esta relacionada con la carga orgánica que afecta a la CE. Finalmente, la velocidad del cuerpo de agua permite el ingreso de dosis importantes de oxígeno superficial al cuerpo de agua lótico. EL CP2 correlaciona el caudal y el pH. El caudal se incrementa o se reduce, por la incorporación de aguas residuales de distintos tipos que caracterizan las seis estaciones, ya sea industrial, doméstica o agrícola, y que indudablemente afectan los niveles de pH (Bispo
Resumen del análisis de componentes principales (CP) de los parámetros fisicoquímicos.
Los valores más altos en cada componente para cada variable son mostrados en negrita.
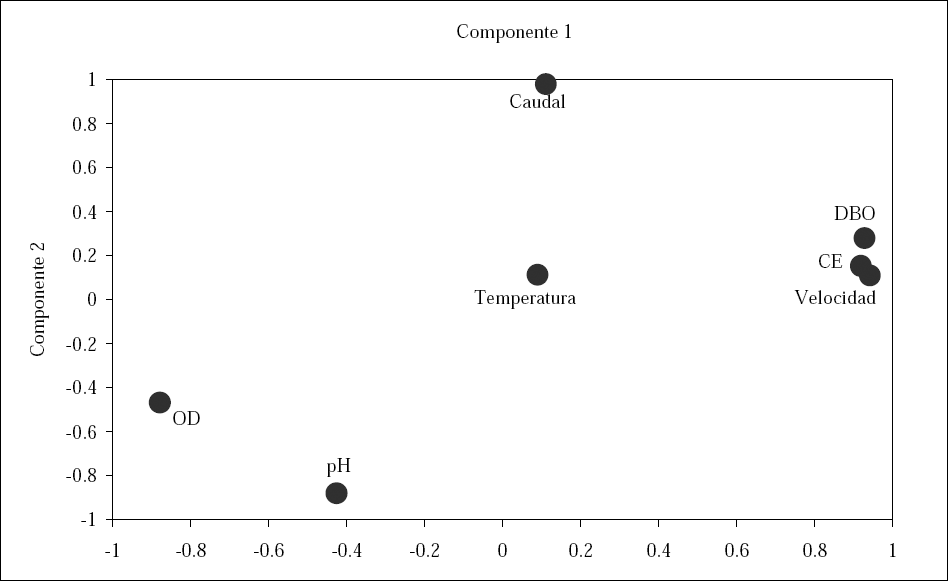
Ordenación de ACP de los parámetros fisicoquímicos del río Rímac, Lima, Perú.
Se registraron 35 taxa con predominancia de Oligochaeta (28 %), Psychodidae (24 %), Physidae (20 %), Chironomidae (14 %) y Dixidae (8 %) (Tabla 5). Los cinco taxones más abundantes presentaron una distribución espacial contagiosa por presentar una relación S2/ X > 1, como Oligochaeta (49,9), Psychodidae (194,8), Physidae (203,5), Chironomidae (56,2) y Dixidae (36,7). Los cuatro primeros taxa son considerados tolerantes y capaces de habitar en lugares con elevadas concentraciones de detritus orgánico que forma parte de su dieta y en tenores de concentración de oxígeno bajos (Figueroa
Abundancia de macroorganismos por estaciones de muestreo colectados en el río Rímac, Lima-Callao, Perú. Muchos de ellos son Macroinvertebrados Bentónicos (MIB)
No todos los taxa son órdenes o familia. *Phylum **Clase ***Subclase ****Orden *****Suborden ******Género
Familia no acuática, foránea al sistema pudo caer en las trampas por accidente.
Se obtuvo un puntaje biótico de 29 (Tabla 6), que según el BMWP’ modif. caracteriza al río Rímac como de calidad crítica o de aguas muy contaminadas (Tabla 2). Según el puntaje obtenido para cada estación, se puede observar que las estaciones uno y dos presentan aguas fuertemente contaminadas o de calidad muy crítica, las estaciones tres y cuatro presentan aguas muy contaminadas o de calidad crítica, y las estaciones cinco y seis presentan aguas contaminadas o de calidad dudosa (Tabla 2). Es importante mencionar que sólo las estaciones cinco y seis cuentan con cercos perimétricos que de alguna manera impiden una mayor influencia antrópica. La Tabla 6 muestra los 14 índices bióticos empleados en el estudio de ecosistemas acuáticos. Podemos notar comparando los índices de dominancia evaluados que existe una notable variación. El valor promedio anual del índice de Simpson (C) y el de Berger-Parker (d) podrían estar diagnosticando buena calidad a las aguas evaluadas, en contraste, para el índice de McIntosh (D) éstas son de pobre calidad. Tal incongruencia de resultados se observa también para el índice de Goodnight y Whittley, el cual valora a las aguas del río Rímac como de buena condición. Finalmente, evaluando el índice de Shannon-Wiener (H) (1,85), el río Rímac presentaría aguas moderadamente contaminadas (Tabla 6). Según Oliveira y Bispo (2001) las variaciones en la abundancia de los MIB pueden atribuirse a la disponibilidad de recursos, competencia, depredación y el ciclo de vida. Sin embargo, en ambientes donde impera la degradación ambiental, es importante considerar el efecto antrópico del mismo en la comunidad biótica, la cual evidentemente determina la distribución y estructura de los MIB (Riss
índices bióticos de diversidad alfa (α) de familias para el río Rímac, Lima-Callao, Perú.
De los cinco taxa más abundantes como lo valora el N2 de la serie de Hill, solo la familia Chironomidae obtuvo una correlación positiva significativa con la BMWP’ (r = 0,87; p = 0,02). Los otros cuatro taxa abundantes no presentaron correlaciones con la BMWP’. La DBO2 encontró una correlación negativa con BMWP′ (r = -0,82; p = 0,04) y con H (r = -0,81; p = 0,04); y solo con el taxa Psychodidae una correlación positiva (r = 0,98; p ≤ 0.05). Los otros cuatro taxa abundantes no presentaron correlación significativa con la DBO2 Por otro lado, Dixidae y Oligochaeta presentaron una correlación positiva (r = 0,88; p = 0,02). El aumento de la abundancia de Chironomidae resultó en un aumento en la BMWP’. Hecho que no coincide con lo referido por algunos autores (Figueroa
En adición, se nota la presencia de la familia Dixidae en un ecosistema netamente lótico, cuando esta familia se encuentra relacionada con ambientes lénticos, como lo afirman Merritt y Cummins (1996). Posiblemente han sido traídos por arrastre al río Rímac o quizá estaríamos tratando con una excepción del comportamiento de la familia, lo cuál también quedaría para ser dilucidado en próximos estudios.
Los dendrogramas cualitativos y cuantitativos construidos con base en los índices de diversidad beta evaluados para comparar las estaciones de muestreo se aprecian en las Figuras. 3 y 4. El análisis cualitativo agrupó dos sectores, el primero conformado por las estaciones cuatro, cinco y seis, y el segundo conformado por las estaciones uno, dos y tres; distinguiéndose a sí un sector alto y uno bajo, éste último más comprometido con la actividad antrópica. El análisis cuantitativo agrupó las estaciones en tres sectores diferenciables; el primer sector conformado por las estaciones tres y cuatro, de bastante similitud; el segundo sector conformado por las estaciones uno y cinco, de regular similitud; finalmente el sector conformado por las estaciones dos y seis, de poca similitud. La estación dos presenta el mayor grado de degradación ambiental y en contraste la estación seis presentó el menor (Figs. 3-4).
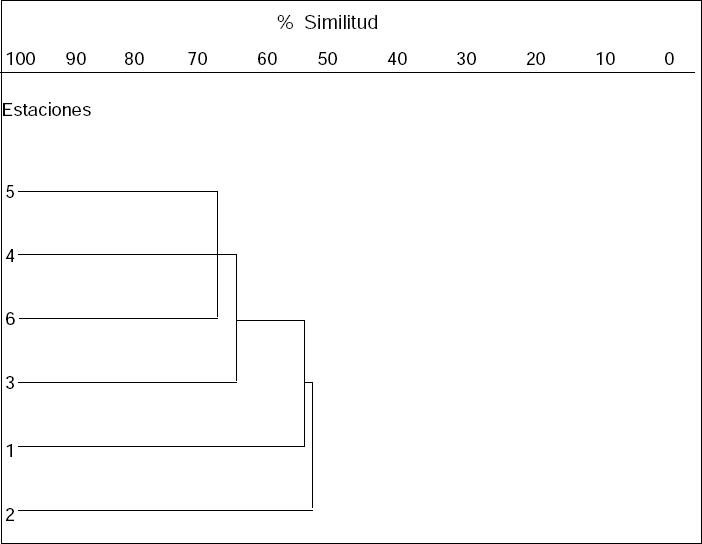
Análisis cualitativo de similitud empleando el índice de Sörensen para las estaciones de muestreo en el río Rímac. 1. Puente Graña; 2. Canal Huatica; 3. Puente Trujillo; 4. Puente del Ejército; 5. Puente Faucett; 6. Puente Gambeta.
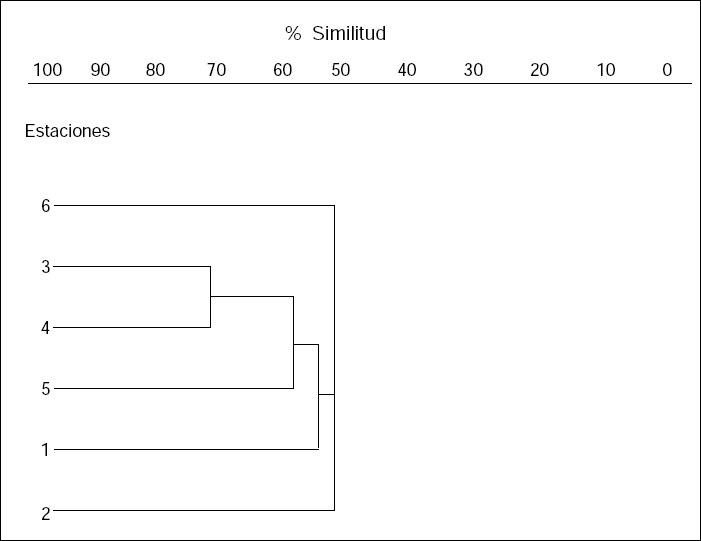
Análisis cuantitativo de similitud empleando el índice de Sörensen para las estaciones de muestreo en el río Rímac. 1. Puente Graña; 2. Canal Huatica; 3. Puente Trujillo; 4. Puente del Ejército; 5. Puente Faucett; 6. Puente Gambeta.
El ACP produjo dos componentes con Eigenvalues > 1 para los índices bióticos (Tabla 7). Los índices bióticos de diversidad alfa fueron ordenados en un espacio de dos dimensiones, de acuerdo al ACP (Tabla 7; Fig. 5). Ocho índices bióticos (Números de Hill-N1, McIntosh, Números de Hill-N2, Simpson, Pielou, Berger-Parker, Shannon-Wiener, Margalef, Goodnight & Whittley, Números de Hill-N0) estuvieron correlacionados con el primer componente, que explicó el 71,084 % de la variabilidad. Otros cuatro índices bióticos (ETP/ ETP + Chironomidae, ETP/Chironomidae, % Chironomidae en Diptera, BMWP’ modif.) estuvieron correlacionados con el segundo componente, que explicó el 20,323 % de la variabilidad (Tabla 7).
Resumen del análisis de componentes principales (CP) de los índices bióticos de diversidad alfa (α).
Los valores más altos en cada componente para cada variable son mostrados en negrita.
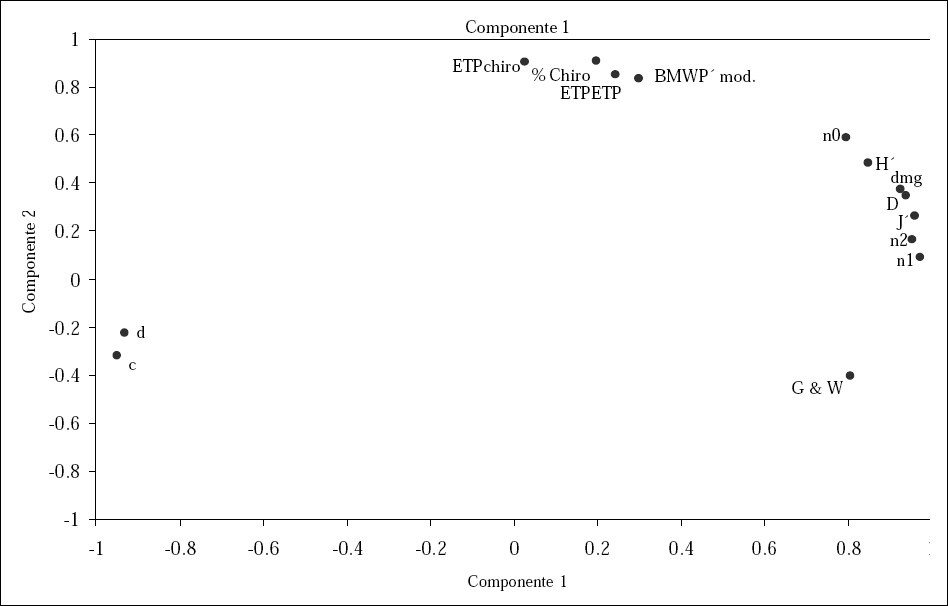
Ordenación de ACP de los índices bióticos de la diversidad alfa de los MIB del río Rímac, Lima, Perú. ETPchiro = ETP/Chironomidae. ETP/ETP = ETP/ETP + Chironomidae. % Chiro = % Chironomidae en Diptera. G y W = Goodnight y Whittley. H'= Shannon-Wiener. C = Simpson. J'= Pielou. Dmg = Margalef. D = McIntosh. d = Berger-Parker. N = Números de Hill- No. N1 = Números de Hill-N1. N2 = Números de Hill-N2.
El estudio de los MIB como organismos indicadores de calidad de agua permite estimar si han sido afectados por cambios físicos o químicos de su hábitat, pero no indica cual es la causa específica que los afecta, lo cual debe ser estimado mediante asociación con información del hábitat físico (e.g. substrato de fondo, velocidad de corrientes, profundidad) y con potenciales fuentes de estrés (e.g. contaminantes acuáticos) (Figueroa
Los resultados sugieren que el BMWP´ es un buen indicador de la calidad de las aguas del río Rímac. Sin embargo, la aplicación del BMWP´ en otras cuencas debiera realizarse con precaución debido a que pueden existir factores diferentes que pudieran afectar a las comunidades acuáticas. Al respecto se sugiere complementar el estudio de los MIB con adecuadas caracterizaciones de la columna de agua, ictiofauna, actividades productivas desarrolladas en la cuenca y evaluaciones experimentales de taxa locales frente a diferentes tipos de contaminantes (Figueroa
Conclusiones
Se registraron 35 familias de macroinvertebrados bentónicos (MIB): Hexapoda (27), Annelidae (2), Mollusca (2), Arachnidae (2), Plathyhelmintes (1) y Chilopoda (1). De los 2.166 especímenes coleccionados Oligochaeta obtuvo la mayor abundancia absoluta; seguido por Psychodidae, Physidae, Chironomidae y Dixidae.
El índice Biological Monitoring Working Party modificado (BMWP´ modif.), valoró el agua del Río Rímac, aguas abajo de la Atarjea, como de calidad crítica o de aguas muy contaminadas (29 puntos).
La Demanda Bioquímica de Oxígeno (DBO5,20), indicó efectos de perturbación en el ecosistema acuático.
Footnotes
Agradecimientos
A Álvaro Torres, Maria Isabel La Torre, Rafael La Rosa, Alfonso Lizarraga, Carlos Santa Cruz, Ana Gutiérrez, Margarita Robles, Augusto Mendoza, Edith Aguilar, Ana Carolina Paucar, Vicenta Morales, Jorge De la Cruz, Eric Carreño, María del Carmen León, Francisco Valdez, Denia Salinas, Pedro José Paredes, Fabiola Isabel Correa, Gloria Asunción Espinal, Víctor Miguel Espinal, Adrián Ernesto Paredes y Óscar Iván García por su ayuda y apoyo en esta investigación.
