Abstract
The genomic DNA was extracted from 20 Aedes aegypti mosquitoes of the Rockefeller strain. The results from a modified protocol for DNA extraction of mosquitoes were evaluated. The modification of the method consisted in grinding up samples in liquid nitrogen before the extraction of genetic material. The results demonstrated that through the modified protocol genetic material was obtained with higher yield (9.55) and concentration (0.46 µg/µl) than the original method. It was corroborated that the resulting DNA was of sufficient quality for RAPD technology and probably other molecular based techniques based on PCR amplification. These results will be used in future genetic studies on Ae. aegypti, the principal vector of dengue.
Introducción
Aedes aegypti (L.) es el responsable directo de la transmisión de los cuatro serotipos del virus del Dengue, por lo que se considera como el principal vector en América Latina (Soper 1967). El rango de muchas poblaciones de este género no es estático y recientemente se ha extendido por los países de Asia y América Latina, incrementando el riesgo del dengue en esas regiones. La reducción de los criaderos del vector, los programas de saneamiento ambiental con la participación comunitaria, son continuos esfuerzos que se han desarrollado para el control del mismo; sin embargo estos no han sido suficientes para la lucha contra el principal vector del dengue (Rodríguez et al. 2004). Las técnicas moleculares aportan importantes resultados que pueden ser utilizados para la confección de estrategias de control de las poblaciones de mosquitos. Estas metodologías han ayudado al entendimiento de los procesos bioquímicos, moleculares y fisiológicos de este importante vector (Hemingway et al. 1998).
La extracción del ADN es el primer paso de muchas técnicas moleculares. A pesar de su aparente sencillez, a menudo existen problemas con el rendimiento de los métodos, la calidad del ADN obtenido encontrándose posibles contaminantes, degradaciones parciales, así como el tiempo de duración de los protocolos. Un estudio detallado de estos importantes parámetros garantizaría las bases para futuros estudios genéticos del principal vector del dengue. El empleo del nitrógeno líquido como variante en los protocolos de extracción de ADN de diferentes especies (Mann et al. 1989; Kang et al. 2004; Nichols et al. 2004), ha permitido aumentar el rendimiento y la calidad del material genético obtenido. En varias familias de insectos esta variante ha sido empleada, demostrándose además del aumento del rendimiento su posible empleo en técnicas moleculares comprobándose la calidad del ADN resultante (Reineke et al. 1998; Fraga et al. 2004). En un estudio reciente, para caracterizar genéticamente dos poblaciones de mosquitos Ae. aegypti de Santiago de Cuba nuestro grupo de trabajo ha empleado esta simple y fácil modificación, obteniéndose un material genético con suficiente calidad para ser utilizado en la técnica del ADN polimórfico amplificado al azar (RAPD) (Bisset et al. en prensa).
En este trabajo se muestran los resultados al modificar un método de extracción de ADN genómico de mosquitos Ae. aegypti (Gaillard y Strauss 1990). Con el protocolo modificado, el cual consiste en macerar con nitrógeno líquido la muestra antes de ser extraído el ADN, se obtienen mejores resultados en el rendimiento y concentración de ADN resultante, el que tiene calidad suficiente para emplearse en técnicas moleculares como el RAPD, y probablemente en otras técnicas moleculares basadas en la amplificación por la PCR, lo que representa una gran ventaja en los estudios genéticos del Ae. aegypti.
Materiales y Métodos
Origen de las muestras
Se utilizaron mosquitos Ae. aegypti de la cepa susceptible de referencia Rockefeller suministrada por el laboratorio del Centro de Control de Enfermedades de San Juan, Puerto Rico. Los mosquitos se mantuvieron en condiciones de laboratorio: 25 ± 2°C de temperatura y 70 ± 5% de humedad relativa, con un foto-período de 10 h de luz y 14 h de oscuridad.
Metodología de trabajo
Se escogieron 20 mosquitos hembras al azar, se dividieron de forma aleatoria en dos grupos de 10 individuos cada uno y se pesaron para que esa variable no afectara los resultados. De un grupo de culícidos se extrajo el ADN por el método de Gaillard y Strauss 1990; mientras que en el segundo grupo se empleó el mismo método con la modificación realizada. La misma consistía en usar el nitrógeno líquido para macerar los individuos antes de la extracción del material genómico. Posteriormente, a ambos grupos se les eliminó el ARN.
Extracción del ADN
Método de Gaillard y Strauss 1990
Se maceraron 10 mosquitos de forma individual en 500 µl del tampón de extracción (SDS al 20%, Tris-HCl 1M pH 8,25, EDTA 0,5 M, Sacarosa 1M). El homogenizado se incubó a 65°C por 10 min, se añadieron 120 µl de acetato de potasio 5M, se colocó en hielo por 10 min y se centrifugó a 10.000 g por 10 min. Al sobrenadante se le adicionaron 35 µl de mezcla de acetato (acetato de sodio 4M y acrilamida al 0,25%) y 1.200 µl de etanol absoluto, incubándose 10 min a temperatura ambiente. El homogenizado se centrifugó a 10.000 g por 20 min, el precipitado se lavó con etanol al 70%, se centrifugó a 10.000 g por 10 min, se secó a temperatura ambiente y se resuspendió en 25 µl del tampón Tris-EDTA (TE 1X) (Tris-HCl 1mM pH 8,0, EDTA 0,1mM pH 8,0). Posteriormente, se adicionaron 2 ul de RNAsa (10 mg/ml), se incubó 1 h a 37°C, se añadió igual volumen de la mezcla cloroformo: alcohol isoamílico (24:1) y se centrifugó a 10.000 g por 10 min. El sobrenadante se conservó a 4°C.
Electroforesis de la extracción del ADN
Para la visualización del producto de la extracción del ADN en las muestras se realizó la electroforesis al 0,8% en geles de agarosa en tampón Tris-Borato-EDTA (TBE 0,5X) (Tris-Borato 0,045 M y EDTA 0,001 M, pH 8,0) conteniendo bromuro de etidio (0,5 mg/ml).
RAPD
El ADN extraído por los dos métodos (50 ng) se amplificó en un volumen de reacción de 25 µL, utilizando los cebadores OPA-1, OPA-2 y OPA-9 (Kit A, Operon Technologies, USA) manteniendo constante el resto de los componentes de la reacción (2,5 µL de tampón de amplificación 10x (Tris-HCl 100 mM pH 8,3, KCl 500 mM; gelatina al 0,01%) (Promega, USA), 200 µM de cada deoxinucleótido trifosfato (Promega, USA), 2,5 mM de MgCl2, 5 pmol de cebador, 2 U Taq ADN polimerasa (Promega, USA) con el objetivo de determinar la calidad del ADN para ser utilizado en la técnica de RAPD. La amplificación se realizó en un termociclador (Perkin Elmer, USA) con el siguiente perfil: desnaturalización inicial a 94°C por 5 min, seguido de 45 ciclos de: desnaturalización a 94°C por 1 min, hibridación a 36°C por 1 min y extensión 72°C por 2 min, con una extensión final después del último ciclo a 72°C por 15 min. Para la detección del producto se analizaron 20 µL de cada mezcla resultante en electroforesis en gel de agarosa al 1,2 %, preparado en tampón TBE 0,5x con bromuro de etidio 0,5 mg/mL. La corrida electroforética se realizó a 150 V durante 1 hora. La visualización de los productos de amplificación se realizó mediante luz ultravioleta.
Análisis estadístico
Se realizaron las lecturas de las muestras del ADN obtenido a las longitudes de onda de 260 y 280 nm en un espectrofotómetro (Pharmacia, LKB, USA). Se calculó el grado de pureza a través del cociente DO 260/280, la concentración y el rendimiento del ADN resultante. Finalmente, se realizó un análisis de varianza de clasificación simple (Statistic version 5.0) para el peso de los mosquitos y los valores del grado de pureza, rendimiento y la concentración del ADN extraído.
Resultados y Discusión
El método de Gaillard y Strauss (1990) es empleado en la extracción de pequeñas cantidades en el orden de los picogramos de material genómico, aprovechando su alta eficiencia debido al uso de la acrilamida (Gaillard y Strauss 1990). El protocolo se extrapola a estudios en muestras de Ae. aegypti porque posee bajo costo y buen rendimiento, además de presentar un tiempo de extracción muy rápido, lo que permite procesar un gran número de muestras y dar resultados fidedignos en un corto tiempo. Estas ventajas indican claros beneficios en la confección de estrategias y toma de decisiones para el control de las poblaciones del vector del dengue.
El análisis de varianza de clasificación simple para la variable peso demostró que no existieron diferencias significativas para los valores comparados (P>0,05). Resultado que indica que esta variable no influye en el análisis del rendimiento.
En la tabla 1 se aprecian los valores de las medias de la variable concentración, grado de pureza y rendimiento para el método original y su modificación. Se demostró que el método modificado tiene un mejor rendimiento en la extracción del ADN genómico (9,55), con diferencias altamente significativas (P = 0,001) con respecto al original, posee además una mayor media de concentración de ADN extraído (0,46 µg/ml), estadísticamente significativo (P = 0,01) a la obtenida por el método original. Este resultado tiene un gran significado, ya que se dispone de mayor cantidad de ADN obtenido para emplearse en más reacciones de técnicas moleculares. Realizando el mismo análisis estadístico, se llegó a la conclusión que las medias del grado de pureza entre el método empleado y su modificación no son significativamente diferentes (P>0,05). En la figura 1, las diferentes intensidades de los patrones de las corridas electroforéticas obtenidos con las dos metodologías evidencian claramente los resultados antes explicados. Es válido añadir que en ninguna de las dos metodologías se observó contaminación con ARN (Fig. 1), lo que es un aspecto importante para emplearse en la técnica del RAPD, técnica muy utilizada en estudios genéticos de poblaciones de mosquitos (Apostol et al. 1996; Zhu et al. 1998; Ayres et al. 2002).
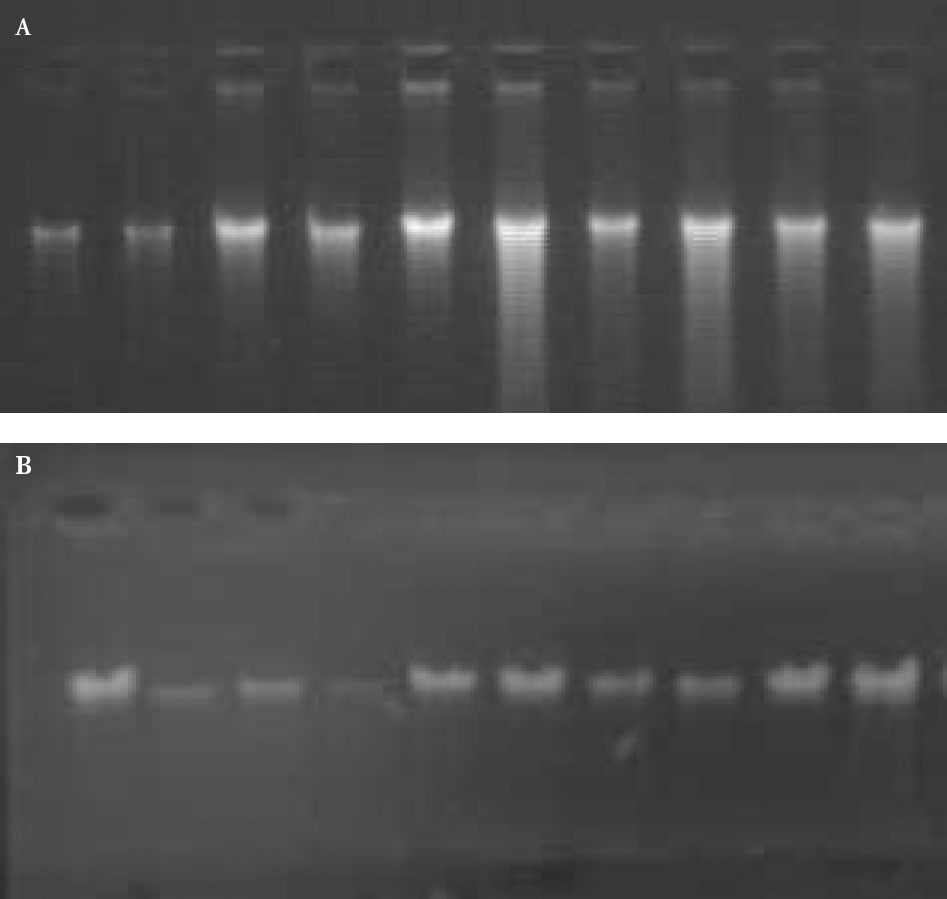
Corridas electroforéticas de las muestras de ADN genómico extraído por las dos metodologías empleadas con los mosquitos Aedes aegypti de la cepa susceptible de referencia Rockefeller. A: método modificado, B: método Gaillard y Strauss 1990.
Valores de las medias de concentración, grado de pureza y rendimiento para las dos metodologías empleadas en la extracción de ADN genómico de mosquitos Aedes aegypti
DE: Desviación estándar.
A pesar de no tener un alto grado de pureza (valores ≥ 1,8) se han obtenido patrones reproducibles en la técnica del RAPD con el cebador OPA-9 (Fig. 2), así como con el resto de los cebadores analizados (datos no mostrados), pudiéndose demostrar con patrones amplificables, claros y reproducibles la calidad del ADN obtenido por ambas metodologías y especular sobre su uso en otras técnicas moleculares que contengan en algunos de sus pasos la PCR. Este resultado se pretende utilizar en futuros estudios genéticos donde se encuentre involucrado el principal vector del dengue en las Américas.
La utilidad del nitrógeno líquido en los protocolos de extracción de ADN genómico en insectos ha sido reportada por muchos autores. Similares resultados a los obtenidos por nuestro grupo fueron reportados por Reineke et al. (1998) al comparar seis protocolos de extracción de ADN de insectos y evaluar su aplicación en la técnica del polimorfismo de la longitud de fragmentos amplificados (AFLP). En hemípteros cubanos, Fraga y colaboradores (2004) demostraron que con el uso del nitrógeno liquido se obtienen mejores rendimientos en la extracción del ADN genómico.
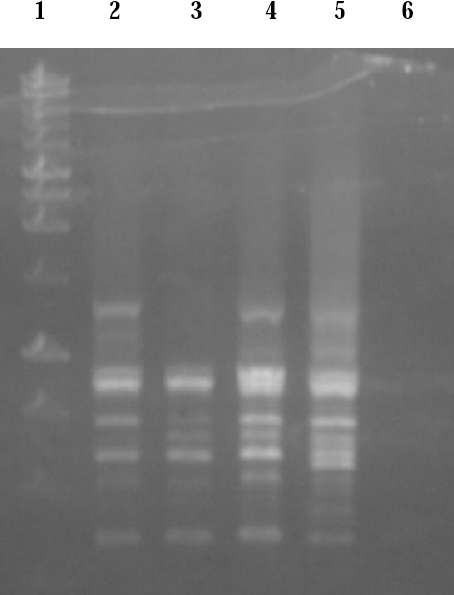
Patrones obtenidos por la técnica del RAPD de las muestras de ADN genómico extraído por las dos metodologías empleadas a los mosquitos Aedes aegypti de la cepa susceptible de referencia Rockefeller. Línea 1: Marcador de Peso Molecular, línea 2, 3: método modificado, línea 4, 5: método Gaillard y Strauss 1990, línea 6: control negativo.
Obtener un material genético con una buena calidad (libre de contaminación y sin degradaciones parciales), unido a un buen rendimiento y concentración, así como en un tiempo breve, sería una herramienta muy importante para el trabajo en la Entomología Molecular. El ADN extraído es el primer paso de muchas técnicas moleculares, que se emplean entre otras cosas, en la confección y elaboración de estrategias que permitan un mejor control sobre los insectos vectores que transmiten enfermedades que afectan al hombre. Por lo que el empleo de la modificación con nitrógeno líquido del protocolo original aquí descrito, proporciona una beneficiosa opción para el trabajo futuro.
Conclusiones
La maceración con nitrógeno líquido antes de extraer el ADN genómico, brinda una nueva y ventajosa variante, que permite contar con un método con mejor rendimiento y concentración del ADN obtenido sin variar significativamente el tiempo empleado en la metodología de la extracción. Obteniéndose un ADN con calidad suficiente para emplearse como molde en la técnica del RAPD y probablemente en otras técnicas moleculares basadas en la amplificación por la PCR.
Footnotes
Agradecimientos
A Alfredo Gutiérrez por la revisión y sus críticas valoraciones del manuscrito.
