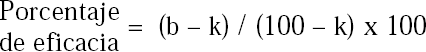Abstract
The entomopathogenic fungus Nomuraea rileyi is one of the most promising alternatives for the control of Spodoptera frugiperda, the most important pest of maize in Colombia. In previous work, a native isolate of N. rileyi was selected that caused 100% mortality on larvae of the pest under laboratory conditions. However, biocontrol activity of microorganisms may be affected by different factors such as preservation method. This study determined the effect of cryopreservation in glycerol and peptone at - 70°C on its viability and biocontrol activity over time. From a suspension of 1 x 107 conidia.ml−1, germination percentage, number of colony-forming units (CFU) and percent efficacy of the microorganism on larvae were determined before cryopreservation (control), after 24 hours, 12 months and 18 months. An effect on the viability of the microorganism expressed as percent germination and as CFU was not evident 24 hours after cryopreservation with respect to the control; but after 12 months there was a delay of 18 hours to reach a percent germination above 90% and a one exponent loss to CFU. However, no significant differences were detected in moth mortality in any of the evaluated times, being higher than 96.4%. It is concluded that cryopreservation over 18 months does not affect the germination or the biocontrol activity but does affect the CFU.
Introducción
El cultivo del maíz ocupa un lugar muy importante dentro de los sistemas de producción agrícola de Colombia al ser el segundo cereal más producido después del arroz. Dicha producción para el 2003 fue de 1.173.800 toneladas, que en términos de rendimiento representó 2.1 toneladas por hectárea (Ministerio de Agricultura y Desarrollo Rural 2004). Sin embargo, el rendimiento de este cultivo se ha visto reducido hasta en un 35% debido al daño ocasionado por el gusano cogollero del maíz Spodoptera frugiperda (J.E. Smith) (Lepidoptera: Noctuidae) (Fernández 2003 citado por Castillo 2003), el cual se ha convertido en la plaga más limitante del cultivo si se tiene en cuenta que, además de ser una plaga polífaga, se encuentra ampliamente distribuida en la zonas productoras de maíz afectándolo en las diferentes etapas de su desarrollo. Ante esta problemática se han venido utilizando diferentes métodos de control, como el cultural el cual, no ha sido suficiente para disminuir los daños ocasionados por la plaga, el control químico ha traído consigo un uso exagerado e inadecuado de plaguicidas que han afectado severamente el ambiente al alterar las poblaciones de enemigos naturales, fauna y flora asociada, así como también ha originado problemas de contaminación. Es así como el control biológico, mediante el uso de hongos entomopatógenos, aparece como una alternativa frente a las debilidades de los demás métodos de control, ya que puede representar una solución duradera y efectiva, amigable con el medio ambiente y altamente específica hacia su hospedero (García et al. 2002).
En el control biológico de S. frugiperda se ha destacado la actividad del hongo Nomuraea rileyi, el cual se encuentra distribuido en diferentes agroecosistemas y zonas geográficas donde frecuentemente ocasiona epizootias naturales sobre este insecto y otros lepidópteros de importancia económica como Anticarsia gemma talis (Hübner) (Lepidoptera: Noctuidae), Pseudoplusia includens (Walker) (Lepidoptera: Noctuidae), Trichoplusia ni (Hübner) (Lepidoptera: Noctuidae) y Helicoverpa virescens (F.) (Lepidoptera: Noctuidae). Es así como este microorganismo se ha convertido en un excelente agente de control biológico con gran potencial para ser utilizado dentro de estrategias de Manejo Integrado de la Plaga (León y Pulido 1991).
Estudios realizados en Venezuela, reportaron una incidencia del 100% sobre larvas de S. frugiperda alimentadas con hojas de maíz provenientes de campo e infectadas con N. rileyi (García y Clavijo 1985). Así mismo, Lezama-Gutiérrez et al. (2000), reportaron a N. rileyi como el entomopatógeno con mayor ocurrencia en larvas de S. frugiperda, en comparación con B. bassiana (Bálsamo) Vuillemin, Metarhizium anisopliae Metschnikov 1879, Hirsutella sp. y Entomophthora sp. Por otra parte, según estudios realizados por García et al, (2002), aplicaciones de este entomopatógeno en forma de cebo en lotes comerciales de maíz en el Valle del Cauca, ocasionaron porcentajes de eficacia superiores al 90% por un tiempo mayor a 20 días después de su aplicación. A pesar de este potencial como agente biocontrolador, no existe ningún bioplaguicida registrado a base de este microorganismo ni en Colombia ni en el mundo (Villamizar et al. 2004).
En este sentido, el Laboratorio de Control Biológico del Programa de Manejo Integrado de Plagas de Corpoica, con su compromiso de producir insecticidas microbianos seguros, eficaces y confiables, ha destinado gran parte de sus esfuerzos de los últimos años hacia el aislamiento, evaluación, producción y formulación de N. rileyi. Es así como actualmente cuenta con el aislamiento nativo Nm006 de este microorganismo obtenido a partir de larvas de S. frugiperda recolectadas en un cultivo de maíz ubicado en el departamento del Meta, que ha ocasionado una mortalidad del 100% sobre éstas, bajo condiciones de laboratorio (Bosa et al. 2004).
A pesar que N. rileyi es un microorganismo exigente en cuanto a los requerimientos necesarios para su adecuado crecimiento y esporulación (Boucias et al. 2000), Villamizar et al. (2004) estandarizaron un medio para su producción masiva con el que se han alcanzado rendimientos de 3.0 x 109 conidios.gramo−1. Así mismo, se desarrollaron diferentes preformulaciones a base de este microorganismo, seleccionándose un concentrado emulsionable con la cual se han obtenido porcentajes de eficacia del 96.6% (L. Villamizar, com. pers.).
Dada la importancia de garantizar la estabilidad de las características necesarias para su producción y para su actividad biocontroladora, el microorganismo fue incorporado al Banco de Germoplasma de Microorganismos con Interés en Control Biológico, el cual tiene como propósito preservar las características originales de los aislamientos allí presentes. Por lo tanto, el objetivo del presente trabajo fue el de evaluar el efecto de la crioconservación en el tiempo sobre la viabilidad y actividad biocontroladora de Nomuraea rileyi contra Spodoptera frugiperda.
Materiales y Métodos
Se determinó la viabilidad y la actividad biocontroladora del aislamiento Nm006 de N. rileyi antes de su crioconservación y a las 24 horas, a los 12 meses y a los 18 meses después de ésta. Para la evaluación de la viabilidad se determinó el porcentaje de germinación y el número de unidades formadoras de colonia (UFC) y para la evaluación de la actividad biocontroladora, se determinó el porcentaje de eficacia y el tiempo letal noventa (TL90) mediante bioensayos bajo condiciones de laboratorio.
Efecto de la crioconservación sobre la viabilidad del aislamiento
A partir del microorganismo crecido y esporulado sobre Agar Extracto de Levadura - Extracto de Malta (YM), se preparó una suspensión madre en el criopreservante, que consistió en una mezcla de glicerol y agua peptonada. Dicha suspensión se ajustó a la concentración de 1 x 107 conidios ml−1 y partir de ésta se hicieron diluciones seriadas desde 10−1 hasta 10−5; para determinar el porcentaje de germinación se utilizó la suspensión madre y la dilución 10−1 sembrando 100 mL de cada una de ellas en cajas de Petri con medio YM. Posteriormente, las cajas se incubaron a 25°C y a partir de las 18 horas de incubación se determinó el porcentaje de conidios germinados en el tiempo hasta que éste superó el 90%. Para ello se registró el número de conidios totales presentes en 10 campos ópticos seleccionados aleatoriamente de tres cajas de Petri. Los resultados se expresaron como el porcentaje de conidios germinados.
Para determinar el número de unidades formadoras de colonia (UFC), se sembraron las diluciones 10−2, 10−3 y 10−5 de la misma manera descrita anteriormente y se hicieron observaciones diarias hasta evidenciar el crecimiento puntual de las colonias.
Por otra parte y con el fin de determinar la viabilidad del microorganismo después de su crioconservación, se prepararon los crioviales necesarios para hacer estas evaluaciones en el tiempo, sirviendo 1 mL de la suspensión que contenía 1 x 107 conidios.ml−1 por criovial. Posteriormente, todos los crioviales se mantuvieron en un ultracongelador a -70°C durante 24 horas, 12 meses y 18 meses. Transcurridos cada uno de estos períodos, se tomó al azar un criovial, se descongeló a 37°C y se determinaron el porcentaje de germinación y el número de UFC siguiendo la metodología anteriormente descrita; así mismo, se determinó el efecto de la crioconservación en el tiempo sobre la actividad biocontroladora del microorganismo contra S. frugiperda.
Para la evaluación del porcentaje de germinación y del número de UFC del microorganismo antes y después de su crioconservación, se utilizó un diseño experimental completamente al azar con tres repeticiones por tratamiento, siendo cada repetición una caja de Petri, y los datos obtenidos se sometieron a un análisis de varianza (ANAVA) y a la prueba de comparación de medias LSD (a=0.05).
Efecto de la crioconservación sobre la actividad biocontroladora
Para determinar el efecto de la crioconservación sobre la actividad biocontroladora de N. rileyi, se realizaron cinco bioensayos en el tiempo, en los cuales se evaluó esta actividad antes de la crioconservación y 24 horas, 6 meses, 12 meses y 18 meses después de ésta. Para tal fin, a partir del microorganismo mantenido en Agar YM antes y después de su crioconservación durante cada uno de los tiempos evaluados, se preparó una suspensión en el tensoactivo Tween 80 al 0.1% ajustada a una concentración de 1 x 107 conidios.ml−1. Posteriormente, por medio de un aspersor manual se asperjó sobre 30 hojas de higuerilla (Ricinus communis) a razón de 1.2 mL sobre el haz y el envés de cada hoja, previamente desinfectada en una solución de hipoclorito de sodio al 0.5%. La unidad experimental consistió en un recipiente plástico de 16 onzas, en cuyo interior se ubicó un papel húmedo, una hoja de higuerilla y una larva de tercer ínstar de S. frugiperda, proveniente de una cría establecida en el Laboratorio de Control Biológico. Estos se mantuvieron bajo condiciones de laboratorio a 25°C y 55% de humedad relativa. Se tomaron datos de mortalidad cada tercer día a partir del quinto día del montaje del bioensayo hasta alcanzar un porcentaje de mortalidad del 100%. Los resultados se corrigieron calculando el porcentaje de eficacia mediante la fórmula de Schneider – Orelli (Ciba – Geigy 1973):
Donde
Se utilizó un diseño experimental completamente al azar con 30 repeticiones por tratamiento, en el cual cada larva fue una repetición. Los tratamientos correspondieron a un testigo absoluto (hojas de higuerilla sin ninguna aplicación), un testigo tratado en el cual se asperjó Tween 80 al 0.1% sobre hojas de higuerilla y a la aplicación del entomopatógeno antes y después de su crioconservación. Debido a que los resultados no se comportaron como una normal, los datos se sometieron a la prueba no paramétrica de Kruskal Wallis (a=0.05). Adicionalmente, se determinó el tiempo letal 90 (TL90) del microorganismo antes y después de su crioconservación; los datos de mortalidad se sometieron a un análisis de varianza (ANAVA) y a la prueba de comparación de medias LSD (α=0.05).
Resultados y Discusión
Efecto de la crioconservación sobre la viabilidad del aislamiento
Se encontró que el porcentaje de germinación fue superior al 90% a las 48 horas de lectura antes de la crioconservación y 24 horas después de la crioconservación. Sin embargo, a partir de los 12 meses después de la crioconservación, se evidenció este mismo porcentaje aproximadamente a las 18 horas de lectura (Tabla 1).
Este retraso en la germinación, que fue más evidente a partir de los 18 meses, podría estar relacionado con un efecto de latencia inducido por el tiempo de crioconservación si se tiene en cuenta que se obtuvo un porcentaje de germinación inferior al 17% al comienzo del período de recuperación del microorganismo que correspondió a 18 horas después de la descongelación y cultivo sobre medio agar YM, pero a medida que este período de recuperación aumentó, también lo hizo su germinación. Así mismo, el tiempo requerido por el microorganismo para alcanzar el 90% de germinación después de los 12 meses de su crioconservación, fue significativamente superior (57.37 horas) con respecto a los tiempos requeridos por el microorganismo antes y 24 horas después, que fueron de 47.47 horas y 44.25 horas, respectivamente (Tabla 2).
Los resultados podrían indicar que la crioconservación afectó el tiempo de germinación de los conidios, pero no su capacidad de germinar. Lo anterior concuerda con estudios realizados por Bahamón et al. (2001), quienes atribuyeron el retardo en la germinación de Beauveria bassiana después de su crioconservación durante seis meses a la latencia inducida del microorganismo por el choque osmótico de los criopreservantes o por cambios en la permeabilidad de la membrana.
Sin embargo, los resultados demostraron que el glicerol favorece la germinación de N. rileyi después del período de recuperación sobre el medio de cultivo, lo que podría deberse a la capacidad del glicerol de penetrar la pared celular y la membrana citoplasmática de las células, protegiéndolas de la desecación y del daño producido por los cristales intracelulares (Simione 1998). Esta misma capacidad, también se ha evidenciado en la conservación de virus, bacterias, micoplasmas, mixomycetes, otros hongos filamentosos, levaduras, algas y protozoos (Hubálek 2003). Adicionalmente, la peptona usualmente es usada como diluyente para microorganismos que van a ser sometidos al proceso de crioconservación, ofreciéndoles protección durante la congelación y la descongelación. Al utilizar este compuesto en combinación con el glicerol, se pudo acentuar el efecto protector de este último (Hubálek 2003).
A pesar de que no se observó pérdida en la germinación de los conidios, a partir de los 12 meses de la crioconservación se presentó una reducción de un exponente en el número de unidades formadoras de colonia (UFC) (Tabla 3). Ésta podría deberse a la alteración de los mecanismos fisiológicos involucrados en la formación de micelio. Sin embargo, es necesario desarrollar trabajos de investigación que generen respuestas a este supuesto, ya que existe una gran cantidad de factores que afectan la eficiencia de la crioconservación de los microorganismos. Tal es el caso de la especie, el aislamiento, el tamaño y forma de las células, la tasa y fase de crecimiento, la temperatura de incubación, la composición del medio de cultivo, el pH, la osmolaridad, la aireación, el contenido de agua celular, la composición del medio de cultivo, la densidad de congelamiento, la tasa de enfriamiento, la temperatura y duración del almacenamiento, la tasa de calentamiento y el medio de recuperación (Hubálek 2003). Sin embargo, uno de los factores más importantes es la composición del medio usado para suspender el microorganismo congelado; aunque algunos microorganismos han sido capaces de sobrevivir a condiciones de congelamiento sin uso de aditivos protectores, la presencia de éstos favorece la supervivencia considerablemente (Hubálek 2003).
Smith y Tomas (1997) al observar mediante un microscopio criogénico de luz la viabilidad de siete aislamientos de hongos durante su congelación y descongelación, encontraron que la ausencia de criopreservantes favoreció la formación de hielo intracelular y el encogimiento de las hifas; características que no fueron letales para el microorganismo, pero que en muchos casos afectaron su tasa y calidad de crecimiento, en contraste con los resultados obtenidos al utilizar glicerol y dimetil- sulfóxido (DMSO).
Aunque no existen registros que hayan determinado el efecto de la crioconservación sobre la viabilidad de N. rileyi; se han realizado algunos trabajos con otros microorganismos. Ryan et al. (2001) en su estudio relacionado con los efectos de la crioconservación y liofilización sobre la viabilidad, fisiología y estabilidad genética de asilamientos de Metarhizium anisopliae, Fusarium oxysporum Link ex Gray y Serpula lacrymans (Wulfen) J. Schröt.; encontraron que algunas de sus características pueden afectarse por la preservación. Tal es el caso de los perfiles de metabolitos secundarios y la producción de enzimas extracelulares, incluso se detectaron mediante la técnica de PCR fingerprinting, polimorfismos en dos aislamientos de M. anisopliae después de su crioconservación y liofilización. Sin embargo, al crioconservar una cepa de Beauveria bassiana durante seis meses en nitrógeno líquido a -196°C usando glicerol al 10% como criopreservante, se obtuvo un incremento en el porcentaje de germinación siendo éste del 70% y del 90.5% al inicio y al final de la evaluación respectivamente (Bahamón et al. 2001).
Por otra parte, Mota et al. (2003) evidenciaron un incremento en el crecimiento micelial, en la producción de biomasa y en la esporulación de los hongos controladores de nematodos Arthrobotrys robusta Dudd y Monacrosporium thaumasium (Drechsler) de Hoog & van Oorschot al ser crioconservados durante 18 meses en glicerol al 10% y nitrógeno líquido a -196°C, con respecto a su conservación a 4°C sin ningún preservante. Así mismo, al conservar especies de hongos entomopatógenos como Paecilomyces fumosoroseus (Wize) Brown & Smith (Hyphomycete), Smittium culisetae Lichtwardt, 1964 (Trichomycete) y Leptolegnia chapmanii Seymour (Oomycete), bajo diferentes métodos tales como agua desionizada, aceite mineral, sílica gel y crioconservación a -20°C y a -80°C, no presentaron pérdida en su viabilidad al ser mantenidas durante 3, 6, 12 y 18 meses bajo este último método (Lastra et al. 2002).
Efecto de la crioconservación sobre la actividad biocontroladora
No se presentaron diferencias significativas entre los porcentajes de eficacia (actividad biocontroladora) antes y después de su crioconservación; siendo estos superiores al 96% al final de la evaluación (Fig. 1).
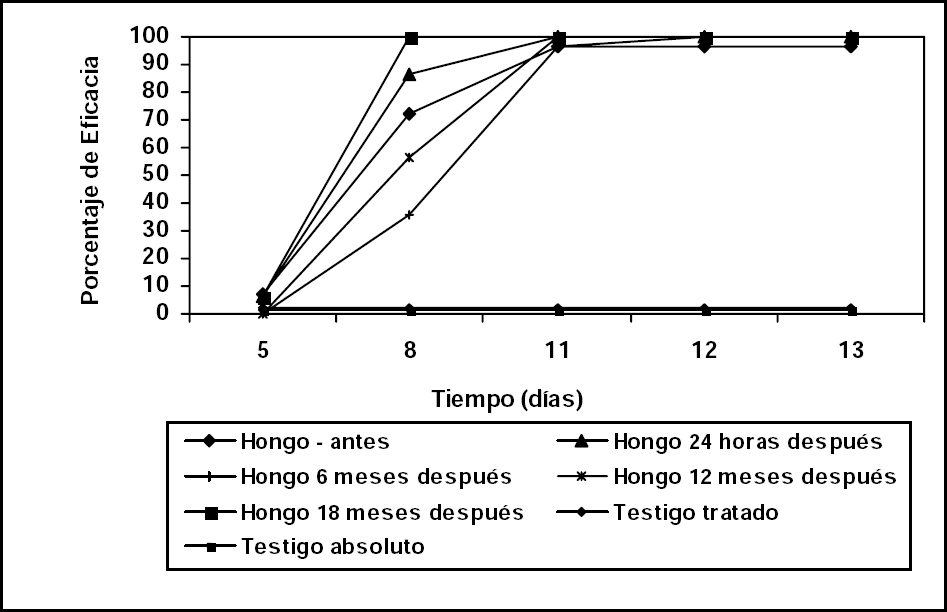
Efecto de la crioconservación en el tiempo sobre la actividad del aislamiento Nm006 de N. rileyi contra S. frugiperda.
Estos resultados obtenidos concuerdan con los reportados por Bahamón et al. (2001), quienes al evaluar la actividad biocontroladora de un aislamiento de B. bassiana contra la broca del café Hypothenemus hampei Ferrari (Coleoptera: Scolytidae) después de seis meses de su conservación en glicerol, obtuvieron un porcentaje de mortalidad del 91.6%. Según Clarkson y Charnley (1996), la capacidad patogénica de un hongo entomopatógeno, como N. rileyi, depende en gran medida de la actividad del complejo enzimático encargado de degradar la cutícula o exoesqueleto del insecto. Tal es el caso de las proteasas, quitinasas y lipasas, las cuales pueden presentar reducción en su actividad a temperaturas entre -12°C y -75°C debido a cambios estructurales en su sitio activo (Shikama y Yamasaki 1961 citados por Bahamón et al. 2001). Sin embargo, el uso del glicerol y de la peptona en la conservación del aislamiento Nm006 de N. rileyi, al actuar como osmoreguladores en la célula pudieron reemplazar las moléculas de agua perdidas, manteniendo la hidratación de las proteínas, especialmente las de bajo peso molecular. Así mismo, el glicerol al ser excluido del dominio de la proteína, pudo evitar la inestabilidad en su composición (Crowe et al. 1984; Crowe et al. 1990 y Fink 1986 citados por Bahamón et al. 2001). Esta misma acción estabilizante ha sido observada en la producción de enzimas ligninolíticas por diferentes Basidiomycetes crioconservados en DMSO y en glicerol (Stoychev et al. 1998; Croan et al. 1999).
Lastra et al (2002) no encontraron pérdida en la actividad biocontroladora de los hongos entomopatógenos Smittium culisetae y Leptolegnia chapmanii al ser evaluados contra Aedes aegypti Linnaeus, 1762 (Diptera: Culicidae), después de 18 meses de su crioconservación a -80°C. También, se ha podido comprobar el efecto protector del glicerol en los hongos fitopatógenos Colletotrichum gloeosporioides Penz, Colletotrichum acutatum J. H. Simmonds, Colletotrichum fragariae Brooks y Phomopsis obscurans Ellis & Everh. [stat. anam.] (1894), ya que no presentaron pérdidas en su viabilidad al ser conservados a -85°C, durante 21 meses, ni presentaron cambios en su patogenicidad después de cuatro años de su conservación bajo las mismas condiciones (Legard y Chandler 2000).
El TL90 del aislamiento Nm006 de N. rileyi crioconservado durante 18 meses, correspondió a 7.67 días y fue significativamente inferior con respecto a los TL90 obtenidos para el microorganismo antes de su crioconservación y 24 horas y 12 meses después de ésta, los cuales correspondieron a 11.25, 10.79 y 11.45 días, respectivamente (Tabla 4). Estos resultados podrían indicar un efecto potencializador de la crioconservación durante 18 meses sobre la actividad biocontroladora del microorganismo. Los polioles, especialmente aquellos de bajo peso molecular como el glicerol, el eritritol y la trehalosa juegan un papel muy importante en el balance osmótico de las células, brindando protección a la membrana y a las proteínas. De igual manera, estos compuestos se han asociado con la tolerancia a ciertas condiciones ambientales, con la aceleración de la germinación e incluso con el incremento en la patogenicidad y en la vida de almacenamiento de los propágulos fúngicos, como ha sido demostrado para los hongos B. bassiana, M. anisopliae y Paecilomyces farinosus (Holm:Fr.) Brown & Smith (Hallsworth y Magas 1996). Es posible que el glicerol utilizado como agente criopreservante en el presente estudio hubiera sido acumulado en la pared celular y en la membrana citoplasmática de las células del microorganismo protegiéndolas; además los polioles u otros metabolitos producidos por éste una vez fue descongelado y sembrado sobre medio de cultivo YM, favoreció la germinación de N. rileyi y su actividad biocontroladora contra S. frugiperda. Debe considerarse que la realización de diferentes bioensayos en el tiempo, impidió el uso de larvas de S. frugiperda provenientes de una misma colonia y de una misma generación; hecho que podría estar relacionado con una mayor susceptibilidad del insecto frente al ataque del hongo entomopatógeno, especialmente al llevarse a cabo la evaluación después de los 18 meses de la crioconservación, repercutiendo en los resultados del efecto de la crioconservación; hay que tener en cuenta que los datos de número de UFC cambiaron a través del tiempo, y en estas evaluaciones no se tuvieron en cuenta lo insectos, por consiguiente se podría decir que si hay un efecto de la crioconservación. Sin embargo, es necesario continuar con estas evaluaciones durante un mayor tiempo para poder confirmar la repetibilidad de las observaciones realizadas. De ser así, esta metodología podría ser incorporada dentro del desarrollo tecnológico del bioplaguicida ya que permitió el incremento de la actividad biocontroladora de N. rileyi.
Efecto de la crioconservación en el tiempo sobre el porcentaje de germinación (%) del aislamiento Nm006 de N. rileyi.
Tiempo en el cual se obtuvo el 90% de la germinación del aislamiento Nm006 de N. rileyi antes y después de su crioconservación.
(*)Letras distintas indican diferencias significativas a un nivel de significancia 0.09 (Prueba LSD).
Efecto de la crioconservación en el tiempo sobre el número de unidades formadoras de colonia (UFC) del aislamiento Nm006 de N. rileyi.
(*) Letras distintas indican diferencias significativas a un nivel de significancia 0.05 (Prueba LSD).
TL90 del aislamiento Nm006 de N. rileyi antes y después de su crioconservación.
(*) Letras distintas indican diferencias significativas a un nivel de significancia 0.05 (Prueba LSD).
Conclusiones
La crioconservación del aislamiento Nm006 de Nomuraea rileyi en glicerol y agua peptonada durante 18 meses, no afectó su germinación ni su actividad biocontroladora, pero sí su número de UFC.
Footnotes
Agradecimientos
Los autores expresan su agradecimiento al Sistema de Bancos de Germoplasma financiado mediante el convenio tripartito entre Corpoica, el Ministerio de Agricultura y Desarrollo Rural y el Instituto Colombiano Agropecuario.