Abstract
Beauveria bassiana strain 9205 (Bb9205) was transformed with protease genes (pr1A and pr1J) and one sterase gene (stel) isolated from Metarhizium anisopliae that are involved in insect pathogenicity. The goal of this research was to increase the pathogenicity of the strain against the coffee berry borer, Hypothenemus hampei. To do this, genes were cloned into the plasmid pBarGPE1 that confers resistance to the herbicide ammonium-gluphosinate. A monosporic line of strain Bb9205 was obtained with pathogenicity of 78% mortality against H. hampei, using 1 x 106 spore/ml. Protoplasts were produced from this monosporic line. The methodology for the protoplast production was optimized obtaining 3 x 107 protoplasts/ml after enzymatic pretreatment for 4 hours under slow agitation at 37°C. Transformation was carried out with the plasmids pBarGPE1- pr1A, pBarGPE1-pr1J and pBarGPE1-stel by PEG and electroporation. Two strains transformed with the pr1A gene and one strain transformed with the stel gen were obtained, that showed resistance to 25 µg/ml of ammonium glufosinate. These strains showed increased proteolytic and sterolytic activity, respectively. Under laboratory conditions, pathogenicity tests of B. bassiana transformants was compared to untransformed monosporic Bb9205. Constitutive over-expression of protease in the transgenic strain Bb9205-pr1A improved its insecticidal activity. The transformed strain showed a 21,7% increase in the insect mortality rate with 14,3% reduction in the time of mortality. The Bb9205-stel transformant strain showed a 9,5% reduction of the time of mortality compared with the untransformed strain. The results indicate that breeding of Beauveria strains by genetic transformation can be achieved for purposes of better biological control.
Introducción
El hongo entomopatógeno, Beauveria bassiana (Bálsamo) Vuillemin ha sido ampliamente usado como controlador biológico de insectos (Ferrón 1978; Charnley 1991), especialmente de la broca del café, Hypothenemus hampei (Ferrari).
B. bassiana se encuentra naturalmente in- fectando H. hampei en casi todas las re- giones de Colombia y experimentos, llevados a cabo en Cenicafé, han demos- trado que el control del insecto en campo es posible empleando dosificaciones de 1x1010 y 1x1012 esporas por árbol, las cuales pueden llegar a causar mortalidades entre 70-95% en las poblaciones de bro- ca, dependiendo de las condiciones de cultivo y ambientales que se presenten (Posada 1998). Sin embargo, el uso de esta concentración de esporas es costosa y una de las formas de reducir estas dosificaciones altas es aumentando la patogenicidad de las cepas de B. bassiana. De esta forma sería posible reducir la dosis de esporas requeri- da para controlar el insecto. Por otra parte, la mortalidad del insecto se lograría en un tiempo más corto, disminuyendo el daño que causa el insecto en los cafetales.
En general, los experimentos de control biológico empleando entomopatógenos han originado frecuentemente resultados inconsistentes en cuanto a la estabili- dad de la formulación y la lentitud en causar la mortalidad, en comparación con los insecticidas químicos, lo que ha de- tenido el desarrollo comercial de estos productos; debido a esto, las considera- ciones acerca de la sostenibilidad de un hongo entomopatógeno con propósitos comerciales inevitablemente conlleva a la posibilidad de mejorar su desempeño como biocontrolador.
El gen de la proteasa Pr1 de M. anisopliae ha sido clonado y expresado en M. anisopliae mejorando su actividad como biocontrolador (St. Leger et al. 1996). Los genes pr1J (proteasa) y stel (esterasa), que también han sido clonados, están involucrados en los pro- cesos de infección y patogenicidad del entomopatógeno M. anisopliae. El pro- pósito de este estudio fue determinar si B. bassiana transformada con los genes pr1A, pr1J y stel incrementa su patogeni- cidad contra la broca del café.
Los genes pr1A, pr1J y stel se introduje- ron mediante transformación genética en B. bassiana cepa Bb9205 monoespórica con el fin de incrementar la actividad proteolítica y esterolítica de la cepa. Las cepas transfor- mantes Bb9205-pr1A, Bb9205-pr1J y Bb9205-stel se evaluaron a nivel molecular, enzimático y de su actividad biocontroladora contra H. hampei en condiciones de labo- ratorio. Se comprobó que la expresión cons- titutiva de la proteasa pr1A en B. bassiana cepa 9205 mejora su patogenicidad contra la broca del café. Adicionalmente, el único transformante Bb9205-stel obtenido pre- sentó una disminución significativa en el tiempo de mortalidad de la broca.
Materiales y Métodos
Entomopatógeno Beauveria bassiana
La cepa 9205 de Beauveria bassiana fue originalmente aislada de Diatraea saccha- ralis (F.) (Lepidoptera: Pyralidae), y con- servada dentro de la colección de hongos entomopatógenos de Cenicafé. Este entomopatógeno se cultivó en agar sa- bouraud dextrosa (SDA) y medio Sam- sinakova (2,3% sacarosa, 2,5% almidón, 2,5% extracto de maíz, 0,5% NaCl, 0,2% CaCO3 y 1,5% agar), mantenido a 26°C durante 15 a 30 días.
Vectores de transformación
Los genes pr1A y pr1J que codifican para proteasas del tipo de las subtilisinas y el gen stel codificador de la esterasa, aisla- dos de M. anisopliae, fueron suministrados a Cenicafé por el Dr. Raymond St. Leger (Department of Entomology University of Maryland, USA). Los códigos de acceso al “Genbank”, para cada uno de los genes uti- lizados se presentan a continuación: Subtilisin-like serine protease pr1A [Metarhizium anisopliae var acridum]. AJ251925; Subtilisin-like protease pr1J gene, exon 1- 2 [Metarhizium anisopliae var. anisopliae] AJ251922 y Esterase stel (stel gene) [Metarhizium anisopliae var. anisopliae] AJ251924. Cada uno de estos genes había sido previamente clonado en el plásmido pBlueScript (PBS) (Stratagene, La Jolla, CA) y para esta investigación se subclonaron individualmente en el plásmido pBarGPE1, el cual fue obtenido del Fungal Genetic Stock Center, (Department of Microbiology, The University of Kansas Medical Center, USA).
El plásmido pBarGPE1 se escogió como plásmido de transformación ya que con- tiene el gen bar que confiere resistencia al herbicida glufosinato de amonio, bajo el control del promotor para la biosíntesis del triptofano-trpC; además, posee un gen de resistencia a ampicilina, y un si- tio de clonación múltiple bajo el control del promotor gliceraldehido 3-fosfato deshidrogenasa-gpdA. Cada uno de los genes de interés se clonaron en este úl- timo sitio.
Obtención de protoplastos
Esporas de la cepa monoespórica Bb9205 logradas a partir de un cultivo del hongo en medio SDA, mantenido a 26°C por 15- 30 días, se resuspendieron en Tween al 0,02% y se transfirieron a un erlenmeyer de 250 ml con 100 ml de medio de cultivo líquido de saboraud dextrosa, suplemen- tado con 0,1% de extracto de levadura, el cual se mantuvo en agitación a 110 rpm durante 36 h. De esta forma se obtuvo micelio joven, el cual se filtró utilizando Miracloth® (Calbiochem, Alemania), se lavó tres veces con agua destilada estéril y una vez con STC (sorbitol 1,2 M, tris 10 mM y CaCl2 20 mM). El micelio se incubó en 20 ml de solución enzimática [sorbitol 1,2M, MES 20 mM, 0,8% de Novozyme 234® de Trichoderma harzianum (Sigma. St Louis, MO) y 0,3% de β- glucuronidasa de Helix pomatia (Sigma), con una activi- dad de 400.000 U/substrato]. Se evalua- ron dos temperaturas distintas, 37°C y temperatura ambiente (± 26°C), durante 4 h. Adicionalmente se preparó una solu- ción que tenía el doble de la cantidad de enzimas y se colocó a temperatura ambien- te. La producción de protoplastos se monitoreó por observación al microsco- pio a intervalos de una hora. La solución enzimática con protoplastos se filtró usan- do Miracloth® para eliminar los restos de micelio sin degradar. Posteriormente, la solución se centrifugó a 3.450 rpm duran- te 10 minutos a 4°C, y se lavó dos veces adicionando 15 ml de STC. Finalmente, los protoplastos se resuspendieron en 800 µl de STC, se cuantificaron utilizando un hemocitómetro, obteniendo una concen- tración promedio de 3 x 107 protoplastos/ ml, los cuales se mantuvieron en hielo has- ta su uso.
Transformación de protoplastos de B. bassiana
La transformación de B. bassiana cepa Bb9205 monoespórica se llevó a cabo con cada uno de los vectores de proteasas pBarGPE1-pr1A, pBarGPE1-pr1J y estera- sa pBarGPE1-stel.
Se emplearon dos metodologías de trans- formación, polietilenglicol (PEG) (St. Leger et al. 1996) y electroporación (St. Leger et al. 1995) para transformar la cepa Bb9205, usando para ambas metodologías, la re- sistencia al herbicida glufosinato de amo- nio como agente de selección. Para la selección de colonias transformadas se determinó previamente la concentración inhibitoria del herbicida glufosinato de amonio de acuerdo con el rango de sensi- bilidad al glifosato de protoplastos de B. bassiana sin transformar.
Análisis molecular de los transformantes
En cada una de las colonias transformadas con los vectores pBarGPE1-pr1A, pBarGPE1-pr1J y pBarGPE1-stel, se verificó la presen- cia del gen marcador bar y de los genes -pr1A, -pr1J y -stel, respectivamente, me- diante su amplificación por medio de la reacción en cadena de la polimerasa (PCR).
Para esto, se extrajo ADN de cada una de las cepas transformadas crecidas en medio con herbicida, la extracción de ADN se rea- lizó siguiendo el protocolo descrito por Jürgen et al. (2001). Los genes de interés se amplificaron con reacciones de PCR en un volumen de 25 µl, que contenían 20 ng de ADN fúngico, 10X PCR buffer, 25 µM de cada oligonucleotido (específicos para la amplificación de cada uno de los genes), 2 mM de deoxinucleotidos, 2,5 mM de MgCl2 y 1 U de Taq DNA polimerasa. Las reaccio- nes se incubaron en un termociclador, si- guieron un ciclo de denaturación inicial de 95°C por 5 min, 94°C por 1 min segui- do de 40 ciclos de alineamiento a diferen- tes temperaturas según el caso (55, 60 y 65°C) por 1 min, extensión a 72°C por 1 min, denaturación a 94° C por 1 min y un ciclo final de extensión a 72°C por 5 min.
El gen pr1A se amplificó utilizando las se- cuencias de oligonucleótidos pr1A F: 5’ GCT GCC CCT GCC ACC AT3’ y pr1A R: 5’TAC GCG CCC GAT AAC AT3’, los cuales se unen en las posiciones 122 y 1.470 de la secuencia del gen pr1A. Estos oligo- nucleótidos se usaron en la reacción de amplificación a una concentración de 12,5 µΜ y una temperatura de alineamiento de 55°C.
Para la amplificación del gen pr1J se pro- baron dos temperaturas de alineamiento 60 y 65° con el fin de incrementar las con- diciones de astringencia en la reacción de PCR. Las secuencias de oligonucleotidos utilizadas fueron pr1JF: 5’ CTG GGT TCG GGA TGT TCA AGT G 3’ y pr1JR: 5’TGC CAG GAG CGA GGG ACA AGA C 3’, los cua- les se unen en las posiciones 204 y 1.046 de la secuencia del gen pr1J.
El gen stel se amplificó utilizando las se- cuencias de oligonucleótidos: ste1F: 5’ TAC GCC GAC GCA TCC ACC AAG AAA 3′ y ste1R: 5′ TAT ATG CTG CCG GGG AAG GAT GT 3’, los cuales se unen en las posiciones 173 y 1.169 de la secuen- cia del gen stel, la reacción fue llevada a cabo siguiendo las condiciones de PCR inicialmente descritas con una tempera- tura de alineamiento de 55°C.
Para la amplificación del gen bar se modi- ficó la reacción de PCR, se probaron dife- rentes concentraciones de magnesio 1,0 mM, 1,5 mM y 2,0 mM. Se aumentó la tem- peratura de alineamiento a 65°C, para in- crementar la astringencia y hacer más específica la amplificación. Las se- cuencias de oligonucleótidos utilizados en esta reacción fueron barF: 5’ATG CGC CCA GAA CGA CGC CC3′ y bar R: 5’AGA TCT CGG TGA CGG GCA GGA C 3’, los cuales se unen en las posiciones 160 y 709 de la secuencia del gen bar.
Se seleccionaron las colonias que tenían tanto el gen bar como el gen de interés y se determinó si expresaban las respecti- vas proteínas.
Ensayos de actividad enzimática
Los niveles de proteasas totales produ- cidas por las colonias transformadas y no transformadas se cuantificaron usan- do ensayos de actividad enzimática.
Se colectaron esporas de 15-30 días con germinación mayor del 90% de cepas sin transformar y transformadas con los genes pr1A y pr1J. Se utilizaron, para inocular a una concentración de 1x108 esporas/ml, erlenmeyers de 125 ml con 25 ml de me- dio mínimo (0,1% KH2PO4 0,05%, MgSO4), suplementado con 1% (p/v) de quitina y quitina más 2% de N-acetyl glucosamida (NAG). Se incubaron los cultivos en agita- ción a 110 rpm, 28°C durante 60 h. Cada 12 horas se tomó una muestra de 250 µl, se centrifugó y se midió la actividad proteolítica sobre el péptido sintético succinil-(alanil) 2-prolil-fenilalanina (PNA: p-nitroanilide) (Sigma), el cual fue prepa- rado diluyendo 3,2 mg de este substrato en 5 ml de dimetil sulfoxido (DMSO) si- guiendo la metodología descrita por St. Leger et al. (1994). Para hacer las lecturas se tomaron 10 µl del medio de cultivo de los hongos previamente centrifugado y a éste, se le adicionaron 90 µl de buffer Tris, HCI 0,1 M a pH 8,0 y 8 µl de substrato 1 mM. Las muestras se colocaron en micro- platos y se midió la cantidad de sustrato degradado a los 60 minutos por reacción colorimétrica en un espectrofotómetro modelo 3550 UV (Bio-Rad) a 405λ.
Para observar la actividad enzimática proteolítica específica de las cepas trans- formadas por isoelectroenfoque (IEF), se tomaron 25 ml de medio de la cepa con- trol Bb9205 sin transformar y de trans- formantes Bb9205-pr1A, creciendo en medio mínimo con quitina y medio míni- mo con quitina más NAG después de 72 h. Los cultivos se filtraron a través de papel filtro Whatman 1 y se concentraron por ultracentrifugación.
Para la ultracentrifugación se utilizaron unidades de ultrafiltración Centricon para 15 ml con membranas de exclusión de 10kDa (Amicon) en los cuales se co- locó el cultivo filtrado y se centrifugó a 1.800 rpm varias veces hasta completar los 25 ml de muestra, luego se lavó dos veces adicionando 10 ml de agua desti- lada y centrifugando nuevamente. Este extracto enzimático se transfirió a uni- dades Centricon para 2 ml (Amicon) en donde se centrífugó por 2 h a 1.800 rpm obteniendo finalmente 500 µl de extracto enzimático concentrado.
Alícuotas de 2 µl de estos extractos con- centrados se aplicaron a un gel hecho con una mezcla de polimerización consisten- te de una solución anfolito-monómero (5,5 ml agua destilada deionizada, 2 ml acrilamida 24,25% - bis acrilamida 0,75%, 2 ml glicerol 25%, 0,5 ml anfolito 3/10 Bio-lyte), la mezcla fue desgasificada por 4 min, luego se adicionó la solución de catálisis (15 µl de 10% persulfato de amonio, 50 µl de 0,1% riboflavina 5’ fosfato (FMN), 3 μΙ Ν, Ν, Ν, N’, tetramethy- lethylenediamine TEMED). Las proteínas fueron separadas así: 100V por 15 min, 200V por 15 min, 450V por 1 h en una mini IEF cell model 111 (Bio-Rad). La ac- tividad proteolítica de los transformantes se visualizó al poner en contacto el gel IEF zymograma de proteasas con un film de radiografía, el cual viene recubierto de una película de gelatina, las proteasas presentes en el gel hidrolizaron la gelati- na en el film, y se observó un halo trans- parente (Bidochka y Khachatourians 1988).
Para observar la actividad enzimática esterolítica se siguió la metodología des- crita por Peterson y Bridge (1994).
Pruebas de patogenicidad en condi- ciones de laboratorio
Para determinar la patogenicidad de las cepas, en condiciones de laboratorio, se utilizaron concentraciones de 1 x 105 y 1 x 106 esporas/ml y se siguió la metodología descrita por Vélez et al. (1997). El experi- mento constó de cuatro tratamientos por cada una de las cepas: Bb9205 no trans- formada, Bb9205-pr1A y Bb9205-ste1 transformadas, más el testigo (brocas sin hongo). Cada tratamiento contenía cua- tro repeticiones y 15 individuos por repe- tición, para un total de 60 brocas por tratamiento. Se realizaron tres réplicas del experimento.
La mortalidad de las brocas se evaluó dia- riamente después de la inoculación du- rante 15 días. Las variables evaluadas en el experimento fueron mortalidad causa- da por el hongo (PMBb), mortalidad por otras causas (POC) y mortalidad por con- taminantes (PMC) expresados en por- centaje a un nivel de significancia del 5%. Se determinaron las diferencias en el tiempo de mortalidad para cada cepa.
Análisis estadísticos
Para el análisis de datos de las pruebas de patogenicidad de las cepas transformadas se compararon los tratamientos entre sí y el control sin transformar mediante un análisis de varianza y se establecieron dife- rencias a través de pruebas de rangos múl- tiples de Duncan a un nivel de significancia del 5% mediante el programa S.A.S.
Resultados
Obtención de la cepa Bb9205 monoespórica
A partir de un cultivo multiespórico se ob- tuvieron 14 colonias monoespóricas, de las cuales se seleccionaron las 5 primeras que esporularon y tuvieron porcentaje de germinación mayor del 90%, para evaluar su patogenicidad contra la broca del café; para estas pruebas se usó una dosis de es- poras de 1 x 106 esp/ml (Tabla 1). Los aisla- mientos monoespóricos presentaron potenciales patogénicos que variaron en- tre el 45 y 78%, utilizando una dosis de 1 x 106 esporas/ml.
Registro de las pruebas de patogenicidad de aislamientos monoespóricos de B. bassiana sobre H. hampei y porcentaje de germinación de esporas. Dosis 1 x 106 esporas/ml.
CV: coeficiente de variación.
Estandarización de la metodología para obtención de protoplastos
La evaluación de dos temperaturas dife- rentes: 37°C y temperatura ambiente (± 26°C) en el proceso de digestión de la pa- red celular de los protoplastos durante 4 h permitió determinar que a 37°C se logra la mayor cantidad de protoplastos, con una concentración de 3 x 107 protoplastos/ml, mientras que en la solución que se colocó a 26°C se obtienen 1,2 x 107 protoplastos/ ml. Al duplicar la concentración de enzimas en la solución y dejarla a 26°C se obtiene menor cantidad (6 x 106 protoplastos/ml) y su membrana celular presenta un dete- rioro evidente por el exceso de enzimas.
Selección de transformantes
Previo al proceso de transformación era ne- cesario conocer la concentración del her- bicida glufosinato de amonio que inhibiera el desarrollo de la cepa Bb9205. Para esto se obtuvieron protoplastos del hongo y se pusieron a crecer en SDA con diferentes concentraciones de herbicida. Al examinar las cajas, después de 20 días, se encontró que la concentración de 50 µg/ml del her- bicida glufosinato de amonio inhibía com- pletamente el crecimiento del hongo B. bassiana no transformado. Sin embargo, cuando se utilizó esta concentración en los experimentos de transformación no se obtuvieron colonias transformantes, lo que sugirió que esta concentración era muy alta y no permitía la regeneración de transfor- mantes. Por lo tanto, se decidió hacer la selección utilizando la concentración de 25 µg/ml del herbicida, recuperando colo- nias transformantes antes de 20 días con el fin de evitar falsos positivos ya que des- pués de este tiempo el tratamiento con- trol de B. bassiana sin transformar puede crecer a esta concentración del herbicida.
Transformación de B. bassiana cepa 9205
Se emplearon dos metodologías de trans- formación, polietilenglicol (PEG) y electro- poración, para transformar Bb9205, usando resistencia al herbicida glufosinato de amonio (25 µg/ml) como agente de se- lección. Se realizaron 16 transformaciones en total. Después de 11 transformaciones por PEG (1 transformación con el gen pr1A, 4 para pr1J y 6 para stel) se obtuvieron 5 colonias putativamente transformadas para el gen pr1A, 3 con el gen pr1J y 3 con el gen stel. Como el número de colonias putativamente transformadas fue bajo, se decidió probar electroporación, método con el cual se hicieron 5 transformaciones (1 para el gen pr1A, 2 para pr1J y 2 para stel), obteniéndose 4 colonias putativa- mente transformadas para el gen pr1A, 16 para el gen pr1J y 12 con el gen stel. La recuperación de colonias putativamente transformadas se realizó entre 10 y 20 días cuando la transformación se hizo por polietilenglicol y desde el día 4 cuando se utilizó electroporación.
Las colonias seleccionadas se transfirieron a SDA con 25 µg/ml del herbicida glufosinato de amonio y se observó su crecimiento en este medio. Se descartaron algunas colo- nias porque no crecieron. Al final se evalua- ron 9 colonias putativamente transformadas con el gen pr1A, 12 con el gen pr1J y 6 con el gen stel, a las cuales se les extrajo su DNA para verificar, en cada una de ellas, la pre- sencia de los genes de proteasas o esterasa y del gen marcador bar.
Presencia de genes
Se seleccionaron nueve colonias putativa- mente transformadas Bb9205-pr1A, las cuales se mantuvieron en SDA y medio Samsinakova con herbicida durante ocho generaciones. En cada colonia se verifi- có la presencia del gen de proteasa pr1A y del gen marcador bar mediante PCR. La amplificación de una banda de 1.348 pb indicó la presencia del gen pr1A, tres colo- nias amplificaron el gen pr1A.
Con el fin de verificar si los hongos putati- vamente transformados en los que se amplificaron bandas del tamaño del gen pr1A, también contenían el gen bar, éste se amplificó por PCR evaluando diferen- tes concentraciones de magnesio. Se de- terminó que con la condición de 1,25 mM de MgCl2 y una temperatura de alinea- miento de 65°C en la reacción, se lograba una amplificación específica del gen. Los resultados de esta amplificación mostra- ron que tres colonias que contenían el gen pr1A también amplificaron el gen bar, una de las nueve colonias sólo am- plificó el gen bar.
Doce colonias putativamente transforma- das con el gen pr1J fueron mantenidas en SDA y medio Samsinakova con herbi- cida durante seis generaciones. En cada colonia se verificó la presencia del gen de proteasa pr1J y del gen bar. Ambos genes fueron amplificados a una tempe- ratura de alineamiento de 65°C. La pre- sencia de una banda de 842 pb indicó la presencia del gen pr1J; los resultados de esta amplificación mostraron que tres colonias que contenían el gen pr1J tam- bién contenían el gen bar. Sólo una co- lonia que tenía el gen pr1J no amplificó el gen bar.
Seis colonias putativamente transforma- das con el stel fueron mantenidas en SDA o medio Samsinakova con herbicida du- rante 6 generaciones. En cada colonia se verificó la presencia del gen stel y del mar- cador bar, una colonia amplificó ambos genes.
Actividad enzimática
Para los ensayos de actividad enzimática proteolítica se evaluó la actividad enzimá- tica proteolítica de Bb9205 sin transformar y de las cepas transformantes Bb9205-pr1A denominadas A4, A6 y la cepa A5 (solo con el gen bar).
En la figura 1 se observa la actividad proteolítica medida en absorbancia a las 24, 36, 48 y 60 horas. Las cepas deno- minadas A5 y A6 produjeron proteasas en cantidades similares al control Bb9205 cuando se pusieron a crecer en medio mínimo con quitina, la cual induce pro- ducción de proteasas. La cepa A4 produce una menor cantidad de proteasas en este medio al compararla con la producción de proteasas de las demás cepas. Solamente las cepas transformadas producen protea- sa pr1A cuando crecen en medio mínimo con quitina más N-acetilglucosamida (NAG), la cual actúa como inhibidor al blo- quear la expresión de proteasas totales en Bb9205 no transformada. En las cepas A5 y A6 se observa una marcada inhibición de crecimiento en medio mínimo con quitina más NAG, similar al control sin transfor- mar. A diferencia de las anteriores, la cepa A4 produce mayor cantidad de proteasas durante su crecimiento en medio mínimo con quitina más NAG, lo cual indica que la proteasa se está expresando constituti- vamente y tanto el gen como su respectivo promotor fueron incorporados dentro del genoma del hongo.
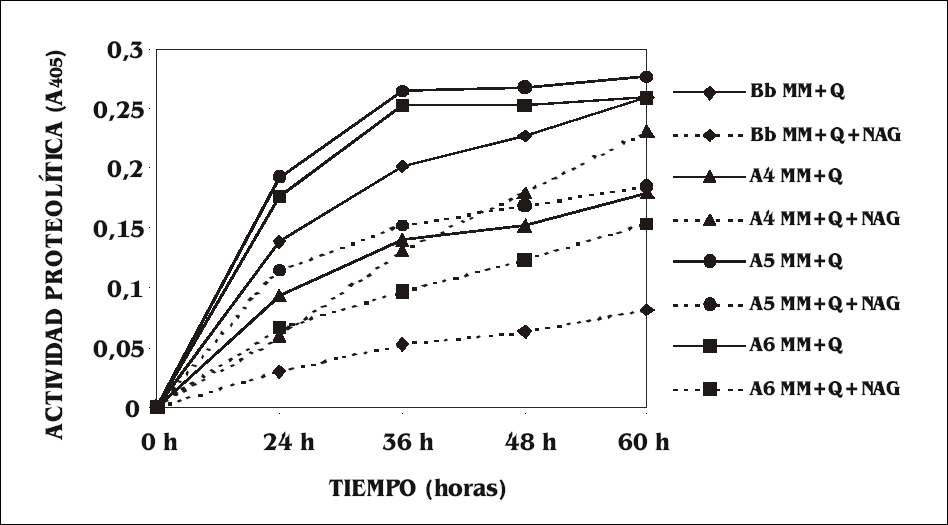
Producción de pr1A en la cepa control Bb9205 y cuatro cepas transformadas con PBARGPE1-pr1A creciendo en medio mínimo (MM) con quitina (Q) y medio mínimo con quitina más N-acetil glucosamida (NAG). Esta gráfica representa el promedio de tres répli- cas del experimento.
De igual manera se evaluó la producción de proteasas en las cepas transformantes Bb9205-pr1J; sin embargo, todas las cepas transformantes presentaron el mis- mo perfil de producción de proteasa pr1J en medio mínimo suplementado con quitina y se inhibieron en la misma pro- porción que la cepa control Bb9205 sin transformar en medio mínimo con quitina más NAG.
Actividad proteolítica por isoelectro- enfoque
Para este experimento se escogieron las cepas Bb9205-pr1A denominadas A3 y A4 en las cuales se había verificado la presencia de los genes pr1A y bar. La cepa A4 demostró expresión constituti- va de la proteasa pr1A, en la cepa A3 no se midió actividad enzimática proteolítica por espectrofotometría debido a que esta cepa presentó disminución en su capa- cidad de esporulación; sin embargo, el isoelectroenfoque permitió conocer su ac- tividad proteolítica específica.
Para observar la actividad enzimática proteolítica, se tomaron extractos enzimá- ticos concentrados de la cepa control Bb9205 sin transformar y de las cepas A3 y A4, creciendo en medio mínimo con quitina y medio mínimo con quitina más NAG. Las proteasas fueron separadas por isoelectroenfoque (IEF), comprobándose la actividad proteolítica por exposición del gel a una película de radiografía, la cual viene recubierta de gelatina. Las proteasas degradaron la gelatina formando un halo transparente. El zimograma mostró que no hubo inhibición de proteasas en las cepas A3 y A4 creciendo en medio mínimo con quitina más NAG, como si es evidente en el control Bb9205 sin transformar. Es- tos resultados confirman la transformación y expresión constitutiva de pr1A en las ce- pas Bb9205-pr1A A3 y A4. Ambas cepas fueron seleccionadas para realizar pruebas de patogenicidad sobre la broca del café.
Actividad esterolítica
El ensayo de actividad esterolítica mostró que la cepa control Bb9205 sin transfor- mar poseía una actividad moderada en el medio Tween 80, dado que la cepa tiene enzimas esterasas; sin embargo, en la cepa transformada Bb9205-stel se observó un incremento de actividad esterolítica debi- do a la transformación con el gen stel. El medio sobre el que creció el transformante contenía 25 ug/ml de herbicida glufosinato de amonio.
Pruebas de patogenicidad en condi- ciones de laboratorio
Se determinaron promedios de porcen- taje de mortalidad causado por B. bassiana y tiempo de mortalidad sobre la broca del café para cada una de las ce- pas transgénicas y control sin transformar.
El análisis de varianza y la prueba de ran- gos múltiples de Duncan con un nivel de significancía del 5% mostraron que hubo diferencia significativa entre el porcentaje de mortalidad causado por la cepa transgénica Bb9205-pr1A y los porcenta- jes de mortalidad causados por el control Bb9205 sin transformar y la cepa trans- génica Bb9205-stel, pero no existió dife- rencia significativa entre el porcentaje de mortalidad causado por Bb9205-stel y el control Bb9205 (Tabla 2 y Fig. 2).
Promedio de porcentaje de mortalidad y tiempo de mortalidad sobre H. hampei de las cepas Bb9205 sin transformar y Bb9205-pr1A y Bb9205-stel transgénicas. Dosis 1x105.
* Valores seguidos de la misma letra en la misma columna, son iguales estadísticamente de acuerdo con la prueba de Duncan al 5%.
CV= coeficiente de variación
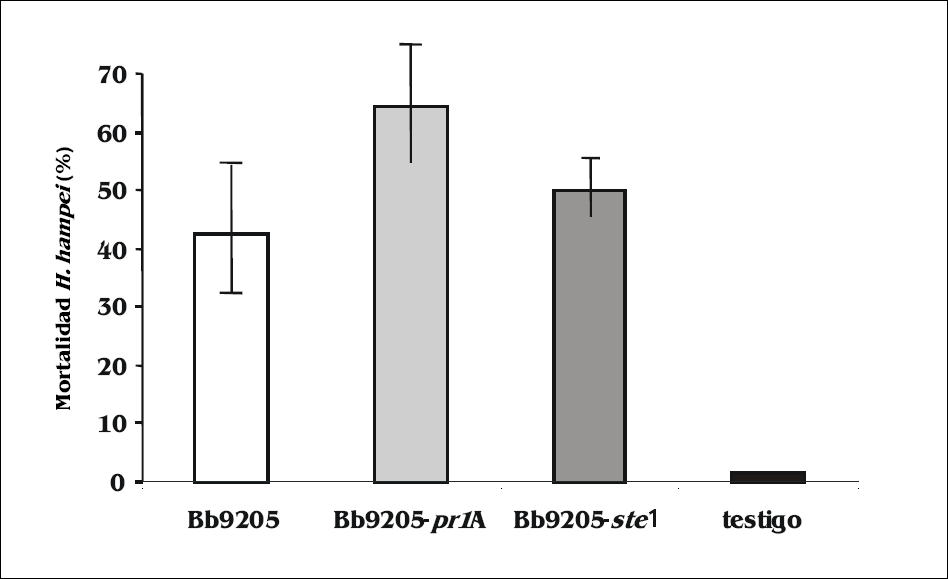
Promedios de porcentaje de mortalidad sobre H. hampei de las cepas Bb 9205 sin transformar y las cepas transgénicas Bb9205-pr1A y Bb9205-stel. Dosis 1 x 105 esp/ml.
La expresión constitutiva de la proteasa pr1A en la cepa transgénica Bb9205-pr1A mejora su actividad insecticida al demos- trar con una dosis de 1 x 105 esporas/ ml un incremento de mortalidad sobre la broca del café del 21,7% al compararse con el control Bb9205 sin transformar. La cepa transgénica Bb9205-ste1 tuvo un incremento del 7,3% en su porcenta- je de mortalidad sobre broca, pero este valor no fue significativamente diferente (P=0,05) del porcentaje de mortalidad sobre broca causado por el control Bb9205 sin transformar.
Para el tiempo de mortalidad (TMOR) el análisis de varianza con un nivel de significancia del 5% y la prueba de rangos múltiples de Duncan, mostró que existe diferencia significativa en el TMOR de las brocas causado por las cepas Bb9205-pr1A y Bb9205-stel con respecto al con- trol Bb9205, pero no existió diferencia significativa entre el TMOR de las cepas Bb9205-pr1A y Bb9205-ste1. Bb9205-pr1A tuvo una disminución del 14,3% en el tiempo de mortalidad y la cepa Bb9205-stel demostró una disminución del 9,5% al ser comparadas con Bb9205 sin trans- formar (Tabla 2).
Adicionalmente, se realizó otra prueba de patogenicidad utilizando una dosis de 1 x 106 esporas/ml, la cepa Bb9205-stel no se incluyó en esta ocasión debido a que no se disponía de esporas con germinación su- perior al 90% de esta cepa para realizar la prueba. Los resultados de esta prueba mues- tran que con una dosis de 1 x 106 esporas/ ml la cepa Bb9205-pr1A tuvo un incremen- to del 25% en su porcentaje de mortalidad y una disminución del 16,2% en el tiempo de muerte sobre la broca del café. Estos resultados concuerdan con los obtenidos cuando se utilizó una dosis de 1 x 105 es- poras/ml ya que el incremento en el por- centaje de mortalidad y la disminución del tiempo de muerte sobre la broca fueron similares con ambas dosis.
Discusión
El uso de un cultivo monoespórico de B. bassiana minimiza los riesgos de variación por la naturaleza mononuclear de estas esporas. En la tabla 1 se observa que en el cultivo multiespórico existen conidias con diferentes potenciales patogénicos, los cuales pueden variar entre el 45 y 78%, utilizando una dosis de 1 x 106 esporas/ml. Resultados similares fueron obtenidos por Estrada et al. (1999) quienes también pro- dujeron aislamientos monoespóricos de B. bassiana cepa Bb9205, ellos mostraron una gran variabilidad en sus cultivos monoespóricos, utilizando una dosis de 1x107 esporas/ml obtuvieron mortalidades menores del 42% y mayores del 70%.
En los experimentos de transformación la calidad de los protoplastos es un factor crí- tico ya que de esto depende la frecuencia de transformación (Valadares e Inglis 1997). Al estandarizar la metodología para Bb9205, se encontró que a 37°C y 4 h de tratamiento enzimático se obtuvo la canti- dad de protoplastos adecuada para el pro- cedimiento de transformación. Estas condiciones fueron similares a las determi- nadas por Florez et al. (2000) para regene- ración de protoplastos y pruebas de fusión en B. bassiana.
Según los resultados de las pruebas de PCR, de 9 colonias que se obtuvieron por PEG, cuatro (45%) fueron transformadas, mientras que de 18 colonias que se ob- tuvieron por electroporación solo tres (17%) fueron transformadas, esto sugie- re que la electroporación no resultó ser eficiente en términos de frecuencia ya que se obtuvieron muy pocos transformantes por este método. Pfeifer y Khachatourians (1992) obtuvieron resultados similares en la transformación de B. bassiana por electroporación.
Al revisar los resultados obtenidos con diferentes metodologías de transformación en diferentes hongos entomopatógenos (Bernier et al. 1989; Goettel et al. 1990; Reis et al. 1996; Barreto et al. 1997; Valadares e Inglis, 1997; St. Leger et al. 1995; Inglis et al. 1999), no se encuentra un patrón claro que permita establecer comparaciones entre ellos, por lo tanto no es posible establecer si las diferencias en la frecuencia de transformación se deben a la especie de hongo o al método utiliza- do, además la información existente sobre B. bassiana sigue siendo limitada.
En general, ambas metodologías de trans- formación permitieron la obtención de transformantes, sin embargo de 27 colo- nias evaluadas solo siete resultaron trans- formadas, tres contenían el gen pr1A, tres contenían el gen pr1J y una contenía el gen stel, lo que indica la presencia de un alto número de colonias falso positivas. Esto posiblemente fue debido a la con- centración de herbicida utilizada para la selección de los transformantes. Otros autores describen el uso de diferentes con- centraciones de glufosinato de amonio para selección de transformantes (Cantone y Vandenberg 1999a, b; Góngora 2004; Screen et al. 2001). Esto conlleva a esta- blecer que la concentración mínima inhibitoria de herbicida varía de acuerdo con la especie y probablemente la concentración mínima inhibitoria de glufosinato de amonio para selección de transformantes de Bb9205 monoespórica es una concentración intermedia entre 25 y 50 µg/ml. El uso de estas concentracio- nes restringiría la posibilidad de obtener colonias falso positivas.
En el análisis molecular de los transforman- tes para amplificar el gen de la proteasa pr1J y el gen bar, fue necesario establecer condiciones muy astringentes en las reac- ciones de amplificación debido a la baja especificidad de los oligonucleótidos o a que B. bassiana tiene muchas proteasas que se desconocen, las cuales pueden ser muy similares a la pr1J de M. anisopliae. En las investigaciones de hongos entomopató- genos, M. anisopliae ha sido modelo glo- bal para patogenicidad, mientras que B. bassiana ha sido menos estudiada. Hasta el momento, en esta última solo se ha he- cho la clonación de una proteasa Pr1 (Joshi et al. 1995) y se ha deducido su secuencia de aminoácidos, demostrando que es si- milar a la proteasa Pr1 de M. anisopliae. Otra proteasa de B. bassiana similar en un 83,3% a la Pr1 antes descrita, ha sido regis- trada por Fang et al. (2002).
En eventos de transformación utilizando el promotor constitutivo “gpdA”, St. Leger et al. (1996), Migheli et al. (1998) y Screen et al. (2001) registran la obtención de transformantes con incremento de activi- dad proteolítica con respecto al control sin transformar. En este caso de tres transfor- mantes que fueron positivos por PCR para el gen pr1A, dos de ellos Bb9205-pr1A AЗ y A4 demostraron expresión del gen pr1A y producción constitutiva de la proteasa cuando fueron comparados con la cepa control Bb9205 sin transformar, bajo con- diciones de crecimiento inducidas y no in- ducidas. Esto apoya la observación de Covert y Cullen (1992), de que los hongos filamentosos son a menudo permisivos con respecto a la expresión de genes foráneos. De igual forma, St. Leger y Joshi (1997) y St Leger et al. (1995) aseguran que los plásmidos son integrados dentro del genoma frecuentemente en múltiples copias, algunas veces en loci homólogos. En esta investigación es sorprendente que con tan pocos transformantes obtenidos se hayan encontrado cepas que presenta- ran una buena expresión de proteínas, te- niendo en cuenta que St. Leger et al. (1996) hablan que de 40 transformantes de M. anisopliae obtenidos para el gen pr1A, sólo 12 (30%) expresaron constitu- tivamente la proteasa Pr1.
Ninguno de los tres transformantes iden- tificados por PCR para el gen pr1J, demostró incremento de actividad proteo- lítica, debido a que la transformación es un proceso completamente aleatorio; sin embargo, a pesar de haber obtenido tan pocos transformantes se podría conside- rar: 1) La probabilidad de que en estos hongos transformados se hubiera presen- tado el fenómeno de silenciamiento de genes dependiente de homología (HDGS), eventos de recombinación homóloga han sido registrados por Inglis et al. (1999), en P. fumosoroseus ypor Cogoni y Mancino (1997, citado por Catalanotto et al. 2000) en Neurospora crassa. 2) El efecto de posi- ción, en el que los genes pueden integrar- se en lugares del genoma que nunca son transcritas (Cantone y Vandenberg 1999b). 3) Exceso en el número de copias del gen, el cual puede causar un silenciamiento (Carthew 2001). Para el caso del único transformante obtenido para el gen stel, éste expresó la proteína, nuevamente rei- terando lo aleatorio del proceso de trans- formación.
Alteraciones fenotípicas se presentaron en uno de los transformantes Bb9205-pr1A-A3 que demostró mayor actividad proteolítica, pero disminuyó su capaci- dad de esporulación, probablemente por la integración del plásmido en diferentes posiciones dentro del genoma. Resulta- dos similares fueron registrados por St. Leger et al. (1996) en M. anisopliae trans- formado con el gen Pr1 y Upchurch et al. (1994) en Cercospora kikuchii trans- formado con el gen bar.
El incremento en la patogenicidad de Bb9205-pr1A del 21,7% de mortalidad y una disminución del 16,3% en el tiempo de muerte de la broca con una dosis de 1 x 105 esporas/ml en comparación al control sin transformar, es atribuido a que la proteasa Pr1 es esencial para la penetra- ción de la cutícula y es un determinante de patogenicidad (Charnley y St Leger 1991). Lo anterior unido al hecho de que aproxi- madamente el 70% de la cutícula del in- secto es proteína (Charnley y St. Leger 1991; Bidochka y Khachatourians 1992; Griesch y Vilsinskas 1998), resultó en me- joramiento de la actividad biocontroladora de la cepa Bb9205. Resultados similares fueron obtenidos por St. Leger et al. (1996) en la transformación de M. anisopliae con el gen Pr1. Es importante resaltar que en esta investigación se presentó incremento de mortalidad del insecto, lo cual no se registró en el trabajo de St. Leger et al. (1996).
Un incremento de la actividad biocontro- ladora utilizando proteasas también ha sido obtenida en otros hongos biocontro- ladores, como ha sido descrito por Flo- res et al. (1997), quienes transformaron Trichoderma harzianum con el gen de la proteasa prb1.
Con respecto a la patogenicidad del transformante Bb9205-stel, se planteó la hipótesis de que el incremento de activi- dad esterolítica mejoraría la patogenicidad de B. bassiana 9205 contra la broca del café, basados en el hecho de que las esterasas son las primeras en ejercer su acción para degradar la cutícula del insec- to. El transformante Bb9205-ste1 incre- mentó su actividad esterolítica pero no mejoró significativamente su patogeni- cidad contra la broca al ser comparada con la cepa Bb9205 no transgénica. Sin em- bargo, el incremento de la actividad esterolítica en la cepa Bb9205-stel puede facilitar la acción de otras enzimas como las proteasas, lo que se demostró al dismi- nuir en un 9,5% el tiempo que tarda el hongo en causar la mortalidad de la broca.
Las cepas transgénicas generadas mostra- ron estabilidad genética bajo condiciones selectivas, por más de seis generaciones.
Finalmente, se demostró que la transfor- mación de Bb9205 con el gen pr1A y ex- presión constitutiva de esta proteasa mejoró la actividad biocontroladora de esta cepa contra H. hampei. Se requiere información adicional de la cepa Bb9205 transformada con el gen stel ya que en este estudio no se cuantificó la actividad enzimática esterolítica, ni tampoco se obtuvieron más transformantes para comparar y poder establecer que no existen diferencias signi- ficativas en la patogenicidad de transfor- mantes Bb9205-stel y la cepa Bb9205 no transformada.
Con respecto a las perspectivas de este tra- bajo es conveniente producir más transfor- mantes para los tres genes evaluados en este estudio, ya que la cantidad obtenida fue muy poca, lo cual limita las conclusio- nes del estudio y se hace necesario evaluar el efecto sinérgico de estos genes con otros genes implicados en patogenicidad, te- niendo en cuenta el hecho de que la mez- cla de varias enzimas puede ser necesaria para una eficiente degradación de la cutí- cula del insecto en la interacción entomo- patógenos, plaga.
Footnotes
Agradecimientos
Las autoras agradecen a Cenicafé y a Colciencias por el apoyo financiero para la realización de esta investigación.
