Abstract
The region of San Sebastián of Buenavista, Magdalena (Colombia), is characterized for being one of the most important producers of lumber derived from eucalyptus plantations. At present, large economic losses have been registered for lumber companies operating in San Sebastián due to the damage caused by termites. These losses reach approximately 83,6% of the production in the study. The control measures carried out are few, mainly using chemical insecticides. In this region, studies have not been conducted on recognizing the termites that attack eucalyptus nor on the microorganisms associated with them. These studies are important because some microorganisms may be regulating termite populations under natural conditions, or have potential as microbiological control agents. In this paper we report the genera of termites present in eucalyptus and the fungi associated with their nests and nearby substrates. The termites found belong to the genera Microcerotermes, Amitermes and Coptotermes. A total of 252 fungal isolates corresponding to 31 genera and 29 species were obtained. The fungal isolates were grouped into categories according to their origin. We identify those isolates recognized as entomopathogenics or previously reported in association with termites. Among the most important fungi were Aspergillus spp. (33,3%), Fusarium spp. (21%), Penicillium spp. (7,9%), Trichoderma spp. (6,8%), Paecilomyces spp. (4,8%) and Entomophthora spp. (2,4%).
Introducción
Las termitas son insectos sociales con un sistema de castas que incluye obreros, sol- dados y alados. Las formas aladas se cons- tituyen en reyes y reinas; estas últimas pueden colocar de 2.000 a 3.000 huevos por día, lo cual indica su capacidad reproductiva alta (Watson y Gay 1991). Estos insectos son altamente perjudicia- les para la industria forestal, agrícola, tex- til y maderera; afectan gravemente la economía y la ecología de un país (Garcés 1997). Las termitas se alimentan de es- tructuras maderables, árboles deciduos, plantas leñosas, cartón y papel. El daño que ocasionan se debe principalmente a que su dieta alimenticia se basa en lignina y celulosa (Hoyos 1974; Pérez-Arbélaez 1994). Estos insectos poseen una comu- nidad microbiana en el tracto intestinal que ayuda a digerir los componentes du- ros de la madera liberando la celulosa que las nutre (Grady 1997). Eucalyptus sp. (Myrtaceae: Leptospermoideae) es una es- pecie ampliamente distribuida en la zona intertropical que posee múltiples aplica- ciones tanto en arboricultura forestal como en la obtención de sustancias antimicro- bianas y en la industria maderera. Así mis- mo, en la producción de papel y en la desecación de terrenos (Hoyos 1974; Lamprecht 1990; Pérez-Arbelaez 1994). Las plantaciones de Eucalyptus colombianas se han visto afectadas significativamente por termitas tanto en los semilleros como en plantaciones adultas (Garcés 1997). En la reforestadora San Sebastián no se han calculado con precisión los daños econó- micos. No obstante, se calculan porcenta- jes por encima del 50% para algunas parcelas. El daño más significativo se ha presentado en Eucalyptus tereticornis, especie que ocupa un área de 1.360 hec- táreas en la plantación total del área don- de se realizó el estudio (1.700 hectáreas, datos sin publicar).
Entre las familias de termitas que afectan eucaliptos se encuentra Rhinotermitidae, que construye los nidos alrededor de la madera y sobre la superficie de los árboles a través de un sistema de galerías y la Termitidae, que construye sus nidos como montículos sobre el suelo y en los árboles (Grace 1989). Por lo tanto, estos sustratos han sido considerados fuente ideal para la búsqueda y el aislamiento de microorga- nismos asociados a termitas con potencial como agentes de control microbial. El con- trol de las termitas ha sido realizado de forma general mediante compuestos preservantes de madera como creosotas, químicos como chlordano, metil bromuro, malatión, deltametrina, preparaciones co- merciales de diclorodifeniltricloetano (DDT) y hexacloruro de benceno (Yoshioba et al. 1991; Valerio et al. 1998). Dichos compuestos además de ser tóxicos persis- ten en la naturaleza por periodos de tiem- po prolongados. También se han utilizado métodos alternativos como el control bio- lógico. Éste incluye el uso de depredadores y patógenos. Entre los patógenos se en- cuentran principalmente virus, bacterias, nemátodos y hongos (Coppel y Liang 1987; Madrigal 1989; Hassan 1990; Logan et al. 1990; Zoberi y Grace 1990; Milner 1992; Alves et al. 1995; Zoberi 1995; Milner et al. 1998a y b). Los hongos que atacan las termitas en condiciones natura- les y otros a los cuales pueden ser suscep- tibles se consideran una alternativa importante para el control biológico de las mismas. En estudios in vitro se ha de- mostrado que hongos como Aspergillus flavus, Entomophthora sp. (Espero 1984), Beauveria bassiana (Zoberi y Grace 1990) y Paecilomyces fumosoroseus (Chai 1995) poseen niveles importantes de patogeni- cidad para termitas. Además, se ha regis- trado el hongo Metarhizium anisopliae atacando, en condiciones naturales, termitas como Reticulitermes flavipes (Zoberi 1995) y Coptotermes formosanus (Sajap y Kaur 1990). Para el caso particu- lar de termitas, la selección de hongos promisorios como agentes de control bio- lógico debe incluir no sólo características propias del hongo como su capacidad de adaptación y sobrevivencia (en el suelo, en el termitero o en un cebo que lo con- tenga), sino también, aspectos de la bio- logía de las termitas. Entre los más importantes están la limpieza que se ha- cen los individuos cuando son infectados con hongos, la remoción y entierro de los cadáveres y la presencia de secreciones de defensa producidas por las termitas (Sajap y Kaur 1990; Delate et al. 1995; Zoberi 1995; Madrigal 1999, Fernández 2001). Adicionalmente, los criterios básicos deri- vados de pruebas in vitro como porcenta- je de mortalidad, DL50, TL50 y mortalidad intrínseca son de gran importancia. En Colombia existen pocos estudios sobre el reconocimiento de hongos entomopató- genos asociados a termitas y en particular a termitas que atacan el eucalipto. En este trabajo se realizó el reconocimiento de termitas de la reforestadora y de hongos asociados a ellas. Este puede considerarse como punto de partida para la selección e implementación del uso de hongos con potencial como agentes de control micro- biológico de termitas que puedan incluir- se en programas de manejo integrado en las áreas afectadas.
Materiales y Métodos
Origen de los aislamientos
La zona de muestreo está localizada en la municipalidad de San Sebastián de Bue- navista (departamento de Magdalena), con una extensión de 7.000 hectáreas. Esta región comprende tres fincas: Los Álamos, El Enredo y Santa María. San Sebastián se encuentra ubicada en la zona de vida bos- que seco Tropical (bs-T) caracterizada por tener una temperatura promedio de 28,8°C, una precipitación media anual de 1.787 mm y una altitud de 25 msnm (Borreros 1996; Espinal 1990). El trabajo se realizó en la finca los Alamos, que tiene una extensión de 1.700 hectáreas, con plantaciones de Eucalyptus tereticornis (80%), E. camaldulensis y E. urophylla (20%).
Colección de termitas
Se localizaron las áreas de la finca con ma- yor incidencia de daño registrado por termitas de acuerdo con la reforestadora y se escogieron al azar siete parcelas de 40 x 40 m muestreándose en promedio 20 ár- boles por parcela. Las termitas se colecta- ron de la superficie y cavidades internas de los árboles (tanto jóvenes como adultos) y de troncos atacados que se encontraban en el suelo. La recolección se realizó usan- do pinceles y pedazos delgados de made- ra. Las termitas se colectaron con su respectivo sustrato: fragmentos de termitero, hojas y suelo. Posteriormente, se depositaron en recipientes plásticos de 16 x 12 cm de diámetro tapados con muselina y sellados con plástico transparente, envuel- to en bolsas oscuras dándoles condiciones apropiadas para el transporte al laborato- rio. También se colectaron termiteros com- pletos. Las termitas se mantuvieron en recipientes plásticos dentro de una cámara climatizada (WTBbinder 78532, Tuttlingen / Germany) con temperatura controlada (26±0,5°C), humedad relativa (80±5% HR) y en oscuridad o en el invernadero del Ins- tituto de Biología de la Universidad de Antioquia (HR 60%, 24,4°C).
Las termitas colectadas fueron identifica- das en la Universidad Nacional de Colom- bia, sede Medellín, en el laboratorio de Entomología por Jhon Albeiro Quiróz G. y Ana Isabel Gutiérrez G. del Grupo de Micología, Instituto de Biología de la Uni- versidad de Antioquia. La identificación se llevó a cabo con las claves taxonómicas de Constantino (1999), Bach (1997), Nickle y Collins (1988, 1992), Watson y Gay (1991), Nutting (1990) y Weesner (1987).
Aislamiento de hongos
Los hongos se aislaron de termitas muer- tas (Tm), termitas vivas (Tv) colocadas vi- vas directamente sobre un medio para el crecimiento de hongos, fragmentos de termitero (Ft), madera (M), hojas de euca- lipto (He), suelo (S), y troncos secos de eucalipto (Tse). Las muestras se colocaron en cajas de Petri estériles, utilizando papel filtro Watman No. 1 húmedo o con una mota de algodón humedecida con agua destilada estéril para observar el desarro- llo de los hongos en estos sustratos. Las cajas se incubaron a temperatura ambien- te (22-26°C). Todos los sustratos fueron transferidos, por triplicado, a cajas de Petri con los medios de cultivo Malta Extracto Agar (MEA), Sabouraud Dextrosa Agar (SDA) y Papa Dextrosa Agar (PDA) (Oxoid LTD., Basingstoke, Hampshire, England).
De los hongos obtenidos se hicieron ais- lamientos puros a partir de cultivos monospóricos siguiendo la técnica descri- ta por Calle (2000). Se realizaron micro- cultivos de los hongos purificados y se estudiaron las características tanto macroscópicas como microscópicas de los hongos. Se identificaron las especies de los hongos según criterios morfológicos y de cultivo, siguiendo las claves de: Barnett (1967), Nelson et al. (1983), Samson et al. (1984), Vélez (1989), Pardo (1990), Goettel e Inglis (1997), Humber (1997), Papierok y Hajek (1997). Los hongos ais- lados se conservan en el Laboratorio de Micología, Instituto de Biología de la Uni- versidad de Antioquia.
Resultados y Discusión
En total se obtuvieron 252 aislamientos de hongos, los cuales corresponden a 31 gé- neros y 29 especies. Las termitas sobre las cuales se realizaron los aislamientos fueron identificadas como Microcerotermes silves- tri, Amitermes silvestri (Termitidae) y Coptotermes Wasmann (Rhinotermitidae).
En la figura 1 se indica la frecuencia de los principales aislamientos fúngicos encontra- dos, la cual se calculó como: número de aislamientos del hongo en las termitas y diferentes sustratos / número total de hon- gos x 100. De acuerdo con esta figura, los hongos encontrados con mayor frecuencia fueron: Aspergillus (Aspergillus fumigatus, A. niger, A. ochraceus), Fusarium (F. oxys- porum, F. sporotrichiodes) y Penicillium. (Penicillium sp. y P. verrucosum). Aunque menos frecuentes Trichoderma spp. y Pae- cilomyces lilacinus merecen especial consideración como agentes de control biológico. Así mismo, Entomophthora spp. por su reconocido efecto como ento- mopatógeno.
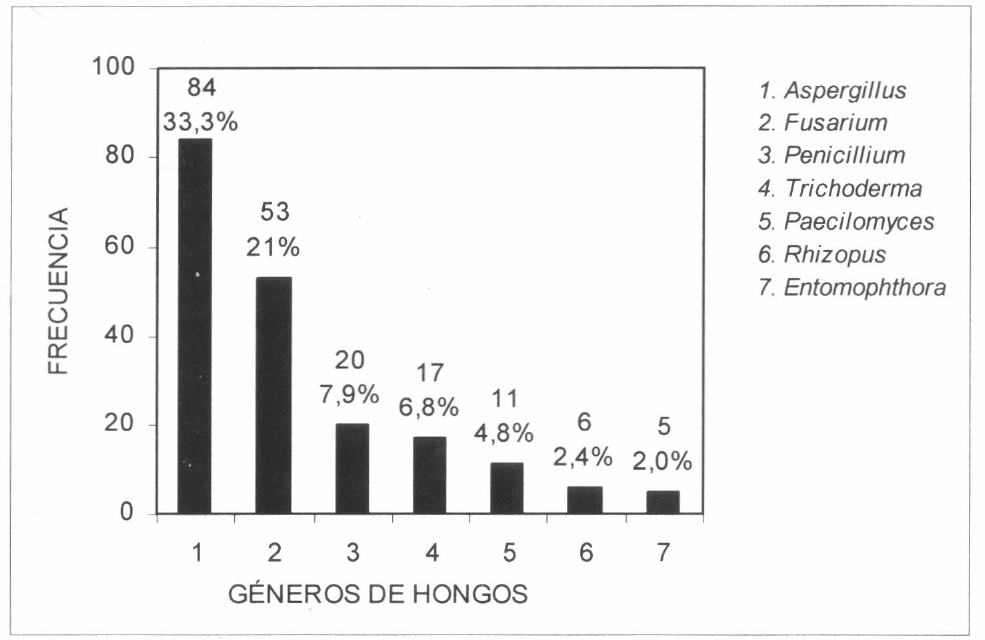
Frecuencia de géneros de hongos aislados de termitas y de diferentes sustratos.
En las tablas 1 y 2 aparecen discriminados los géneros y especies de hongos de acuer- do con su fuente de aislamiento; es decir, de las termitas o directamente de los sustratos como suelo, madera, troncos de eucalipto y fragmentos de termitero. Así mismo, se menciona el medio de cultivo utilizado con éxito para el mejor aislamien- to, crecimiento e identificación de los hongos en el laboratorio. Géneros como Fusarium, Aspergillus, Entomophthora, Penicillium y Paecilomyces fueron aislados tanto de termitas como de los termiteros y uno o más sustratos. Esto da cuenta de su asocio a las termitas y a los sustratos cer- canos a ellas en las condiciones propias del área de estudio. Dichos hongos apare- cen como de especial interés y potenciales candidatos para posteriores pruebas de patogenicidad en el laboratorio y campo.
De acuerdo con el presente estudio y estu- dios de patogenicidad previos realizados por otros autores, es probable que estos hongos estén regulando las poblaciones de termitas en condiciones naturales en las plantaciones de eucalipto en la refo- restadora San Sebastián. Tanto Entomo- phthora, como Aspergillus, Fusarium y Paecilomyces habían sido encontrados previamente en condiciones naturales o de laboratorio asociados a termitas (Espe- ro 1984; Khan et al. 1990a; Khan et al. 1991; Khan et al. 1994; Chai 1995). In vitro se ha encontrado que termitas ex- puestas a superficies tratadas con dosis de Entomophthora tan bajas como 1,4 x 10³ esp/ml presentaron porcentajes de morta- lidad del 95% en 2,5 días (Espero 1984). Las termitas infectadas perdieron locomo- ción y su cuerpo se tornó amarillento. Des- pués de la muerte el cuerpo del insecto se oscureció y fue cubierto de micelio y espo- ras consideradas como nueva fuente de inóculo. Entomophthora es un controla- dor importante en ambientes naturales bajo condiciones cálidas y húmedas. No obstante, su uso como insecticida bioló- gico se dificulta por sus niveles infectivos bajos en condiciones moderadas de hu- medad y por su producción masiva com- pleja (Douglas et al. 2001).
En cuanto al género Fusarium, F. avena- ceum había sido registrado previamente como patógeno de la termita subterránea Coptotermes formosanus en condiciones de laboratorio (Chai 1995). Aunque este es un hongo entomopatógeno facultativo generalista, dada la obtención de varios ais- lamientos nativos de la zona de San Sebastián en el presente estudio, valdría la pena realizar pruebas de patogenicidad para evaluar la infectividad en laboratorio y cam- po. A pesar de que este hongo presenta limitaciones para aplicaciones inundativas por la producción de toxinas y la patogenicidad de algunas especies para plantas y animales, se ha recomendado para aplicaciones localizadas como lo que sería el uso de cebos en el control de termitas.
El hongo Paecilomyces es ampliamente reconocido como hongo entomopatógeno por causar la enfermedad llamada muscardina amarilla. Entre las especies entomopatógenas han sido descritas P. farinosus, P. fumosoroseus, P. javanicus, P. ramosus, P. cinnamomeus y P. lilacinus (Tanada y Kaya 1993). Esta última se ha registrado de forma natural infectando termitas (Khan et al. 1990a, Khan et al. 1991). En el presente estudio P. lilacinus se encontró en una frecuencia alta (Fig. 2).

Termita (soldado) cubierto de micelio por el hongo Paecilomyces lilacinus. Fotografía Felipe Cardona, U. de A.
Crecimiento de hongos Ascomycetes y Anamórficos aislados de los diferentes sustratos en medios de cultivo
Fuentes de aislamiento: Tv = Termitas vivas, Tm = Termitas muertas, S = Suelo, M= Madera, Tse = Tronco seco de eucalipto, He = Hojas de eucalipto, Ft=Fragmento de termitero. Medios de cultivo: PDA = Agar papa dextrosa, MEA = Agar extracto de malta, SDA = Agar sabourad dextrosa
Fuentes de aislamiento: Tv = Termitas vivas, Tm = Termitas muertas, S = Suelo, M = Madera, Tse = Tronco seco de eucalipto, He= Hojas de eucalipto, Ft = Fragmento de termitero. Medios de cultivo: PDA = Agar papa dextrosa, MEA = Agar extracto de malta, SDA = Agar Sabouraud dextrosa.
Goettel e Inglis (1997) señalan que esta especie parece ser más frecuente en regio- nes cálidas como la región en la cual se encuentran los eucaliptos afectados por termitas. Adicionalmente, es típicamente aislada de suelos, lo cual la convierte en un candidato potencial como biocontro- lador en el área de San Sebastián de Buenavista (Magdalena) en especial para las termitas subterráneas como Coptoter- mes encontradas en el presente estudio.
El efecto patogénico de otras especies de Paecilomyces como P. caterniannulatus, P. farinosus y P. variotu ha sido probado en condiciones de laboratorio sobre termitas utilizando como inóculo suspensiones acuosas de 6 x 107 esp/ml aplicadas a una termita cebo. P. fumosoroseus fue el más efectivo mostrando una infectividad del 86,7% (Chai 1995).
El hongo más abundante en el presente estudio fue Aspergillus. Muchas de las es- pecies de este hongo son saprofíticas, lo cual probablemente explica el porcentaje alto y frecuencia de su hallazgo (Fig. 1). No obstante, en condiciones naturales Aspergillus ha sido encontrado infectan- do un amplio rango de insectos (Tanada y Kaya 1993; Ulloa y Herrera 1994). En el presente estudio, tanto en el laboratorio como en el invernadero donde se estable- cieron algunas colonias, se registraron al- tos porcentajes de mortalidad de termitas causados por Aspergillus. El efecto patogénico sobre las termitas fue verifica- do in vitro. Previamente, algunos autores registraron A. ochraceus causando morta- lidades altas para termitas en condiciones de laboratorio. En pruebas in vitro se ob- tuvieron mortalidades del 70% sobre termitas cuando éstas se trataron por as- persión con concentraciones de 1,4 x 10³ esp/ml. A. niger causó también altas mor- talidades sobre termitas Microtermes uni- color, Microcerotermes championi y Heterotermes indicola cuando fueron puestas a caminar sobre cultivos del hon- go durante diferentes tiempos. Observán- dose porcentajes de mortalidad del 100% a los 10, 20 minutos después de la exposi- ción (Khan et al. 1994).
El hongo Cunninghamella, encontrado en el presente estudio en sustratos rela- cionados con las termitas, fue previamen- te registrado en nidos de termitas Reticulitermes flavipes (Ramakrishnan et al. 1999). Este hongo ha sido también reconocido como entomopatógeno de huevos y larvas de Diptera en condicio- nes de laboratorio y huevos de reptiles en condiciones naturales (Vallejo et al. 1996).
En cuanto a las especies del género Penicillium se encontraron Penicillium sp., el de mayor frecuencia, seguido por P. verrucosum y P. chrysogenum, P. para- herquei y P. expansum. Penicillium es quizá el hongo más ubicuo de todos, con gran cantidad de especies (Samson et al. 1984; Ulloa y Herrera 1994). En condiciones de campo se ha evaluado la diseminación del hongo Penicillium verrucosum en termiteros de Anacanthotermes ahnge- rianus encontrándose persistencia del mis- mo en las condiciones ambientales evaluadas (Tanada y Kaya 1993; Samson et al. 1984 L[j]utikova 1990). Esto sugiere el potencial de algunos de los aislamien- tos del presente estudio para evaluacio- nes posteriores. Del hongo Verticillium, conocido como entomopatógeno para al- gunas especies de insectos, se encontró un sólo aislamiento que corresponde al 1,39% del total de hongos aislados.
Entre los hongos ambientales y saprofíticos aislados se encontraron Mucor (M. circine- lloides, M. racemosus, M. hiemalis y M. plumbeus), Syncephallastrum y Zygorr- hynchus. Del género Rhizopus se hallaron especies como Rhizopus stolonifer y Rhizpus arrhizus. Además, Absidia corymbifera, Pythium, Allomyces javanicus, Acrostalag- mus, Acremonium, Byssochlamys, Discosia, Tritirachium, Chalaropsis, Plasmodiophora, Eurotium, Pestalotia, Rhizoctonia y Clados- porium. Estos hongos son saprófitos y viven en el suelo o en lugares húmedos (Samson et al. 1984; Ulloa y Herrera 1994).
En conclusión, de las especies de hongos aislados se encontraron ocho entomopa- tógenos, los cuales se han señalado pre- viamente para termitas (Espero 1984; Khan et al. 1990a; L[j]utikova 1990; Khan et al. 1991, 1994; Chai 1995; Ramakrishnan et al. 1999). Entre los hongos más promi- sorios como agentes de control microbio- lógico para termitas en la reforestadora está Paecilomyces spp. De acuerdo con Wright et al. (2001), Paecilomyces fumoso- roseus y P. javanicus son útiles para controlar infestaciones de termitas subte- rráneas, particularmente de la familia Rhinotermitidae entre la cuál se encuen- tra el género Coptotermes registrado ata- cando Eucalyptus tereticornis en el presente estudio. Propágulos del hongo como blastosporas y conidias, que pue- den ser cultivadas de forma fácil y econó- mica e incorporadas en formulaciones, han sido utilizados con éxito para proteger ár- boles vivos, estructuras de madera y otros materiales celulósicos susceptibles a la in- festación y daños.
Existen diferencias de opinión respecto a la utilidad de aislamientos originarios de los insectos a los cuales se dirigen las apli- caciones de dichos hongos como medida de control. Algunos autores sugieren un aumento en la efectividad cuando los ais- lamientos provienen de otros hospederos o cuando han sido reactivados sobre el insecto a controlar (Khan et al. 1990b; González et al. 1993). En este sentido los aislamientos encontrados en el presente estudio directamente sobre las termitas y que poseen características de adaptación a las condiciones climáticas y ecológicas del área, deberán seleccionarse cuidado- samente en pruebas de laboratorio y cam- po, antes de poder recomendarse como elementos de un manejo integrado de termitas. No obstante, su presencia aso- ciada a las termitas en los eucaliptales de la reforestadora los convierte en candida- tos potenciales como agentes biocon- troladores. Así mismo, es importante considerar aquellos aislados a partir de los sustratos, para los cuales debe verificarse la patogenicidad aún cuando se hayan re- gistrado previamente afectando termitas. Entre los criterios de selección más impor- tantes de los aislamientos, se encuentran los mencionados previamente en la intro- ducción como mortalidad intrínseca de las termitas, dosis letal 50 (DL50) y tiempo letal 50 (TL50), entre otros.
El reconocimiento de los hongos asociados a las termitas en condiciones naturales y de laboratorio constituye un elemento básico como punto de partida para el control mi- crobiológico de las mismas. No obstante, la inclusión de aislamientos derivados de otros insectos con actividades importantes de patogenicidad comprobada y efectividad en campo, debería considerarse en las pruebas de susceptibilidad in vitro
Footnotes
Agradecimientos
Los autores agradecen al personal de la reforestadora San Sebastián por su hospi- talidad y colaboración; al profesor Abel Díaz Cadavid M.Sc por el análisis de distri- bución y frecuencia de los hongos, a la profesora Gloria Machado por la revisión del manuscrito, a Mónica Zuluaga, Beatriz Betancur, Carmén Vásquez, Inés Elena Giraldo y Beatriz Cardona por el soporte técnico y trabajo de campo y a la Corpora- ción de Patologías Tropicales, al Instituto de Biología de la Facultad de Ciencias Exac- tas y Naturales y al CODI de la Universidad de Antioquia por el apoyo y financiación de esta investigación.
