Abstract
Many species of higher plants produce secondary metabolites, to which ecological functions and defense against microorganisms and phytophages are attributed. The objective of this work was to understand the susceptibility of Ae. aegypti and An. albimanus larvae to two types of acetogenins extracts obtained from seeds of Annona muricata. The two species of Culicidae studied were highly susceptible to both kinds of extracts under laboratory conditions. The mean lethal concentrations (CL50) for the polar, nonpolar and mix of acetogenins extracts for Ae. aegypti were 74,7 ppm, 236,2 ppm and 20,3 ppm, respectively, while in An. albimanus they were 0,8 ppm, 16,2 ppm and 1,4 ppm. The diagnostic doses are presented with their respective range of variation. The differences in mortality produced by the extracts were not statistically significant. An option for its use could eventually be determined when the residuality of both compounds and the cost-benefit ratio are evaluated.
Introducción
Dengue y malaria son dos enfermedades transmitidas por vectores, de gran importancia en salud pública. La prevalencia del dengue está asociada a su principal vector Aedes aegypti (Linnaeus), es endémica en más de 100 países y unos 2.500 millones de personas están ahora en riesgo de contraer la enfermedad. Según la Organización mundial de la salud (O. M. S) pueden presentarse unos 50 millones de infecciones por dengue cada año. En el año 2002 se presentó la cifra más alta de casos de dengue en las Américas, 1'019.196 casos fueron registrados, de los cuales 17.363 fueron de dengue hemorrágico, presentándose 225 muertes. Colombia mostró un comportamiento similar con 81.831 casos, de los cuales 5.245 fueron de dengue hemorrágico (OPS 2002). Se considera que en Colombia aproximadamente 18 millones de personas se encuentran en áreas de riesgo para dengue (Camacho 1991).
La malaria humana es transmitida por mosquitos del género Anopheles. En el ámbito mundial se calcula que aproximadamente el 40% de la población está expuesta a esta enfermedad en unos 91 países o áreas y en el continente Africano es responsable por la muerte de 1,4 a 2,6 millones de personas cada año (WHO 1995). Se ha calculado una incidencia anual de 488 millones de casos en el mundo, de los cuales 14,8 millones se presentan en Centro y Suramérica (Sturchler 1989). En las Américas el 36,5% de la población vive en zonas ecológicamente propicias para la transmisión de la malaria. En éstas, para 1998 y 1999, se presentó una morbilidad de 418,3 y 404,4 casos por 100.000 habitantes (OPS 1999).
La malaria representa un grave problema de salud en el 85% del territorio rural colombiano (MINSALUD 2002). En la actualidad una serie de factores sociales, económicos, climáticos y administrativos han contribuido al incremento en la tasa de prevalencia de la malaria, la cual fue especialmente alta en 1998 cuando alcanzó una cifra de más de 250.000 casos (OPS/OMS 2000).
Aedes aegypti como vector del dengue clásico, dengue hemorrágico y fiebre amarilla urbana y Anopheles albimanus Wiedemann, como vector de malaria, son vectores primarios en las Américas, por lo tanto es prioritario adelantar estrategias de manejo y desarrollar nuevas tecnologías que permitan tener alternativas química o biológicas, en el caso de que las ya existentes no sigan siendo útiles por problemas de resistencia o tengan poca eficiencia en su control.
En la actualidad más de 200 especies de artrópodos de importancia médica han mostrado resistencia a muchos de los pesticidas contemporáneos; cada vez es más necesario desarrollar químicos más potentes, originando mayores costos económicos y ambientales (Brown 1986). Estos problemas han popularizado el concepto de manejo integrado de plagas, que implica trabajar no sólo en la búsqueda de controladores biológicos y manejo ambiental, sino también en la investigación del posible uso de insecticidas botánicos, los cuales tienen la ventaja de proveer modos de acción novedosos que reducen el riesgo de resistencia cruzada, que sean eficaces, más seguros para el medio, que sean degradables y más específicos para las especies de mosquitos, produciendo poco o ningún impacto ambiental (Arnanson et al. 1989).
Numerosas especies de plantas superiores producen metabolitos secundarios a los cuales se les atribuye funciones ecológicas y de defensa contra microorganismos y fitófagos (Rosenthal 1986). Actúan principalmente como toxinas a través de los estados de vida de las especies de insectos, otros interfieren en el desarrollo y la reproducción o pueden actuar a nivel de los receptores olfatorios siendo responsables de atracción o repelencia (Sukumar et al. 1991).
Varios insecticidas orgánicos han sido extraídos y/o sintetizados a partir de plantas. Entre los innumerables compuestos insecticidas de origen botánico que han sido sintetizados son de renombre la nicotina, las piretrinas y la rotenona (Matsumura 1975). Cambell et al. (1933) usando alcaloides extraídos de Anabasis aphylla L (Caryophyllales: Amaranthaceae), demostró efectividad sobre larvas de Culex pipiens Linnaeus, Cx. territans Walker y Cx. quinquefasciatus Say.
De las semillas de Annonaceae se han aislado sustancias conocidas como acetogeninas. En esta familia se incluyen más de 2.000 especies. De éstas solamente 150 (7%), pertenecientes a 43 géneros (33%), han sido investigadas (Leboeuf et al. 1982).
Las acetogeninas de Annonaceas son una serie de productos naturales de origen policétido derivados de ácidos grasos con 35 a 37 carbonos, su estructura general está caracterizada por una gran cadena alifática con un grupo metil terminal, una gran lactona insaturada con un metil como sustituyente, uno o dos anillos tetrahidrofurano y varios sustituyentes hidroxilo o cetónicos (Roblot et al. 1993). Éstas presentan un amplio rango de actividades biológicas inmunosupresivas, antiparasitarias, citotóxicas, antimicrobianas, pesticidas y antitumorales (Correa y Bernal 1989). La primera acetogenina aislada fue el uvaricin (Cavé 1993).
Entre las especies del género Annona se destacan por sus propiedades insecticidas: A. cherimolia, A. glabra, A. muricata, A. squamosa, A. melitu, A. palustri, A. reticulata y A. spinescens (Atheortua 1994). Las acetogeninas características de A. muricata son las monotetrahidrofuránicas. La primera acetogenina aislada de esta especie fue el Annonacin en 1987 (Myint et al. 1991). Mikolajczak et al. (1988, 1989) patentaron acetogeninas de annonaceas como sustancias para el control de plagas, Moeschler et al. (1986, 1987) patentaron la acetogenina Annonin como un insecticida.
Una posible utilización de semillas de A. muricata es su procesamiento para obtención de acetogeninas naturales para control de algunas plagas. En este trabajo se presentan y analizan los resultados de evaluaciones realizadas bajo condiciones de laboratorio de extractos de semillas de A. muricata (mezcla de acetogeninas) así como el extracto polar y no polar obtenido de la mezcla, sobre larvas de Ae. aegypti y An. albimanus.
Materiales y Métodos
El trabajo se desarrolló en los laboratorios de Entomología de la Universidad del Valle, con una temperatura promedio de 26°C y una humedad relativa del 70%. La extracción de los principios biológicamente activos de A. muricata se realizó en los laboratorios de productos naturales del departamento de Química de la Universidad del Valle.
El análisis químico de las semillas mostró la presencia de acetogeninas lactónicas monotretrahidrofuránicas. La extracción del extracto no polar se hizo con éter de petróleo en un equipo soxleht a partir de 325 g de semilla molida, previamente secada a 60°C. Este extracto se sometió a temperaturas bajas para lograr la precipitación de las acetogeninas. Al marco obtenido después de esta extracción se le adicionó etanol como solvente y se obtuvo el extracto polar. Luego, la muestra se trasladó a un rotoevaporador con el fin de eliminar el solvente a presión reducida y obtener la muestra concentrada libre de solvente orgánico, el rendimiento promedio de la extracción fue de 22,5% de extracto no polar, 6,39% de extracto polar y 0,80% de acetogeninas.
Los especímenes de Ae. aegypti se obtuvieron de una colonia de la sección de Entomología de la Universidad del Valle. Los de An. albimanus fueron proporcionados por el insectario del Instituto de Inmunología de la Universidad del Valle.
Establecimiento de la línea base de susceptibilidad
Con base en ensayos preliminares de laboratorio, se establecieron cuatro a siete concentraciones de cada uno de los extractos a ser evaluados, cada concentración se probó con 20 a 25 larvas de tercer y cuarto estadio temprano de Ae. aegypti y An. albimanus en vasos de precipitado de 600 ml, previamente esterilizados en autoclave. Para preparar las concentraciones se utilizó un volumen de 250 ml de agua filtrada, teniendo tres a cuatro repeticiones por tratamiento y las siguientes dosis para Ae. aegypti: extracto no polar 1.800, 600, 300, 150, 75 y 37,5 partes por millón (ppm). Para el extracto polar, además de las dosis anteriores se adicionó otra de 18,7 ppm.
Para An. albimanus se evaluaron las siguientes dosis del extracto no polar: 600, 150, 75, 37,5, 18,7 y 9,4 ppm. Para el extracto polar se adicionó una dosis de 4,7 y se eliminaron las de 150 y 300 ppm. La mortalidad se evaluó a las 24 h postratamiento. Se consideraron como larvas muertas aquellas que al ser punzadas en la región cervical o en el sifón no presentaron movimiento alguno. Con ambas especies, para cada extracto, se tuvo su respectivo control; para el extracto no polar se utilizó como emulsionante triona (aceite mineral), el cual fue adicionado también a su respectivo control. Las larvas que se transformaron en pupas durante la prueba, fueron desechadas del análisis. Para porcentajes de mortalidad menores que el 20%, se hicieron ajustes con respecto a lo observado en el grupo testigo de cada ensayo, mediante la formula de Abbott (1925).
La construcción de la línea de regresión dosis mortalidad, así como las diferentes concentraciones letales, se calcularon por medio del programa de análisis Log-Probit elaborado por Raymond (1985). También se hizo un análisis de varianza de dos vías en donde la variable de respuesta fue la mortalidad observada y los factores las dos especies y tipo de extracto. Previamente se realizó una validación de los supuestos de normalidad y de homogeneidad de varianza (prueba de Bartlett) y con base en los resultados un postanova de Tukey entre las medias de mortalidad de los tratamientos (extractos) seleccionando como variables las dosis.
Residualidad
Con base en la línea base de mortalidad calculada anteriormente, se prepararon 9.000 ml con la dosis diagnóstica de cada extracto en frascos bomboneros de vidrio previamente esterilizados. Estos se taparon con papel aluminio y se expusieron a 12 h de luz solar diariamente. Para los extractos no polar y mezcla de acetogeninas se adicionó Kembol® como coadyuvante. Durante los primeros ocho días, cada dos días se probaron cuatro repeticiones en vasos de precipitado con 250 ml de cada extracto con larvas de Ae. aegypti de tercero y cuarto estadio temprano. Las pruebas se continuaron cada 15 días en los días subsiguientes. Este procedimiento se mantuvo hasta los ocho meses o hasta obtener una mortalidad menor que el 50%.
Resultados
A las 24 h postratamiento ambos tipos de extractos produjeron mortalidad. Con el extracto no polar en Ae. aegypti la dosis mayor (1.800 ppm) produjo 100% de mortalidad, mientras que la menor (37,5 ppm) produjo 3% de mortalidad (Tabla 1). En An. albimanus la dosis que produjo el 100% de mortalidad fue de 600 ppm; con la de 37,5 ppm se obtuvo una mortalidad corregida del 64,7% (Tabla 2). Con el extracto polar las concentraciones letales fueron más bajas. En Ae. aegypti si bien fue necesaria la concentración de 1.800 ppm para obtener el 100% de mortalidad, la dosis de 37,5 ppm produjo 24% de mortalidad (Tabla 3).
Mortalidad larval de Ae. aegypti obtenida con seis concentraciones de extracto no polar de acetogeninas, bajo condiciones de laboratorio
gl = 3 Xβtab 0,05 = 7,815 Xβtab < Xβcal
Mortalidad en el control 2%.
Mortalidad larval de An. albimanus obtenida con seis concentraciones de extracto no polar de acetogeninas, bajo condiciones de laboratorio
gl = 4 Xβtab 0,05 = 9,49 Xβtab > Xβcal
Mortalidad en el control 10%.
Mortalidad larval de Ae. aegypti obtenida con siete concentraciones de extracto polar de acetogeninas, bajo condiciones de laboratorio
gl = 5 Xβtab 0,05 = 11,070 Xβtab > Xβcal
Mortalidad en el control 0%.
En An. albimanus fue necesario únicamente una concentración de 75 ppm para obtener un 100% de mortalidad (Tabla 4). Con las mezclas de acetogeninas, en las dos especies se obtuvieron respuestas de mortalidad con la misma tendencia de susceptibilidad observada en los extractos. En Ae. aegypti como en An. albimanus 75 ppm causaron el 100% de mortalidad, pero la dosis de 9,2 ppm causó una mortalidad del 9% en Ae. aegypti (Tabla 6), mientras que en An. albimanus fue del 79,6% (Tabla 7). La mortalidad causada por los extractos fue significativamente diferente entre las dos especies de mosquitos (P=0,0003) y tanto en Ae. aegypti como en An. albimanus los extractos polar y no polar actuaron significativamente diferente al igual que entre el polar y la mezcla de acetogeninas. Entre los extractos no polar y la mezcla de acetogeninas no se observaron diferencias significativas en cuanto a la mortalidad producida por ellos.
Mortalidad larval de An. albimanus obtenida con cinco concentraciones de extracto polar de acetogeninas, bajo condiciones de laboratorio
gl = 3 Xβtab 0,05 = 7,81 Xβtab > Xβcal
Mortalidad en el control 0%.
El análisis de varianza realizado, considerando la especie y el tipo de extracto, mostró diferencias significativas entre la mortalidad causada por el tipo de extracto en las dos especies de mosquitos (F = 11,5; P = 0,0003). El análisis postanova de Tukey mostró que en ambas especies los dos extractos y las mezclas de acetogeninas actuaron de manera significativamente diferente (P< 0,005) (Tabla 5). Para ambas especies, entre el extracto no polar y la mezcla de acetogeninas, no se presentaron diferencias estadísticas significativas; sin embargo, presentaron pendientes diferentes (Figs. 1 y 2).
Postanova de Tukey para comparar la mortalidad promedio causada por los extractos polar no polar y mezcla de acetogeninas sobre larvas de Ae. aegypti y An. albimanus
Significativamente diferente con una probabilidad de 0,005.
Mortalidad larval de Ae. aegypti obtenida con cuatro concentraciones de mezcla de acetogeninas, bajo condiciones de laboratorio
gl = 2 Xβtab 0.05 = 5,99 Xβtab > Xβcal
Mortalidad en el control 0%.
Mortalidad larval de An. albimanus obtenida con cinco concentraciones de mezcla de acetogeninas, bajo condiciones de laboratorio
gl = 3 Xβtab 0,05 = 7,81 Xβtab > Xβcal
Mortalidad en el control 10%.
Establecimiento de la línea base de susceptibilidad
Al graficar la línea base de susceptibilidad del logaritmo de la dosis versus porcentaje de mortalidad observada sobre Ae. aegypti, se obtuvo una línea recta de pendiente elevada (Fig. 1) producto de puntos bien ajustados a una línea de regresión (nivel de confianza del 95%) lo cual influye en los rangos estrechos de las concentraciones letales (Tabla 8) y aporta a la CL 50 una varianza baja (0,0004) mostrando además que los resultados obtenidos son homogéneos. Las pendientes obtenidas con el extracto polar y no polar fueron menores que las de la mezcla de acetogeninas; sin embargo, los datos también son homogéneos y la amplitud de los intervalos de confianza fue mayor que la de la mezcla. En el proceso de cálculo de las concentraciones letales del extracto no polar sobre Ae. aegypti (Tabla 8), el análisis mostró que los datos no representaban una línea recta bien ajustada, esto se manifestó en el valor total de Chi cuadrado resultante de la interacción entre la mortalidad esperada versus la mortalidad observada, el cual fue muy elevado en la dosis de 150 ppm (X2 = 6,13); lo anterior condujo a un valor total de Chiβ calculado más alto (X2 = 11,58) que el Chiβ tabulado (X2 = 7,8) (Tabla 1).
Todos los valores de las pendientes de las líneas, obtenidas con los tres tipos de extractos evaluados en An. albimanus, fueron bajos, con datos bien ajustados a una línea de regresión, (Fig. 2) pero a diferencia de Ae. aegypti las concentraciones letales fueron más bajas (Tabla 8) y con intervalos de dosis muy amplios en el caso del extracto polar de la mezcla de acetogeninas, especialmente la CL99. Con base en estos resultados las dosis diagnósticas para Ae. aegypti fueron de 3.046 ppm, 4.072 ppm y 148,1 ppm para el extracto polar, no polar y mezcla de acetogeninas, respectivamente.
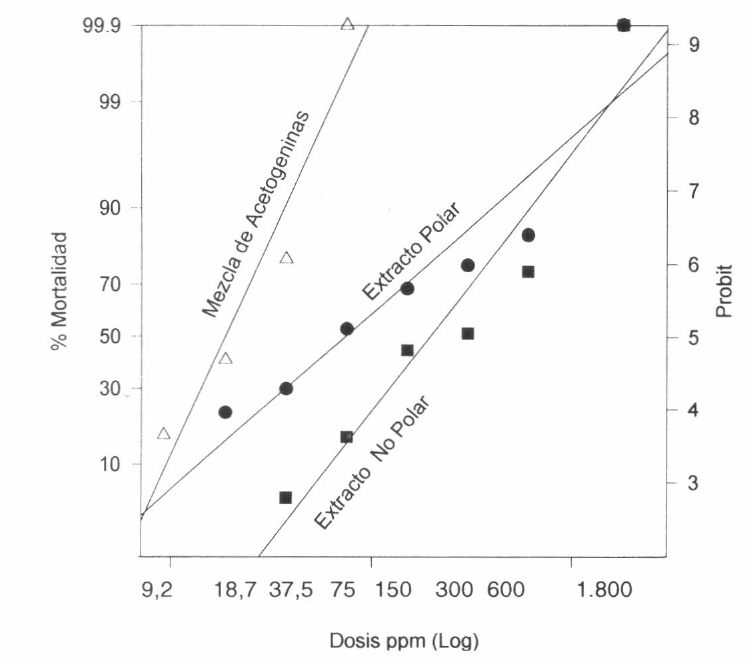
Líneas de regresión del porcentaje de mortalidad observada de Ae. aegypti vs. el logaritmo de la dosis de extractos polar, no polar y mezcla de acetogeninas, bajo condiciones de laboratorio.
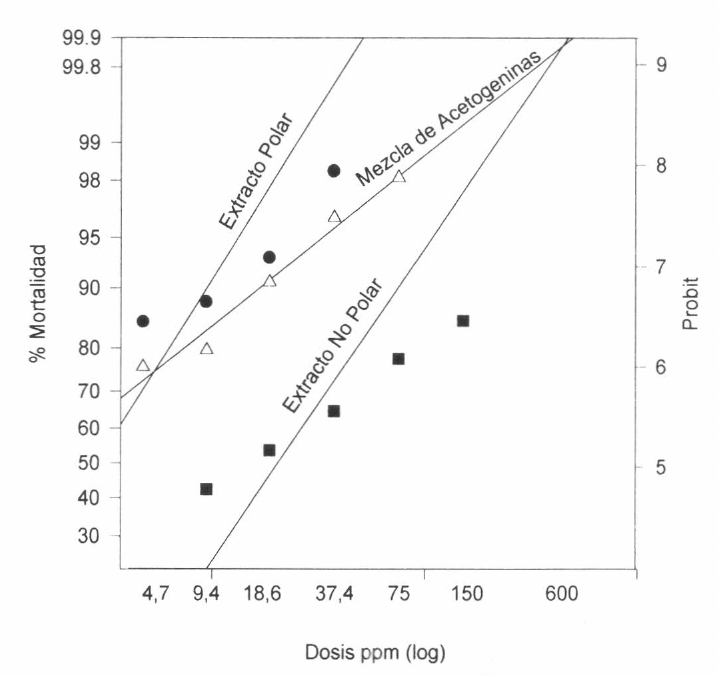
Líneas de regresión del porcentaje de mortalidad observada de An. albimanus vs. el logaritmo de la dosis de extractos polar, no polar y mezcla de acetogeninas, bajo condiciones de laboratorio.
Residualidad
Las pruebas realizadas en Ae. aegypti hasta ocho meses después de exponer los dos tipos de extractos a luz solar, fueron compatibles con una residualidad alta (100%), con variaciones en el tiempo letal medio. Con el extracto no polar se observó adicionalmente una posible acción mecánica sobre larvas y pupas ya que aparentemente la condición aceitosa del extracto bloquea la entrada de aire a través del sifón de las larvas y las trompetas respiratorias de las pupas. Sin embargo, la residualidad se redujo considerablemente cuando se utilizó el producto de las acetogeninas sin separación de los extractos polar y no polar, ya que a partir de los 20 días no se observó mortalidad de larvas.
Discusión
Los resultados con estos extractos se pueden considerar promisorios, ya que se encuentran por debajo de la concentración máxima (5.000 ppm) recomendada por la Agencia de Cooperación Técnica Alemana (GTZ) para condiciones de laboratorio (Hellpap 1993).
No es sorprendente la actividad insecticida de los dos extractos de A. muricata sobre larvas de Ae. aegypti. Ohsawa et al. (1990), con extractos de Annona glabra, A. montana, A. muricata, A. squamosa, A chirimolia y A. reticulata, observaron un porcentaje variable de mortalidad sobre Callosobruchus chinensis (Coleoptera: Bruchidae) al actuar por contacto. A. squamosa presenta acetogeninas bistetrahidofuránicas las cuales poseen una acción biológica mayor que las monotetrahidrofuránicas de A. muricata (Rupprecht et al. 1990). Feras et al. (1999) en una revisión sobre este tema, señalaron un exitoso manejo de cucarachas (Blatella germanica) resistentes a los grupos insecticidas tradicionales, utilizando acetogeninas de anonáceas.
Sobre Culicidae, extractos de hojas y semillas de A. squamosa han mostrado actividad insecticida sobre larvas de Anopheles. Saxena et al. (1993 a), utilizando extractos de hojas de esta planta, obtuvieron una CL50 que varió entre 126 y 178 ppm sobre larvas de An. stephensi. Saxena et al. (1993 b) utilizando extractos de semillas obtuvieron una CL50 de 213,79 ppm sobre larvas de An. culicifacies. Por otro lado, Cepleanu (1993) con extractos de A. purpurea observó una CL100 de 10 ppm en larvas de segundo ínstar de Ae. aegypti.
Dosis letales obtenidas con extracto polar y no polar de acetogeninas sobre larvas de Ae. aegypti y An. albimanus, bajo condiciones de laboratorio. (Nivel de confianza 0,95)
Posiblemente los dos tipos de extractos actúan por ingestión, pero habría que diseñar una metodología diferente para precisar su modo de acción. Considerando el tiempo letal de los extractos sobre larvas de Ae. aegypti y An. albimanus, la mayor rapidez con que se inicia la acción de los extractos polares se debe posiblemente a que las larvas ingieren más fácil y rápidamente el extracto polar a diferencia del extracto no polar, el cual queda en mayor cantidad en la superficie y las larvas sólo al respirar por el sifón se impregnan de aceite y lo ingieren cuando limpian su sifón con los peines bucales. Por lo menos en las concentraciones más elevadas del extracto no polar, se presenta aparentemente cierto efecto mecánico. Es de suponer que el extracto polar forma una solución más homogénea que el no polar. Para poder emulsionar el extracto no polar y la mezcla de acetogeninas, se ensayaron varios productos comerciales tales como Triona®, Dimetil sulfóxido (DMSO) y Kemkol®, los cuales no necesariamente tienen los mejores resultados al mezclarse con el agua y aparentemente retrasan la acción del ingrediente activo. Esta dificultad hizo que posiblemente los resultados observados con el extracto no polar, produjeran en el análisis probit valores relativamente altos de X2, lo cual es indicativo de que el grado de distribución de los datos alrededor de la línea de regresión dosis-mortalidad sea alto. La interpolación de dos de los datos fue suficiente para obtener un mejor ajuste de la línea de regresión e hizo que los datos no fueran significativamente heterogéneos, la cual en este caso, puede ser atribuido a factores claramente ambientales.
La buena residualidad observada de los extractos polar y no polar indican que posiblemente presenten otros componentes adicionales a las acetogeninas que les confieren buena estabilidad a la luz especialmente a luz ultravioleta.
Estos resultados son promisorios para el control de larvas de Ae. aegypti y An albimanus, y posiblemente para otras larvas de Culicidae. Sin embargo, parece ser que la respuesta de cada especie es variable con respecto a la dosis diagnóstica y al rango de toxicidad de las dosis, para An. albimanus se debió haber establecido un mayor rango de dosis hacia las de menor concentración, por que según lo observado fueron más susceptibles que las de Ae. aegypti.
La alta toxicidad y residualidad de los dos extractos conteniendo acetogeninas, observadas bajo condiciones de laboratorio, ameritan la realización de evaluaciones a pequeña escala en condiciones de campo, en donde se evalúe igualmente si la estabilidad del producto, determinante de su residualidad, observada en laboratorio, es igualmente válida en condiciones naturales y determinar cuál es el impacto ambiental sobre la fauna asociada de los criaderos de Ae aegypti y An. albimanus u otras especies de mosquitos que se reproduzcan en aguas lénticas o en donde sea viable de realizar este tipo de aplicación. De igual modo, se debe evaluar en condiciones naturales, el por qué de la poca estabilidad observada en la mezcla de acetogeninas, posiblemente esto sea más bien un problema de la dosis diagnóstica empleada (148,1 ppm), la cual fue comparativamente mucho más baja que la de los extractos por separado y no de la formulación propiamente dicha. En este sentido es recomendable evaluar una dosis diagnóstica más alta, similar a la de los extractos polar y no polar.
Footnotes
Agradecimientos
Los autores agradecen a Sandra Garzón por el trabajo de laboratorio, a los profesores de la sección de Entomología, del departamento de Biología, por la revisión del manuscrito. Así mismo, a la Universidad del Valle por el apoyo y la colaboración brindada para la realización de esta investigación. A los laboratorios de productos naturales del departamento de Química y Entomología del departamento de Biología por proveer facilidades logísticas. Al Instituto de Inmunología de la Universidad del Valle por proporcionar larvas de An. albimanus.
