Abstract
Summary
The phylogenetic route of Drosophila starmeri (Wasserman, Koepfer & Ward), chromosome 2, was established from two populations in the Colombian North Coast (Camarones and Santa Marta) and from a third one located in the Tatacoa desert (Rosalía). The latter was separated from the first two populations by more than 1.200 kilometers. The phylogenesis is summarized in the map, that was made using the method of the overlapped inversions and the techniques of chromosomal microphotography and scanner digitization. According to the results, the standard arrangement of the Drosophila starmeri chromosome 2 stems from the Drosophila martensis standard for four overlapped inversions. This chromosome shows polymorphism in three different arrangements. In this paper, we propose a new phylogenetic for chromosome 2. The results could be interpreted as a reflection of the genetic divergence between the populations of the North Coast and the Tatacoa, with a presumed interruption of the genetic flow. This divergence begins to be observed through the morphological and reproductive isolation studies done on the same populations, by groups researching cytogenetic, phylogeny and populations evolution, from the Universities of Tolima and Andes.
Introducción
El grupo repleta es uno de los más grandes del género Drosophila. Cuenta actualmen te con 89 especies descritas y posiblemen te existan otras formas aún sin describir. En la evolución cromosómica del grupo, se re gistran 300 inversiones, que han logrado mantenerse (Wasserman 1954, 1982; Polanco 1999).
Las especies del grupo repleta son de gran importancia en los estudios de evolución, ya que aportan evidencia científica tangible de especiación en diversas poblaciones na turales. Un ejemplo de especiación en el grupo repleta es señalado por Ruiz y Wasserman (1993), quienes afirman que los tres enjambres del complejo buzzatii son alopátricos y que el enjambre stalkeri po dría ser tanto, el más primitivo, como el más avanzado evolutivamente. Este hecho se puede corroborar con estudios citogenéti cos, de biología molecular, morfológicos, ecológicos, o de aislamiento reproductivo, los cuales son comúnmente utilizados para determinar las relaciones filogenéticas en tre las especies del grupo repleta y entre otros miembros del género Drosophila (Wasserman 1982).
El enjambre martensis está compuesto por cuatro especies: D. martensis (Wasserman & Wilson), D. uniseta (Wasserman, Koepfer & Ward), D. starmeri (Wasserman, Koepfer & Ward) y D. venezolana (Ruiz y Fontdevila). Inicialmente se ubicó en el complejo mu lleri, pero ha sido trasladado por Ruiz y Wasserman (1993), al complejo buzzatii, que agrupa las especies de Suramérica, por no poseer la inversión 3a si no la 3rβ.
La evolución citológica del enjambre martensis sigue siendo en esencia la mis ma descrita por Wasserman y Koepfer (1979), la única diferencia radica en que en la evolución de la especie D. martensis ha cia D. buzzatii (Patterson & Wheeler), debe ser reversada. El ancestro del enjambre martensis debió haber presentado un alto polimorfismo que ha evolucionado en el presente a D. starmeri, el cual muestra una marcada diferenciación geográfica entre sus poblaciones. Las otras especies del enjambre emergieron de este ancestro fijando sus propias inversiones (Polanco 1998).
Se han realizado diversas investigaciones encaminadas hacia el esclarecimiento de los procesos evolutivos en el enjambre martensis, aprovechando las poblaciones naturales aisladas (costa norte colombiana y Desierto de la Tatacoa). Una de ellas es la de Castañeda (2000), quien realizó un aná lisis morfométrico para 8 caracteres. En este trabajo se afirma que entre las poblaciones de D. starmeri de Rosalía y las de la costa norte, existe una distancia genética, atribui da al obligado aislamiento geográfico y genético que se da entre ellas, lo que se guramente ha permitido que a lo largo del tiempo se vaya acumulando una gran can tidad de diferencias genéticas.
En el trabajo de Rojas (2001) se analiza el aislamiento reproductivo en especies del enjambre martensis (D. martensis, D. star meri y D. uniseta) y se concluye de forma general que entre las poblaciones de la mis ma especie se alcanza un grado de diver gencia genética representado en una disminución de los híbridos. Esta disminu ción es típica de poblaciones alopátricas, y aisladas como en el caso de la costa norte o la del Desierto de la Tatacoa. En contraste con lo anterior, cuando las poblaciones son relativamente aledañas como en el caso de Camarones y Santa Marta, no se observa una disminución en la productividad de los híbridos. Castañeda (2000) propone que aunque las poblaciones de la costa han pre sentado divergencia para algunos caracte res morfológicos, ésta parece no haber afectado la productividad de los híbridos pro venientes de cruces interpoblacionales.
Estudios realizados a nivel citológico en D. starmeri, en Suramérica, han arrojado di ferentes datos, como los presentados por Wasserman y Koepfer (1979), que plantean un cromosoma 2 hipotético 2abdβs⁶fβx y los arreglos 2abdβs⁶fβx⁶z⁶y⁶a⁷c⁷ y 2abdβs⁶fβx⁶z⁶a⁷ como posibles polimorfismos. Ruiz y Fontdevila (1981) registran la presencia de dos razas de D. starmeri, a las que se les denominó Occidental y Oriental. Una de las razas posee las inversiones 2z⁶, 2y⁶, 2a⁷, 2t⁶, 2q⁹, Xs y Xy y está restringida a la región Occidental que incluiría las localidades de Sta. Rita y Riohacha, en Colombia, y Cata y Lagunillas en Venezuela. La inversión 2w⁶ se encuentra solamente en la raza Orien tal, en la que se hallan las localidades de Zuata y Guaca en Venezuela.
Ruiz y Wasserman (1993) también señalan el arreglo 2abmnz¹eβ como el estándar y los arreglos 2eβ, 2fβ y 2z como posibles poli morfismos para D. starmeri.
Por otro lado, Polanco (1998) plantea una posible ruta filogenética para el cromosoma 2 estándar de D. martensis (el arreglo 2ABCDEFGabcd), de la población de Rioha cha, que difiere de los arreglos propuestos por los autores Wasserman y Koepfer (1979), Ruiz y Fontdevila (1981) y Ruiz y Wasserman (1993).
Materiales y Métodos
Los sitios de muestreo fueron: Camarones en cercanías a la ciudad de Riohacha (La Guajira), Santa Marta (Magdalena), y Rosalía en el Desierto de la Tatacoa (Huila) (Fig. 1). Dichos sitios se seleccionaron con base en trabajos anteriores, en los que se ha detecta do la presencia del enjambre martensis.
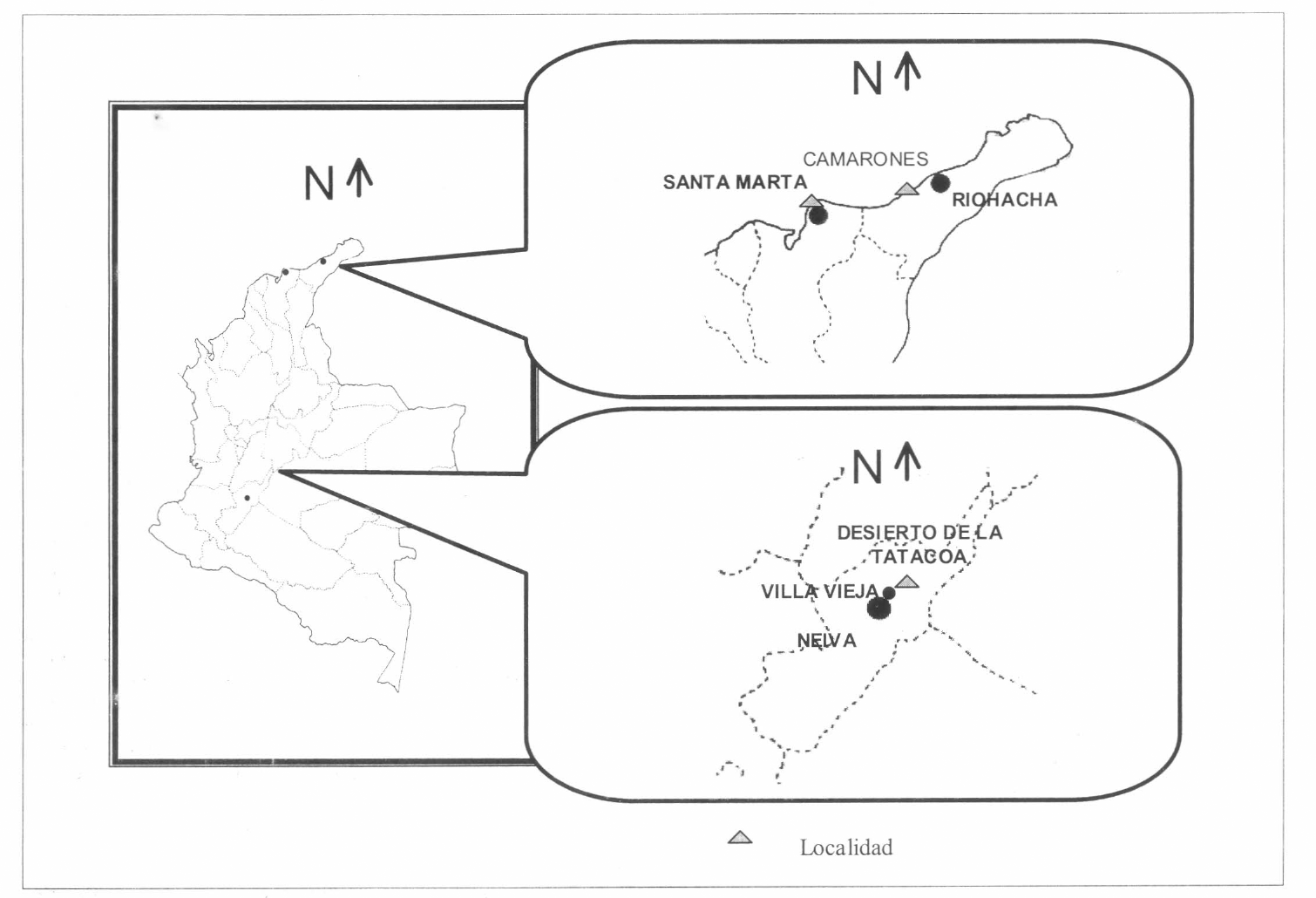
Sitios de muestreo. Costa Norte (Parte superior), en donde se observan las localidades de Santa Marta y Camarones. (Parte inferior) el Desierto de la Tatacoa (Huila). Obsérvese que en el mapa de la izquierda entre las poblaciones de la costa norte y el Desierto de la Tatacoa (Huila), existe una distancia de más de 1.200 kilómetros.
Las colectas se realizaron entre las 5:30-7:30 y 17:30-18:30 h. Una hora antes se colocaron las trampas para cebar las mos cas, las cuales estaban compuestas de di versas frutas fermentadas. Posteriormente, se capturaron las moscas con una jama de nylon, se clasificaron y cultivaron en labo ratorio.
Se realizaron cruces intraespecíficos, en los cuales se evidenciaron heterocariotipos, que constituyen un material ideal para ve rificar las filogenias ya que las zonas que comprenden los lazos (loops) permiten, en la mayoría de los casos, detectar los pun tos críticos que revelan las roturas que die ron origen a los arreglos que los conforman (Polanco 1982). Estos cruces intraes pecíficos se muestran con mayor detalle en la tabla 1.
Se disecaron las glándulas salivares de las larvas en tercer estadío, provenientes de los cultivos de D. starmeri y de los híbridos intraespecíficos y se les adicionó una gota de carnoy (o solución fijadora) por 1 minu to. Para la población de D. starmeri de la Tatacoa, el carnoy, se preparó en una pro porción de 3:1 de etanol, ácido acético. Para la población de D. starmeri, Santa Marta y Camarones y para todos los híbridos, se útilizó carnoy "modificado" en una propor ción de 4:3:1 de agua, etanol y ácido acéti co, respectivamente. Para la tinción se utilizó acetorceína láctica por tres horas, posteriormente se cubrió el preparado y se realizó el aplastamiento con un golpe de martillo de reflejos.
Una vez obtenidas las placas, se tomaron diversas fotografías del cromosoma 2 de cada una de las poblaciones muestreadas (Polanco 1998), a partir de las mismas se hizo el bandeo y se obtuvieron los mapas, que sirvieron como patrones para estable cer las secuencias de inversión de cada población. El patrón básico de bandeo uti lizado fue el mapa fotográfico de D. repleta (Wollaston) de Polanco (1998), por ser esta la única especie monomórfica del grupo repleta.
Posteriormente, se realizaron comparacio nes con las diferentes propuestas presen tadas por otros autores, para verificar la concordancia.
Para la elaboración de los mapas se utiliza ron un escáner ScanJet 6200C y el progra ma Adobe FotoDeluxe 2.0, que permitió intensificar los contrastes, ampliar varias veces determinadas zonas para facilitar el bandeo, modificar la posición de las imá genes, rotándolas en la dirección que se desea, adicionar la nomenclatura de ban deo y, finalmente, imprimirlas con un máximo de fidelidad, con la ayuda de una impresora láser.
Por último, se planteó la posible ruta filogenética del cromosoma 2 de D. starmeri por el método de las inversiones trasla padas (también llamadas complejas), el cual presenta una gran ventaja, pues se puede seguir el rastro que dejan las diferentes in versiones en un cromosoma determinado a lo largo de la evolución del mismo, y en consecuencia se puede postular una ruta filogenética en la que se evidencian las su cesivas reordenaciones, mas no la dirección de la evolución (Polanco 1998; Sturtevan y Dobzansky 1986; Ruiz et al. 1992).
Resultados y Discusión
El resultado del mapeo de D. starmeri muestra un homocariotipo igual para las tres poblaciones, observándose un heterocariotipo para la población de Santa Marta, la cual es polimórfica para las inversiónes f´ y e´ (Figs. 2-4).
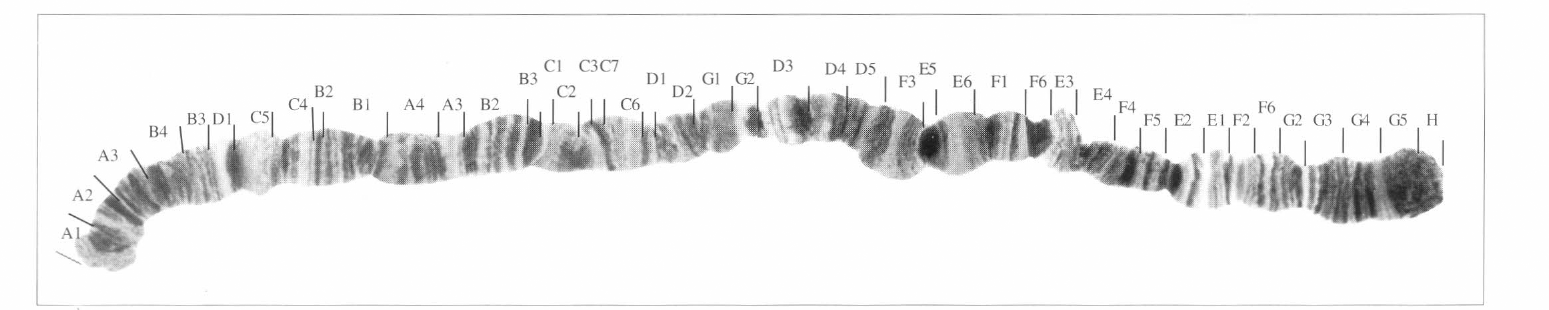
Cromosoma 2 estándar de D. starmeri 2 abcd ABCDEFG a'b'c'd' para las tres poblaciones (las letras con comillas denotan las inversiones detectadas en el cromosoma 2 a partir del cromosoma del estándar de D. martensis. Cromosoma 2 de D. starmeri (Santa Marta)
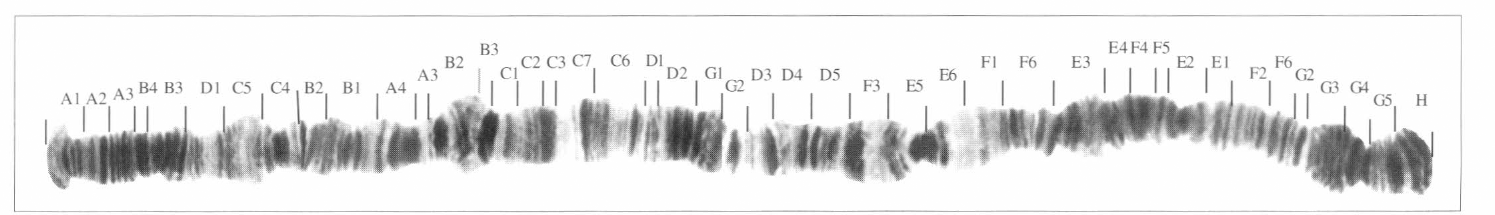
Cromosoma 2 de D. starmeri (Camarones)
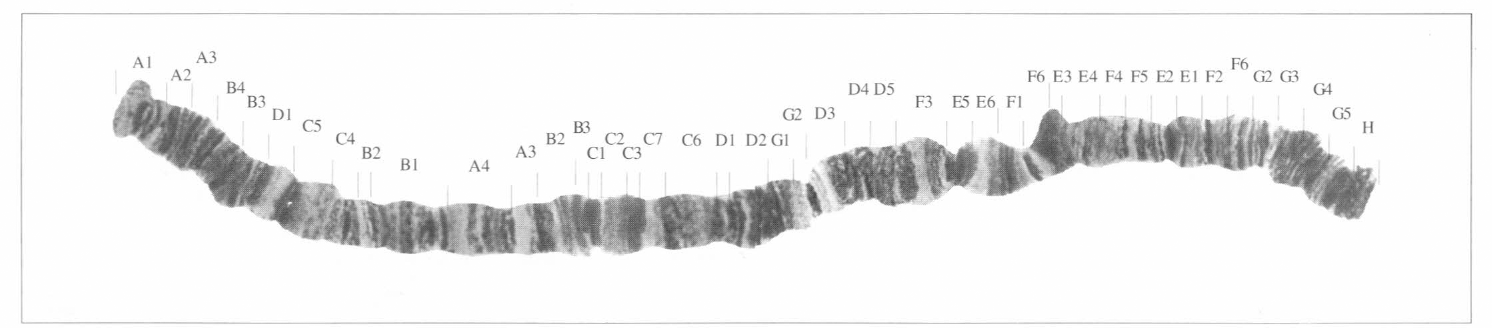
Cromosoma 2 de D. starmeri (Tatacoa).
En los cromosomas 2 de los cruces híbridos A, a, B y b, se observó un heterocariotipo con 2 lazos. El mapeo de estos lazos da una secuencia que se repite en todos los cromosomas 2 híbridos para las dos zonas; determinándose, de forma exacta, los pun tos de rotura de las inversiones. De acuer do con esto, las secciones implicadas en estas dos inversiones son: B₂B₃C₁C₂C₃C₇ y D₅F₃E₅E₆ (Figs. 5 - 7).
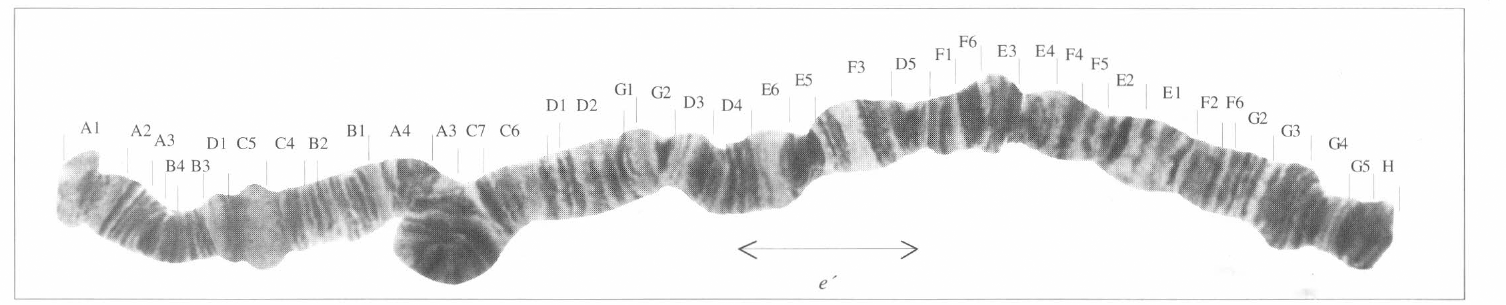
Heterocariotipo de Santa Marta, la cual es heterocariotípica para la inversión ƒ´ y homocariotípica para la inversión e΄.
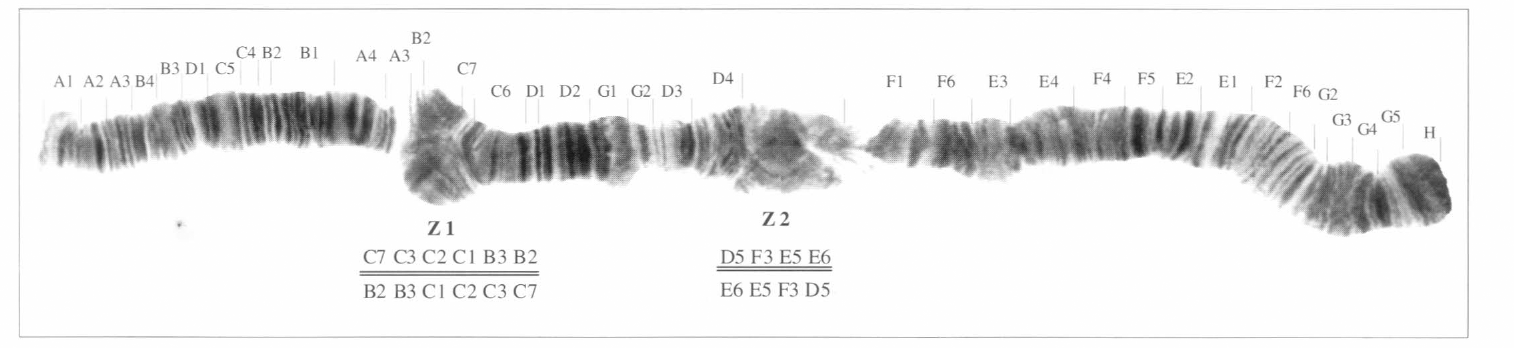
Híbrido A (Camarones por Tatacoa), en donde se observan los lazos 1 y 2.
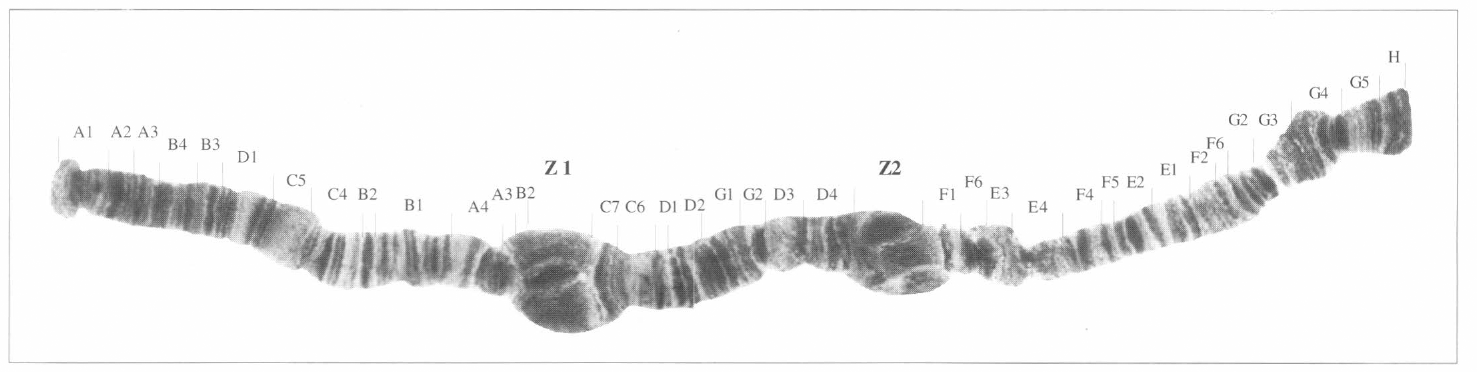
Híbrido B (Santa Marta por Tatacoa), en donde se observan los lazos 1 y 2 en las mismas zonas del híbrido A.
Las fórmulas de cada uno de los arreglos observados en los heterocariotipos híbridos A y B, son:
Tatacoa/Santa Marta-Camarones: B₂B₃C₁C₂ C₃C₇/C₇C₃C₂C₁B₃B₂, D₅F₃E₅E₆/E₆E₅F₃D₅.
Cruces Híbridos interpoblacionales de Drosophila starmeri, de costa norte y Tatacoa
H= hembras, M= machos, ** fértiles.
En la comparación de los mapas de las tres poblaciones, con las secuencias estándar señaladas por Wasserman y Koepfer (1979), Ruiz y Fontdevila (1981) y Ruiz y Wasserman (1993), se evidencia una amplia diferencia, tanto con el arreglo estándar como en los polimorfismos observados en este estudio. El análisis realizado a la ruta filogenética del cromosoma 2 estándar de D. martensis registrada por Polanco (1998), muestra que la misma se ajusta bien a la filogenia del cromosoma 2 de D. starmeri y, teniendo en cuanta la cercanía evolutiva entre las dos especies, se ha tomado como base para proponer la evolución del cromosoma 2 en D. starmeri.
El cromosoma 2 estándar de D. starmeri propuesto en este trabajo, se originó por cuatro inversiones (a', b', c', y d') a partir del cromosoma 2 estándar de D. martensis propuesto por Polanco (1998) (Fig. 8).

Filogenia del cromosoma 2 de D. starmeri propuesta para las poblaciones de la costa norte colombiana (Santa Marta y Riohacha) y del Desierto de la Tatacoa en el Huila (basada en el cromosoma 2 de D. martensis de Polanco 1998). Se observa que del estándar de D. martensis por Polanco (1998), hay cuatro inversiones: a'b'c'd'e'f', de las cuales la b', c'y d' son traslapadas. Además se ven tres posibles polimorfismos cromosómicos.
La filogenia muestra que el arreglo estándar del cromosoma 2 de D. starmeri es 2ABCDEFGabcda'b'c'd' y existen además, otros tres arreglos en el mismo cromosoma: 2ABCDEFGabcda'b'c'd'e', 2 ABC DEFGabcda'b'c'd'e'f', 2ABCDEF Gabcda'b'c'd'f'.
Los cruces A y B (Tabla 1) muestran una posible divergencia a nivel cromosómico entre las poblaciones de la costa norte co lombiana y la del Desierto de la Tatacoa, ya que en la descendencia híbrida se observa ron lazos que evidencian el polimorfismo presente en el cromosoma 2.
Estos resultados concuerdan con los aná lisis morfológicos realizados por Castañeda (2000) y de aislamiento reproductivo rea lizado por Rojas (2001) en los cuales se manifiesta un grado de divergencia genética entre las poblaciones de la costa norte y de la Tatacoa. En las poblaciones de Santa Marta y Camarones no se obser van diferencias a nivel cromosómico, lo cual es consistente con lo observado por Rojas (2001), aunque existe un grado de polimorfismo, señalado en diferentes in vestigaciones como las de Castañeda (2000), Sánchez (1987) y Hoenigsberg et al. (1987).
Conclusiones
Existe un grado de divergencia en las ordenaciones del cromosoma 2, en las po blaciones de la costa norte y el Desierto de la Tatacoa, representado en el arreglo estándar y tres inversiones diferentes.
La ruta filogenética nueva planteada para el cromosoma 2 de D. starmeri, de las po blaciones muestreadas, se deriva de la de Polanco (1998) por cuatro inversiones traslapadas.
Los resultados de los análisis cromo sómicos son consistentes con los de Castañeda (2000) y Rojas (2001) y confir man la divergencia entre las poblaciones de los dos ecosistemas.
Agradecimientos
Los autores agradecen la colaboración y paciente revisión de la profesora Adriana P. Rojas. M. Sc. de la Facultad de Ciencias de la Universidad del Tolima y la financiación de la investigación por parte del Comité Central de Investigaciones de la Universi dad del Tolima y el Instituto de Genética de la Universidad de los Andes.
