Abstract
Laboratory bioassays were performed to determine the susceptibility of 5th instar nymphs of the insect Rhodnius ecuadoriensis to the entomopathogenic fungi, Beauveria bassiana stock UdeA-13. The insects were bred and kept at the Mycology Laboratory, Biology Department, University of Antioquia. The bioassays consisted in direct contact on insect with a canvas 100% cotton, impregnated with a solution of 3×105, 1×107, 3×108 conidias/ml of the fungi B. bassiana (UdeA-13). The insects were kept in controlled conditions of temperature (25-26°C) and relative humidity (70-80%) in darkness. It was found that survival of insects treated with the fungi was low with the three doses; the LT50 for the doses 3×105, 1×107, 3x108 conidias/ml varied between 5.5, 6 and 7 days respectively. The average time of apparition of micelia in the cadavers varied between 7-8 days. The results show that B. bassiana (UdeA-13) could be considered a good element in management programs of vectors of Chagas disease to interrupt the transmission cycle.
Introducción
La enfermedad de Chagas constituye un serio problema de salud pública en África, el sur de Estados Unidos, México, Centro y Sudamérica. En Colombia afecta 3.4% de la población y 3.6 millones de personas habitan zonas de alto riesgo (Calle 2000). Esta es una parasitosis crónica causada por el protozoario flagelado Tripanosoma cruzi (OMS 1991) el cual se transmite al hombre a través de insectos hematófagos. Los parásitos infectantes salen en las deyecciones del vector y pueden introducirse al organismo a través del orificio de la picadura, heridas o excoriaciones de la piel o atravesando directamente la mucosa ocular, nasal o bucal (Botero y Restrepo 1998).
Los vectores de la enfermedad son insectos del orden Hemiptera, familia Reduviidae, subfamilia Triatominae, los cuales poseen cinco estadíos ninfales. Al igual que los adultos, todos son hematófagos estrictos. Por lo tanto su ciclo de vida está condicionado por una monodieta ingerida en comidas abundantes, seguidas por largos períodos de ayuno (CIDEIM 1994).
Para Sur América uno de los vectores más importantes en la transmisión de esta enfermedad es la especie Rhodnius ecuadoriensis el cual ha sido encontrado naturalmente infectado con T. cruzi (Lent y Wygodzinsky 1979) y T. rangeli (Herrer et al. 1972). Este triatomíneo es muy versátil en cuanto a sus hábitos, pues se adapta con relativa facilidad a ambientes domésticos, peridomésticos y silvestres. Dicha versatilidad le da condiciones especiales para su papel de vector de parásitos que suelen alcanzar al hombre (Herrer et al. 1972). R. ecuadoriensis se ha encontrado en países como Ecuador y el norte de Perú (Lent y Wygodzinsky 1979).
La lucha contra los insectos vectores de enfermedades tropicales se ha basado principalmente en la utilización de insecticidas químicos (dicloro difenil tricloroetano (DDT), Lindano (HCH) y carbamatos); sin embargo, factores como el aumento de la resistencia de los insectos a estos insecticidas y los efectos adversos del uso generalizado de químicos en el control de plagas y vectores, han fomentado el uso de hongos entomopatógenos como sustitutos potenciales de los insecticidas químicos (Ferron et al. 1991; Lacey y Goettel 1995; Fargues y Luz 1998).
Muchos autores han señalado la susceptibilidad de diferentes especies de Triatominae a los hongos hyphomycetes Beauveria bassiana y Metarhizium anisopliae (Messias et al. 1986; Romaña y Fargues 1987; Romaña et al. 1987; Romaña y Fargues 1992; Fargues y Luz 1998). El hongo B. bassiana es uno de los entomopatógenos más ampliamente estudiado por su potencial como agente de control biológico (Soto et al. 1997).
Luz et al. (1998) indican al B. bassiana como posible agente de biocontrol para insectos vectores de la enfermedad de Chagas, probándolo con Triatoma spp., Rhodnius spp., Panstrongylus spp. y Dipetalogaster maxima (Uhler). Romaña y Fargues (1992) probaron la susceptibilidad de diferentes estadíos de R. prolixus a la acción de una cepa de B. bassiana, encontrando que ésta se puede utilizar como candidato para el control microbiológico.
El objetivo de este estudio fue evaluar la susceptibilidad del insecto vector Rhodnius ecuadoriensis del V estadío de desarrollo a la acción del hongo entomopatógeno B. bassiana (Udea-13) procedente de una cepa aislada en la región de San Onofre (Sucre), Colombia.
Materiales y Métodos
Origen de los insectos
La población de R. ecuadoriensis utilizada para la investigación se obtuvo a partir de una colonia proveniente del Ecuador, donada por la Dra. Cristina Romaña de la Facultad de Medicina Necker de la Universidad París V. Fue mantenida y reproducida en el laboratorio de Micología del Departamento de Biología de la Universidad de Antioquía dentro de cristalizadores plásticos de 16 × 12 cm, con tapa plástica de cierre hermético con un agujero central cubierto de muselina; dentro una escalerilla de cartón en forma de cruz para facilitar a los insectos el desplazamiento y la alimentación, la cual se hizo de 1 a 2 veces por semana con sangre de ratón (Mus musculus), hasta obtener la población necesaria para los ensayos.
Hongo entomopatógeno
La cepa Beauveria bassiana UdeA-13 se aisló de Rhodnius pallescens capturado en la región de San Onofre (Sucre) y se cultivó en el laboratorio de Micología del Departamento de Biología de la Universidad de Antioquia. Este hongo se repicó cada 20 días en Agar Saburaud y Agar extracto de Malta; se mantuvo a temperatura ambiente hasta obtener una esporulación adecuada (aproximadamente 15 días).
Bioensayo
Contaminación de los insectos
Los insectos, Rhodnius ecuadoriensis, se alimentaron en forma natural durante 2 a 3 horas, veinticuatro horas antes del ensayo garantizando que hubieran consumido la mayor cantidad de sangre. Cada insecto se colocó de forma individual dentro de un tubo de ensayo de 10 ml, el cual contenía una lona de 100% de algodón previamente humedecida con una suspensión de agua destilada estéril más la concentración de conidias del hongo. Las conidias se obtuvieron de la superficie del cultivo directamente por raspado con una barra de vidrio estéril; el inóculo se suspendió en agua destilada estéril, a la cual previamente se le había adicionado una gota de Tween 80 (0.005%). La suspensión se homogenizó por agitación. La concentración de esporas se calculó mediante conteo en la cámara de Newbauer. Para el ensayo se utilizaron dosis de 3×105, 1×107 y 3×108 conidias/ml. Como testigo se utilizó la lona impregnada en agua destilada estéril.
Los tubos se cerraron con papel parafilm al cual se le hicieron agujeros para la aireación. Los lotes se mantuvieron en cámara climatizada a una temperatura de 22 a 26.5°C y a una humedad relativa de 80% en oscuridad durante 30 días.
Los ensayos se controlaron diariamente durante un mes registrando la mortalidad y el tiempo que tarda el micelio del hongo para salir sobre la superficie del cadáver del insecto (micosar). Los insectos vivos se contaron y los muertos se colocaron en cajas de petri estériles con papel filtro estéril y húmedo llevándose a la incubadora a 25°C durante 30 días. Los insectos se dejaron esporular completamente, para luego hacer placas coloreadas con azul de lactofenol y observar las diferentes estructuras morfológicas del hongo, tomar las medidas de dichas estructuras, y verificar la identidad del B. bassiana.
Resultados
Para los análisis estadísticos se utilizó el test de Kaplan-Meier con un alpha = 0.5%.
De los 240 R. ecuadoriensis sometidos en total a la acción del hongo entomopatógeno B. bassiana cepa UdeA-13 a las dosis de 3×105, 1×107 y 3×108 conidias/ml, un 99.6% murieron entre los días 3 y 14 de ensayo, con la excepción de un insecto que sobrevivió hasta el día 29 (Fig. 1). De éstos, 227 presentaron la aparición de micelio del hongo entomopatógeno, y un número reducido (13 insectos) no micosaron (Fig. 2). La aparición del hongo en los cadáveres se tomó como un parámetro para medir la acción patógena y el potencial de los cadáveres esporulados como fuente de inóculo del hongo para otros insectos.
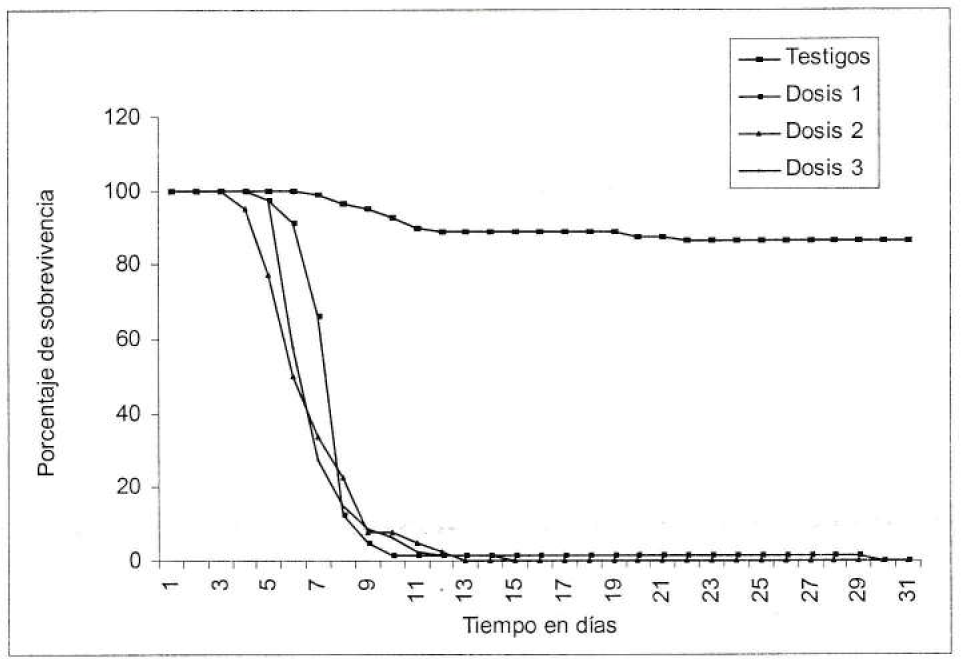
Evolución de la sobrevivencia de Rhodnius ecuadoriensis de V estadío de desarrollo en presencia de B. bassiana en función del tiempo y la dosis aplicada.
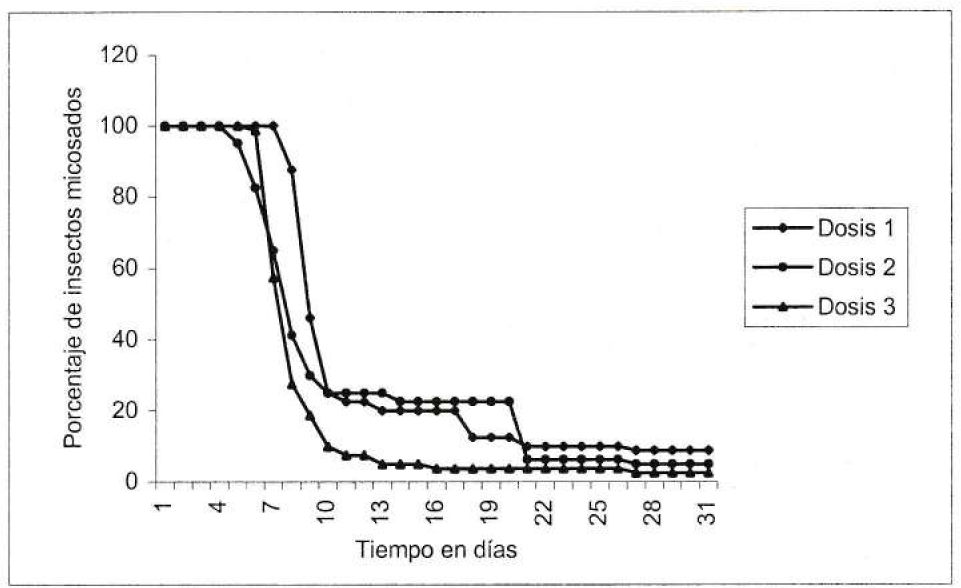
Evolución de la micosis de B. bassiana sobre cadáveres de Rhodnius ecuadoriensis de V estadío de desarrollo en función del tiempo y la dosis aplicada.
Un 86,25% de los insectos utilizados como control sobrevivieron durante todo el tiempo del ensayo (30 días). De los 13,75% que murieron ninguno presentó micosis con B. bassiana.
En cuanto a sobrevivencia, los tratamientos con la concentración mayor (3×108 conidias/ml) y menor (3×105 conidias/ml) presentaron un TL50 de 6 y 7 días respectivamente, mientras que el tratamiento con la concentración media (1×107 conidias/ml) mostró menor TL50, de 5.5 días (Tabla 1).
Sobrevivencia de R. ecuadoriensis con 3 dosis de B. bassiana (3×105, 1×107 y 3×108 conidias/ml) según el test estadístico de Kaplan-Meier
Los análisis estadísticos muestran diferencia significativa cuando se comparan los tiempos de las tres dosis con el control (X2 = 187.21, P < 0.0001). Al analizar las tres dosis sin el control se encontró igualmente diferencia significativa (X2 = 22.55, P < 0.001). La dosis menor (3×105 conidias/ml) fue la más diferente respecto a las otras dos dosis (1×107y 3×108 conidias/ml), siendo la que causó la mortalidad más baja, ya que al comparar las dosis mayores entre sí se obtuvo un P = 0.28, o sea, sin diferencia significativa, lo que indica un comportamiento similar entre estas dos (Tabla 2).
Comparación de las diferentes dosis evaluadas (3×105, 1×107 y 3×108 conidias/ml) para mortalidad bajo el test estadístico de Kaplan-Meier con un alpha de 0.5
Dosis. 0: Controles; 1: 3×105 conidias/ml; 2: 1×107 conidias/ml; 3: 3×108 conidias/ml.
Analizando el número de insectos micosados se encontró que la dosis de 3×105 conidias/ml presentó diferencia significativa con respecto a las otras dos dosis (3×108 y 1×107 conidias/ml), siendo menor el número de insectos micosados (Tabla 3).
Comparación de las diferentes dosis evaluadas (3×105, 1×107 y 3×108 conidias/ml) para la micosis bajo el test de Kaplan-Meier, con un alpha de 0.5
Dosis. 1: 3×105 conidias/ml; 2: 1×107 conidias/ml; 3: 3×108 conidias/ml.
Los insectos tratados con las dosis de 1×107 y 3×108 conidias/ml tuvieron un tiempo medio de micosis igual, de 7 días; los insectos tratados con la dosis menor (3×105 conidias/ml) tardaron un poco más de tiempo en esporular, siendo su tiempo medio de 8 días (Tabla 4).
Micosis en R. ecuadoriensis con 3 dosificaciones de B. bassiana (3×105, 1×107 y 3×108 conidias/ml) según el test de Kaplan-Meier
Discusión
La cepa B. bassiana UdeA-13 utilizada en los ensayos produjo una mortalidad alta de ninfas de V estadío y esporulación de los cadáveres.
Los bioensayos llevados a cabo con B. bassiana cepa UdeA-13 mostraron una diferencia significativa al compararlos con los testigos, lo que concuerda con estudios realizados por Burges y Thompson (1971), quienes demostraron también que la respuesta de mortalidad es directamente proporcional a la dosis del inóculo. Sin embargo, comparando los bioensayos entre sí mostraron que la dosis media 1×107 conidias/ml presentó la mayor mortalidad en menor tiempo, mientras que las dosis de menor y mayor concentración (3×105 conidias/ml y 3×108 conidias/ml) necesitaron más tiempo para matar la mitad de la población (TL50) (Tabla 1).
Analizando la micosis se encontró que los insectos tratados con la dosis menor tardaron más tiempo para esporular (8 días) que las otras dos dosis lo que demuestra que al aumentar las concentraciones de las esporas del hongo disminuyó el tiempo en la aparición del micelio.
En los bioensayos realizados con las concentraciones de esporas de B. bassiana se observó un tiempo letal medio entre 7 y 14 días; al recuperarse el hongo de un porcentaje alto de los insectos muertos se confirma la acción entomopatógena de éste. En especial si se compara con los insectos testigos para los cuales el tiempo letal medio fue de 30 días y en ningún caso se aisló el hongo B. bassiana, demostrando que la muerte de estos insectos fue por otras causas.
Es importante señalar que los cadáveres de los Rhodnius con crecimiento de abundante micelio se pueden constituir en fuente de infección de los insectos vivos cercanos, lo cual sería de gran utilidad para un control natural en el campo, reduciéndose así el número de aspersiones necesarias para el manejo de este insecto vector.
Conclusiones
Las ninfas de V estadío de desarrollo R. ecuadoriensis presentaron una susceptibilidad alta al hongo B. bassiana cepa UdeA-13, por lo cual se puede considerar como un buen candidato para el control de este vector en condiciones ambientales favorables.
La mortalidad en las ninfas de V estadío de desarrollo de R. ecuadoriensis fue atribuida a la micosis causada por Beauveria bassiana cepa UdeA-13 debido a que ésta fue recuperada de los cadáveres.
Es necesario realizar pruebas de campo para conocer el comportamiento del B. bassiana cepa UdeA-13 en el ambiente doméstico y peridoméstico, lugares donde se aplica el control de los vectores de la enfermedad de Chagas.
Footnotes
Agradecimientos
Los autores agradecen, a la Corporación de Patologías Tropicales; a la Facultad de Ciencias Exactas y Naturales, al Departamento de Biología y al CODI de la Universidad de Antioquia por la financiación y el apoyo en la ejecución de esta investigación; al profesor Abel Díaz Cadavid, MSc. por el análisis estadístico de la investigación; a la profesora Sandra Uribe Soto por las sugerencias hechas al manuscrito; al profesor Gustavo García G., a las Biólogas Carmen A. Vásquez, Ana Isabel Gutiérrez, Inés Elena Giraldo y Beatriz Cardona, por la asistencia técnica en la investigación.
