Abstract
Known the importance those have the entomonematodes as agents of biological control and given the techniques used for isolation and storage at world level, were evaluated different procedures that permitted the manipulation of the infective juveniles (J3) recovered. Therefore, from samples collected in three areas cultivated with potato in the vereda Casablanca (Villapinzón -Cundinamarca-Colombia), working with an insect trap modified technique (TBA) and solutions of Baermann funnel (TIB), the entomonematode Steinernema feltiae Filipjev, 1934, were isolated with larvaes of last instar of the greater moth from the beehives Galleria mellonella, then adjusting suspensions of 200 nematodes/ ml, consequently obtaining infective juveniles (J3), to evaluate three solutions of them that were going to be storage, for a period six month. Therefore of 300 exposed larvaes with the technical TBA, just 27 (23%), were found parasitized for S. feltiae and with TIB were obtained 12881 nematodes pertaining to Rhabditidae (7024), Steinernematidae (3297), Dorylaimidae (943), Panagrolaimidae (962) and Tylenchidae (654) families; just 25 of 300 exposed larvae were affected by J3 of S. feltiae. In the storage assay done was possible to stablish that the solution of 1ml of distilled water and 30 µl of TritonX100 up to 10°C, permitted the infective juveniles to survive for six months, without affecting the pathogenicity on last instar larvae of G. mellonella.
Introducción
Atributos tales como infectar un amplio rango de insectos, ser inocuos a mamíferos y plantas (Nickle 1991), lograr una rápida muerte al hospedero (24-48 horas) (Woodring y Kaya 1988), producirse masivamente in vivo e in vitro (Bedding 1981, 1984) y la fácil aplicabilidad en campo (Jansson y Scott 1994), han hecho de los entomonemátodos organismos útiles como agentes de control biológico en programas de manejo integrado de plagas a nivel mundial. Durante las dos últimas décadas en Colombia se vienen desarrollando investigaciones con este grupo de organismos, que han permitido mostrar la variedad de especies nativas y su control sobre algunas plagas de importancia económica para el país, tal como lo muestran los trabajos de Caicedo y Bellotti (1996) evaluando el parasitismo de Steinernema carpocapsae (Weiser 1955) y de nemátodos nativos asociados a Cyrtomenus bergi Froeschner (Hemiptera: Cydnidae) y Garzón et al. (1996); quienes establecen el potencial del nemátodo Steinernema sp, para el control biológico del gusano blanco de la papa Premnotrypes vorax (Hustache) (Coleoptera: Curculionidae). A pesar de estas investigaciones y partiendo del hecho que Colombia es considerado país Megadiverso (Andrade 1993; Etter 1993), es indudable que falta bastante por indagar sobre nuestras especies y su potencial uso en el control de plagas locales; deficiencia que tal vez puede presentarse no solo por la falta de dinero, sino también, por desconocer y/o evaluar alternativas para el aislamiento y manipulación de tales especies, ya que algunos procedimientos clásicos presentan ventajas y desventajas que los hacen eficientes solo para aislar ciertas especies (Kaya y Stock 1997).
Bajo este contexto, el presente estudio evaluó una alternativa de aislamiento de entomonemátodos usando la técnica del insecto trampa, con soluciones de nemátodos obtenidas de embudos Baermann (Southey 1986) y comparando su eficiencia respecto a la propuesta por Bedding y Akhurst (1975); además de normalizar una solución para el almacenamiento de juveniles infectivos (J3) de Steinernema feltiae, que permitió evaluar su sobrevivencia y patogenicidad.
Materiales y Métodos
Area de estudio y toma de muestras
El area de muestreo correspondió a una zona de cultivo de papa y rotación de pastos a 2900 m.s.n.m en la vereda Casablanca (Villapinzón); caracterizada por un clima subhúmedo a húmedo, temperatura promedio de 11°C y precipitación mayor de 1000 mm al año, suelos Franco-Arenosos, con una proporción de 36% de arenas, 14% de arcillas y 50% de limos. En tres lotes cultivados con papa se tomaron 15 muestras de suelo de 1500 grs cada una. a 30 cm de profundidad (utilizando una pala de mano) y con sus respectivos registros de temperatura. Las muestras fueron debidamente etiquetadas y transportadas, en bolsas plásticas, al laboratorio de Control Biológico en la Facultad de Agronomía de la Universidad Nacional, en Santafé de Bogotá D.C.
Material biológico
Para las pruebas de patogenicidad y multiplicación de los entomonemátodos aislados se usaron larvas de ultimo ínstar (peso aproximado de 0.25-0.35gr y longitud 2-3cm) de Galleria mellonella (L) (Lepidoptera: Pyralidae), obtenidas de la cría del laboratorio de Control Biológico de la Facultad de Agronomía en la Universidad Nacional, criadas en dieta artificial.
Aislamiento de juveniles infectivos
Técnica Bedding y Akhurst (TBA)
Cada una de las 15 muestras de suelo se colocó en 2 recipientes de 250gr, a los que posteriormente se le adicionaron 10 larvas (300 en total) de último instar de G. mellonella, disponiéndolas de manera invertida, en total oscuridad a 20°C y 60% de humedad relativa, durante tres días.
Técnica del insecto trampa a partir de soluciones Baermann (TIB)
100gr de suelo de cada una de las 15 muestras se dispusieron dentro de papel absorbente en embudos de vidrio de 100ml, con agua destilada durante 8 horas, tiempo al cual se colectó la muestra de agua por Baermann (procedimiento que se replicó tres veces). Con la ayuda de un estereoscopio se contabilizaron e identificaron, a nivel de familia, los nemátodos presentes, ajustando de inmediato soluciones a 1ml. Posteriormente, con 50ml de esta solución (conteniendo entre 35 a 49 nemátodos), se inocularon, individualmente 20 larvas (300 en total) de último instar de G. mellonella, en cajas de cultivo de tejidos de 12 cavidades (Falcón 3043), con papel de filtro Whatman #1 de 1cm de diámetro; cada caja se etiquetó y almacenó a 20°C y 60% de humedad relativa.
Para los dos montajes TBA y TtB, se examinaron cada 24 horas las larvas con el fin de determinar sintomatologías propias de ataque por entomonemátodos (Kaya y Stock 1997), como la coloración y consistencia general del cuerpo, además del ataque por otros patógenos (ácaros, virus, bacterías, hongos). Las larvas muertas se dispusieron en cámaras de incubación (cajas de petri de 60X15mm y papel filtro Whatman # 1 de 5 cm de diámetro) durante 48 horas; posteriormente, se ubicaron en trampa de White modificada (White 1927) o trampa de recuperación de juveniles infectivos (J3), consistente en un vidrio de reloj, tapa de caja de petri invertida o soporte similar, cubierto con papel de filtro ubicado en una caja de petri 100X15 mm. A cada trampa se le adicionaron 5 ml de agua desionizada para que los bordes del papel de filtro hicieran contacto con el agua y los J3 migraran del hospedero, ubicado radialmente en el papel. Con el fin de retirar restos de tejido y papel, las cosechas de J3 se enjuagaron en agua desionizada o se pasaron por tamices de 125, 53, 43, 38 y 25 micras. Las soluciones que presentaron gran cantidad de residuos se centrifugaron por 2 ó 3 minutos a 250 revoluciones por minuto (81.2 g).
Para la cuantificación de los J3, producidos por cada trampa de White, se utilizó el conteo directo cuando el número de J3 fue menor de 50 nemátodos/ml, y el de dilución volumétrica, cuando fue superior (Stock 1998).
Identificación del nemátodo aislado
El material aislado se identificó a nivel de familia, siguiendo las claves propuestas por Nickle (1991). Los nemátodos aislados se enviaron para identificación específica a la Dra. Patricia Stock del Departamento de Nematología en la Universidad de California Davis, en Estados Unidos. Para este propósito juveniles infectivos se fijaron por el método rápido TAF (Stock 1998) y se dispusieron en viales de vidrio. Para el análisis de nemátodos adultos, larvas infectadas de G.mellonella se cubrieron con papel aluminio y se ubicaron en viales de vidrio. El envío se realizó vía aérea, previa autorización de entidades como Minambiente en Colombia y USDA en USA.
Almacenamiento de juveniles infectivos
A partir de J3 obtenidos de 120 larvas de G.mellonella inoculadas con 200 J3/ml (dispuestas en 12 cajas de petri de 100 x 15 mm, con 10 larvas cada una) se ajustaron concentraciones de almacenamiento de 5000 J3/ml (Kaya 1993), para cada una de las soluciones de almacenamiento a evaluar, propuestas por Garzón et al. (1996), Caicedo y Bellotti (1996), Kaya y Stock (1997). El diseño utilizado fue un diseño completamente al azar con tres tratamientos y seis repeticiones. Los tratamientos se dispusieron de la siguiente manera:
Para todos los ensayos la temperatura se fijó en 10°C, de acuerdo con la temperatura registrada en el momento del muestreo de suelo. Las observaciones se realizaron tomando al azar, cada treinta días, un recipiente por tratamiento para determinar él numero de nemátodos muertos y vivos en la solución de almacenamiento (movimiento y forma de J),
Patogenicidad de J3 almacenados
Los ensayos se realizaron sobre 20 larvas de último ínstar de G. mellonella, las cuales se confinaron individualmente en platos de 12 cavidades con papel filtro, 80 ml de agua destilada estéril y 20 nemátodos provenientes de los tratamientos de almacenamiento. Al testigo se le adicionaron 2 ml de agua estéril. Las cajas se sellaron con vinilpel, mantenidas bajo oscuridad y condiciones de laboratorio (20°C y 60% HR). A las 96 horas el número de larvas muertas y vivas se contaron, las larvas muertas se disecaron en una caja de vidrio (60X15mm) con dos agujas de disección y 0.1 ml de agua, para facilitar la observación de los nemátodos bajo estereoscopio. Los valores obtenidos se analizaron con la ecuación de Abbott (Nguyen y Smart 1991). Estas observaciones se realizaron por un periodo de seis meses.
Análisis Estadístico
El análisis estadístico para el ensayo de almacenamiento correspondió a un análisis de varianza de una vía (ANOVA), además de rango múltiple de Duncan en los factores que presentaron diferencias significativas, utilizando el paquete estadístico SPSS, versión 6.
Resultados y Discusión
Identificación del entomonemátodo aislado
De acuerdo con los análisis morfométricos, pruebas de retrocruce y RFLP's (Restriction fragment length polimorphims), realizados por la Dra. P. Stock en UCDAVIS, se identificó el entomonemátodo como perteneciente al orden Rhabdhitida, familia Steinernematidae, género Steinernema, especie Steinernema feltiae Filijep 1934.
Técnica Bedding y Arkust (TBA)
De las 300 larvas expuestas al suelo murieron 117 larvas y 183 siguieron con vida hasta el final del ensayo, dentro del respectivo capullo. De las 117 larvas se encontró el 23% (27) parasitadas con S. felriae, caracterizadas por presentar un color marrón oscuro, consistencia flácida e inodoras; no presentaron infección externa por hongos, invasión por ácaros o bacteriosis. De las 27 larvas, 10 alcanzaron a formar capullo, pero dentro de éste se encontraban las larvas con las características anteriormente mencionadas. De las 90 restantes presentaron sintomatología propia de ataque por bacterias, hongos, nemátodos y ácaros (Tabla 1). Sin embargo, las 11 larvas afectadas por nemátodos del género Rhabdithis (Rhabdithidae) presentaron máculas negras dispuestas de manera irregular en toda la pared externa del cuerpo y al realizar disecciones, el sistema digestivo, las fibras musculares y el tejido graso se encontraron completos o poco afectados; además, aunque son considerados como saprófagos fungívoros (Bovien 1986), ocasionalmente pueden atacar otros organismos blanco, lo cual no les asume la categoría funcional de entomopatógenos estrictamente (Stock 1998). Igualmente las larvas halladas con ácaros del género Rhizoglyphus (Acaridae: Rhizoglyphinae) dispuestos ventralmente cerca a las pseudopatas, se les considera más como detritívoros (Acosta, A comunicación personal 1998) y no como depredadores, por lo que se puede asumir que éstos no causaron la muerte de las larvas. Por tanto, la muerte de las larvas halladas con Rhabdithis y Rhizoglyphus se asume más a condiciones de estrés causadas por el ensayo, como asfixia, reducción de nutrientes, humedad, temperatura, entre otras.
Técnica Insecto trampa a partir de soluciones Baermann (TIB)
De los 45 cmbudos Bacrmann se obtuvicron 12881 nemátodos, colectando en promedio 286 nemátodos por Baermann y 859 por mucstra (en las tres replicas por cada una de las 15 muestras, Tabla 2).
De las 300 larvas expuestas a TIB, fueron afectadas 119 por hongos, bacterias y entomonemátodos (Tabla 3). Analizando las posibles relaciones de ataque entre los diferentes patógenos dentro de las muestras, se encontró correspondencia entre S. feltiae y hongos en siete muestras (46%), mientras que entre S. feltiae y bacterios y/o virus no se halló ninguna relación de coincidencia de ataque en larvas por muestra. Es decir, que cuando se presentó ataque por bacterias y/o virus no se presentó ataque por S. feltiae, mientras que, donde se reportó ataque de S. feltiae también hubo larvas atacadas por hongos.
Para los dos procedimientos de extracción evaluados se advierten posibles factores antagónicos ampliamente conocidos como antibiosis, competencia y enemigos naturales (Kaya 1990), lo cual impacta sobre los entomonemátodos registrados. Tal antibiosis puede presentarse por liberación de metabolitos de plantas en restos de raíces en suelo consumido esporádicamente por G. mellonella (para el caso de exposición directa al suelo) lo cual afecta, dentro del hospedero fecundidad, tamaño, relación de sexos y en general el comportamiento de búsqueda de los J3 (Benz 1987). Este posible efecto pudo verse limitado en soluciones de Baermann, ya que restos de plantas han sido eliminados por el filtrado. En términos de competencia con bacterias y/o virus se evidencia una marcada diferencia de efecto de exclusión del entomonemátodo, principalmente en las exposiciones a soluciones Baermann, donde aparentemente fue más eficiente la patogenicidad de bacterias y/o virus. Caso contrario en exposiciones directas a suelo, donde si se evidencia cierta acción sinérgica entre nemátodos y estos patógenos, atribuida posiblemente, a la produccion por parte de S. feltiae de la bacteria Xenorhabdus, acción esta que permite "marcar" al hospedero evitan-do así el ataque por otros patógenos. Koppenhofer y Kaya (1997) han demostrado acciones sinérgicas entre especies de Steinernema con Bacillus thuringiensis, aumentando así la capacidad de control sobre algunas plagas. Esta condición brinda la posibilidad de identificar con cual bacteria y/o virus ha ejercido acción sinérgica este nemátodo, pero no queda duda que para el caso de este ensayo, bajo condiciones de exposición a soluciones Baermann, este sinergismo no se observó.
Acción antagónica se evidenció con especies de hongos entomopatógenos, quienes para algunas otras especies de nemátodos son potenciales enemigos naturales (Kaya y Koppenhofer 1996). Para estos ensayos, aunque no se encontraron nemátodos afectados por hongos, se presentó competencia indirecta, en términos de mortalidad de larvas, tanto en exposición directa a suelo (38%) como en exposición a soluciones Baermann (42.8%), además los dos organismos se desarrollaron normalmente. Los mecanismos de exclusión de hongos por parte de S. feltiae, involucraron antibiosis producidos por la bacteria simbionte Xenorhabdus bobienii inhibiendo su crecimiento, además de la condición dependiente, por parte del hongo a la humedad y temperatura. La inhibición del nemátodo por el hongo puede ser dada por antibiosis a través de la produccion de micotoxinas (Roberts 1981). En general es evidente que en los ensayos, los hongos compitieron por la fuente, la cual pudo verse reprimida por la variedad de hongos y disponibilidad de larvas.
En términos de eficacia para la recuperación de entomonemátodos como S. feltiae las dos técnicas muestran poca diferencia tanto en porcentajes de recuperación para, exposición directa a suelo (23%) y para exposición a soluciones Baermann (21%), como en la recuperación de otros patógenos y la importancia que tienen éstos en el ambiente natural de los entomonemátodos, pues a pesar de la riqueza presentada en especies de diferentes taxa, el uso de larvas de G.mellonella como fuente de recuperación es válida, aunque es necesario incrementar su número por área de suelo y solución, para mejorar la disponibilidad de blancos. Es clara la rapidez en recuperación de entomonemátodos expuesta por el uso de soluciones Baermann. Así, si se desea recuperar y multiplicar juveniles infectivos para diferentes usos, es necesario implementar estas dos técnicas con un buen número de insectos cebo, en lo posible G. mellonella, dado que es el insecto blanco mundialmente usado en ensayos con entomonemátodos y en especial para establecer determinaciones taxonómicas, dada la alta variabilidad morfométrica que presentan los nemátodos al ser expuestos a diferentes hospederos (Nguyen y Smart 1996). De igual manera, es evidente que la presión ejercida por otros patógenos del suelo, disminuyen la capacidad infectiva, patogenicidad y recuperación de los nemátodos, demostrando así, que la alta multiplicación en condiciones de laboratorio in vivo y variando la técnica de Bedding y Akhurst (1975), posibilitan que otros patógenos se vean afectados y se incremente la probabilidad de recuperación; para más de una especie de entomonemátodo por muestra y área de estudio.
La patología demostrada por esta cepa no diverge demasiado de la presentada en cepas de la misma especie (Poinar 1990). Los juveniles infectivos emergen por los espiráculos, pliegues segmentales, ano y parte dorsal de la cutícula, principalmente. Al tercer día de emergencia, se observan en el papel filtro restos de tejidos, al octavo y décimo día las larvas empiezan a tomar una coloración más clara y se encuentra mayor cantidad de tejidos en las suspensiones. Cuando la producción de J3 decrece, su cutícula empieza a ser traslúcida, en las suspensiones no se encuentran J3, las larvas quedan completamente planas y sin presencia de tejidos.
Durante los ensayos la emergencia de J3/llarva se presentó en los nueve primeros días, decreciendo gradualmente hasta el día veinte. Esto indica que para la obtención de J3 viables se debe realizar la cosecha de los juveniles infectivos diariamente y a partir del décimo día realizarla cada 2 o 3 días, dada la reducción de infectivos por larva.
De las 120 larvas inoculadas con suspensiones ajustadas a 200 J3/ml/10 larvas/caja, para uso en el ensayo de almacenamiento, se registró un 71.66% de mortalidad, mostrando tres picos de producción en el tercer, sexto y noveno día (Fig. 1). Sin embargo, a partir de la segunda semana, la producción disminuyó notablemente. Los juveniles infectivos recuperados de estas reinfecciones fueron colectados diariamente, los diez primeros días para obtener J3 viables. A partir del día once la producción en todas las cajas empezó a decrecer lo que indica que las cosechas se podían realizar día de por medio. Esto debido a que los juveniles infectivos migran rápidamente del cadáver del insecto, en busca de otro hospedero para reiniciar el ciclo de vida nuevamente. Al igual que en los ensayos con la técnica Bedding y Akhurst y soluciones de Baermann, las emergencias se inician a diferentes tiempos a partir de la primera observación, esto pudo resultar de la interacción hospedero nemátodo, es decir, de la capacidad de escape de la propia larva y de ataque por los nemátodos, del número de machos y hembras que logren madurar, luego de penetrar el juvenil infectivo al hospedero, disponibilidad de nutrientes para la obtención de la nueva generación de juveniles infectivos, la rapidez de los J3 en migrar del hospedero y a las condiciones generales del ensayo.
Almacenamiento y patogenicidad de S. feltiae.
Para cada una de las soluciones evaluadas, los resultados se resumen en las figuras 2a, 2b y 2c. Además, de acuerdo al análisis de varianza la sobrevivencia de los J3 se afecta significativamente por el tipo de solución de almacenamiento utilizada (F= 3.7949; df= 2; P= 0.0328; α= 0.05); presentando diferencias el T3, por un promedio mayor de recuperación de J3 viables en los seis meses, el cual fue de 4075.37 nemátodos/mes. Por otra parte, se presentan diferencias significativas en la patogenicidad de los J3 recuperados/tratamiento, en cada mes de muestreo (F= 5.7863; df=2; P=0.0129; α= 0.05), siendo significativamente diferente de acuerdo a la prueba de rango múltiple de Duncan, el T3 con un promedio de patogenicidad de 83.62% en los seis meses de observación.
Durante los seis meses de evaluación la sobrevivencia de los J3, en la solución T1, se sostuvo hasta el quinto mes, presentando en promedio un porcentaje de patogenicidad de 73%, la mortalidad progresiva de nemátodos se puede presumir al volumen alto de agua lo que disminuye la disponibilidad de oxígeno en el medio (Fig. 2a). Para la solución T2, se logró la sobrevivencia de los J3 sólo hasta el cuarto mes del ensayo, y la patogenicidad decreció sensiblemente del segundo mes (89%) al cuarto mes (25%) (Fig. 2b); estos resultados se atribuyen al estrés causado por el airedor sobre los J3, los cuales generalmente se hallaban siempre agregados hacia las áreas del recipiente donde se presentaba menor turbulencia. De igual manera la constante aireación disminuyó la cantidad de oxígeno disponible y aumentó la evaporación, además de producirse contaminación por hongos, que incrementaron su densidad a medida que se presentaron nemátodos muertos. La solución de almacenamiento en la que los nemátodos mostraron mayor capacidad de sobrevivencia correspondió a T3, no se afectó la patogenicidad de los nemátodos ni se observó contaminación por otros patógenos (Fig. 2c). El volumen de 1 ml permitió un recambio de oxígeno continuo y mejor movilidad de los J3, aunque al disminuir la temperatura por debajo de 10°C, la conformación de cristales de agua fue la causa principal para la muerte que se registro en esta solución. A la fecha se encuentran 545 frascos con 5000 J3/ml, almacenados desde finales de diciembre de 1996, para un total de 2'720.000 J3. Este procedimiento de almacenaje permite no solo la disposición de material biológico para los próximos estudios programados, sino la posibilidad de seguir evaluando la máxima sobrevivencia de los ejemplares además de su patogenicidad.
Organismos aislados de larvas de último instar de Galleria mellonella con la Técnica Bedding y Arkust (TBA)
Familias de nemátodos en orden de abundancia obtenidas con TIB
Patógenos aislados de larvas de último instar de Galleria mellonella con TIB
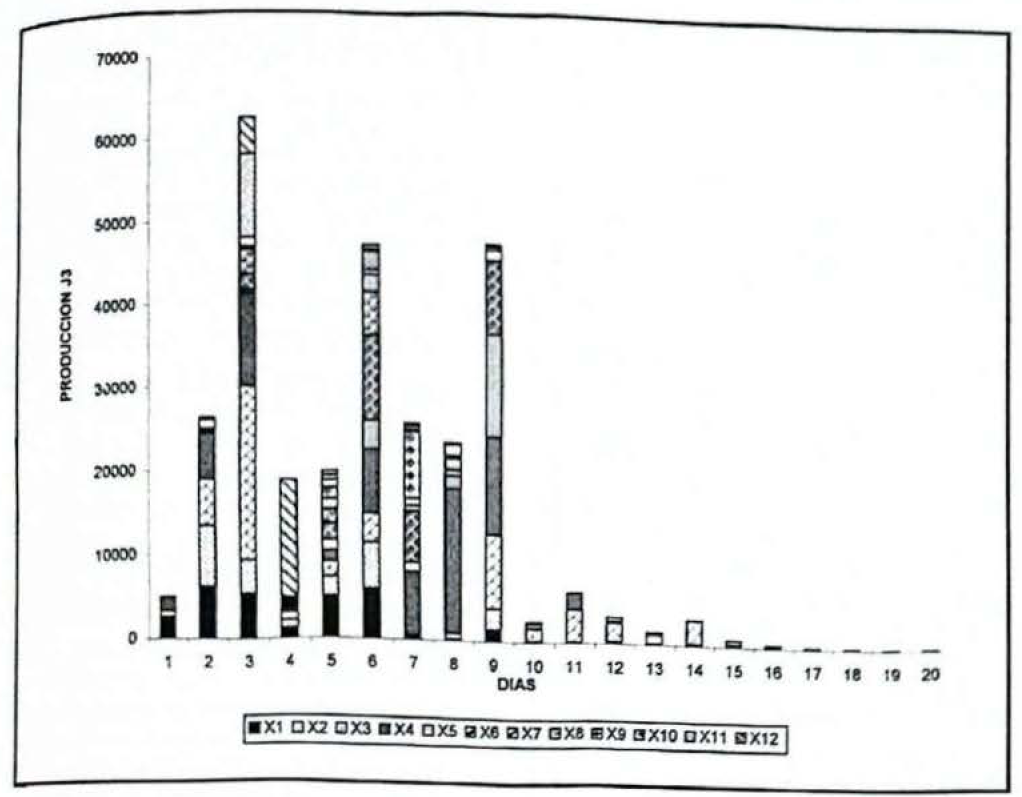
Producción de juveniles infectivos de Steinernema feltiae en trampas de White (X1-X12) durante 20 días
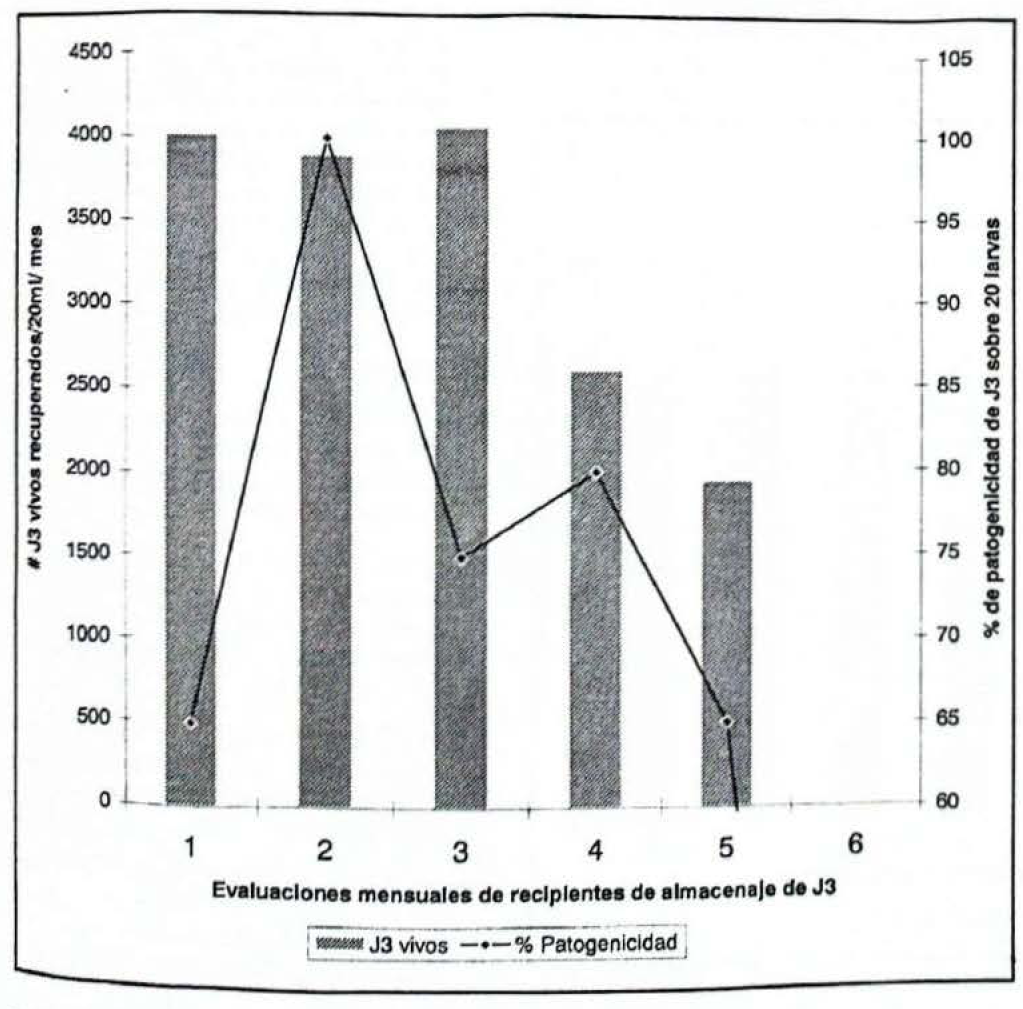
Capacidad patogénica de juveniles infectivosde Steinernema feltiae recuperados en solución (Caicedo y Bellotti 1996) durante seis meses de almacenamiento.
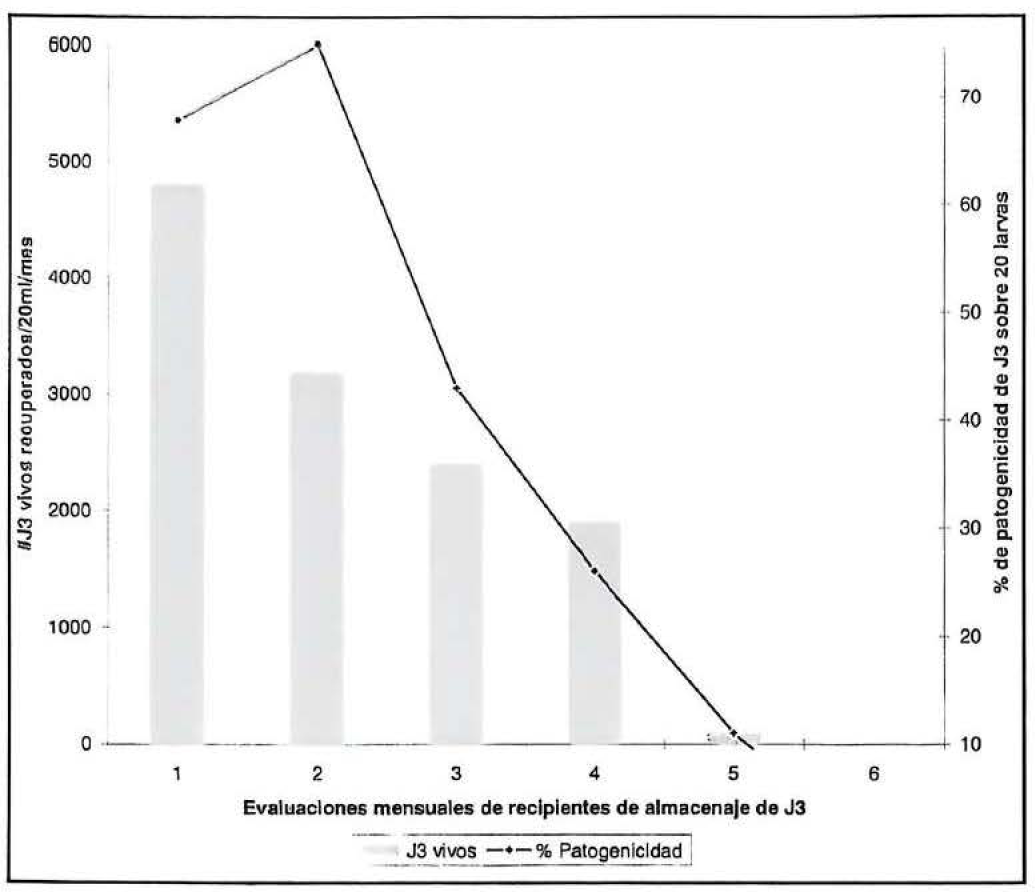
Capacidad patogénica de juveniles infectivosde Steinernema feltiae recuperados en solución (Garzón et al. 1996) durante seis meses de almacenamiento.
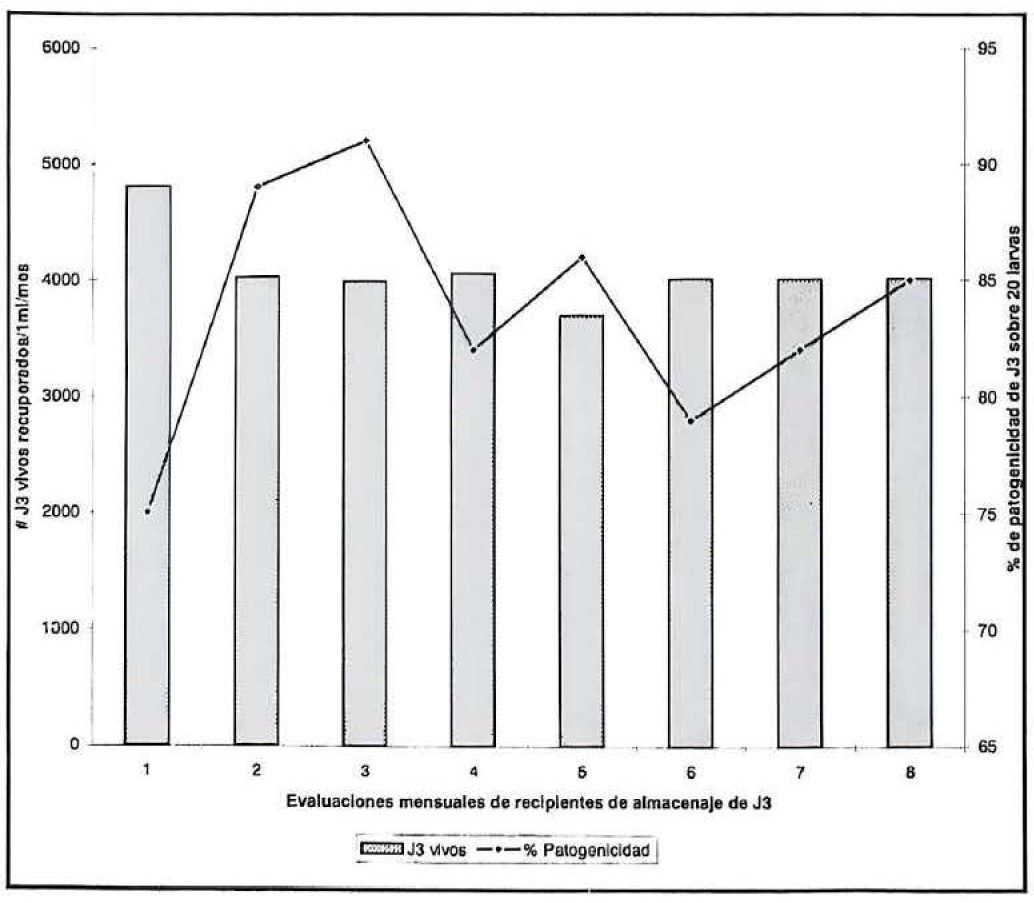
Capacidad patogénica de juveniles infectivosde Steinernema feltiae recuperados en solución (Kaya y Stock 1997) superior a seis meses de almacenamiento.
Conclusiones y Recomendaciones
Las dos técnicas evaluadas para aislamiento de entomonemátodos son eficientes, simples, económicas y no requieren de monitoreo constante para la recolección de los juveniles infectivos. Además, permiten la recuperación e identificación de otros patógenos para su posible utilización como agentes de control biológico.
Las cosechas diarias de juveniles infectivos en los diez primeros días de producción en trampas de White posibilitan, en un 90%, la obtención de J3 vivos para su posterior utilización.
El almacenamiento de 5000 juveniles infectivos en 1ml de agua y 30ml de Triton X100, permiten la sobrevivencia y patogenicidad de los J3 de manera constante, por tiempos superiores a seis meses. Por ello, para mantener bajo estas condiciones entomonemátodos se recomienda cambiar mensualmente la solución. conservando el volumen inicial.
Durante el ensayo de almacenamiento se observaron ciertos cambios morfológicos, como cierre de todos sus orificios y contracción del esófago que se deben más a "posturas" de los juveniles infectivos, como respuesta a las condiciones de hacinamiento en que se encuentran, que no afectan su patogencidad, pero si pueden confundir su identidad específica; por tal razón, no se deben realizar trabajos de tipo taxonómico con especies provenientes de almacenamiento.
