Abstract
The use of entomopathogenic fungi like Beauveria bassiana and Metarhizium anisopliae have shown a great potential as a control method of several insects like the coffee berry borer (Hypothenemus hampei). A close relationship between the activity of some enzymes that attack the cuticle structural components and the infection process of the fungi over the insect has been found. At first stage, the growing rate, culture medium pH changes, pathogenicity and enzymatic activity (total proteases and lipases) in Bb 9620 (monosporic) and Bb 9205 (multisporic) of B. bassiana isolations and Ma 9303 (monosporic) and Ma 9236 (multisporic) of M. anisopliae isolations were quantified. At second stage nine isolations of B. bassiana and five of M. anisopliae with different pathogenicity levels over H. hampei were studied. Enzymatic activity were measured by spectrophotometry using extinction coefficients of ε340 = 98 M−1cm−1 for the azo group released by the proteases and ε400 = 18.77M−1cm−1 for the p-nitrophenol released by lipases. The total proteases show maximum activity peaks between fifth and seventh days of incubation. The M. anisopliae proteolitic activity is significative higher (p<0.05) than B. bassiana activity. The total lipases showed maximum activity between third and fifth days of incubation, but there is not significative difference among isolates. The results point out that both lipases and proteases play an important role at the initial infection mechanism of fungi over the H. hampei cuticle.
Introducción
Entre los métodos utilizados para el manejo integrado de plagas, el uso de hongos entomopatógenos como Beauveria bassiana y Metarhizium anisopliae ha mostrado un gran potencial para el biocontrol. Diversos estudios corroboran la existencia de una estrecha relación entre la actividad enzimática y el proceso infectivo del hongo sobre los insectos (Castellanos 1997; Paterson et al. 1994 a; Leger et al. 1986; Smith et al. 1981).
El patógeno ataca a los insectos a través de la cutícula o por vía digestiva, lugares donde germinan las esporas del hongo y se produce una hifa invasora que penetra los tejidos del hospedero. Las hifas se ramifican, colonizan y llegan hasta la cavidad hemocélica donde se liberan toxinas que causan la muerte del insecto (Kaijiang y Roberts 1986; Kucera 1971). Algunas partes de la cutícula son más susceptibles al ataque enzimático que otras, siendo importante no sólo la actividad catalítica del complejo enzimático producido por los hongos estudiados, sino también el sitio específico de la acción de las enzimas sobre la cutícula (Castellanos 1997, Paterson et al. 1994a).
Diversos estudios ultraestructurales e histoquímicos sugieren que en el proceso inicial de degradación de la cutícula actúan varias enzimas casi todas pertenecientes al grupo de las hidrolasas (proteasas, lipasas, n-acetilglucosaminidasas, fenoloxidasas y quitinasas). Aunque la acción enzimática es muy compleja, es posible relacionarla con la capacidad infectiva de B. bassiana y M. anisopliae y su patogenicidad sobre H. hampei (Smith et al. 1981, Castellanos 1997). En B. bassiana se han encontrado varias proteasas entre las cuales está la quimioelastasa (Pr1), proteasa extracelular relacionada estrechamente con la patogenicidad y cuya máxima actividad catalítica se presenta a pH entre 6.6 y 8.5 (Bidochka y Khachatourians 1990, Paterson et al. 1994b). En M. anisopliae también se ha detectado la actividad de proteasas y lipasas, pero han sido menos estudiadas y su relación con la patogenicidad no está muy clara (Castellanos 1997; Paterson et al. 1994b).
El presente trabajo tuvo como objetivo desarrollar un método para la cuantificación por espectrofotometría de la actividad de lipasas y proteasas de diferentes aislamientos de B. bassiana y M. anisopliae y establecer su relación con la patogenicidad sobre H. hampei (Segel 1982; Colomick 1970; Bergmeyer 1984).
Materiales y Métodos
Aislamientos
Los ensayos iniciales se realizaron sobre los aislamientos (Ma 9236) (multiespórico), (monoespórico), (Bb 9205) (multiespórico) y Bb 9620 (monoespórico) que presentaban porcentajes de patogenicidad sobre H. hampei mayores del 80%. Los estudios enzimáticos se llevaron a cabo sobre nueve aislamientos de B. bassiana y cinco aislamientos de M. anisopliae procedentes de la micoteca de Cenicafé, reactivados en medio agar (1.5% W/V) - macerado de broca 7.27 g de adultos licuados en 750 ml de H2O, esterilizado en autoclave a 121° C y 15 libras de presión durante 15 minutos. El medio inoculado con cada uno de los aislamientos se incubó a temperatura ambiente (Tabla 1).
Aislamientos seleccionados de Beauveria bassiana y Metarhizium anisopliae para la cuantificación enzimática
Clasificación según la patogenicidad tomada del trabajo realizado por (Vélez et al. 1998; Padilla 1998)
Propagación
El conteo de esporas se hizo a partir de una solución madre con nueve días de incubación a la cual se le agregaron 10 ml de Tween 80 al 0.1% y glicerol 0.25%. Se inocularon 1 X 107 esporas en 100 ml de medio líquido (buffer fosfato 0.1 M PH 6.6, MgSO4.7H2O 2.028 mM, ZnSO4 0.006199 mM, NaCl 3.4 X 10−5 mM y 0.4 g de cutícula de broca) y se incubaron bajo agitación rotacional a 2.0 Hz y a 24± 2℃ durante 0.75, 3, 5, 7, 9, 11, 15 y 20 días.
Las cutículas de broca se prepararon a partir de insectos adultos lavados con agua esterilizada en una malla de nylon, se sumergieron en una solución de K2B4O7 del 1% durante 2 horas, se secaron a 30° C, se maceraron en un mortero de ágata, se lavaron con 50 ml de K2B4O7 del 1% y luego dos veces con agua esterilizada. Se separaron las partes blandas mediante filtración en malla de nylon y se esterilizaron en autoclave a 121°C y 15 libras de presión durante 15 minutos. En todos los casos se monitoreó el pH del medio y el crecimiento del hongo mediante los cambios en la densidad óptica a 540 y 680 nm. Se estudió la patogenicidad y la germinación de los hongos mediante bioensayos con el insecto (González et al. 1993). Las características morfológicas de los hongos se determinaron mediante microscopía óptica de fluorescencia en presencia de Calcofluor White.
Extractos proteicos
Para separar las proteínas extracelulares se filtraron los medios obtenidos luego de la incubación de los entomopatógenos sobre papel Rundfilter 595 y al vacío. El filtrado se centrifugó a 8000 g durante 20 min y el sobrenadante se concentró por ultrafiltración sobre membranas Micropor de 100 kDa de exclusión bajo flujo de N2 a 4°C. El concentrado se dializó sobre membranas de Micropor de 10 kDa de exclusión para eliminar los compuestos de baja masa molecular.
Ensayos enzimáticos
La actividad de las dos enzimas estudiadas se cuantificó espectrofotométricamente y los cálculos se realizaron usando la ley de Beer-Lambert (A = ε.C I) (Segel, 1982), contrario a las metodologías registradas por Peled y Krenz (1981), Robert y Messing (1985), Hedeus y Khachatourians (1988), Veeraragaran (1990), Bidochka y Khachatourians (1987, 1990), quienes no tienen en cuenta la capacidad de los medios líquidos para absorber la luz de acuerdo con un coeficiente de extinción propio de las moléculas utilizadas en el buffer de actividad.
Lipasa
Se usaron 100 μl del concentrado proteico para medir la hidrólisis del p-nitrofenil laureato a p-nitrofenol luego de 30 min de incubación a 37°C en presencia de buffer fosfato 0.05 M pH 7.0, p-nitrofenil laureato 0.025 M. La reacción se paró con NaOH 0.1 M y la mezcla se centrifugó a 11000 g durante 10 min en una microcentrífuga Eppendorf. Se registró la liberación del p-nitrofenol a 400 nm usando un ε = 18.77 M−1cm−1 en un espectrofotómetro Unicam UV2.
Proteasa
Se usaron 100 μL del concentrado proteico para medir la hidrólisis de la azocaseína a grupo azo y aminoácidos libres luego de 30 min de incubación a 37° C en presencia de buffer fosfato 0.05 M pH 7.0, 100 μL de solución de azocaseína 1% (P/V). La reacción se paró con 100 μL de ácido tricloroacético del 10 % y la mezcla se centrifugó a 11 000 g durante 10 min en una microcentrífuga Eppendorf. Se registró la liberación del grupo azo a 340 nm usando un ε = 98 M−1cm−1.
El contenido de proteína en los extractos se midió mediante el método de Bradford (1976) y los análisis estadísticos corresponden a un diseño completamente aleatorio con 10 repeticiones por tratamiento.
Se realizó una observación de la composición proteica de los extractos concentrados a partir de los medios de crecimiento y de extractos proteicos de cutícula de broca (NaCl 0.4 M y buffer fosfato 0.4 M) mediante electroforesis sobre gel desnaturalizante de poliacrilamida (PAGE SDS) del 12 % en una cámara Protean II de Biorad, corrida bajo una diferencia de potencial de 250 V y 30 mA durante 6 horas (Laemmli 1970).
Resultados y Discusión
Tanto B. bassiana como M. anisopliae mostraron un crecimiento rápido con formación abundante de micelio y conidios en el medio líquido utilizado. En ambos casos se formaron pigmentos (de naturaleza no determinada en el experimento), amarillos en el medio con B. bassiana y verdes en el medio con M. anisopliae, siete días después de la inoculación. Según el estudio con el microscopio óptico de fluorescencia, hacia el tercer día los hongos se encuentran adheridos a los fragmentos de cutícula, lo cual es un criterio que permite sugerir la utilización del medio con macerado de cutícula de H. hampei para la propagación rápida y eficiente de los dos hongos estudiados (Fig.1). El pH se mantuvo notoriamente estable (6.6± 0.2) durante todo el proceso de crecimiento, lo cual parece indicar que, los hongos no liberan al medio cantidades importantes de protones o de hidroxilos o de ácidos o bases de Brónsted-Lowry, o que por otro lado, liberan compuestos (pares conjugados ácido-base) que actúan como amortiguadores naturales (Segel 1982). No se encontró diferencia en los patrones de crecimiento medidos a 540 y 680 nm para cada uno de los hongos pero sí se encontró una diferencia notable entre el crecimiento del aislamiento monoespórico Bb 9620 comparado con el del multiespórico Bb 9205. Probablemente la ausencia de competencia intraespecífica en el aislamiento monoespórico permite un mejor aprovechamiento de los componentes nutritivos del medio; de igual manera fue el comportamiento presentado por los aislamientos de M. anisopliae donde el crecimiento fue mayor en el caso del cultivo monoespórico.
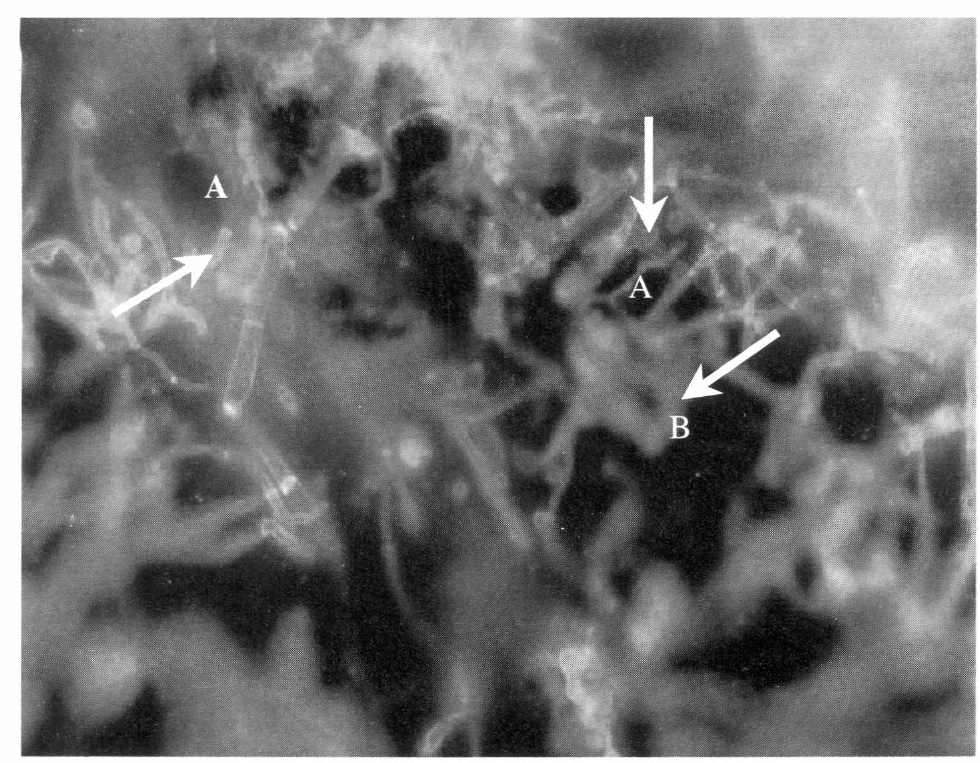
Microfotografía de fluorescencia con Calcofluor White mostrando
Patogenicidad
El análisis de varianza muestra que la patogenicidad de los aislamientos de B. bassiana y M. anisopliae tienen un alto índice de variabilidad durante el tiempo del experimento. Los dos aislamientos de B. bassiana presentan picos de patogenicidad a los 3, 7 y 20 días y no hay diferencia significativa entre ellos (p= 0.05), mientras que la patogenicidad de Ma 9303 (monoespórico) es significativamente diferente de la de Ma 9236 (multiespórico). El porcentaje de patogenicidad de los aislamientos se mantuvo superior al 80% en todos los casos. Los datos muestran que en el caso de M. anisopliae la utilización de los cultivos monoespóricos pueden significar niveles de patogenicidad sobre H. hampei más altos y constantes. Los niveles de germinación de los diferentes aislamientos (>90%) indicaron una excelente viabilidad de los materiales estudiados.
Actividad enzimática
Proteasas
Los resultados del análisis de varianza muestran que la actividad proteolítica es significativamente mayor (p=0.05) en los dos aislamientos de M. anisopliae que en los dos de B. bassiana. La actividad proteolítica de los diferentes aislamientos tuvo su máxima magnitud entre los 5 y los 7 días de incubación y coincidió con valores altos de infectividad. Luego de un aumento en la actividad proteolítica de las muestras se observó que los valores de patogenicidad se hacen mayores; este resultado sugiere que la capacidad infectiva del hongo está estrechamente relacionada con la degradación de las proteínas de la cutícula del insecto.
Lipasas
Los niveles máximos de actividad en los aislamientos tanto de B. bassiana como de M. anisopliae se presentaron entre los 3 y 5 días después de inoculados, sin evidenciar diferencias significativas (p=0.05) entre las dos especies de entomopatógenos. De acuerdo con su actividad enzimática. Sin embargo, el aislamiento Ma 9303 (monoespórico) mostró niveles de actividad de lipasas superiores (p= 0.05) a los de Ma 9236 (multiespórico).
Los resultados anteriores son confirmados por la comparación de nueve aislamientos multiespóricos de B. bassiana y cinco de M. anisopliae.
M. anisopliae mostró niveles elevados de actividad proteolítica, asociados con la patogenicidad de los aislamientos (r=0.77, p<0.01).
En la mayoría de los aislamientos no se encontró una relación directa entre la actividad proteolítica y la patogenicidad; sin embargo, Ma 9236 y Ma 9003 presentó relación entre la patogenicidad y la actividad catalítica (Fig 2).
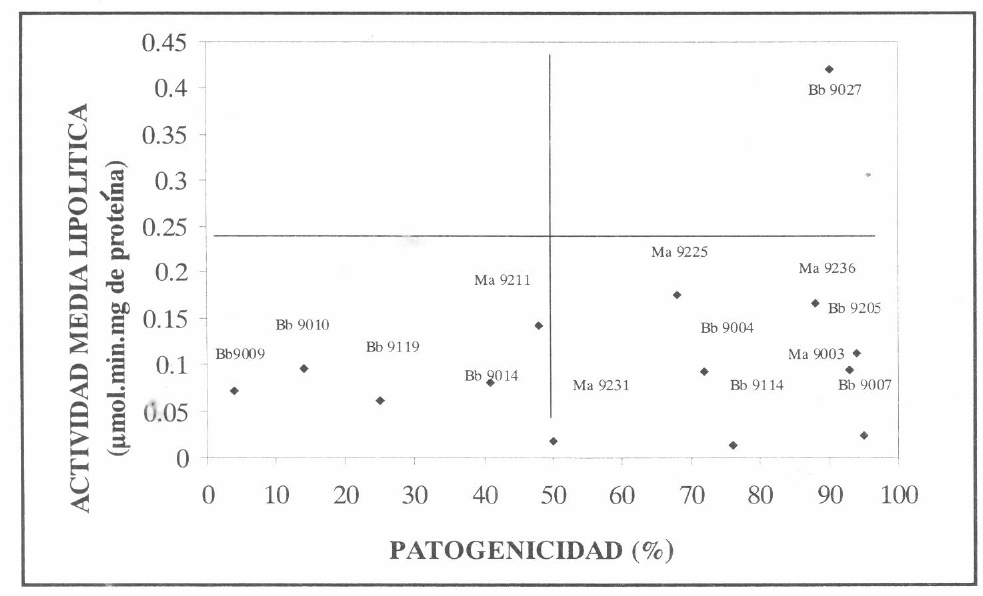
Actividad proteolítica de aislamientos de Beauveria bassiana y Metarhizium anisopliae relacionado con la patogenicidad.
Para la actividad lipolítica Bb 9027 mostró relación entre la patogenicidad y la actividad lipolítica; también se encontró, en varios aislamientos con baja patogenicidad una actividad lipolítica inferior al 50% de la actividad total (Fig 3).
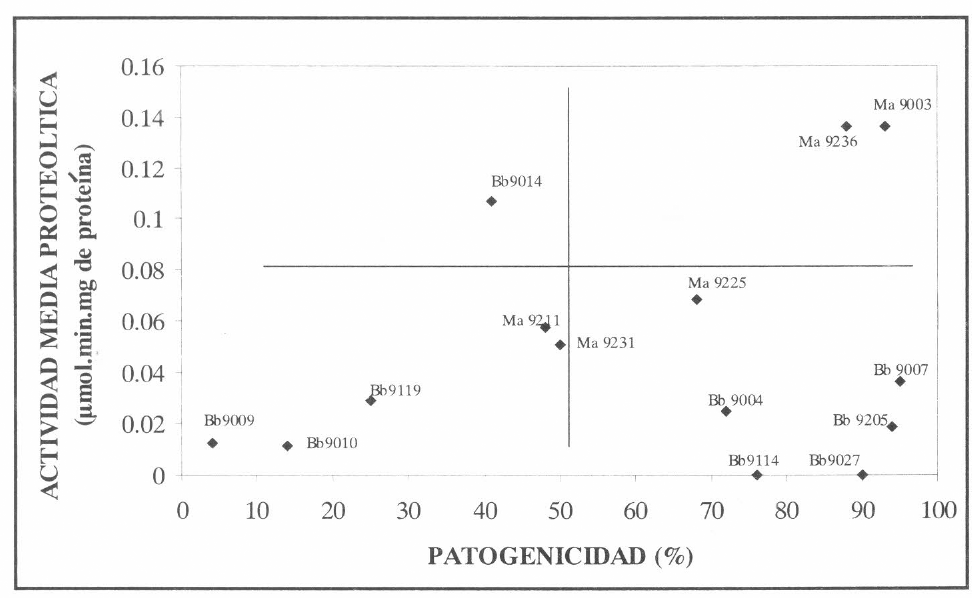
Actividad lipolítica de aislamientos de Beauveria bassiana y Metarhizium anisopliae relacionado con la patogenicidad.
Los datos encontrados no son comparables con las actividades señaladas por Peled y Krenz (1981), Robert y Messing (1985), Hedeus y Khachatourians (1988), Veeraragaran (1990), Bidochka y Khachatourians (1987, 1990), debido a que éstas han sido expresadas como unidades enzimáticas clásicas (µmol de sustrato convertido o liberado por minuto), y no como en los resultados obtenidos en esta investigación (0.1066 µmol de azo/min.mg de proteína en Bb 9014, 0.136211066 µmol de azo/min.mg de proteína en Ma 9236) de lipasas (0.4199 µmol de p.nitrofenol/ min.mg de proteína en Bb 9027 0.1745 µmol de p.nitrofenol/min.mg de proteína en Ma 9225).
Los valores de actividad máxima de proteasas, de ambos hongos, pueden ser bajos si se comparan con las actividades de otras enzimas del metabolismo animal o vegetal cuya velocidad de conversión de sustrato es mucho mayor.
Análisis electroforético
El contenido de proteína medido según Bradford (1976) es mayor en los medios que contenían sales basales y cutícula de broca, lo cual muestra que la presencia de fragmentos de cutícula en el medio es importante para el crecimiento del hongo. Sin embargo, la concentración absoluta de proteína en el medio es muy baja (Tabla 2), lo que ocasionó dificultades para la medición de la actividad enzimática.
Cuantificación de proteínas de aislamientos de B. bassiana y M. anisopliae por el método de Bradford
A pesar de la dificultad para la realización de la PAGE-SDS por la baja concentración de proteína en el medio de crecimiento, se encontró que tanto los aislamientos de B. bassiana como de M. anisopliae presentan una banda similar de una proteína de masa molecular menor a 47 kDa cuya naturaleza se desconoce.
La electroforesis de la muestra de proteína extraída de cutícula por NaCl y buffer fosfato, muestra un patrón de banda similar, en donde aparecen varias proteínas con masas moleculares entre 89 y 206 kDa y particularmente una proteína de gran concentración con masa molecular de 40 kDa, que aparentemente corresponde a la resilina, proteína implicada en la flexibilidad de las articulaciones de los artrópodos, cuya concentración es muy abundante en la cutícula (Gilmour 1968).
Conclusiones
La actividad de las proteasas de M. anisopliae es significativamente diferente de la de B. bassiana y en los dos hongos su máximo valor se encontró entre 5 y 7 días (0.166 µmol de azo.min.mg de proteína en Bb 9014, 0.1362 µmol de azo.min.mg de proteína en Ma 9236). Aunque no hay diferencia en la actividad de las lipasas entre B. bassiana y M. anisopliae, su mayor actividad se presentó entre los 3 y 5 días (0.4199 µmol de p.nitrofenol.min.mg de proteína en Bb 9027, 0.1745 μmol de p.nitrofenol.min.mg de proteína en Ma 9225). Los resultados sugieren que las lipasas y proteasas juegan un papel muy importante en los primeros días de contacto del patógeno con el hospedero, participando en la degradación de los lípidos y proteínas de la cutícula, lo cual facilita la penetración del hongo a los tejidos del insecto. Sin embargo, no se puede asegurar que sea la actividad de tales enzimas la causante directa de la muerte del insecto, en la cual también estarían implicadas las toxinas segregadas por los hongos entomopatógenos entre las cuales se pueden citar, la destruxina y beauvericina (Kaijiang y Roberts 1986; Kucera 1971).
Footnotes
Agradecimientos
El presente estudio se realizó gracias al apoyo financiero del Instituto Colombiano para el Desarrollo de la Ciencia y la Tecnología "Francisco José de Caldas" COLCIENCIAS y la Federación Nacional de Cafeteros a través de su centro de investigaciones Cenicafé.
