Abstract
An experiment was conducted to evaluate the compatibility in vitro of a mixture of Beauveria bassiana (Balsamo) Vuillemin used in the control of coffee berry borer, Hypothenemus hampei, and three insecticides incorporated in a fungus growth media and mixed in an aqueous suspension simulating a spray tank. A combination of factors were created using three different sources of B. bassiana: isolates Bb9205 and Bb9002 produced on rice substrate, and a commercial product Brocaril®, and three insecticides (diazinon in three formulations: Wetable Powder (WP), Wetable Emulsion (WE) and Encapsulated Suspension (ES); isazofos and metacrifos). All the insecticides were tested in the mixture using the commercial dosage (CD), half of the commercial dosage (½ CD) and one fourth of the commercial dosage (¼CD). Evaluations were made measuring the rate of fungus radial growth of the colony and the effect of the insecticides on fungus germination. It was found that diazinon WP and metacrifos had a heavy colony growth inhibition for isolate Bb9205 and Brocaril®. Isazofos caused the lowest inhibition on Bb9205 accounting for a reduction of fungal growth in the media from 19.1% at the commercial rate to 11.7% when ¼ CD was used. Diazinon ES in mixture with Brocaril® caused a reduction on growth from 17% at CD to 6.8% at ¼ CD. Total inhibition of germination of B. bassiana Bb9205 and Bb9002 was achieved when using diazinon WE at CD when mixed in an aqueous suspension for a period of up to 6 h; however, diazinon ES did not cause inhibition which may be attributed to the solvents used in the formulations. Diazinon WP and metacrifos had the same inhibitory effect on germination as showed when the radial growth was measured. Isolate Bb9002 was more sensible to the insecticides, this finding demonstrates that there are differences among isolates of a same fungus, which poses the necessity of selecting isolates more resistance to pesticides in IPM programs. In the experiment on conidia germination of Bb9205 reactivated in H. hampei using mixtures times for 1, 3, 6, 12 and 24 h with diazinon WE and isazofos, no significant differences were found compared to the control. Inhibition was lower with the isolate Bb9205 reactivated in H. hampei than with the one not reactivated.
Introduction
La broca del café, Hypothenemus hampei (Ferrari), es la plaga más importante de este cultivo, su llegada a Colombia ha he- cho que se desarrolle un programa de manejo integrado dentro de un marco ecológico para proteger la zona cafetera de un uso irracional de insecticidas (Bustillo et al. 1998). El uso del hongo Beauveria bassiana en el control de la bro- ca es un arma biológica muy importante porque se ha logrado establecer en toda la zona cafetera del país infestada con ésta y por sus efectos en las poblaciones de este insecto plaga cuando se asperja utili- zando preparados artesanales en las fin- cas (Antia et al. 1992) o formulaciones industriales (Morales et al. 1991, Bustillo et al. 1998).
Los insecticidas químicos son un compo- nente dentro del manejo integrado de la broca del café, pero pueden alterar nega- tivamente el medio ambiente. Una alter- nativa la constituye las mezclas con entomopatógenos como B. bassiana pen- sando en obtener una reducción en la do- sis del insecticida y un mayor efecto sobre las poblaciones de la plaga y así amino- rando el impacto ambiental. El efecto de insecticidas sobre B. bassiana ha sido bas- tante estudiado en otras situaciones (Osborne y Boucias 1985). Los agroquí- micos pueden reducir las epizootias de los entomopatógenos en campo al afectar la esporulación y su infectividad (Ferron et al. 1991). El efecto de agroquímicos sobre B. bassiana in vitro, se puede estudiar en varias formas, incorporándolos al medio de cultivo, o colocándolos en discos de papel impregnados del químico sobre el hongo, ó también haciendo mezclas entre el hongo y el plaguicida para evaluar la compatibilidad. Normalmente se registra la zona de inhibición ó medidas cuantifi- cables, como el crecimiento radial de la colonia (Ramaraje et al. 1967; Olmert y Kenneth 1974; Clark et al. 1982; Anderson et al. 1989; Moorhouse et al. 1992; Rivera 1993), sin embargo, la germinación de la conidia puede ser el criterio más impor- tante de compatibilidad (Rivera et al. 1994). Los solventes en las formulaciones pueden jugar un papel importante en la viabilidad de los hongos como fue demos- trado para el endosulfan, en el cual el xilol reduce la viabilidad de B. bassiana (Anderson y Roberts 1983; Rivera et al. 1994).
El objetivo de este trabajo fue evaluar in vitro la compatibilidad del hongo B. bassiana producido en sustrato de arroz y formulado comercialmente (Brocaril®) con los insecticidas: diazinon en tres formulaciones (PM, EM, SE), isazofos y metacrifos de la compañía Novartis S.A.
Materials and Methods
Para evaluar la compatibilidad de los in- secticidas con el hongo B. bassiana se mi- dieron las siguientes variables:
Crecimiento radial de la colonia mez- clando el insecticida con el medio de culti- vo; para lo cual se utilizó el aislamiento Bb9205 originalmente obtenido de Diatraea saccharalis producido en sustrato de arroz en el laboratorio de Entomología de Cenicafé, y un formulado en polvo mojable, Brocaril®, producido por Labora- torios Laverlam de Cali, Colombia.
Germinación de conidias a las 24 y 48 h después de estar en mezcla con los in- secticidas, simulando tanques de equipos de aspersión; se evaluaron al cabo de 1, 3 y 6 h de contacto. Se utilizaron los aisla- mientos del hongo B. bassiana Bb9205 у Bb9002 (activos contra H. hampei) pro- ducidos en sustrato arroz. Para las evalua- ciones iniciales no se tuvo en cuenta su reactivación en broca y de acuerdo con los resultados obtenidos en este ensayo se hizo una evaluación adicional con el aisla- miento Bb9205 reactivado en broca, utili- zando los insecticidas que presentaron menor inhibición sobre el hongo.
Crecimiento radial
La compatibilidad de B. bassiana aisla- miento Bb9205 producido en arroz y la formulación Brocaril® se evaluó en mezcla con insecticidas (Tabla 1) a través del cre- cimiento radial de la colonia, utilizando cajas de Petri con el medio Sabouraud Dex- trosa Agar (SDA). Se preparó el SDA, se esterilizó, se le adicionó ácido láctico al 0,37% y luego los insecticidas en las dosis establecidas (Tabla 1). Posteriormente, se sirvieron cajas de Petri con 15 ml de me- dio, una vez solidificada la mezcla se ino- culó el hongo en el centro de la caja con una alícuota de 5 µl, en concentración de 1x106 conidias /ml, las cajas se incubaron a 25°C. Después se midió el diámetro de la colonia, con un noniómetro de precisión (0.02 mm) marca Mitutoyo; a los 5, 7, 9, 12, 15, 18, 21, 24, 27 y 30 días. Como testigo se utilizó el hongo solo crecido en SDA (Rivera 1993). La variable se analizó empleando análisis de varianza y se ajustó una regresión lineal simple a través del tiempo con cada producto.
Insecticidas y concentraciones evaluadas en el estudio de compatibilidad con B. bassiana
DC: dosis comercial
PM: polvo mojable
EM: emulsión mojable
SE: suspensión encapsulada
SM: suspensión microencapsulada
CE: concentrado emulsionable
Germinación de conidias
Para evaluar la germinación de los aisla- mientos Bb9002 y Bb9205 cultivados en sustrato de arroz, frente a cada uno de los insecticidas, simulando las mezclas en tan- ques de equipos de aspersión, se preparó una suspensión acuosa de conidias del hongo (1x108 con/ml) con aceite Carrier® al 0.1%, de ésta se adicionaron 100 ml en erlenmeyer estériles de 250 ml y la canti- dad adecuada de los insecticidas (Tabla 1). Como testigo se tuvo sólo suspensión del, hongo. Las mezclas se colocaron en agitación (110 rpm). Se evaluaron los pe- ríodos de tiempo de 1, 3 y 6 h de contacto entre los dos agentes. Transcurrido cada intervalo de tiempo, se inocularon siete alícuotas de 5 µl en medio SDA más ex- tracto de levadura al 1%, de cada uno de los tratamientos (Rivera et al. 1994).
El experimento se organizó bajo un dise- ño completamente aleatorio con el erlenmeyer como UE, con cuatro repeticio- nes por tratamiento a un nivel de significancia del 5%. Para evaluar el efecto de los insecticidas sobre el hongo, se mi- dió la variable germinación de conidias, en porcentaje a las 24 y 48 h. Los resulta- dos se analizaron empleando análisis de varianza.
Germinación del hongo después de reactivado en broca
Con base en los resultados de los dos en- sayos anteriores, se evaluó la compatibili- dad en mezcla del aislamiento Bb9205 reactivado en broca, en una concentración de 9.7x108 con/ml, utilizando las dosis y los insecticidas de la Tabla 1, excepto diazinon PM y metacrifos que presentaron una alta inhibición; se alargaron los tiem- pos de mezcla a 1, 3, 6, 12 y 24 h. La varia- ble germinación de conidias se analizó empleando el mismo procedimiento del experimento anterior.
El criterio para usar las dosis y tiempos de mezcla, propuestas en cada uno de los ex- perimentos, está basado en la idea de esti- mar hasta qué punto existe compatibilidad de los productos con B. bassiana.
Results and Discussion
Crecimiento radial
Los insecticidas diazinon PM y metacrifos inhibieron completamente el crecimiento micelial de B. bassiana en todas las dosis evaluadas tanto con Bb9205 producido en arroz, como con la formulación comer- cial Brocaril®. Resultados similares encon- traron Cadatal y Gabriel (1970) y Alves (1986) con diazinon PM sobre este hon- go. Una mayor inhibición sobre el creci- miento micelial puede deberse al contacto continuo insecticida-hongo, como es el caso de diazinon PM, al compararlo con las otras formulaciones, indicando que posiblemente los inertes tienen un efecto mayor sobre la viabilidad que el ingredien- te activo.
El insecticida diazinon EM en la DC y la ½ DC produce inhibición desde los primeros momentos de contacto tanto con el hon- go comercial (Brocaril®) como con Bb9205 producido en arroz (Figs. 1-2). Diazinon SE, en mezcla con Bb9205, causó una re- ducción en el crecimiento de la colonia en la DC de 28,1 hasta 12,2% en ¼ DC, con el hongo producido comercialmente la inhi- bición fue menor (Tabla 2, Figs. 3-4). Isazofos causó la inhibición más baja so- bre Bb9205, siendo de 19,1% en la DC hasta 11,7 en ¼ DC. Con Brocaril® la inhi- bición fue mayor en la DC (31,6%) redu- ciéndose cuando se usó ¼ DC (2,6%) (Ta- bla 2, Figs. 5-6). Las dosis más bajas de los insecticidas fueron menos inhibitorias y en general tuvieron un comportamiento similar al testigo. Estos resultados están de acuerdo con los hallados por Olmert y Kenneth (1974) y Vainio y Hokkanne (1990) que observaron que diazinon CE no causa un mayor efecto sobre el hongo Beauveria bassiana.
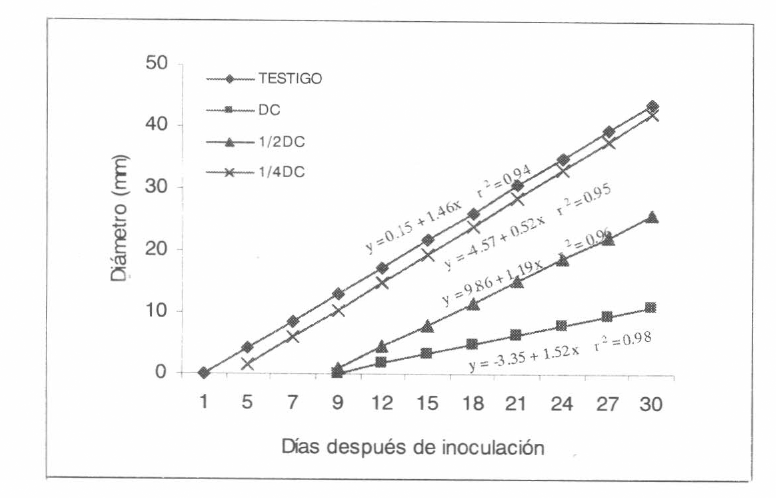
Crecimiento de la colonia de Beauveria bassiana (Brocaril) en medio de cultivo (SDA) al cual se le adicionó diazinon EM en diferentes dosis, DC (dosis comercial); ½DC y ¼DC.
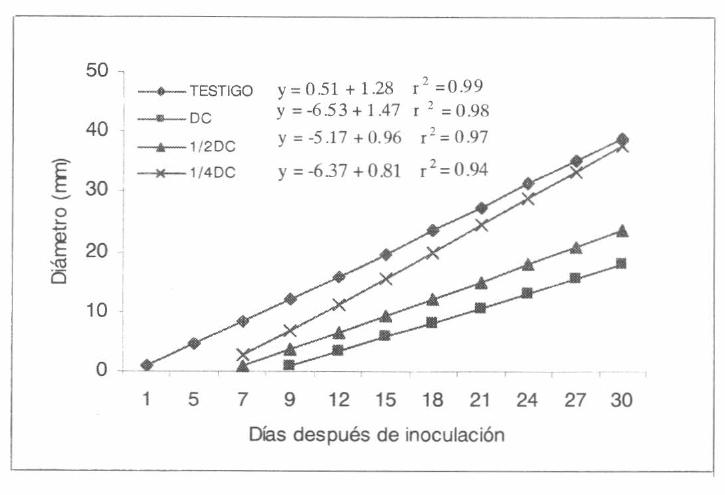
Crecimiento de la colonia de Beauveria bassiana (Bb9205-arroz) en medio de cultivo (SDA) al cual se le adicionó diazinon EM en diferentes dosis, DC (dosis comercial); ½DC y ¼DC.
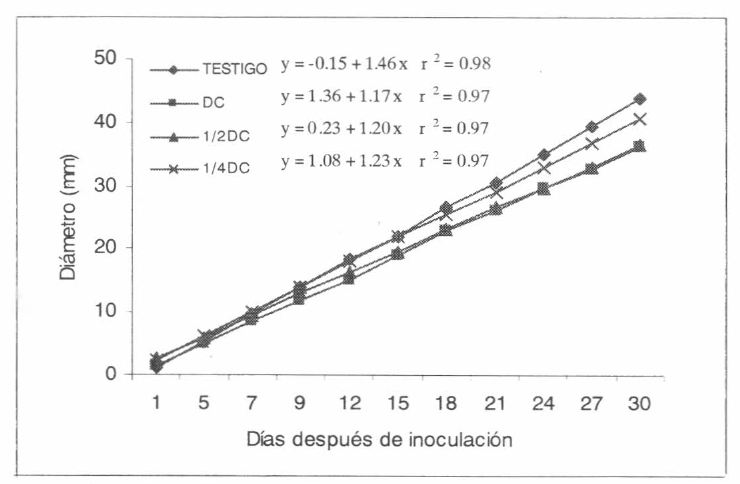
Crecimiento de la colonia de Beauveria bassiana (Brocaril) en medio de cultivo (SDA) al cual se le adicionó diazinon SE en diferentes dosis, DC (dosis comercial); ½DC y ¼DC.
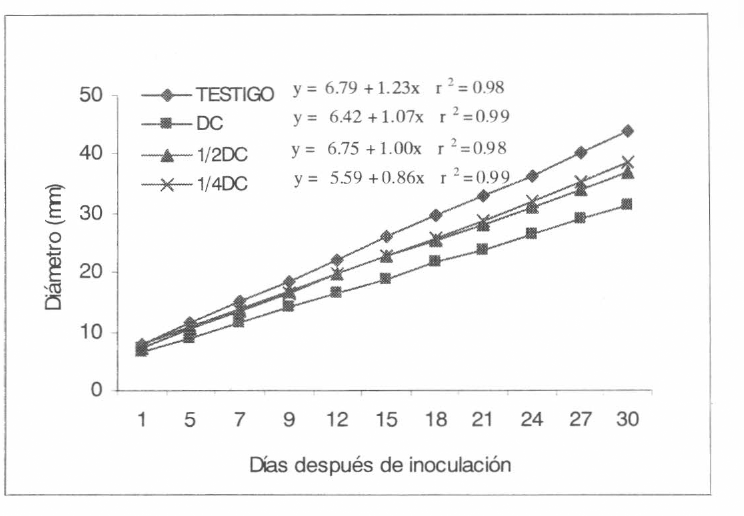
Crecimiento de la colonia de Beauveria bassiana (Bb9205-arroz) en medio de cultivo (SDA) al cual se le adicionó diazinon SE en diferentes dosis, DC (dosis comercial); ½DC y ¼DC.
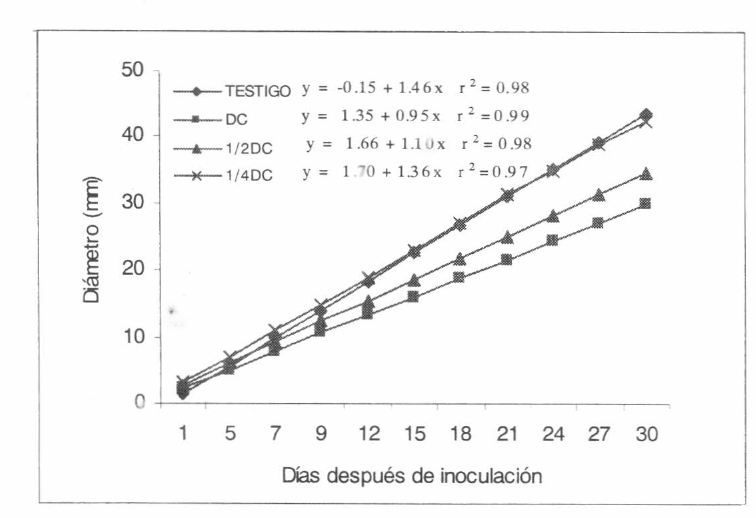
Crecimiento de la colonia de Beauveria bassiana (Brocaril) en medio de cultivo (SDA) al cual se le adicionó isazofos en diferentes dosis, DC (dosis comercial); ½DC y ¼DC.
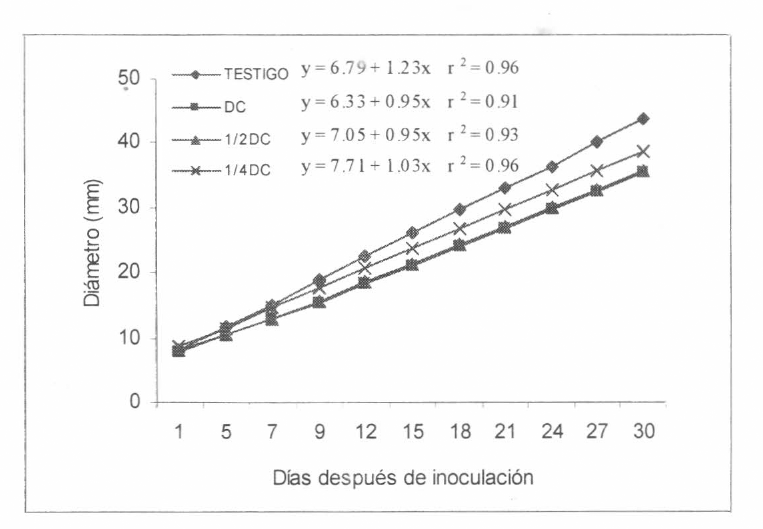
Crecimiento de la colonia de Beauveria bassiana (Bb9205-arroz) en medio de cultivo (SDA) al cual se le adicionó isazofos en diferentes dosis, DC (dosis comercial); ½DC y ¼DC.
Crecimiento radial (CR/ mm) y porcentaje de inhibición (PI/ %) de B. bassiana Bb9205 producido en arroz y Brocaril comercial en presencia de insecticidas, 30 días después de la inoculación
Compatibilidad en mezcla
Al evaluar la compatibilidad en mezcla, si- mulando tanques de equipos de asper- sión, se encontró a las 24 horas de evaluación que Diazinon PM y metacrifos causaron alta inhibición como sucedió so- bre el crecimiento micelial en el experimen- to anterior.
Se observaron diferencias estadísticas sig- nificativas (Tukey 5%) con los dos aisla- mientos del hongo evaluados y el insecti- cida diazinon EM; a la DC produjo una alta inhibición de la germinación conidial con ambos aislamientos desde los primeros momentos, siendo mayor al aumentar el tiempo de contacto (Figs. 7-8). Sin em- bargo, la formulación SE de diazinon no causó inhibición estadísticamente signifi- cativa, lo que se puede atribuir al solvente utilizado en esta formulación. Con isazofos y el aislamiento Bb9205 no se presenta- ron diferencias (Tukey 5%) entre el testigo y ¼ DC, pero si con las dosis mas altas, algunas combinaciones de dosis menores a la DC no tienen mayor efecto sobre los dos aislamientos y el efecto es creciente al aumentar la dosis (Figs. 9-10). El aisla- miento Bb9002 fue más sensible a los in- secticidas, este resultado demuestra que hay diferencias entre aislamientos de un mismo hongo, lo cual indica la necesidad de seleccionar aislamientos más resistentes a plaguicidas para ser utilizados en pro- gramas de MIP.
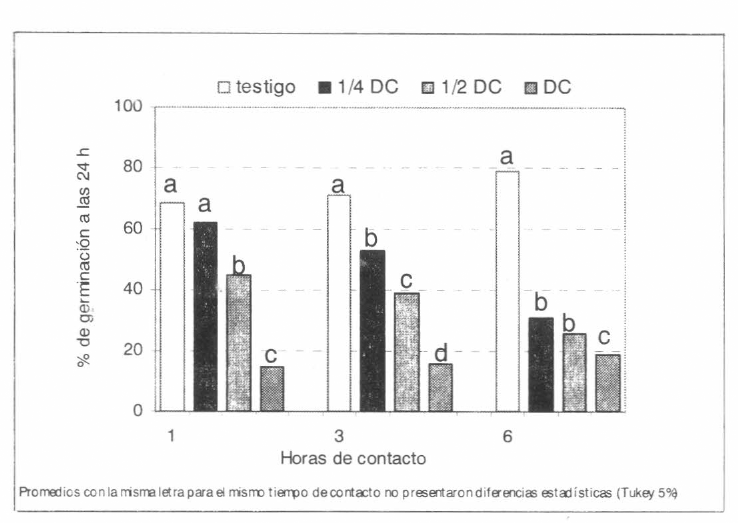
Germinación de Beauveria bassiana Bb9002, varias horas después de permanecer en contacto con una mezcla de diazinon EM en tres dosificaciones (DC: dosis comercial; ½DC y ¼DC).
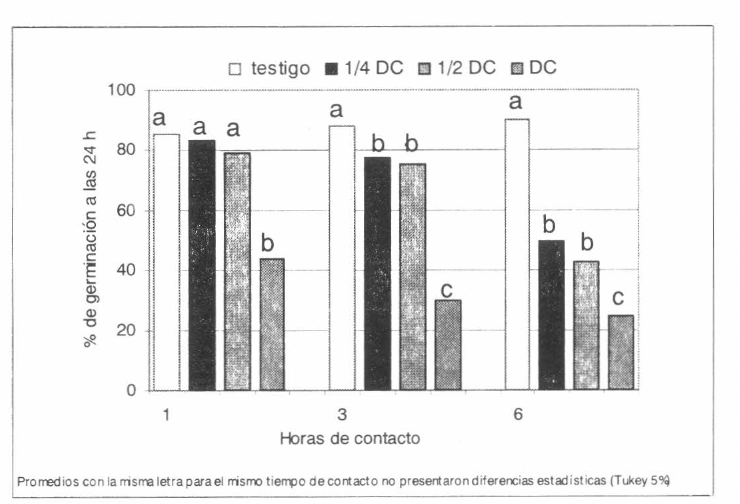
Germinación de Beauveria bassiana Bb9205, varias horas después de permanecer en contacto con una mezcla de diazinon EM en tres dosificaciones (DC: dosis comercial; ½DC y ¼DC).
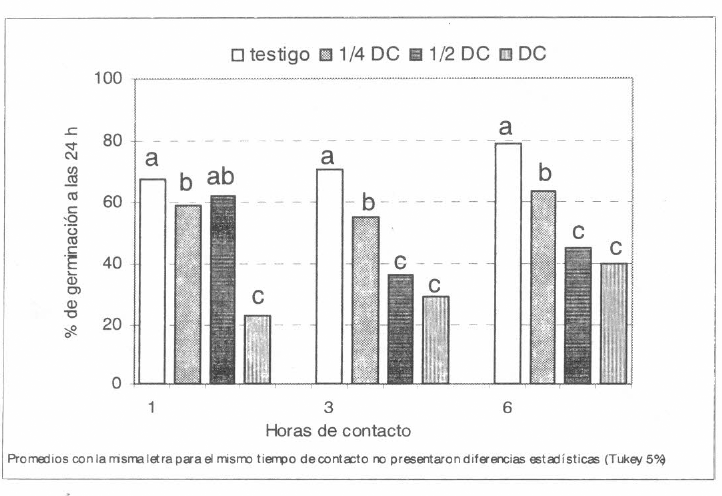
Germinación de Beauveria bassiana Bb9002, varias horas después de permanecer en contacto con una mezcla de Isazofos en tres dosificaciones (DC: dosis comercial; ½DC y ¼DC).
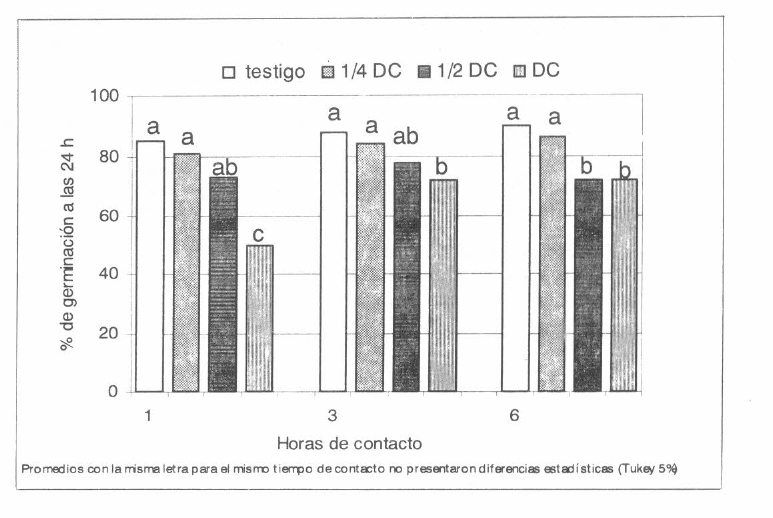
Germinación de Beauveria bassiana Bb9205, varias horas después de permanecer en contacto con una mezcla de Isazofos en tres dosificaciones (DC: dosis comercial; ½DC y ¼DC).
El efecto de los insecticidas diazinon EM, diazinon SE e isazofos a las 48h de evalua- ción fue inocuo, pues la germinación mos- tró diferencias no significativas con respecto al testigo, en las dosis evaluadas con los dos aislamientos. diazinon PM y metacrifos inhibieron totalmente al hon- go durante todo el tiempo de evaluación.
No hay registros en la literatura que su- gieran razones sobre la variación en la respuesta de las pruebas de los aisla- mientos del hongo frente a los insectici- das; por ejemplo Olmert y Kenneth (1974) no explicaron las diferencias en sensibilidad a Diazinon in vitro. Lyr (1977) mencionó que ciertas diferencias se han observado en cuanto a sensibili- dad de fitopatógenos a ingredientes ac- tivos, lo que se podría atribuir a sensibilidad de estructuras celulares, di- ferencia en la potencia de los mecanis- mos de defensa o diferencias en la penetración o acumulación del compues- to fungicida en el sitio de acción y detoxificación dentro de la célula. Varias de las suposiciones de Lyr podrían ser aplicadas a los hongos entomopa- tógenos.
Compatibilidad en mezcla del aislamiento Bb9205 reactivado en broca
Para evaluar la compatibilidad en mezcla del aislamiento Bb9205 reactivado en bro- ca se alargaron los tiempos de contacto a 1, 3, 6, 12 y 24 h. Los resultados mostra- ron que diazinon EM e isazofos tuvieron cierto efecto inhibitorio gradual en orden descendente de acuerdo con las dosis uti- lizadas pero los resultados no difieren estadísticamente del testigo, además de alcanzarse la germinación total a las 48 h. El insecticida diazinon SE no exhibió nin- gún efecto sobre el hongo y su comporta- miento fue igual al testigo.
En este experimento, el aislamiento reactivado en broca presentó una mayor tolerancia a los insecticidas. Se ha demos- trado que los insecticidas reducen la via- bilidad de la conidia, pero no previenen la producción de enzimas que degradan el medio en las conidias germinantes, esto podría explicar la ventaja del aislamiento reactivado. Por ejemplo, pectinasas aso- ciadas con la patogénesis de Penicillium digitatum aparentemente son secretadas por los tubos germinativos inhibidos por benomyl, aquellas degradan la pared de las células circundantes en el sitio de inoculación, liberando nutrientes que incrementan la viabilidad de las conidias resistentes en el inóculo (Wild y Eckert 1982); esto refuerza la necesidad de utili- zar aislamientos previamente reactivados para darle una mayor oportunidad de con- trol al patógeno al ser mezclado con in- secticidas.
Anderson et al. (1989) sugieren que hay variabilidad genética entre aislamientos por la sensibilidad a los plaguicidas ob- servada entre ellos. La sobrevivencia de biotipos persistentes parece depender de la naturaleza de la resistencia y las propie- dades individuales del aislamiento, aun- que este comportamiento puede no ser representativo de toda la población; ade- más, que los biotipos tolerantes pueden proliferar fácilmente en campo (Smilanick y Eckert 1986). Investigaciones recientes también sugieren que varios niveles de resistencia a plaguicidas son la manifesta- ción de polimorfismo en un solo gen mendeliano (Fabritius et al. 1997).
Otra estrategia para el biocontrol de in- sectos sería la selección o manipulación genética de estos hongos resistentes a plaguicidas comunes; estudios en este campo han demostrado el uso potencial de cepas transgénicas de hongos entomopatógenos con otros componen- tes del Manejo Integrado donde se pueda hacer una aplicación simultánea de los dos agentes (Goettel et al. 1990).
Los resultados de este experimento no se pueden extrapolar con lo que sucede en el campo, se deben realizar evaluaciones pos- teriores bajo condiciones reales, verifican- do la reducción en la capacidad patogénica del hongo, pues los productos tóxicos in vitro no necesariamente causan daño a los entomopatógenos en campo.
Footnotes
Agradecimientos
La autora principal agradece a Cenicafé y a las personas que de una u otra forma cola- boraron para la realización de este trabajo y a la compañía Novartis S.A. por el apoyo logístico.
