Abstract
Amylase is an enzyme with high activity in the digestive system of H. hampei. Its function allows the insect to actively digest the starch present in the digestive system of coffee berry borer, providing the glucose that is required to fulfill its metabolic functions. The amylolytic activity knowledge from CBB, is an essential study for inhibitors selection, which can be used for the transgenic coffee production. In order to determine the best extraction solution, pH and optimal temperature for the amilolytic activity of the insect, 1g of adults insects were pestled with different solutions containing either 5 ml of water, 1% NaCl, or extraction buffers with differents pH. Enzyme activity was determined by spectrophotometry at 580nm. An amylolytic activity zymogram was prepared using whole adults and adult intestines in homogeneus gels 15%. The best amylase extraction solution was a solution containing 1% NaCl. The optimal activity pH for the enzyme was 5,0 and the optimal activity temperature 40°C. The amylolytic activity zymogram showed several activity bands. Two main bands with enzyme activity are present in the digestive system of the CBB.
Introducción
En los estudios dirigidos a combatir y proteger los cultivos de los insectos que atacan a las plantas, es importante tener un mejor conocimiento sobre la bioquímica de los insectos y en particular sobre las enzimas más importantes involucradas en los procesos digestivos, de forma que conociendo estas enzimas, pueda diseñarse una estrategia que permita bloquear o interrumpir su función, es decir, producir una inhibición dirigida específicamente contra esta enzima (Blanco-Labra et al. 1996).
El metabolismo digestivo de los insectos se asemeja al de los vertebrados. Como éstos, poseen enzimas adaptadas a la dieta de la que se alimentan. Si viven de una dieta particularmente rica en una sustancia, generalmente producirán las enzimas apropiadas para su digestión en abundancia (ej. amilasas para dietas ricas en carbohidratos), y si por el contrario, la dieta es altamente restringida, las enzimas presentes serán correspondientemente limitadas (Applebaum 1985). La mayor parte del alimento requerido para la nutrición de los insectos consiste de polímeros como el almidón, celulosa, hemicelulosa y proteínas. El proceso digestivo de éstos ocurre en tres fases, durante la fase inicial, se lleva a cabo la disminución en el peso molecular de compuestos poliméricos mediante la acción de hidrolasas poliméricas (amilasas, celulasas, hemicelulasas y endoproteasas); los oligómeros resultantes son hidrolizados en la etapa intermedia por hidrolasas oligoméricas, que actúan sobre fragmentos parcialmente degradados. Los productos de esta fase son dímeros o pequeños oligómeros tales como maltosa, celobiosa y dipéptidos. En la etapa final de la digestión, los dímeros se rompen en monómeros por hidrolasas como maltasa, celobiasa, dipeptidasas, tripeptidasas, aminopeptidasas y carboxipeptidasas las cuales se hallan generalmente localizadas en la membrana epitelial del intestino (Terra 1990). Es muy probable que las carbohidrasas digestivas de los insectos hidrolizen poli, oligo y disacáridos a sus correspondientes monosacáridos, para prepararlos para su absorción de manera similar a las carbohidrasas de vertebrados. En estos últimos, las hidrolasas poliméricas son secretadas principalmente por las glándulas salivales y el epitelio del intestino medio. Se reconocen dos categorías de carbohidrasas, las cuales se denominan comúnmente como a-amilasas y β-amilasas. Las a-amilasas (1,4-a-D-glucan glucanohidrolasas) se caracterizan por atacar enlaces glicosídicos internos de almidón o glicógeno. Se considera que el ataque (α-1,4) produce rompimientos al azar que generan una mezcla de dextrinas de longitudes de cadena variable, aunque algunas evidencias señalan que la hidrólisis del almidón sigue un cierto orden (Bohinski 1983).
Las amilasas de los insectos juegan un papel muy importante en la digestión del almidón presente en la semilla. El orden Coleoptera es extremadamente grande, en consecuencia es difícil hacer generalización acerca de la distribución de las enzimas digestivas de éstos o de un insecto en particular. La digestión del almidón por amilasas de insectos ha sido demostrada en S. granarius (Silano et al. 1975; Baker 1983); Tribolium castaneum (Krishna y Saxena 1962); Trogoderma spp. (Krishna 1955); Rhyzopertha dominica (Baker 1991); Sitophillus zeamais (Baker 1983; Sandoval-Cardoso 1991); Sitophillus orizae (L) (Baker 1987; Yetter et al. 1979); Callosobruchus maculatus (Campos et al. 1989); Zabrotes subfasciatus (Lemos et al. 1990) y Tenebrio molitor (Applebaum 1964). Un mejor entendimiento de las enzimas involucradas en la utilización del alimento por el insecto, y de sus principales propiedades, permitirá un mayor entendimiento del papel que desempeñan en los mecanismos de resistencia del insecto frente a potenciales inhibidores. En el presente trabajo se describen varias propiedades de amilasas encontradas en adultos de Hypothenemus hampei.
Materiales y Métodos
Material Biológico
Se utilizaron brocas adultas recién emergidas de café pergamino seco con una humedad del 45%, provenientes de la unidad de cría de parasitoides de Cenicafé (Chinchiná-Caldas). Las condiciones ambientales para la cría de broca son a temperatura de 27°C y humedad relativa del 65% - 75%.
Evaluación de la actividad amilasa
La actividad amilasa fue determinada de acuerdo con el método de Hopkins y Bird (1954).
50 µl de solución de la enzima se incubaron por 15 minutos a 30°C con 650 µl de buffer citrato 0.05M pH 5,0 conteniendo 10 mM de NaCl y 20 mM de CaCl₂ y 500 µl de una solución 0.125% de almidón (Almidón soluble, Sigma Chemical Co.) en 50 mM de buffer citrato pH 5,0. La reacción se detuvo por la adición de 5 ml de una solución de Iodo (I: 0.5% y KI: 5%). Las muestras se leyeron a 580 nm utilizando un espectrofotómetro UV/VIS marca UNICAM. Para cada prueba, la actividad se determinó a partir de 5 repeticiones.
Medios de extracción
Las amilasas fueron extraídas homogeneizando 1g de brocas adultas con 5 ml de cada uno de los siguientes medios de extracción: NaCl 1%, H₂O, buffer succínico 0.05M pH 4,0 y 6,0; buffer citrato 0.05M pH 3,0 y buffer Tris- HCl 0.05M pH 8,0. El homogeneizado se centrifugó a 10000 x g durante 30 minutos y el sobrenadante resultante (fuente de la enzima) se almacenó a -20°C. Todas las etapas se realizaron a 4°C.
pH óptimo
El pH óptimo de las amilasas en H. hampei se determinó en soluciones buffer 0.05M conteniendo 10 mM de NaCl y 20 mM de CaCl₂. Los buffers utilizados fueron: buffer citrato pH 3,0 y 5,0; buffer succínico pH 4,0 y 6,0; buffer fosfato pH 7,0; buffer tris-HCl pH 8,0 y buffer borato pH 9,0.
Estabilidad térmica
La estabilidad térmica de las amilasas, en presencia de NaCl y CaCl₂, se determinó preincubando la solución de la enzima en buffer de actividad durante 5 minutos a 25, 30, 40, 50, 60 y 70°C. Se tomaron cinco repeticiones de cada tratamiento evaluado.
Zimograma de actividad
La actividad amilolítica se detectó en zimogramas in situ empleando el método de Campos et al. (1989). Las muestras de la enzima se analizaron sobre geles de poliacrilamida (PAGE) al 15% en condiciones nativas, utilizando cámara de electroforesis vertical (Bio-Rad laboratories, Modelo Miniprotean II), en los cuales se incluyó almidón coopolimerizado a una concentración del 0,25%. La electroforesis se corrió durante 3 horas a 100 voltios y a 4°C. Posteriormente, el gel se lavó suavemente con agua desionizada y se colocó en buffer de actividad (buffer fosfato pH 5,0; 10 mM NaCl y 20 mM CaCl₂) por 2 horas a 35°C. Las bandas de actividad se detectaron por coloración del gel durante 30 minutos, con una solución de Iodo. Las zonas de actividad aparecieron en todos los casos como bandas claras sobre un fondo azul oscuro. Finalmente, el gel se fotografió y la imagen se digitalizó.
Resultados y Discusión
Medios de extracción
La figura 1 muestra el efecto de los diferentes medios de extracción utilizados sobre la actividad relativa de la enzima. La actividad máxima se presentó cuando se utilizó NaCl al 1% como medio de extracción. La actividad amilasa de insectos como S. zeamais y S. granarius se incrementa significativamente cuando la enzima es preincubada con NaCl (Baker 1983); de manera similar a lo encontrado para H. hampei en este estudio. Es bien conocido, que la activación por cloro es una característica de muchas amilasas de mamíferos y bacterias (Robyt y Whelan 1968), así como también de varios insectos (Baker 1983; Doane 1969; Hori 1971; Terra et al. 1977). Sin embargo, la amilasa presente en C. chinenesis fue inhibida por el cloro (Podoler y Applebaum 1971). Cabe destacar que en todos los medios de extracción evaluados fue posible encontrar actividad relativa amilasa superior al 60%.
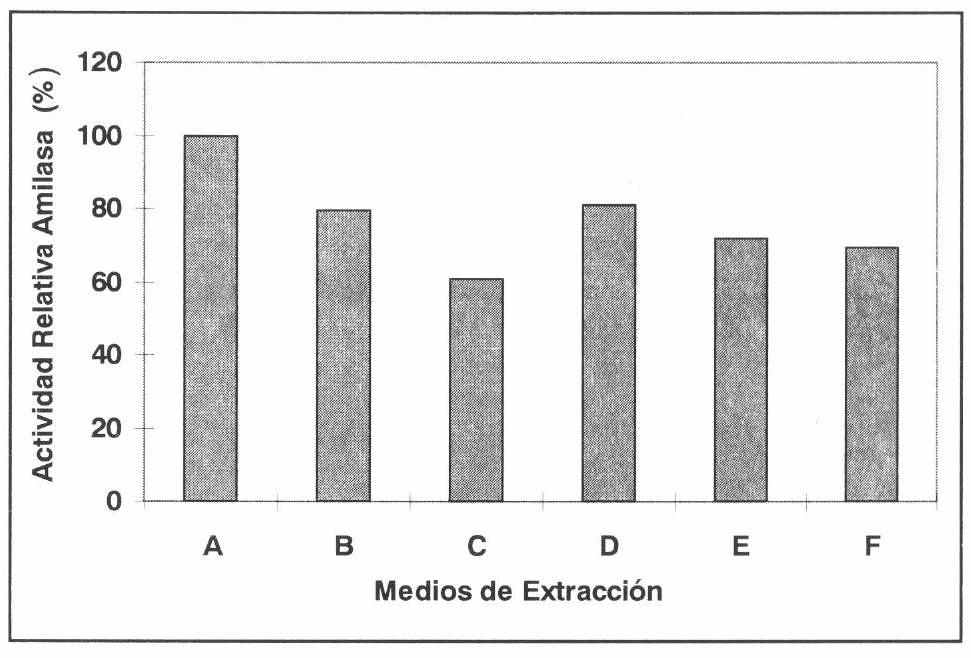
Efecto de seis medios de extracción sobre la hidrólisis del almidón por amilasas de Hypothenemus hampei. A, NaCl 1%. B, H₂O. C, Buffer citrato pH 3,0. D, Buffer succínico pH 4,0. E, Buffer succínico pH 6,0. F, Buffer tris-HCl pH 8,0.
pH óptimo
Las amilasas de insectos son generalmente muy activas en rangos de pH ligeramente ácidos a neutros (Baker 1983). En H. hampei los resultados muestran un mayor pico de actividad a pH 5,0 (Fig. 2), el cual se encuentra en el rango de 4,6 - 5,8 señalado para varios insectos del orden Coleoptera. Así por ejemplo, en Callosobruchus chinensis el pH óptimo es de 5,2 a 5,4 (Podoler y Applebaum 1971); en Tribolium castaneum el pH 4,6 a 5,2 (Applebaum y Konijn 1965); pH 5,8 para la amilasa de Tenebrio molitor (L) (Buonocore et al. 1976); pH 6,5 a 7,0 en Costelytra zealandica (Biggs y McGregor 1996) y pH 4,5 a 5,5 para Sitophilus zeamais y Sitophilus granarius (Baker 1983). El pH óptimo para la actividad amilasa de H. hampei, determinado en presencia de cloro y calcio, muestra igualmente que la enzima es muy activa en un rango de 4,0 a 7,0, y que por fuera de estos valores su actividad disminuye considerablemente. Además, en todos los casos la enzima fue activada por cloro y estabilizada por calcio. Todas estas propiedades coinciden con aquellas típicas de las α-amilasas (Ming - Shun Chen et al. 1992).
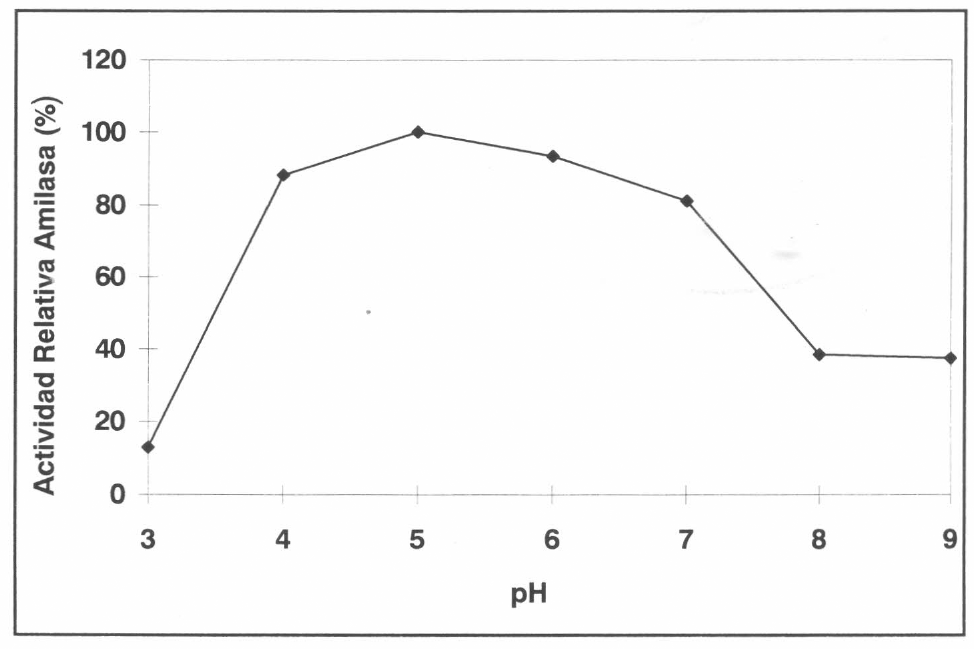
Efecto del pH sobre la hidrólisis del almidón a 30°C por amilasas de Hypothenemus hampei.
Estabilidad térmica
La temperatura óptima de actividad de la enzima se observó a 40°C con una ligera disminución a 50°C. Después de los 50°C la actividad de la enzima disminuye notablemente, debido posiblemente a la desnaturalización de la enzima al ser sometida a temperaturas altas (Fig. 3). En general, la amilasa proveniente de H. hampei presenta buena estabilidad térmica en el rango comprendido entre 30- 55°C, lo cual se atribuye a la presencia de calcio en los buffers de actividad, debido a que las amilasas son metaloenzimas que requieren calcio para la actividad catalítica (Robyt y Whelan 1968). La incubación de la amilasa de H. hampei por más de 5 minutos a 70°C conlleva a la pérdida completa de la actividad enzimática. Igual resultado fue encontrado con amilasas de S. zeamais y S. Granarius (Baker 1983). Las enzimas tienen diferente energía de activación y de conversión, por lo tanto, una modificación en la temperatura puede ocasionar un cambio en una de ellas (Lee y Anstee 1995).
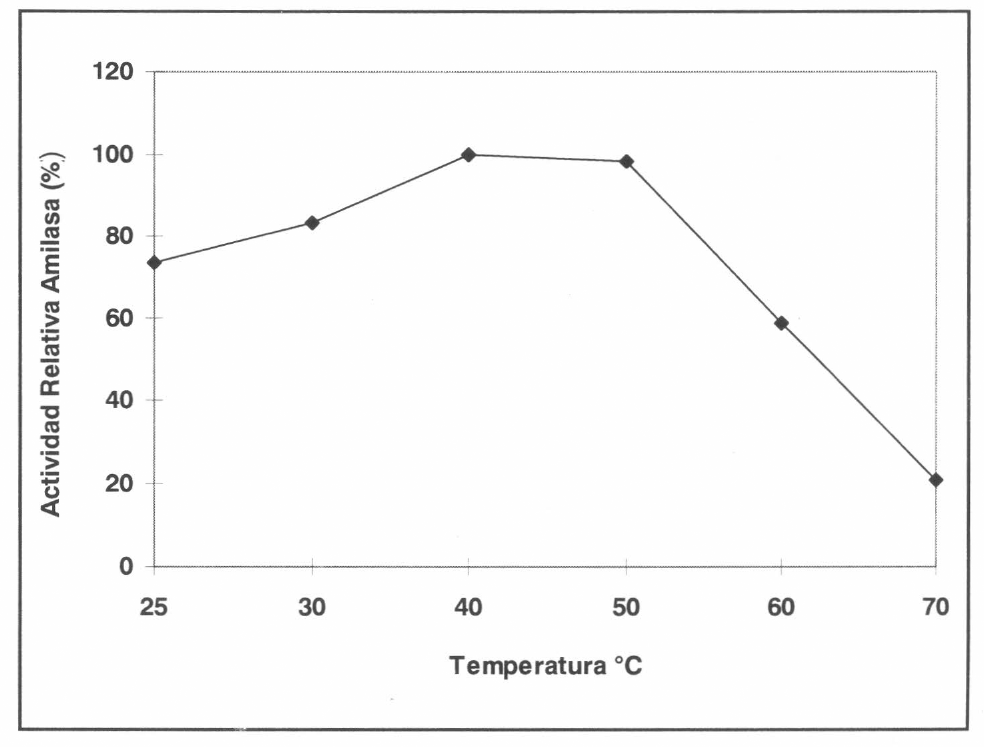
Efecto de la temperatura sobre la actividad amilasa de Hypothenemus hampei.
Zimograma de actividad
El análisis isoenzimático realizado para el extracto de adultos de H. hampei (Fig. 4) mostró 3 bandas de actividad amilasa una de las cuales representa más del 80% del total de la actividad enzimática. Esto indica que es posible purificar y caracterizar esta enzima con miras a evaluar posibles inhibidores, los cuales pueden ser incorporados en la planta de café y obtener de esta forma resistencia a H. hampei.
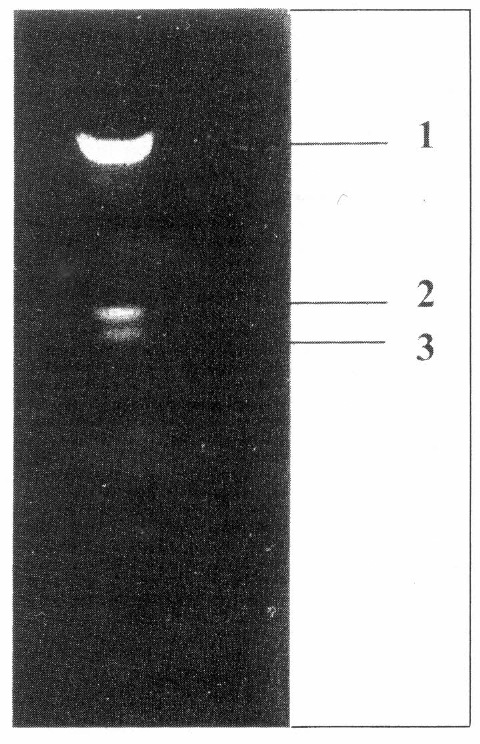
Zimograma de actividad amilasa de Hypothenemus hampei en gel de electroforesis nativo del 15 %. Después de la electroforesis, el gel se incubó en buffer citrato 0.05M pH 5,0 conteniendo 10mM de NaCl y 20mM de CaCl₂ por 120 minutos a 30°C. Tinción con solución de Iodo. Las zonas claras indican 3 bandas de actividad enzimática.
Similares resultados se encontraron en S. zeamais el cual presenta dos isoenzimas de amilasas en geles de poliacrilamida del 7.5 %. Mientras que las amilasas de H. hampei bajo estas condiciones son fuertemente catiónicas, según Baker (1983) las de S. zeamais se movieron cerca del frente de corrida indicando su naturaleza aniónica. La presencia de un número mayor de pequeñas bandas de actividad cerca de las bandas principales, puede ser el resultado de artefactos (Doane 1967). Dos de estas bandas se encontraron igualmente en extractos de intestinos, lo cual evidencia que estas bandas corresponden a amilasas intestinales (Imagen no mostrada).
Terra et al. (1985) mostraron que esencialmente toda la actividad de las a-amilasas en T. molitor está asociada con el tracto digestivo (80% con el intestino medio y 20% con el intestino anterior). Sin embargo, Silva y Terra (1994) en trabajos posteriores demostraron que la actividad de estas enzimas se inicia cuando los insectos sienten hambre y se incrementa con el consumo del alimento por el insecto. A pesar de los estudios con homogenizados de insectos, larvas o bien con los intestinos, el conocimiento de la distribución espacial de la digestión en insectos se limita al conocimiento de las zonas en las cuales ocurre (Vázquez - Arista 1997), quedando la necesidad de aislar y caracterizar enzimas digestivas de glándulas salivales, buche y espacios luminares fuera y dentro de la membrana peritrófica que envuelve el alimento en el intestino medio, así como identificar los mecanismos amortiguadores de pH que pueden afectar la digestión.
Ishimoto y Kitamura (1988) encontraron que los inhibidores de a-amilasas son los responsables de la protección de P. vulgaris al ataque de Callosobruchus chinensis. Al igual, una alta toxicidad del inhibidor, puede causar la muerte a las larvas cuando estas se alimentan de dietas artificiales conteniendo este inhibidor. El conocimiento generado en esta investigación es muy importante ya que permite conocer las principales propiedades de las amilasas de la broca del café, a la vez que posibilita la evaluación de potenciales inhibidores proteicos con actividad específica hacia a-amilasas provenientes de la broca.
Footnotes
Agradecimientos
Los autores agradecen ampliamente a Colciencias y a la Federación Nacional de Cafeteros de Colombia por el gran apoyo financiero para la ejecución del trabajo.
