Abstract
For the development of improved bean lines resistant to Acanthoscelides obtectus (Say), an important bean storage insect pest, it is indispensible to elucidate the genes involved in antibiotic resistance. The RNA differential display technique is a useful tool in the isolation of genes which show differential expression in different tissues. Up to this moment we have implemented both radioactive, and non radioactive techniques. Total RNA has been isolated from different genotypes of P. lunatus with varying levels of resistance to A. obtectus and then bulked into groups of resistant and susceptible genotypes. The messenger RNA (protein coding sequence) was isolated by chromatography and used in reverse transcription experiments. Hexanucleotide primers were used for first strand synthesis and the amplification of cDNAs was done through the polymerase chain reaction (PCR). The synthesis of the second strand was performed using random primers ten nucleotides in length each. The isolated bands were confirmed through differential display of total RNA in each of the genotypes. The evaluation of 76 random decanucleotides has made evident 6 differential bands sized between 200 and 600 bp. The purified amplified bands were assessed against resistant and susceptible genotypes through northern blots. Bands present in resistant genotypes have been reamplified and cloned in pCRII plasmids. Simultaneously, other experiments have been developed to identify factors involved in resistance through subtractive hybridization and the use of degenerate primers.
Introducción
El gorgojo común del fríjol, Acanthoscelides obtectus (Say), constituye la principal plaga del fríjol almacenado en América Latina y Africa. Las pérdidas postcosecha en este cultivo, a causa del daño producido por brúchidos, se calculan en un 13-14%. A pesar que diferentes sustancias antinutritivas se han analizado en relación con la resistencia del fríjol a A. obtectus (Gatehouse et al. 1987; Fory et al. 1996a), el factor de resistencia permanece aún sin dilucidar. Aunque se han identificado fuentes de resistencia al insecto en varias especies del género Phaseolus, como P. vulgaris L, P. lunatus L y P. acutifolius (A. Gray), la resistencia de tipo antibiótico, no ha podido ser introducida en variedades comerciales, al parecer por presentar un patrón de herencia complejo (Kornegay y Cardona 1991).
Conciente de la necesidad de resolver el problema de la introgresión y transferencia de genes de resistencia a A. obtectus a variedades comerciales de fríjol, el CIAT ha venido desarrollando, desde 1991, investigaciones encaminadas a dilucidar la base bioquímica y molecular de la resistencia a este insecto.
En los últimos cinco años los avances en la ingeniería genética de plantas han permitido la obtención de plantas transgénicas resistentes a insectos. La transferencia de genes foráneos como Cry1Aa, Cry1Ab y Cry1Ac, inhibidores de proteasas, quitinasas y alfa amilasas a plantas por mecanismos de transformación genética ha sido exitosa para cultivos como tomate, tabaco, papa, maíz y arroz (Estruch et al. 1997). A pesar de estos avances, en la actualidad no existen muchos genes de resistencia identificados.
En este estudio se empleó la técnica de visualización diferencial descrita por Liang y Pardee (1992) para comparar genotipos resistentes y susceptibles a A. obtectus e identificar AND copias (ADNC) localizados en el genoma de fríjoles resistentes al insecto. Esta técnica se puede constituir en una herramienta alternativa, rápida y económica para el mejoramiento genético tradicional y puede contribuir en el desarrollo de una agricultura sostenible, disminuyendo el uso de agroquímicos utilizados en el control de este insecto y constituiría el primer paso para la transferencia de genes a variedades comerciales de fríjol.
Materiales y Métodos
Caracterización de ARN mensajeros (ARNm): métodos radiactivo y no radiactivo
Basicamente la técnica descrita por Liang y Pardee (1992) consiste en sintetizar fragmentos de ADN copia (ADNc) a partir de ARN mensajero (ARNm) de dos tipos de células, mediante la transcripción reversa, aumentando posteriormente el número de copias a través de una reacción en cadena de la polimerasa (RCP). Las secuencias cortas (100-600 pares de bases) son separadas y comparadas sobre un gel de secuencia (Fig. 1). Yoshida et al. (1994) y Sokolov y Prockop (1994) modificaron la técnica utilizando un método no radiactivo logrando, de una manera más sencilla, diferenciar fragmentos hasta de 3000 pares de bases (pb).
Preparación del ARN
Para determinar diferencias en la expresión genética a nivel de ARNm se extrajo ARN total de genotipos cultivados de P. lunatus (Tabla 1) con diversos niveles de resistencia a A. obtectus (Datos no publicados de Entomología de Fríjol, informe anual 1995). El ARN total fue aislado utilizando el método descrito por Hall et al. (1978). Tres gramos de cotiledones de cada genotipo se pulverizaron en nitrógeno líquido; una vez evaporado el nitrógeno se adicionaron 7.8 ml de una solución de extracción que contenía borato de sodio 0.2 M, (pH 9.0); EGTA 30 mM; DDT 5mM; SDS 1%. El extracto resultante se incubó a 70°C por 3 minutos. Posteriormente, para desnaturalizar las proteínas, se adicionaron 3.9 mg de proteinasa K y se incubó a 37°C por 1 hora. La extracción de proteínas se realizó con fenol/cloroformo. El ARN presente en la solución acuosa fue precipitado con LiCl. El ARNm fue aislado mediante cromatografia de afinidad utilizando columnas de Oligo (dT) celulosa (BRL).
Síntesis de ADN copia (ADNc)
El ARN total y ARNm o ARN Poli (A)+ se utilizaron como molde para la síntesis de ADNc usando el kit comercial de SuperScript II RNAse H¯; Grand Island, NY (GIBCO BRL). En el método no radiactivo para cada muestra se utilizaron 500 ng de ARNm y 5 µg de ARN total, 100 ng de hexanucleótidos al azar sintetizados por Operon Techologies, Inc; 500 µM de cada uno de los cuatro nucleótidos trifosfatos (dNTPs), MgCl₂ 2.5 mM y 400 U de la trascriptasa reversa. En la reacción se utilizó solución tampón de la transcripción TR 5X [Tris-HCl 250 mM (pH 8.3); KCl 375 mM; MgCl₂ 15 mM], un volumen final de 40 µl de reacción se alcanzó con agua bidestilada estéril tratada con DEPC. La reacción fue incubada en un termociclador PTC-100 TM (MJ Research, Inc) programado de la siguiente manera: 20°C por 15 minutos; 42°C por 50 minutos; 99°C por 6 minutos y 95°C por 5 minutos. La muestra fue digerida con 4 unidades de ribonucleasa H (GIBCO BRL). Para el método radioactivo la síntesis de ADNC se realizó a partir de ARN total siguiendo las instrucciones del Kit RNAimage TM (GenHunter Corporation). Después de la síntesis del ADNc, se realizó la amplificación de la primera cadena con primer de secuencia al azar. Cada reacción de Reacción en cadena de la polimerasa (RCP) fue llevada a cabo en un volumen de 25 µl, adicionando 5 µl de ADNc obtenidos, con una mezcla de MgCl₂ 1.5 mM, dNTP's 200 µM Taq polimerasa 2-5 U la combinación de diferentes oligonucleotidos de 10 bases (Operon Technologies). La reacción se completó con 1/10 de volumen de buffer RCP 1X [Tris-HCl 200 mM (pH 8.8); KCl 500 mM y Triton 1%] y agua destilada. La reacción se realizó por 45 ciclos, en un termociclador PTC-100TM (MJ Reserch, Inc) empleando el siguiente programa: 94°C 1 minuto, 34°C 1 minuto, 72°C 1 minuto, seguido por un ciclo de 10 minutos a 72°C. Para el método radiactivo la reacción de RCP fue realizada en 20 µl, que contenían 2 µl de ADNc, MgCl₂1.5 mM, dNTP's 2 µM y 0.25 µl de α [32P]dATP, Taq polimerasa 0.33 U y la combinación de decanucleótidos. Se empleó el mismo programa aumentando la temperatura de apareamiento a 38°C. Los productos de RCP fueron separados a través de electroforesis en geles de agarosa (2.0%) y visualizados por tinción con bromuro de etidio. Los fragmentos diferenciales entre los individuos resistentes y susceptibles se aislaron del gel. Para eliminar la agarosa de los fragmentos de ADNc extraídos se utilizó el método de purificación de "USBioclean". La amplificación se llevó a cabo utilizando los mismo cebadores empleados en la síntesis de la doble cadena
Clonación de fragmentos específicos -Transformación
Los fragmentos de interés se clonaron en el vector PCRTMII. La mezcla de ligación se colocó en presencia de células competentes de E. coli de la cepa DH5 α, permitiendo la introducción del plásmido recombinante por choque térmico. Los clones positivos se seleccionaron debido a la coloración blanca en presencia de Isopropil-B-D-Tiogalactosido (IPTG) y 5-Bromo-4-Cloro-3-Indolil-b-D-Galactósido (X-Gal) y la resistencia a ampicilina.
Análisis de los insertos; lisis por calentamiento
Para confirmar el origen de los insertos en las colonias recombinantes se realizó la extracción de los plásmidos presentes en las bacterias por el método de lisis por calentamiento (Sambroock et al. 1989). El tamaño de los insertos se determinó por la digestión del ADN con la enzima de restricción Eco RI (GIBCO- BRL). Los productos de la digestión se analizaron en geles de agarosa al 1.2%.
Algunas características generales de los genotipos de Phaseolus lunatus utilizados en la extracción de ARN total
Días a Emergencia
R, resistente; S susceptible
No ocurrió emergencia del insecto
Transferencia de ARN a membranas de nylon e hibridización de las bandas amplificadas con la membrana-ARN
Mediante esta técnica se unieron covalentemente 50 µg de ARN denaturado a una membrana de nitrocelulosa Hybond N+ (Amersham). La membrana fue prehibridizada a 65°C con una solución de SSC 5X, Denhardt's 5X y SDS 0.1% en agitación constante durante 3 horas. Posteriormente, cada filtro se hibridizó a igual temperatura con un fragmento diferencial reamplificado que se empleó como sonda. Las sondas se marcaron radiactivamente con (32P dATP) utilizando el kit "Multiprime DNA labelling systems" (Amersham) que se basa en la utilización de hexanucleótidos al azar y el fragmento Klenow de ADN polimerasa de E. coli (Feinberg y Volgelstein 1983). Las sondas se purificaron a través de columnas de sephadex G-50 (SIGMA) de 1 cm. Después de 18 horas de hibridación, los filtros se lavaron a 65°C con las siguientes soluciones: SSC 2X y SDS 0.1%, 20 min; SSC 1X y SDS 0.1 %, 20 min; SSC 0.5 X y SDS 0.1% durante 15 min. Las señales de hibridación se visualizaron en un película autorradiográfica (Kodak XL) por exposición a -80° C durante 16 horas (Sambroock et al. 1989).
Resultados y Discusión
Aislamiento del ARN total y purificación del ARNm
El patrón de proteínas totales se comparó antes de realizar la extracción de ARN total, mostrando la homogeneidad de los genotipos resistentes y susceptibles. Por lo cual se realizó la caracterización de los transcritos diferenciales específicos de genotipos resistentes a A. obtectus. Se aisló el ARN total de tres genotipos resistentes al insecto (G25007, G25008 y G25046) y tres susceptibles (G25277, G25259 y G25292). El espectro obtenido de cada material en el rango de 220 a 320 nm mostró baja contaminación con proteínas. La electroforesis en gel de agarosa de las muestras determinó bandas de ARN ribosomal con definición nitida y clara, demostrando la integridad del ARN total. El análisis electroforético del ARN ribosomal aislado mostró 2 bandas correspondiente a los: ARN ribosomales 28S y 18S (Fig. 2A).
El ARN mensajero se aisló a partir del ARN total mediante cromatografía de afinidad. Para la visualización del ARNm se formaron dos grupos de comparación; el grupo de los genotipos resistentes y el grupo de los susceptibles. Los ARNm se visualizaron en gel de agarosa para determinar la presencia de contaminación con ARN ribosomal y ARN de transferencia.
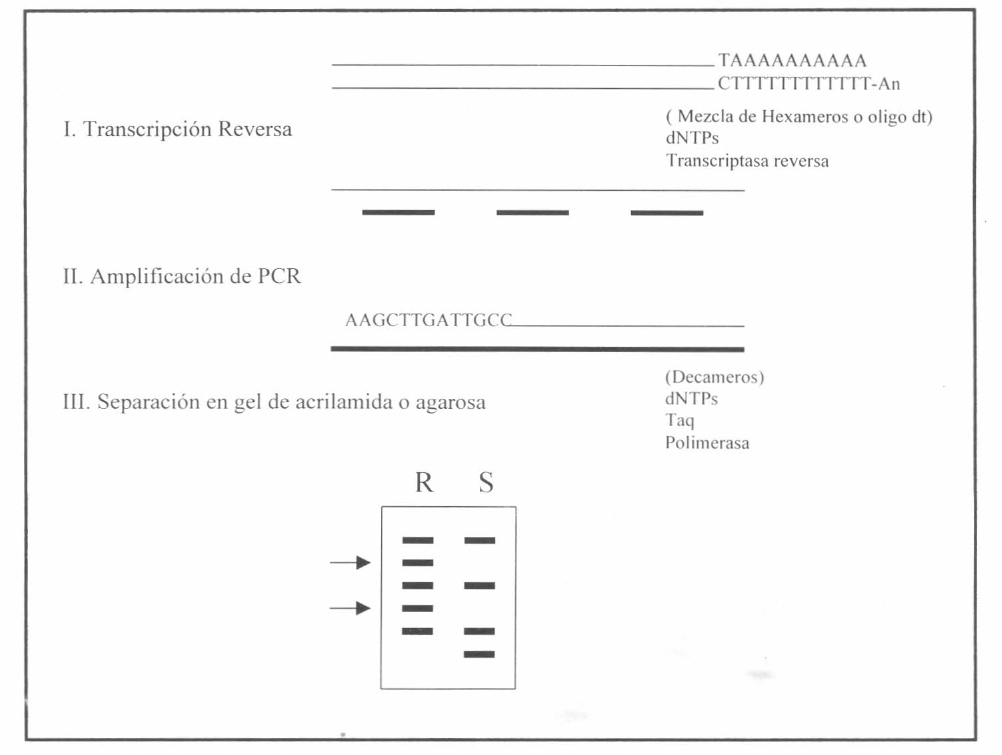
Esquematización del proceso de visualización diferencial del ARNm.
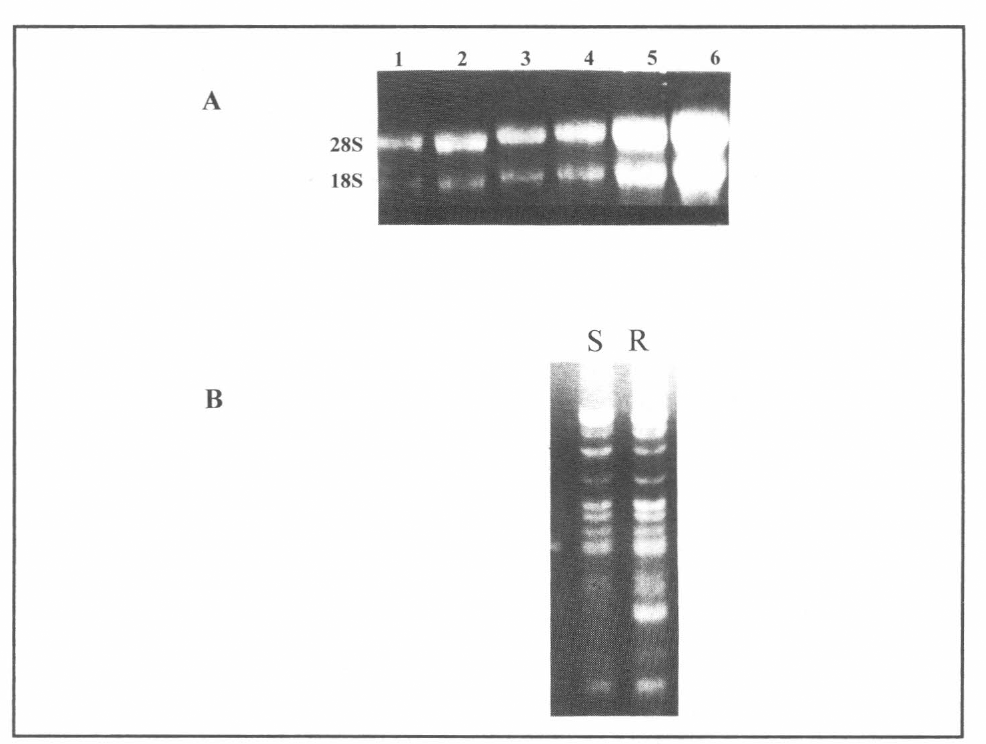
Visualización de los transcritos diferenciales (método no radiactivo)
Investigaciones realizadas por Sokolov y Prockop (1994), al desarrollar la visualización a nivel no radiactivo, sugieren la necesidad de digerir completamente los productos de la transcripción reversa con RNasa H antes de realizar el RCP para obtener fragmentos de alto peso molecular. Los autores, con la metodología desarrollada, han identificado en diferentes tejidos humanos, como corazón, pulmón y cerebro, transcritos hasta de 3000 pares de bases. Teniendo en cuenta este hallazgo, el ARN molde se hidrolizó con la enzima RNasa H antes de la amplificación.
En la amplificación de los ADNC por RCP, utilizando 27 hexanucleótidos, se observaron 7 bandas en promedio en los dos grupos de comparación, con un peso molecular entre 100 y 1500 pares de bases. El tamaño de los transcritos diferenciales en los materiales resistentes, osciló entre 100 a 900 pb. Trabajos anteriores en arroz señalan amplificados entre 200 a 2000 pb a partir de ARN mensajeros obtenido de callos vegetales (Yoshida et al. 1994).
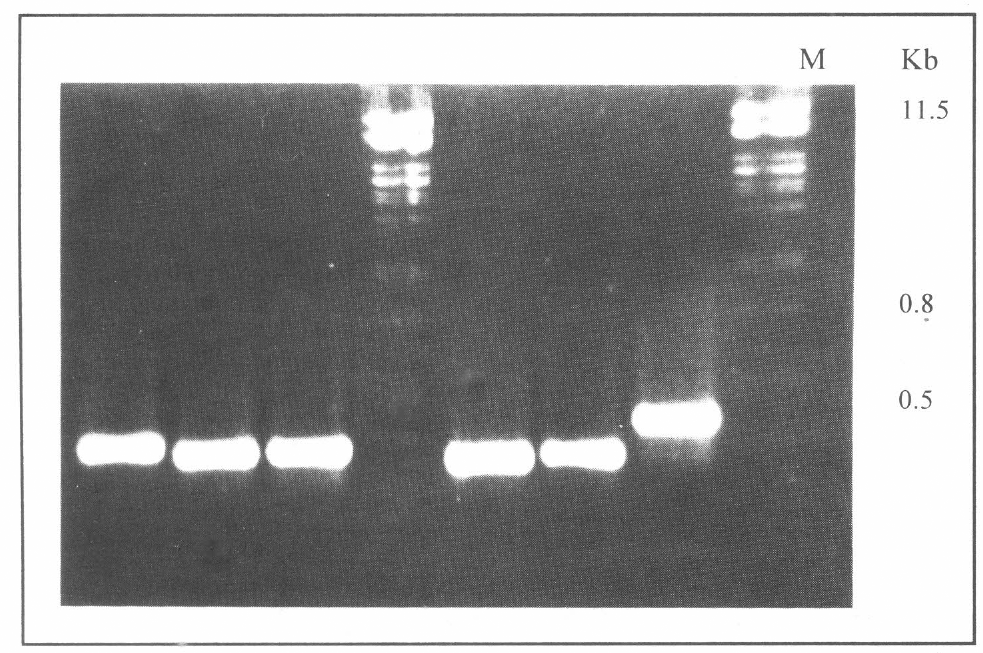
Eletroforesis de la amplificación de las bandas diferenciales aisladas y purificadas de los individuos resistentes. M. Marcador de Peso molecular λ/PstI.
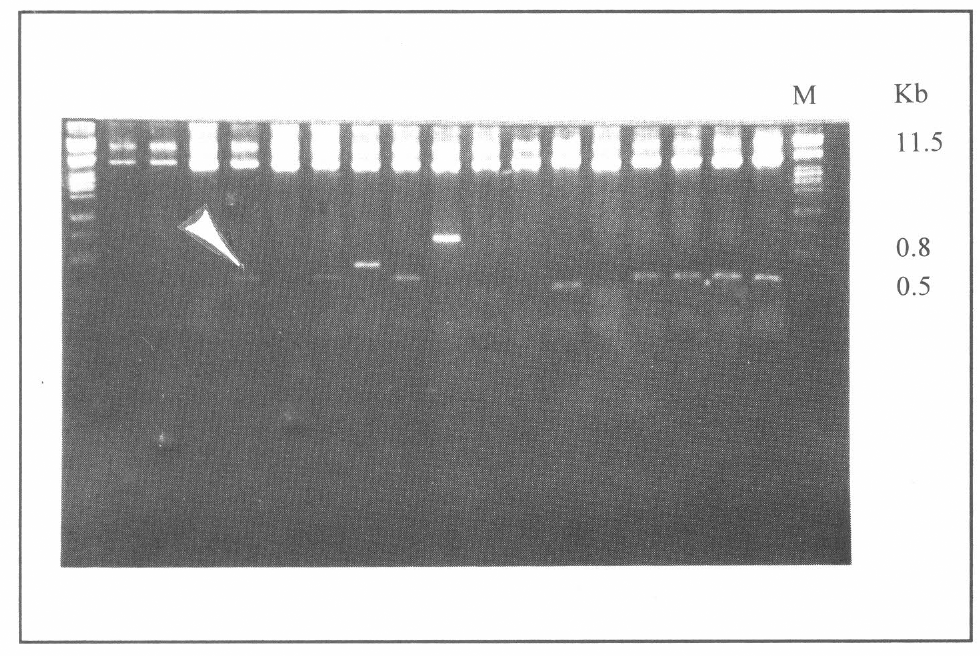
Electroforesis de clones recombinantes digeridos con la enzima de restricción Eco RI. M. Marcador de Peso molecular λ/PstI. La flecha indica los insertos obtenidos.
Al comparar el grupo de genotipos resistentes y susceptibles a A. obtectus se observaron tanto bandas comunes en los dos grupos como bandas especificas o propias del grupo de materiales resistentes al insecto (Fig. 2B). Los transcritos comunes corresponden a mensajeros que codifican proteínas comunes en los dos grupos de estudio, por tratarse de materiales de origen cultivado y de la misma especie, P. lunatus. Una vez aislados y purificados los transcritos diferenciales se amplificaron por RCP y fueron visualizados mediante la electroforesis de los amplificados (Figs. 3 y 4). Para ver la especificidad del transcrito, todas las bandas diferenciales se evaluaron al hibridizarlas con los genotipos resistentes al insecto.
Hibridización de los transcritos diferenciales
Mediante la hibridización por mancha o "dot blot" se han evaluado 59 insertos, de los cuales 4 no muestran hibridización y 38 hibridizaron inespecíficamente con genotipos resistentes al insecto y susceptibles. Solamente 13 insertos mostraron una hibridización más fuerte con los individuos resistentes. La tasa alta de falsos positivos puede explicarse por dos factores: primero, por la inespecificidad de la técnica, errores ocasionados por la temperatura baja utilizada en la alineación de los cebadores al molde de ADNc, y segundo, debido a la variación genética en el grupo de comparación, aunque todos los materiales resistentes son cultivados, y originarios de Brasil. Pueden existir ARNs mensajeros que codifican características que no tienen ningún papel en la resistencia y sólo corresponde a caracteres generales de cada genotipo, como por ejemplo el color de la semilla.
Para descartar los transcritos propios de algunos genotipos resistentes y determinar los transcritos diferenciales, presentes en todos los individuos del grupo de comparación que pueden estar relacionados realmente con la resistencia, se realizó la visualización diferencial individualmente, aplicando el método radiactivo descrito por Liang y Pardee (1992) y adaptado para fríjol por Rocha (1995).
Visualización de los transcritos diferenciales (método radiactivo)
Según las instrucciones del manufacturador esta metodología es más sensible, por lo tanto requiere menor cantidad de muestra y se obtiene una mejor resolución cuando se utiliza ARN total en lugar de ARNm. La síntesis de ADNc generalmente se realiza con cadenas pequeñas de nucelótidos (3'CGTTTTTTTTTTT'5) utilizando dos nucleótidos selectivos y se pueden visualizar entre 50-100 ARN mensajero por carril. En este trabajo se realizó una sencilla modificación a la metodología original, sintetizando el ADNc con hexanucleótidos al azar, como en el método no radiactivo y utilizando los híbridos de ARN- ADNc como cebadores en la primera amplificación por RCP, de esta manera se han obtenido alrededor de 60 bandas en promedio, mayores de 300 pares de bases (Fig. 5).
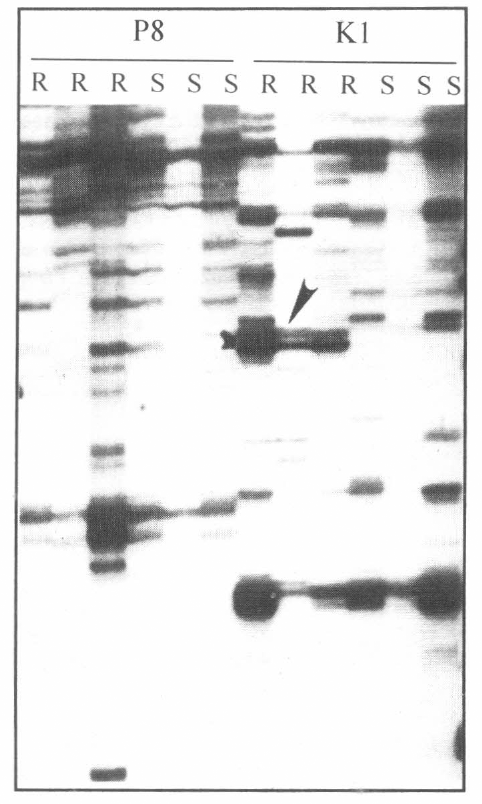
Autorradiografía de la visualización diferencial del ARN total de P. lunatus (R: G25008, G25007 y G25046; S: G25259, G25277 y G25292). La flecha indica la banda diferencial.
Al evaluar 76 decanucleótidos al azar, se han evidenciado 6 bandas diferenciales con tamaños que oscilaron entre 200 y 600 pb. Las bandas purificadas y amplificadas fueron evaluadas con genotipos resistentes y suceptibles mediante "northern blot", en el cual se hibridiza ARN total con las bandas marcadas individualmente. Los ensayos no mostraron bandas específicas o propias de los individuos resistentes. Es posible que el ó los ARNm específicos de la resistencia sean muy escasos, y por consiguiente no detectables mediante la técnica de "northern blot". Debido a esto se debe realizar la hibridización directamente con el ARNm en lugar de ARN total. Las siete bandas diferenciales mencionadas serán secuenciadas con el objetivo de comparar sus secuencias con secuencias de genes de resistencia ya caracterizados.
La reproducibilidad de la técnica se comprobó al encontrar que el patrón de bandas obtenido por cada cebador es reproducible, independiente de la extracción de ARN o de la síntesis de ADNc. No obstante existe una variación en algunas bandas de menor intensidad, también se pueden presentar alteraciones en el patrón electroforético al aumentar o disminuir la concentración de Taq polimerasa, dNTPs, y la cantidad de molde utilizado en la síntesis de ADNc.
Existen registros recientes que han mostrado el potencial de los procedimientos implicados en la transcripción y amplificación de múltiples fragmentos de ADNc representativos de las secuencias codificantes (Goormachtig et al. 1995). No obstante, aunque se han identificado genes diferenciales en mamíferos y plantas, hasta el momento es poca la evidencia de la identificación de genes de resistencia a insectos. El aislamiento y caracterización de genes de resistencia a A. obtectus, sería una contribución importante en el establecimiento de un adecuado programa de mejoramiento genético. En la búsqueda de factores de resistencia a A. obtectus se ha establecido que la resistencia es de tipo antibiótico (Cardona et al. 1989). El efecto antinutritivo puede ser causado por una o varias sustancias aún sin identificar e involucra uno o varios genes. Estudios realizados en CIAT confirman el efecto antibiótico. Resultados promisorios se han obtenido al fraccionar proteínas de genotipos resistentes al insecto (Fory et al. 1996b), razón por lo cual sería muy importante asociar alguna secuencia identificada en este trabajo, con proteínas presentes en la fracción antibiótica o con otras sustancias involucradas en el mecanismo de resistencia a insectos establecidas en el banco de genes.
Vale la pena anotar que realmente para concluir que la o las secuencias identificadas codifican para factores involucrados en la resistencia, la proteína tendría que ser expresada y evaluada en ensayos in vitro con el insecto. Sin embargo, la técnica de visualización diferencial genera en ciertos casos falsos positivos lo que ha conducido a que paralelamente se desarrollen técnicas complementarias para la identificación de genes involucrados en la resistencia a A. obtectus como la hibridización substractiva.
Otras investigaciones encaminadas a esclarecer el factor de resistencia a A. obtectus
Hibridización substractiva
El clonar genes aislados por la técnica de hibridización substractiva es una estrategia ampliamente utilizada en la identificación de genes de resistencia y usualmente involucra una separación de los híbridos formados entre ADNc del genotipo resistente y el ARNm del genotipo susceptible con columnas de hidroxiapatita o avidina-biotina. En este trabajo se usó un método basado en la utilización de un agente químico (2,5 diaziridinil 1-4-benzoquinona) que no permite la separación física del híbrido de ADNC-ARN, evitando de este modo la contaminación y la perdida de ADNc (Hampson et al. 1992).
Después de realizar la extracción de ARN total y purificación del ARNm, se realizó la hibridización subtractiva siguiendo las instruciones del kit de hibridización diferencial de (Amersham) para lo cual se utilizaron 400 ng de genotipos resistente (ADNc) y 10 µg de ARNm proveniente de genotipos susceptibles. El ADNc substraído ha sido digerido con dos enzimas de restricción (Msel y Eco RI) y amplificado utilizando la técnica de AFLPs (Amplificación polimórfica de fragmentos de restricción). En el futuro se espera clonar la subtracción diferencial.
Utilización de oligonucleótidos degenerados
En la identificación y comparación de varios genes de resistencia a enfermedades en diferentes plantas se ha evidenciado la similaridad entre las secuencias de aminoácidos, las cuales muestran regiones conservadas. Utilizando esta característica se han sintetizado cebadores con secuencias degeneradas que corresponden a regiones de ADN que se unen a nucleótidos pertenecientes a ciertas proteínas kinasas involucradas en la resistencia a enfermedades (Yu et al. 1996). Estos cebadores permiten la posible identificación de genes nuevos debido a que muchos genes presentan homología en su secuencia.
En este trabajo se extrajo ADN de los parentales de P. lunatus con diferente expresión de resistencia a A. obtectus utilizados en el cruce G25042 (R) x G25410 (S) siguiendo el método descrito por Dellaporta et al. (1983). Las tres combinaciones de primer utilizadas fueron S1-AS1; S2-AS2 y S2-AS3. Hasta el momento se han obtenido resultados promisorios con la primera combinación en la que se registró polimorfismo y se aisló y purificó un fragmento polimórfico mayor de 1000 pb en el parental resistente. Dicho fragmento se empleará en la evaluación de la progenie, mediante la amplificación por RCP del ADN de los individuos de la cruza.
Recientemente el uso de técnicas de biología molecular han permitido el aislamiento de genes que confieren resistencia a bacterias, hongos, virus y nemátodos (Leister et al. 1996; Ronald 1997). Sin embargo, pocos factores implicados en la resistencia a insectos se han aislado y caracterizado. Uno de ellos ha sido la identificación de una proteína llamada arcelina; algunas variantes de esta proteína están implicadas en la resistencia de Phaseolus vulgaris a Zabrotes subfasciatus, coleóptero también perteneciente a la familia Bruchidae (Osborn et al. 1986; Santino et al. 1991; Hartwee et al. 1991). Los genes que codifican esta proteína han sido analizados y caracterizados (Goossens et al. 1994) y se están usando actualmente en experimentos de transformación (G. Angenon, Comunicación Personal).
Se espera que usando técnicas de biología molecular como las descritas en este articulo, se logren aislar los genes que codifiquen el o los factores que están implicados en la resistencia a A. obtectus en el género Phaseolus.
