Abstract
It was determined that 18 indigenous strains of Bacillus sphaericus (Bs) highly toxic (80-100 %) to third instar larvae of Culex quinquefasciatus had high molecular weight plasmids, and in order to associate the strains toxicity with the presence of these plasmids it was done a treatment with curing agents, like temperature and acridine orange. For the curing with temperature it was cultured the strains at 40-41°C and for acridine orange it was tested differents concentrations that were permisives for bacilia growth (20-100 µg/ml). In order to confirm the curing of the strains that were treated, it was done a plasmid DNA preparation and agarose gel electrophoresis. The toxicity lost of the cured strains was evaluated by biological assays against Culex quinquefasciatus larvae. Of the 18 strains of B sphaericus studied at the beginning 5 were cured with temperature, and in this study 8 were cured with acridine orange and in 3 strains the plasmid remained. The bacilia that lost their plasmid continued been pathogenic for larvae which indicate that the genes involved in toxicity belong to the chromosome. There were found differences among the strains with respect to the resistance to curing agents and in general it was observed great stability of the plasmids.
Introducción
A partir de un proyecto inicial realizado en el Centro de investigaciones Microbiológicas-CIMIC y financiado por Colciencias (Dussan et al. 1995), se seleccionaron 269 cepas de bacilos esporoformadores aisladas de diferentes regiones de Colombia (Llanos Orientales, Costa Atlántica, Zona cafetera, Costa Pacífica y Sabana de Bogotá) y se evaluó la toxicidad en el laboratorio utilizando larvas de tercer instar de Culex quinquefasciatus, Aedes aegypti y Anopheles albimanus, con el fin de agrupar las patógenas y clasificarlas como Bacillus sphaericus (Bs) o Bacillus thuringiensis (Bt).
B sphaericus, de interés en este estudio, es una bacteria gram positiva, forma espora circular-terminal que deforma al bacilo (Holt et al. 1994) y varias cepas pueden ser toxigénicas para larvas de algunas especies de mosquitos transmisores de enfermedades tropicales (Burgues 1982; Davidson et al. 1993; Liu et al. 1993; Lord y Fukuda 1990; Priest 1992).
De las cepas nativas evaluadas anteriormente se determinó que 18 correspondientes a la especie de Bs, presentaban patogenicidad del 80-100% en larvas de tercer ínstar de C. quinquefasciatus y a la vez plásmidos de alto peso molecular. El plásmido es una molécula extracromosomal de ADN de doble cadena con replicación autónoma, el cual se puede encontrar en diferentes géneros y especies de bacterias y les confieren características específicas, tales como, resistencia a antibióticos, toxicidad, producción de enzimas, resistencia a infección de virus, etc (Norris 1988; Moineau et al. 1995; Bauma y Lenski 1988). Debido a que las cepas de Bs presentaron una mayor estabilidad plasmídica que las cepas de Bt, se decidió probar otro agente, como el Naranja de Acridina, el cual se ha utilizado para curaje de otras especies de bacilos (Hara et al. 1982) y determinar si la presencia del ADN plasmídico está involucrada de alguna manera con la patogenicidad de estas cepas nativas. En varios registros se ha estudiado, a nivel molecular, el mecanismo de la toxicidad y los genes involucrados en ésta para pocas cepas (Bernhard 1979; Davidson et al. 1993; McDonald y Burke 1984; Porter et al. 1993; Sattabongkot y Pantuwatana 1990), pero no se ha evaluado si en la patogenicidad está involucrado el plásmido como ha sido señalado para cepas con cristal paraesporal de Bt. (Miteva et al 1986; Gonzáles et al 1981; Heierson et al. 1987; Mettus y Macaluso 1990; Ward y Ellar 1984).
Materiales y Métodos
Para determinar la asociación del plásmido y la patogenicidad es necesario extraer el plásmido de la bacteria, método conocido como curaje, y a la vez evaluar el porcentaje de mortalidad que causa esta bacteria sin ADN plasmídico en larvas de tercer ínstar, en este caso, de C. quinquefasciatus.
Para ello existen diferentes tratamientos en los cuales se utilizan agentes curantes físicos, biológicos y químicos (Norris 1988; Hara et al. 1982) y en términos generales lo que hacen estos agentes curantes es alterar la replicación del ADN.
Después de esta incubación se titulaba cada medio para conocer el número de células por mililitro y de esta manera calcular el porcentaje de sobrevivencia en el medio caldo nutritivo con NΑ.
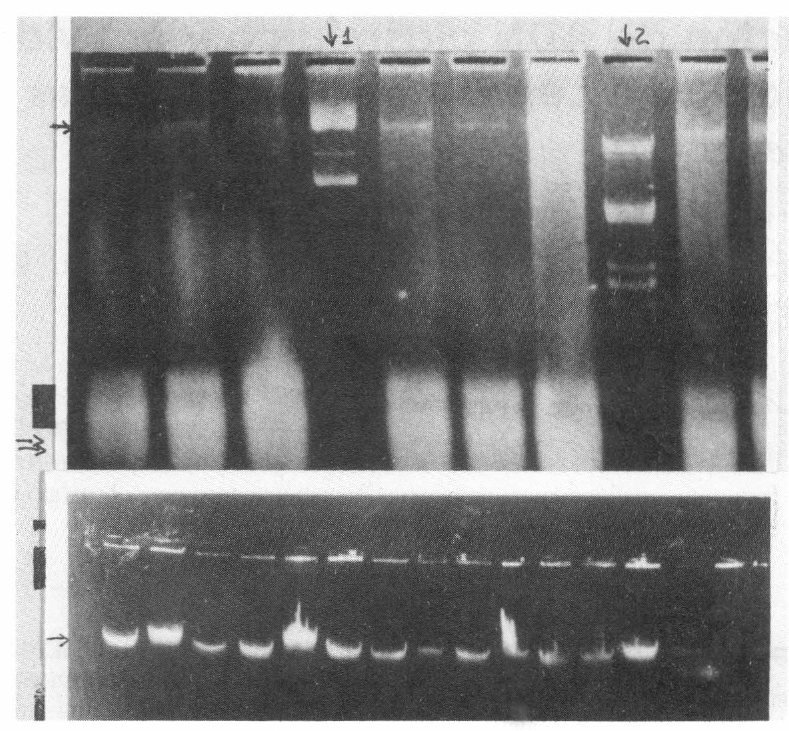
Electroforesis de ADN plasmídico de las cepas de B. sphaericus. → Banda de ADN plasmídico ↓Patrón de peso molecular: 1- Col El 2- ADN Lambda con Hind III → RNA
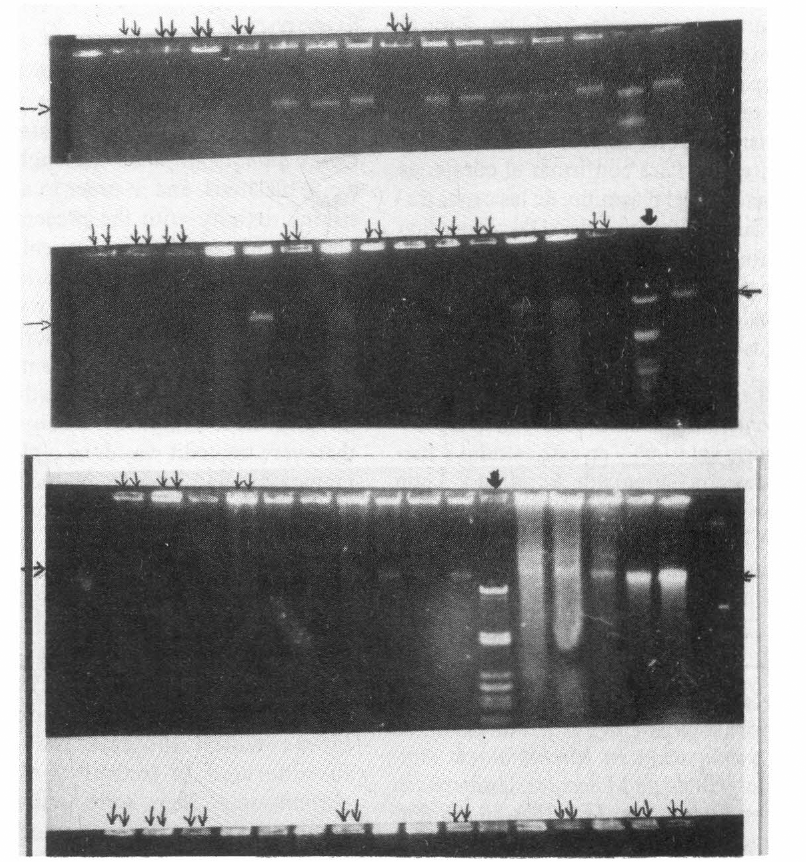
Electroforesis de ADN plasmídico de las cepas tratadas con Naranja de Acridina. ↓Patrón de peso molecular: ADN Lambda con Hind III ↓↓Cepas curadas con tratamiento de naranja de acridina → ← Banda plasmídica
Resultados
De las 18 cepas seleccionadas para el estudio, inicialmente se obtuvieron cinco cepas curadas con temperatura de las cuales tres revirtieron, es decir las generaciones bacterianas adquirieron nuevamente el plásmido, y en una cepa se presentó también la pérdida de la toxicidad.
Larvas muertas de C. quinquefasciatus (tercer ínstar).
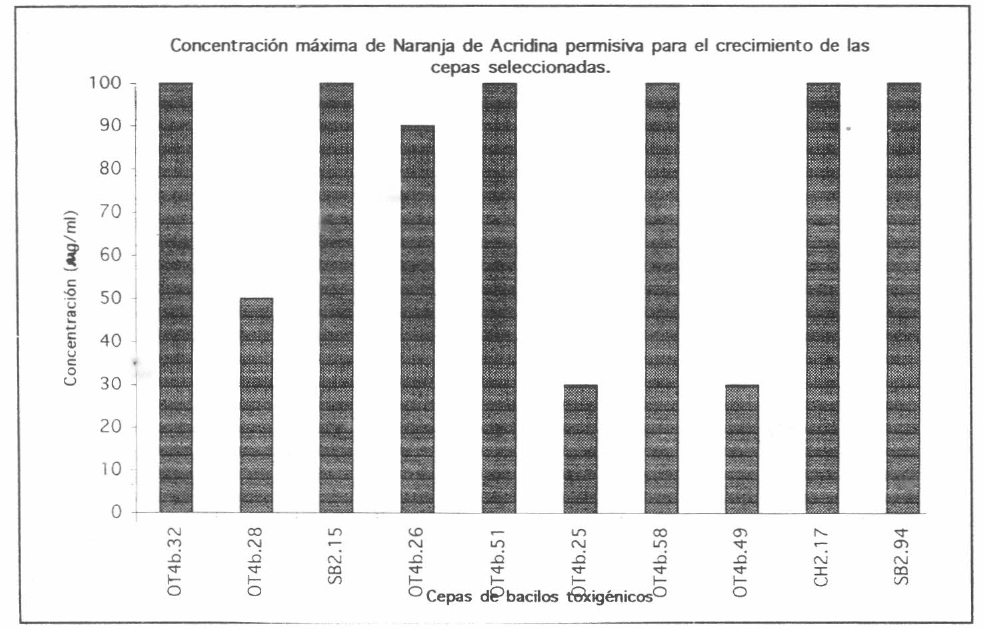
Concentración máxima de Naranja de Acridina permisiva para el crecimiento de las cepas seleccionadas.
Clasificación de las cepas sometidas a tratamiento de curaje.
Se observaron diferencias en cuanto a la concentración máxima de Naranja de Acridina soportada para crecimiento (Fig. 4). La concentración mínima de NA fue de 30 µg/ml y la máxima soportada, por casi la mayoría, fue de 100 µg/ml. En este estudio se presentaron 8 cepas curadas con NA, pero continuaron siendo patógenas para larvas de Culex quinquefasciatus de tercer instar igual que las cepas originales sin tratamiento con este agente; tres cepas no se lograron curar por ninguno de los dos métodos y continuaron siendo toxigénicas.
Dos cepas mostraron un comportamiento no esperado como lo fue el curaje espontáneo.
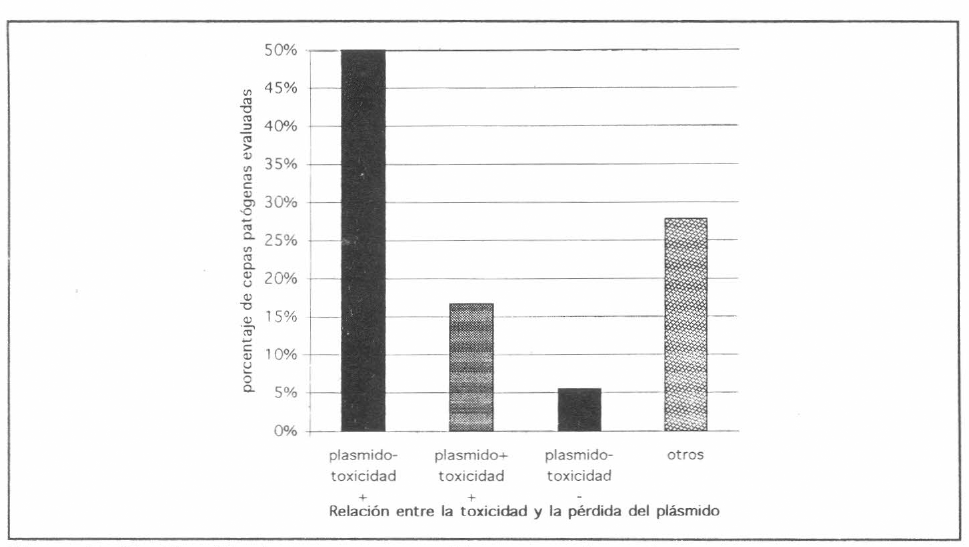
Reuniendo los datos inicialmente obtenidos para curaje con temperatura con los de curaje con Naranja de Acridina (Fig. 5), se afirma que:
El 50% de las 18 cepas después del tratamiento de curaje no presentaron plásmido, es decir fueron curadas, pero continuaron siendo patógenas para larvas de tercer ínstar de C. quinquefasciatus.
El 5,5% no presentaron plásmido ni toxicidad, porcentaje que corresponde a una cepa de Bs curada por temperatura.
El 16,7% de las cepas estudiadas no fueron curadas y el 27,8% presentaron un comportamiento no esperado, como lo fue el curaje espontáneo o la reversión del curaje.
Discusión
El curaje con pases sucesivos a alta temperatura se realizó con el fin de acelerar el crecimiento bacteriano y por ende la replicación cromosomal, por lo tanto la replicación del ADN plasmídico o plásmido no se da con la misma frecuencia que la del cromosoma y por ello no se alcanza a duplicar cuando ya hay división celular, de esta forma el plásmido termina por perderse en las generaciones siguientes (células hijas).
Las cepas no curadas con temperatura se sometieron a otro tipo de tratamiento más drástico, utilizando Naranja de Acridina, este compuesto presenta gran afinidad por el ADN y al unirse a él evita su replicación; por esta razón es importante escoger previamente la concentración adecuada de este agente que en una óptima cantidad inhiba la replicación del plásmido y permita la replicación del ADN cromosomal, así sea en un menor grado.
A pesar de haberse aislado bacilos esporoformadores de la misma especie (B. sphaericus), se observaron diferencias en cuanto a resistencia de cada cepa a las concentraciones de Naranja de Acridina utilizadas. La mayoría de las cepas alcanzaron a sobrevivir en 100 µg/ml de Naranja de Acridina, sin embargo dos cepas (OT4b25 y OT4b49) crecieron hasta 30 µg/ml. Una vez realizada la ronda de curaje con Naranja de Acridina se realizaron extracciones del ADN plasmídico con el fin de comprobar la pérdida del plásmido (Fig. 2) y de esta manera evaluar la asociación que puede tener con la patogenicidad de la bacteria hacia las larvas. Para este método se hace necesario estandarizar un protocolo de extracción de ADN plasmídico rápido que permita probar un mayor número de colonias.
De acuerdo con los resultados, se observa gran estabilidad de los plásmidos, es decir que la bacteria no los pierde fácilmente y esto se corrobora con los resultados obtenidos para el curaje con temperatura, tratamiento en el cual la mayoría de cepas de Bs no fueron curadas. Esta estabilidad del plásmido en la bacteria hace suponer que podría ser esencial para la sobrevivencia de las cepas que no fueron curadas y de las cuales se curaron posteriormente con Naranja de Acridina, por tanto ellas, por medio de algún mecanismo molecular, evitan perderlo.
De las cepas curadas con los dos tratamientos sólo una presentó pérdida de la toxicidad indicando que el plásmido posiblemente está involucrado en la patogenicidad de esta cepas. En la mayoría de las cepas evaluadas, que fueron curadas, se continuó presentando la patogenicidad hacia larvas de C. quinquefasciatus, lo que significa que la expresión de los genes de la toxicidad es cromosomal o por lo menos los plásmidos aislados no están comprometidos con ésta.
Este estudio con cepas patogénicas de bacilos Bs nativos se convierte en la base de posteriores investigaciones en esta línea de control biológico, para la caracterización tanto a nivel fisiológico como genético-molecular, además de abrir la posibilidad de la búsqueda de marcadores genéticos para diferenciar cepas toxigénicas para larvas de las que no lo son y con una información más integrada evaluar el potencial de estas cepas nativas para el control biológico a nivel piloto en campo.
La permanencia del plásmido en estas cepas debe cumplir un papel importante en su metabolismo o ciclo de vida, por lo que es necesario conocer más a fondo estos plásmidos para estudios de clonaje y expresión, puesto que son estables y resistentes a condiciones adversas asegurando su mantenimiento dentro de la bacteria en diferentes hábitats.
Conclusiones
La mayoría de las cepas fueron resistentes a condiciones adversas (alta temperatura, Naranja de Acridina).
Existen diferencias a la resistencia a tratamientos de curaje entre las cepas de B. sphaericus.
No se observa un patrón general en cuanto a la asociación de la presencia del plásmido y la toxicidad de las cepas, puesto que sólo en una cepa se encontró esta relación.
Footnotes
Agradecimientos
Los autores agradecen a Colciencias por la financiación de la investigación y al Instituto Nacional de Salud (INS), en especial al Dr. Victor Olano, Unidad de Entomología, por la asesoría y el suministro de larvas.
