Abstract
The aim of this paper is to compare the cost for managing severe haematological toxicities (HTs: anaemia, neutropenia, thrombocytopenia) in patients with pretreated, relapsed BRCA-mutant positive (+) ovarian cancer (OC) receiving second-line therapy with olaparib or niraparib. As reported for treatment groups of randomized controlled trials, the incidence of anaemia, neutropenia and thrombocytopenia for olaparib (niraparib) was 0.071, 0.432 and 0.062 (0.253, 0.196 and 0.338), respectively. A one-year decision-tree cost-minimization analysis and a three-year budget impact analysis (BIA) were performed from the viewpoint of the Italian National Health Service (INHS). Health care resources funded by the INHS were identified and quantified based on the literature and expert opinion; they were costed via published sources and expressed in 2018 euro (€) amounts on a per-patient basis. One-way sensitivity analysis (OWSA) and scenario analysis tested the robustness of the base case findings. Our results show that the costs for managing anaemia, neutropenia and thrombocytopenia with olaparib (niraparib) are €440.63, €1032.76 and €171.01 (€1568.82, €468.90 and €936.06), respectively. The overall cost for HT management reaches €1644.41 and €2973.78 for olaparib and niraparib, respectively. Overall savings in favour of olaparib is €1329.37. BIA shows that olaparib can save the INHS €2.322m over a three-year timespan. Sensitivity analyses confirm the robustness of the baseline findings. Despite some limitations in our study, the results of the cost-minimization analysis show that olaparib is a safe and cost-saving health care programme for the INHS for the management of HTs in patients receiving second-line therapy for BRCA+ OC.
Introduzione
In Italia, l’incidenza del carcinoma ovarico (CO) è pari a circa 5.200 nuovi casi/anno. 1 Una percentuale compresa tra 80% ed il 90% dei casi di CO si presenta in pazienti di età compresa tra 20 e 65 anni, 2 per le quali la sopravvivenza attesa a 5 e 10 anni dalla diagnosi sarà pari, rispettivamente, al 39% ed al 31%. 1 I CO si suddividono in neoplasie di tipo I e II. 2 Le seconde, tra le quali si annovera il CO sieroso di alto grado, rappresentano circa il 70%-75% della totalità dei CO diagnosticati,2,3 sono caratterizzate da una marcata aggressività e spesso giungono all’osservazione del clinico in stato già avanzato. 2
Mentre nella popolazione generale femminile il rischio di sviluppare un CO nel corso della propria vita è pari all’1,8%, 2 tale percentuale aumenta dal 20% al 60% in presenza di mutazione nei geni BRCA 1 e 2, 2 diagnosticata mediante prelievo ematico (test germinale) o diagnosi del tessuto neoplastico (test somatico). 4 Poli ADP-ribosio polimerasi (PARP) identifica una famiglia di proteine attive deputate, tra l’altro, alla riparazione del DNA in seguito a danni a singolo filamento (single-strand breaks) e alla apoptosi cellulare. 5 L’inibizione di PARP e del suo meccanismo di riparazione provoca la persistenza di danni a singolo filamento portando alla formazione di danni a doppio filamento, riparati dal sistema di ricombinazione omologa che viene guidato da BRCA 1 e 2. Tuttavia, in cellule portanti mutazione BRCA, BRCA 1 e 2 non sono in grado di riparare il danno a doppio filamento causando la morte cellulare per accumulo di mutazioni. 6
Olaparib (Lynparza®; AstraZeneca, Londra, Regno Unito) è stato il primo PARP-inibitore (PARPi) a ottenere negli Stati Uniti d’America (USA) dalla Food and Drug Administration (FDA) l’indicazione per CO avanzato pretrattato (⩾3 pregressi protocolli chemioterapici) con mutazione BRCA 7 e, più recentemente, anche per il trattamento del carcinoma della mammella localmente avanzato o metastatico human epidermal growth factor receptor 2-negativo nelle pazienti con mutazione BRCA. 8
Niraparib (Zejula®; Tesaro, Waltham, MA, USA) è stato recentemente approvato per la terapia di mantenimento di pazienti adulte con CO epiteliale ricorrente, carcinoma delle tube di Falloppio o carcinoma peritoneale primario che abbiano ottenuto risposta completa o parziale dopo chemioterapia a base di platino. 9
Per quanto attiene al profilo di tollerabilità, una caratteristica comune ai diversi PARPi è la frequenza di tossicità ematopoietiche (anemia, neutropenia, trombocitopenia), variabili in monoterapia o in associazione con chemioterapia, l’incidenza delle quali si qualifica, inoltre, per un’apprezzabile variabilità tra le diverse esperienze di ricerca.6,10 Tra le principali conseguenze cliniche delle tossicità ematopoietiche da PARPi, si annoverano la riduzione della posologia 11 e la dilazione delle successive somministrazioni della terapia,12,13 con possibili riflessi sulla gestione della neoplasia sottostante e, dunque, sulla sopravvivenza della paziente.
Sotto il profilo economico, due recenti esperienze di ricerca statunitensi12,14, hanno sottolineato che i costi unitari di gestione delle tossicità ematopoietiche da PARPi (espressi in US$ a valori 2017) variano tra US$5.737 (trombocitopenia) e US$13.633 (anemia), pari, rispettivamente, a euro (€)5.052,84 e €12.007,22, (tasso di cambio €/US$=1,1354, non aggiustato il tasso d’inflazione USA 2017-2018). 15
Obiettivo
In assenza di pregressi contributi di ricerca relativi al nostro Paese, obiettivo del presente manoscritto è la descrizione della metodologia e dei risultati relativi al confronto tra le risorse sanitarie consumate per la gestione delle tossicità ematopoietiche, quali anemia, neutropenia e trombocitopenia 6 di grado severo (>3 secondo la vigente classificazione), 16 quando si impiegano olaparib o niraparib nella terapia di seconda linea del CO recidivante con mutazione BRCA.
Materiali e metodi
Tipologia della valutazione economica effettuata
In quanto addendi di costo di trattamenti appartenenti alla medesima categoria terapeutica, caratterizzati da efficacia sovrapponibile sulla salute delle pazienti, 17 i costi delle tossicità ematopoietiche oggetto di indagine sono stati confrontati mediante analisi di minimizzazione dei costi,18,19 condotta secondo la prospettiva del Servizio Sanitario Nazionale (SSN).18,19
L’analisi di minimizzazione dei costi è stata supportata da un modello del tipo albero decisionale,19,20 caratterizzato da un singolo ciclo di durata annuale (Figure MSI & MSII). Tale intervallo temporale è conservativo rispetto alla sopravvivenza libera da progressione di malattia (progression-free survival, PFS) mediana riportata in alcuni degli studi clinici randomizzati e controllati (randomized controlled trials, RCTs) considerati nella presente ricerca.21,22
Posta la manifestazione di una delle tossicità ematopoietiche oggetto di indagine, l’albero decisionale, popolato da una serie di parametri separatamente dettagliati (Tabelle 1–3), considera due stati di salute esaustivi e mutuamente esclusivi:18,20,23 sopravvivenza (tale stato di salute rappresenta la condizione della paziente all’ingresso nel modello) e mortalità età-specifica per paziente affetta da CO.24,25
Parametri per popolazione albero decisionale – I.
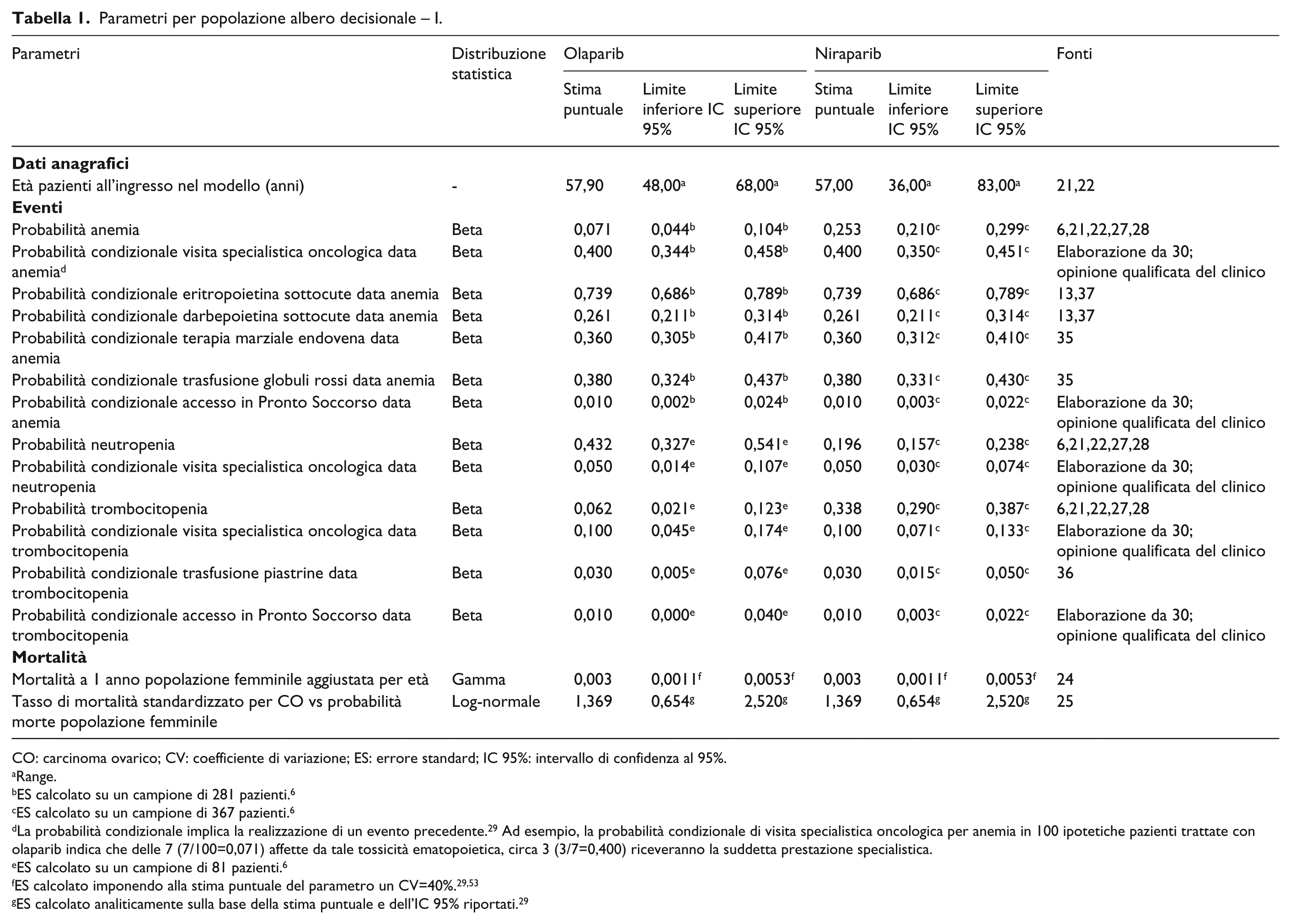
CO: carcinoma ovarico; CV: coefficiente di variazione; ES: errore standard; IC 95%: intervallo di confidenza al 95%.
Range.
ES calcolato su un campione di 281 pazienti. 6
ES calcolato su un campione di 367 pazienti. 6
La probabilità condizionale implica la realizzazione di un evento precedente. 29 Ad esempio, la probabilità condizionale di visita specialistica oncologica per anemia in 100 ipotetiche pazienti trattate con olaparib indica che delle 7 (7/100=0,071) affette da tale tossicità ematopoietica, circa 3 (3/7=0,400) riceveranno la suddetta prestazione specialistica.
ES calcolato su un campione di 81 pazienti. 6
ES calcolato analiticamente sulla base della stima puntuale e dell’IC 95% riportati. 29
Parametri per popolazione albero decisionale – II.
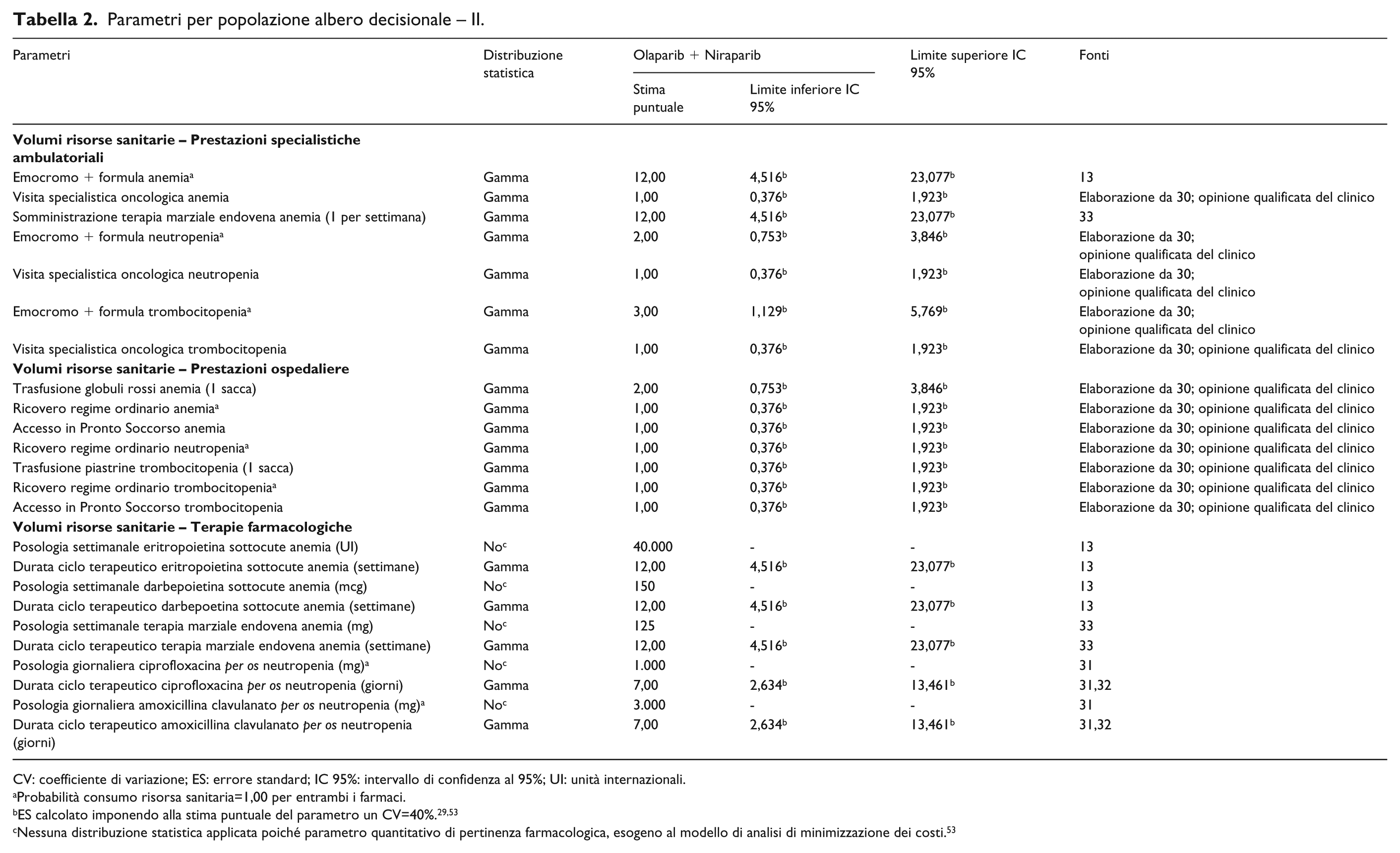
CV: coefficiente di variazione; ES: errore standard; IC 95%: intervallo di confidenza al 95%; UI: unità internazionali.
Probabilità consumo risorsa sanitaria=1,00 per entrambi i farmaci.
Nessuna distribuzione statistica applicata poiché parametro quantitativo di pertinenza farmacologica, esogeno al modello di analisi di minimizzazione dei costi. 53
Parametri per popolazione albero decisionale – III.
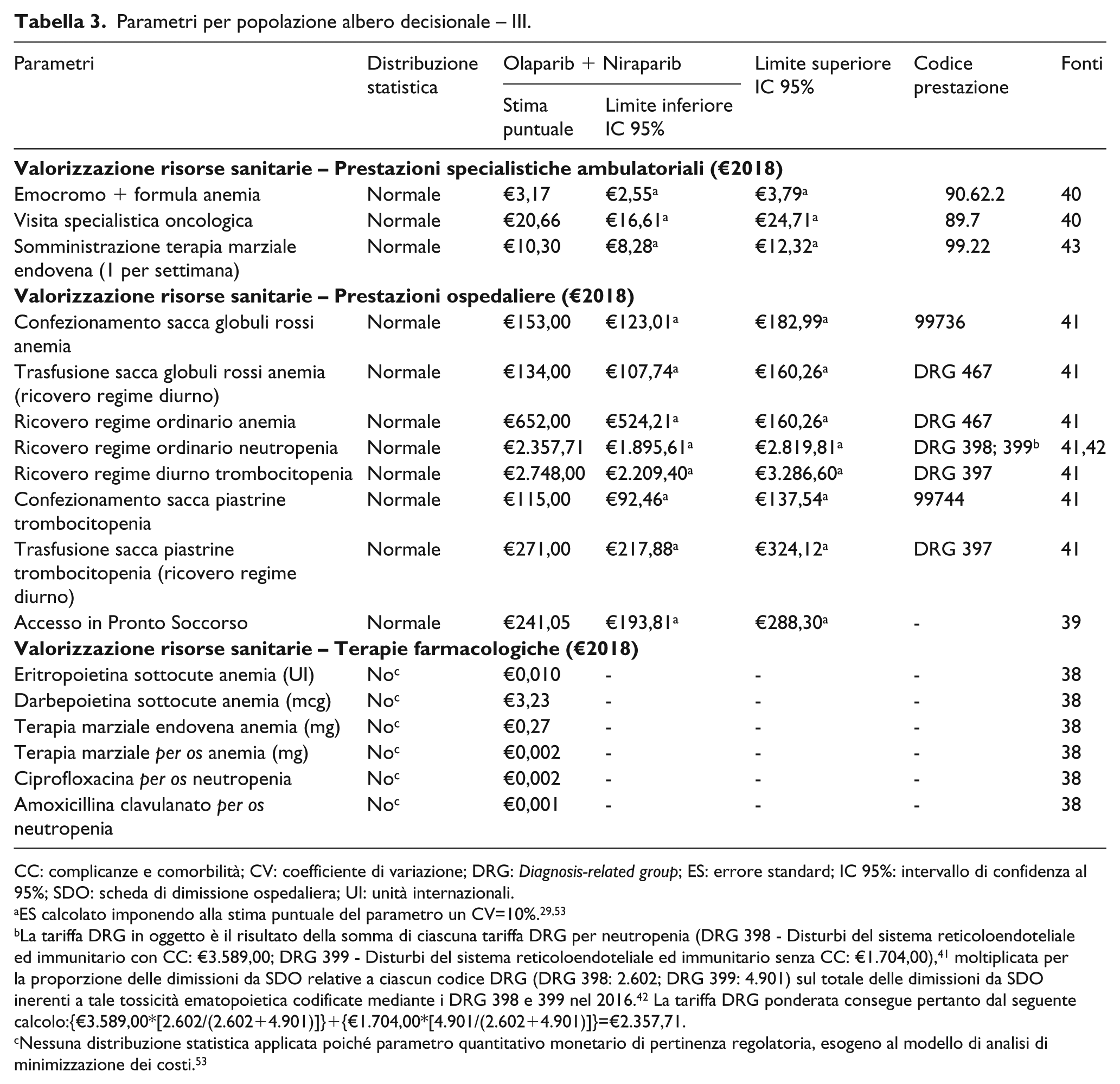
CC: complicanze e comorbilità; CV: coefficiente di variazione; DRG: Diagnosis-related group; ES: errore standard; IC 95%: intervallo di confidenza al 95%; SDO: scheda di dimissione ospedaliera; UI: unità internazionali.
La tariffa DRG in oggetto è il risultato della somma di ciascuna tariffa DRG per neutropenia (DRG 398 - Disturbi del sistema reticoloendoteliale ed immunitario con CC: €3.589,00; DRG 399 - Disturbi del sistema reticoloendoteliale ed immunitario senza CC: €1.704,00), 41 moltiplicata per la proporzione delle dimissioni da SDO relative a ciascun codice DRG (DRG 398: 2.602; DRG 399: 4.901) sul totale delle dimissioni da SDO inerenti a tale tossicità ematopoietica codificate mediante i DRG 398 e 399 nel 2016. 42 La tariffa DRG ponderata consegue pertanto dal seguente calcolo:{€3.589,00*[2.602/(2.602+4.901)]}+{€1.704,00*[4.901/(2.602+4.901)]}=€2.357,71.
Nessuna distribuzione statistica applicata poiché parametro quantitativo monetario di pertinenza regolatoria, esogeno al modello di analisi di minimizzazione dei costi. 53
Non è stata invece indagata l’evenienza della contemporanea presenza di due o più tipologie di tossicità ematopoietiche nella medesima paziente, ipotesi che avrebbe potuto generare economie di scopo 26 nell’impiego delle risorse sanitarie necessarie alla loro gestione contestuale.
Nel calcolo dei costi si è applicata l’half-cycle correction,20,23 mediante la quale si ipotizza che il decesso della paziente avvenga a metà del ciclo di transizione (cioè a 6 mesi, nel caso in questione), anziché, alternativamente, all’inizio o al termine del medesimo, con riflessi sul calcolo del costo di gestione delle tossicità ematopoietiche totalizzato da olaparib e niraparib.
Il modello di analisi di minimizzazione dei costi è stato sviluppato su fogli di calcolo Microsoft® Excel® per Windows® 2010 (Microsoft Corporation, Redmond, WA, USA).
Modalità raccolta dati
Ad eccezione di alcune ipotesi di ricerca, i dati descritti ai paragrafi successivi sono stati ottenuti da fonti di letteratura, selezionate in collaborazione con il clinico co-autore del presente manoscritto. L’opinione qualificata del clinico ha inoltre consentito di confermare la plausibilità, con riferimento alla normale pratica clinica, della probabilità di utilizzo e del volume delle risorse sanitarie necessarie alla gestione degli eventi avversi di pertinenza ematologica considerati.
La collaborazione con il clinico si è articolata in una serie di quattro interviste de visu avvenute nei mesi di Agosto-Settembre 2018.
Incidenza delle tossicità ematopoietiche
Da una recente meta-analisi realizzata su 12 RCTs condotti su 2.479 pazienti affetti da diverse neoplasie (CO recidivante con mutazione BRCA [5 RCTs]; carcinoma polmonare non a piccole cellule (non small-cell lung cancer, NSCLC) [2 RCTs]; carcinoma della mammella [2 RCTs]; melanoma [1 RCT]; tumore gastrico metastatico [1 RCT]; carcinoma polmonare a piccole cellule [1 RCT] sottoposti a terapia con PARPi, 6 è stata identificata l’incidenza delle tossicità ematopoietiche sopra citate per olaparib21,27,28 e niraparib 22 con esclusivo riferimento al CO pretrattato recidivato con mutazione BRCA.
Per olaparib, le incidenze degli eventi avversi ematologici sono state ricavate da tre RCTs per quanto riguarda l’anemia21,27,28 e da un unico RCT per quanto concerne neutropenia e trombocitopenia (Tabella 1). 21
Le probabilità di anemia, che differivano nei tre RCTs, risultavano pari a 0,086 (7/81 pazienti) assumendo olaparib 200 mg bid in combinazione con chemioterapia (docetaxel + carboplatino) verso chemioterapia, 21 0,094 (6/64 pazienti) a seguito di somministrazione di olaparib 200 o 400 mg in monoterapia due volte al giorno (bid) verso doxorubicina pegilata liposomiale 27 e 0,051 (7/136 pazienti) con olaparib 400 mg in monoterapia bid verso placebo. 28
Il valore medio della probabilità di anemia nelle pazienti trattate con olaparib (0,071) è stato calcolato ponderando le stime puntuali sopra indicate per il numero di pazienti avviate a olaparib in ciascuna delle tre fonti considerate, diviso per la somma di tali dimensioni campionarie (81/281, 64/281 e 136/281, rispettivamente) (Tabella 1).
Sempre per olaparib, l’incidenza di neutropenia e trombocitopenia risultavano pari a 0,432 (o 35/81 pazienti) e 0,062 (o 5/81 pazienti), rispettivamente 21 (Tabella 1).
Con riferimento a niraparib, l’incidenza delle tre tossicità ematopoietiche (anemia: 0,253 o 93/367 pazienti; neutropenia: 0,196 o 72/367 pazienti; trombocitopenia: 0,338 o 124/367 pazienti) era riportata nel medesimo RCT, che prevedeva, nel confronto con placebo, la somministrazione, in monoterapia di mantenimento, della posologia di principio attivo per la quale esistono evidenze di efficacia, pari a 300 mg una volta al giorno. 22
Identificazione e quantificazione delle risorse
A motivo della prospettiva adottata nel modello di analisi di minimizzazione dei costi, sono state considerate esclusivamente le risorse di pertinenza del settore sanitario 19 finanziate dal SSN, consumate per la gestione delle tossicità ematopoietiche, a proposito delle quali sono state definite, unitamente a identità e volume, le probabilità condizionali 29 di utilizzo (Tabelle 1 e 2).
Le risorse sanitarie comprendono accertamenti laboratoristici ambulatoriali (limitati ad emocromo + formula, nell’ipotesi che ulteriori parametri ematici e bioumorali siano invece monitorati in regime di ricovero ordinario); 30 farmaci a somministrazione sottocutanea per gestione in contesto extraospedaliero di anemia (eritropoietina; darbepoietina) 13 e neutropenia (amoxicilina/clavulanato e ciprofloxacina per os),31,32 farmaci a somministrazione endovenosa in regime ambulatoriale per anemia (esclusivamente per terapia marziale); 33 visite specialistiche oncologiche; 30 confezionamento sacche di emazie (anemia) e di piastrine (trombocitopenia) e relativa trasfusione in regime di ricovero diurno;34–36 ospedalizzazione in regime ordinario (anemia, neutropenia e trombocitopenia); 30 accessi in Pronto Soccorso (anemia e trombocitopenia) 30 (Tabelle 1 e 2).
La probabilità di consumo di eritropoietina o darbepoietina, prescritte quali alternative alle totalità delle pazienti con anemia, 13 è stata determinata costruendo un rapporto avente al denominatore la somma delle più recenti defined daily dose (DDD) per 1.000 abitanti di epoetina alfa (1,7) e darbepoietina (0,6) ed al numeratore la DDD per 1.000 abitanti della prima. 37 Applicando tale procedimento, si è stimato che la probabilità di prescrizione di epoetina alfa fosse pari a 0,739 (1,7/2,3), ricavando, quale complemento all’unità, la probabilità di prescrizione per darbepoietina, pari a 0,261 (cioè: 1-0,739).
Poiché per la totalità degli studi considerati21,22,27,28 non risultava una chiara distinzione tra incidenza di neutropenia febbrile e non febbrile, si è considerata quest’ultima, ipotizzando la profilassi antibiotica verso il rischio di evoluzione febbrile.31,32
Ancora con riferimento alla neutropenia, non sono stati considerati i fattori di crescita mieloide, poiché né indicati in pazienti con neutropenia non febbrile, 13 né raccomandati in associazione ad antibioticoterapia.13,32
Per quanto concerne l’ospedalizzazione, si è assunto che il ricovero in regime ordinario fosse finalizzato, alternativamente, alla valutazione polispecialistica volta alla diagnosi differenziale delle possibili cause sottostanti a ciascuna tossicità ematopoietica conseguente alle terapie oncologiche, o all’effettuazione di idonei approfondimenti laboratoristici o strumentali, nei casi in cui l’attivazione delle restanti risorse sanitarie non risultasse sufficiente alla risoluzione della problematica clinica. In particolare, all’interno dell’episodio di ricovero ordinario, è stata ipotizzata l’esecuzione di almeno una delle seguenti procedure: esofagogastroduodenoscopia e colonscopia (anemia); somministrazione di ciclo di terapia antibiotica a somministrazione esclusivamente ospedaliera (es.: vancomicina endovena) 32 in aggiunta a terapia antifungina e antivirale 32 (neutropenia); ecografia addome completo e biopsia osteomidollare (trombocitopenia).
Valorizzazione delle risorse
I costi di pertinenza del settore sanitario sostenuti dal SSN includono la totalità delle risorse sanitarie consumate per la gestione delle tossicità ematopoietiche esaminate.
I farmaci sono stati valorizzati mediante il prezzo al pubblico, 38 mentre le restanti prestazioni sanitarie, erogate in ambito ambulatoriale od ospedaliero (regime diurno ed ordinario; emergenza ed urgenza) sono state monetizzate impiegando i riferimenti tariffari più recenti di libera consultazione39–43 (Tabella 3). Tutte le voci di costo considerate, calcolate per paziente, sono espresse in € a valori 2018.
Poiché il confronto tra olaparib e niraparib non eccede l’anno, coerentemente a quanto stabilito da linee-guida internazionali e nazionali sulla valutazione economica dei programmi sanitari,18,19,44 i costi unitari di gestione delle tossicità ematopoietiche non sono stati oggetto di attualizzazione.
Determinazione di impatto budgetario
La determinazione di impatto budgetario45,46 sulle disponibilità economico-finanziarie del SSN di durata triennale (2018-2020), conseguente alla prescrizione di olaparib invece di niraparib, si è focalizzata sulle pazienti affette da CO pretrattato recidivato BRCA+ diagnosticate in Italia, per le quali sussiste indicazione al trattamento con entrambi i PARPi comparati.7,9,47,48
Pertanto, le pazienti eleggibili a olaparib sono state stimate isolando, dai casi di CO incidenti annui,2,49 la tipologia di CO sieroso ad alto grado in seconda linea di trattamento con ricaduta platino-sensibile, risposta completa o parziale alla chemioterapia a base di platino e mutazione BRCA1,3,4,49–52 (Tabella 4).
Parametri per determinazione di impatto budgetario e flusso pazienti.
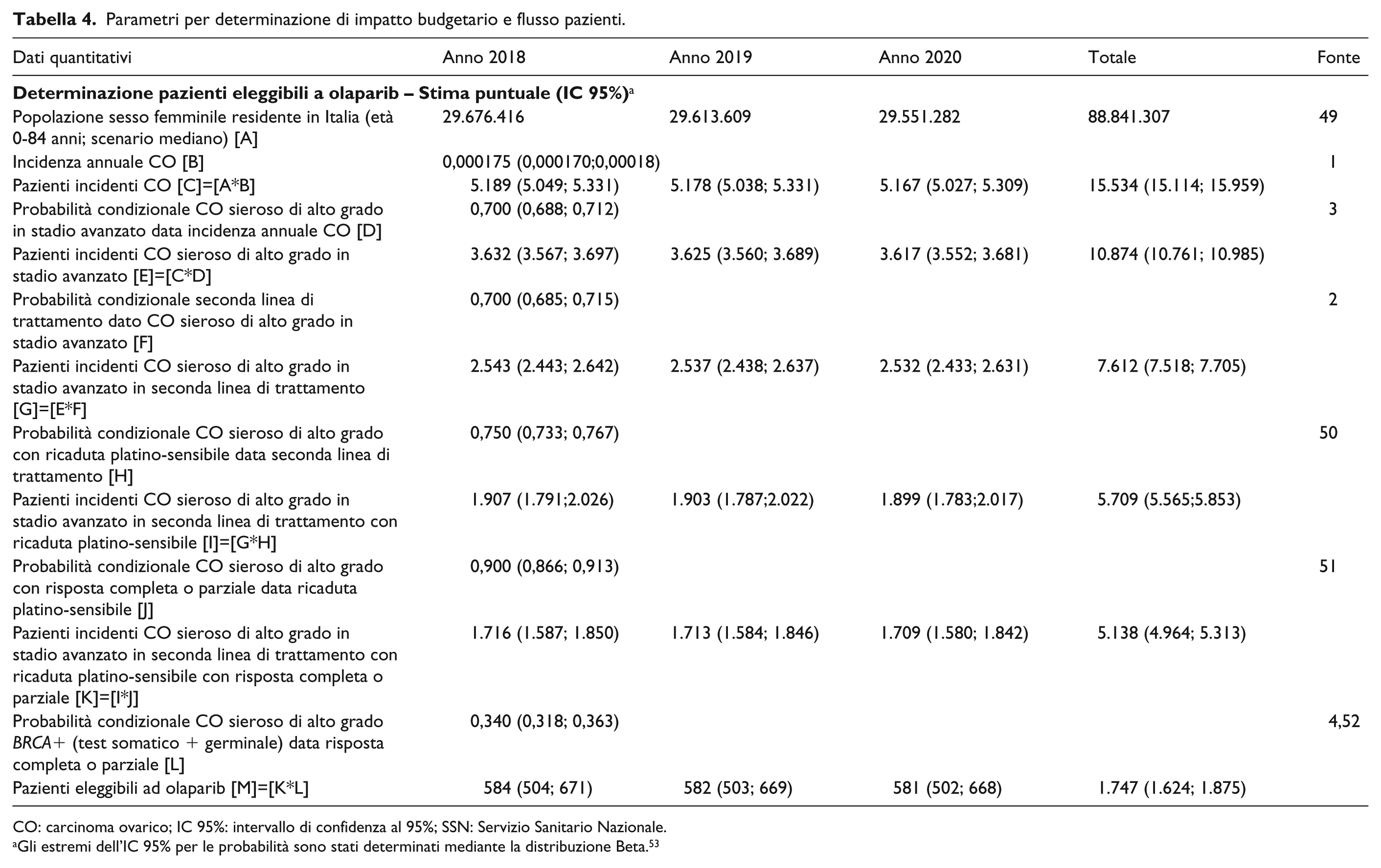
CO: carcinoma ovarico; IC 95%: intervallo di confidenza al 95%; SSN: Servizio Sanitario Nazionale.
Gli estremi dell’IC 95% per le probabilità sono stati determinati mediante la distribuzione Beta. 53
Sono state inoltre adottate le seguenti ipotesi di ricerca:
permanenza degli assunti e dei risultati del modello di analisi di minimizzazione dei costi;
assenza di impedimenti di carattere clinico e/o vincoli logistici al passaggio delle pazienti da niraparib a olaparib;
assenza di attualizzazione dei costi manifestatisi nel secondo e terzo anno compresi nel modello di determinazione di impatto budgetario. 46
Analisi statistica
L’analisi statistica si è limitata alla determinazione, per la maggioranza dei parametri utilizzati nel modello di analisi di minimizzazione dei costi e nella determinazione di impatto budgetario, dell’IC 95%, calcolato utilizzando alcune distribuzioni statistiche codificate in letteratura,20,53 quali Beta (probabilità eventi dicotomici), Gamma (volumi risorse sanitarie, a esclusione della posologia dei farmaci, e mortalità a un anno popolazione generale aggiustata per età), Normale (costi unitari risorse sanitarie, ad esclusione dei farmaci) e Log-normale (moltiplicatore mortalità per CO rispetto a mortalità a un anno popolazione generale aggiustata per età) (Tabelle 1–3).
Quando non determinato analiticamente, l’errore standard della distribuzione campionaria della media di ciascun parametro, necessario per la determinazione dell’IC95%, è stato calcolato imponendo, alla stima puntuale utilizzata nell’analisi di base, un coefficiente di variazione 29 raccomandato dalla letteratura (volumi risorse sanitarie=40%; costi unitari risorse sanitarie=10%) 53 (Tabelle 1–3).
L’analisi statistica è stata supportata dal software Excel per Windows® 2010 (Microsoft, Redmond, WA, USA).
Analisi di sensibilità
La robustezza dei risultati ottenuti con l’analisi di base è stata verificata mediante due tipologie di analisi di sensibilità: univariata e, per quanto concerne la sola analisi di minimizzazione dei costi, di scenario.18,19,54
Analisi di sensibilità univariata
L’incertezza relativa alla stima puntuale dei parametri che hanno popolato il modello di analisi di minimizzazione dei costi è stata indagata mediante l’analisi di sensibilità univariata,18,19,54 la quale prevede il cambiamento di un singolo parametro per volta, mantenendo i restanti costanti, cioè al medesimo valore impiegato nell’analisi di base.
L’analisi di sensibilità univariata si è orientata alla sostituzione della stima puntuale della maggioranza dei parametri utilizzati nel modello con i limiti inferiori e superiori dei rispettivi IC 95% o range di variazione (Tabelle 1–3).
I risultati dell’analisi di sensibilità univariata sono stati riportati su un grafico Tornado, 18 gli assi cartesiani del quale si incrociano in prossimità della differenza tra i costi complessivi per paziente di olaparib e niraparib risultanti dall’analisi di base.
Per quanto concerne la determinazione di impatto budgetario, si sono sostituiti gli estremi dell’IC 95% della distribuzione Beta alla stima puntuale della probabilità di manifestazione degli eventi che concorrono alla definizione del numero delle pazienti eleggibili a olaparib (Tabella 4).
Analisi di sensibilità di scenario
Nell’analisi di sensibilità di scenario, 54 le probabilità di manifestazione delle tossicità ematopoietiche utilizzate nell’analisi di base, 6 mantenute invariate, sono state moltiplicate per i costi unitari di gestione dei medesimi eventi avversi di grado ⩾3 riportati in due recenti esperienze di ricerca condotte nel nostro Paese, riferite a due differenti neoplasie (adenocarcinoma del pancreas 30 e NSCLC con mutazione epidermal growth factor receptor, EGFR 55 ).
In entrambi gli studi, le risorse sanitarie necessarie alla gestione delle tossicità ematopoietiche sono state identificate e quantificate sulla base dell’opinione degli esperti (raccolta mediante un sondaggio realizzata presso nove centri oncologici 30 o pannelli Delphi che ha coinvolto tre clinici esperti 55 ) e monetizzate in €2017 secondo la prospettiva del SSN.
Le analisi di sensibilità sono state supportate dal software Excel per Windows® 2010 (Microsoft, Redmond, WA, USA).
Risultati
Analisi di minimizzazione dei costi
Analisi di base
I costi unitari relativi alla gestione delle tossicità ematopoietiche indagate sono pari ad €6.190,92 (anemia), €2.390,11 (neutropenia) e €2.770,43 (trombocitopenia) (Tabella 5).
Analisi di base – Analisi di minimizzazione dei costi - Costi per paziente (€2018).
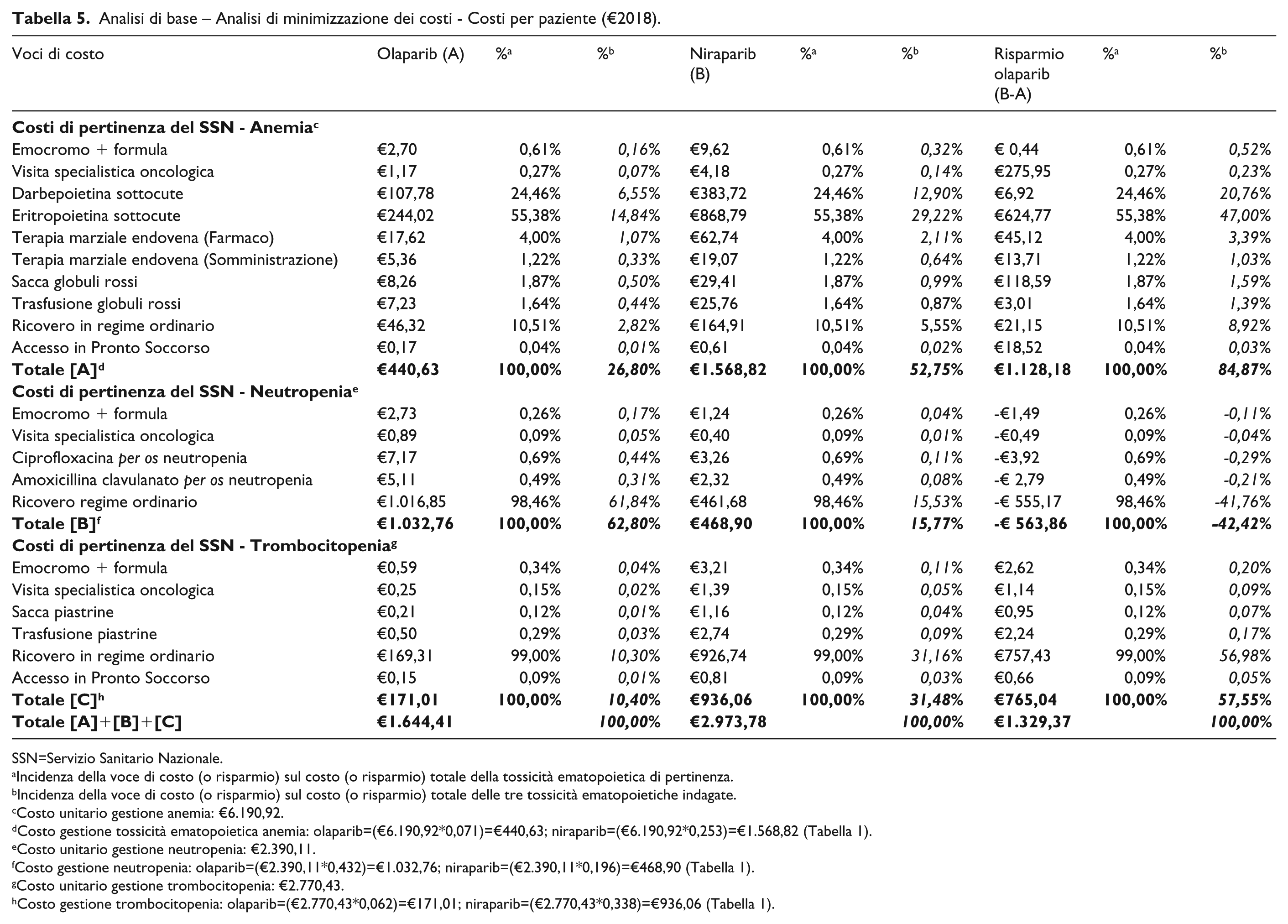
SSN=Servizio Sanitario Nazionale.
Incidenza della voce di costo (o risparmio) sul costo (o risparmio) totale della tossicità ematopoietica di pertinenza.
Incidenza della voce di costo (o risparmio) sul costo (o risparmio) totale delle tre tossicità ematopoietiche indagate.
Costo unitario gestione anemia: €6.190,92.
Costo gestione tossicità ematopoietica anemia: olaparib=(€6.190,92*0,071)=€440,63; niraparib=(€6.190,92*0,253)=€1.568,82 (Tabella 1).
Costo unitario gestione neutropenia: €2.390,11.
Costo gestione neutropenia: olaparib=(€2.390,11*0,432)=€1.032,76; niraparib=(€2.390,11*0,196)=€468,90 (Tabella 1).
Costo unitario gestione trombocitopenia: €2.770,43.
Costo gestione trombocitopenia: olaparib=(€2.770,43*0,062)=€171,01; niraparib=(€2.770,43*0,338)=€936,06 (Tabella 1).
Per entrambi i PARPi comparati, i costi di pertinenza del SSN relativi alle suddette tossicità ematopoietiche sono stati calcolati moltiplicando i rispettivi costi unitari per la probabilità di manifestazione di tali eventi avversi (Tabelle 1 e 5).
Nel corso di un anno, olaparib e niraparib presentano i costi totali per paziente minori (€1.644,41) e maggiori (€2.973,78), rispettivamente (Tabella 5).
Per quanto concerne olaparib (niraparib), la tossicità ematopoietica che genera i maggiori costi per paziente a carico del SSN, pari a €1.032,76 (€1.568,82) è rappresentata dalla neutropenia (anemia), che incide per il 62,80% (52,75%) sul costo totale per paziente.
Per converso, l’effetto avverso di pertinenza ematologica ascrivibile a olaparib (niraparib) che comporta i costi minori per il terzo pagante, che eguagliano €171,01 (€468,90), pari al 10,40% (15,77%) del costo totale per paziente, si identifica nella trombocitopernia (neutropenia).
Per entrambe le molecole, i driver dei costi delle singole tossicità ematopoietiche sono rappresentati dall’eritropoietina sottocute (55,38% del costo totale per paziente relativo all’anemia) e dal ricovero in regime ordinario (98,46% e 99,00% del costo totale per paziente, relativo alla neutropenia ed alla trombocitopenia, rispettivamente).
Nel corso di un anno, il risparmio complessivo per paziente a favore di olaparib risulta pari a €1.329,37; l’84,87% di tale importo deriva dai minori costi per paziente totalizzati da tale principio attivo per la gestione dell’anemia.
Analisi di sensibilità univariata
Limitando la descrizione dei risultati ai 10 parametri che determinano le maggiori variazioni rispetto all’analisi di base, il risparmio per paziente a favore di olaparib risulta moderatamente sensibile alla sostituzione della stima puntuale con i limiti dell’IC 95% del volume di ricoveri in regime ordinario per trombocitopenia (da -35,53% a +52,59% vs analisi di base) e del numero di settimane di terapia con eritropoietina in caso di anemia (da -29,31% a +43,38% vs analisi di base) (Figura 1).
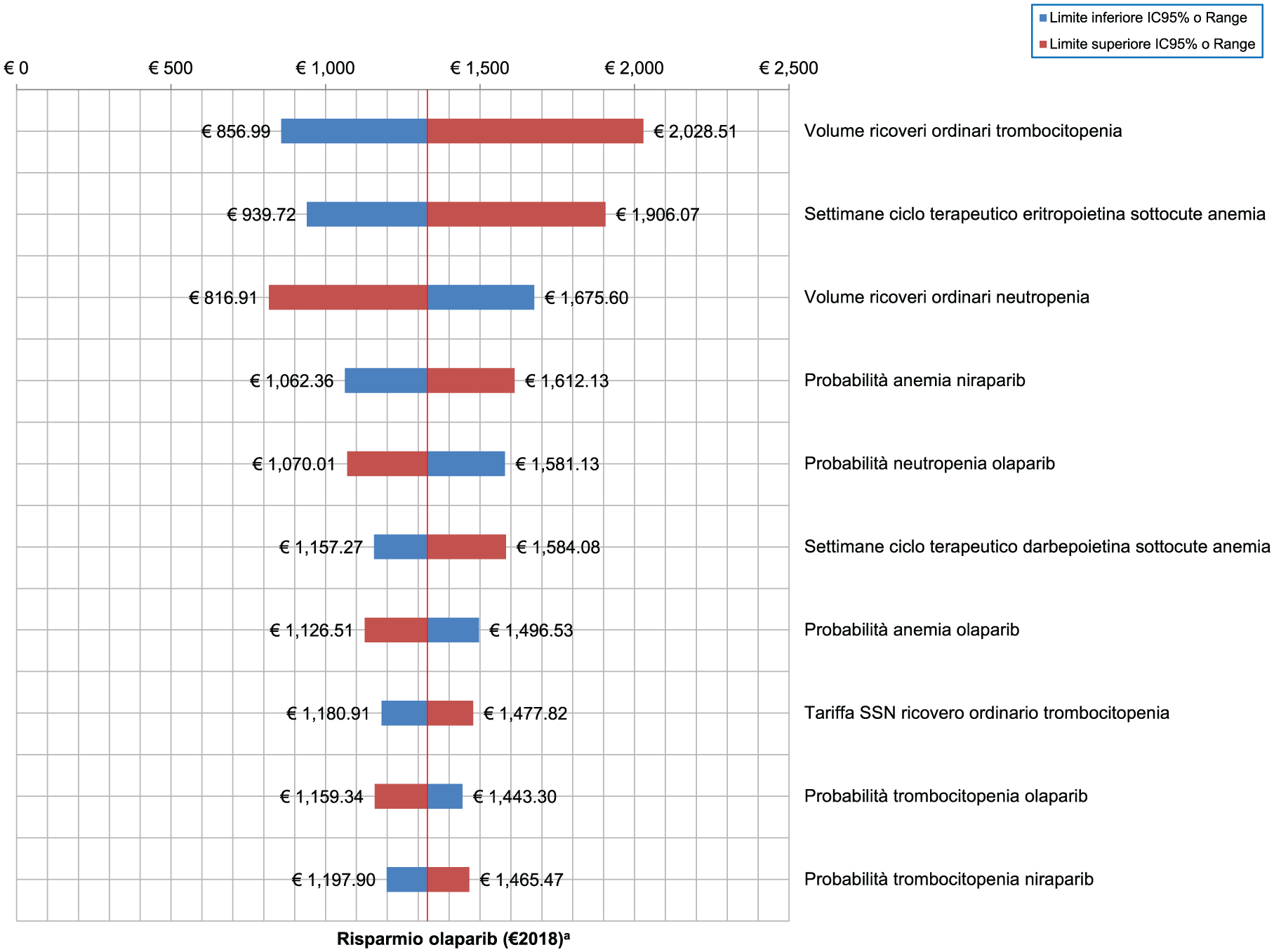
Analisi di sensibilità univariata – Analisi di minimizzazione dei costi - Risparmi per paziente (€2018).
Anche a motivo della minore dispersione intorno alla stima puntuale dei parametri, i riferimenti utilizzati per la monetizzazione delle risorse sanitarie necessarie alla gestione delle tossicità ematopoietiche indagate, rivestono un ruolo trascurabile nella verifica della maggiore efficienza economica di olaparib determinata con le ipotesi di partenza. Si discostano da tale tendenza i limiti dell’IC 95% della valorizzazione del ricovero in regime ordinario per trombocitopenia (da -11,17% a +11,17% vs analisi di base).
Producono, infine, diminuzioni e aumenti più contenuti, variazioni indotte nella probabilità di trombocitopenia sia per olaparib (da -12,79% a +8,57% vs analisi di base), che per niraparib (da -9,89% a +10,24% vs analisi di base).
Analisi di sensibilità di scenario
Con riferimento all’anemia, i costi unitari di gestione variano da €293,80 ad €469,21, ampiamente inferiori al valore di €6.190,92 da noi calcolato (Tabella 6).
Analisi di sensibilità di scenario – Analisi di minimizzazione dei costi - Costi per paziente (€2017-2018).
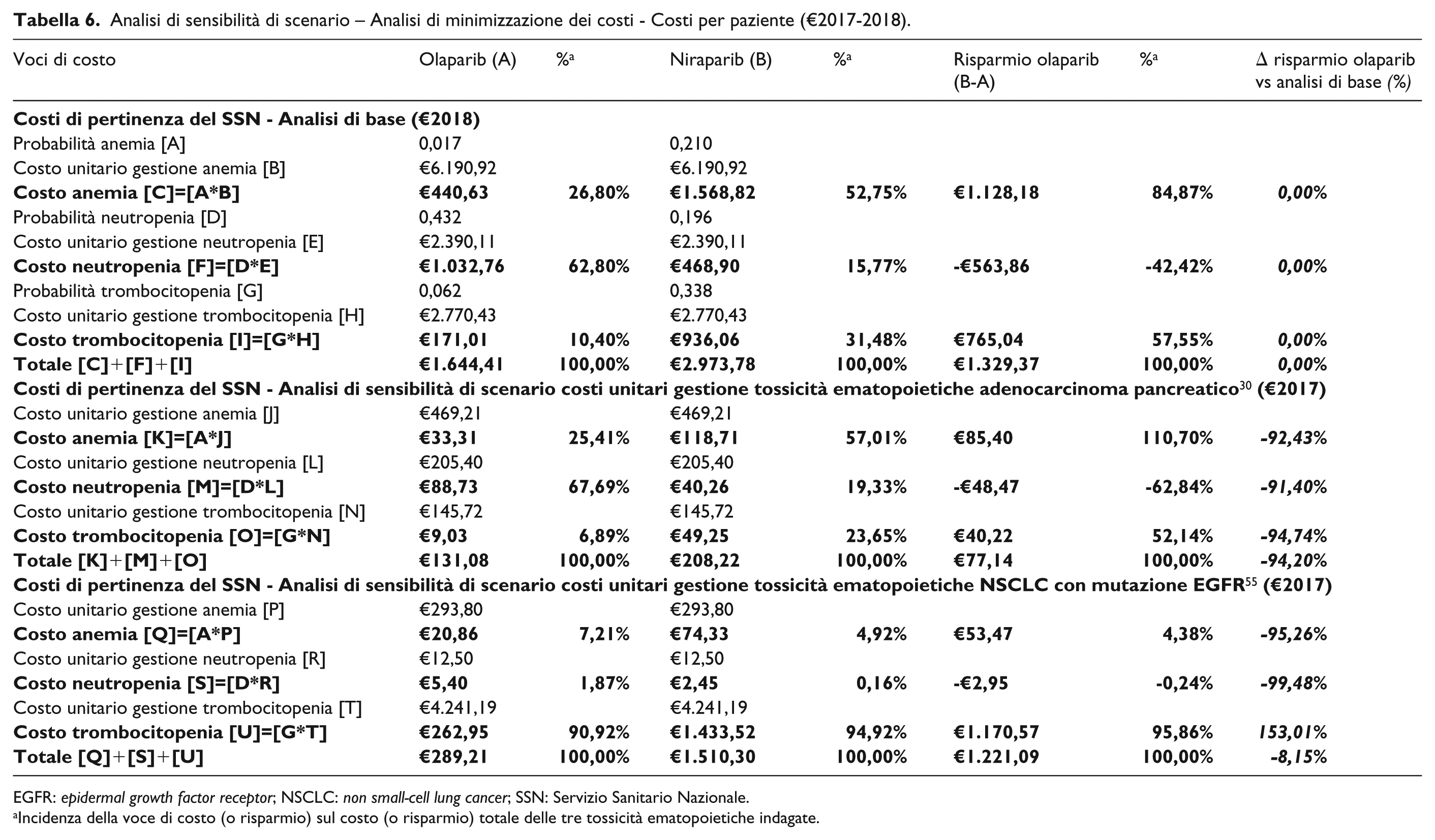
EGFR: epidermal growth factor receptor; NSCLC: non small-cell lung cancer; SSN: Servizio Sanitario Nazionale.
Incidenza della voce di costo (o risparmio) sul costo (o risparmio) totale delle tre tossicità ematopoietiche indagate.
La neutropenia non febbrile assorbe risorse per un valore compreso tra €12,50 e €205,40, anche in questo caso assai inferiore a quanto determinato nel modello di analisi di minimizzazione dei costi dettagliato alle pagine precedenti (€2.390,11).
Infine, per la trombocitopenia gli importi oscillano tra €145,72 ed €4.241,19; quest’ultimo valore risulta, invece, notevolmente superiore a quanto calcolato nella presente esperienza di ricerca (€2.770,43).
Complessivamente, i costi totali a carico del SSN a motivo delle tossicità ematopoietiche indagate, sono compresi tra €131,08 e €289,21 per olaparib (da -92,03% a -82,41% vs analisi di base) e €208,22 e €1.510,30 per niraparib (da -92,30% a -49,21% vs analisi di base)
Indipendentemente dalla fonte utilizzata nell’analisi di sensibilità di scenario, il risparmio a favore di olaparib permane positivo, anche se caratterizzato da evidente variabilità, sia in termini assoluti (da €77,14 a €1.221,09), sia in termini di variazione percentuale (da -94,20% a -8,15% vs analisi di base).
Determinazione di impatto budgetario
Analisi di base
Nel corso del triennio ipotizzato dal modello di determinazione di impatto budgetario, 1.747 (IC 95%: 1.624; 1.875) pazienti incidenti risultano eleggibili a terapia con olaparib (Tabella 7). Date le previsioni in diminuzione dello scenario mediano della popolazione femminile, che condiziona coerentemente il numero di nuovi casi di CO diagnosticati per anno, il numero delle pazienti eleggibili a olaparib segue una tendenza decrescente, ed è compreso tra 584 (IC 95%: 504;671) pazienti (anno 2018) e 581 (IC 95%: 502;668) pazienti (anno 2020).
Analisi di base e di sensibilità univariata – Determinazione di impatto budgetario - Risparmi aggregati SSN (€m 2018) a .
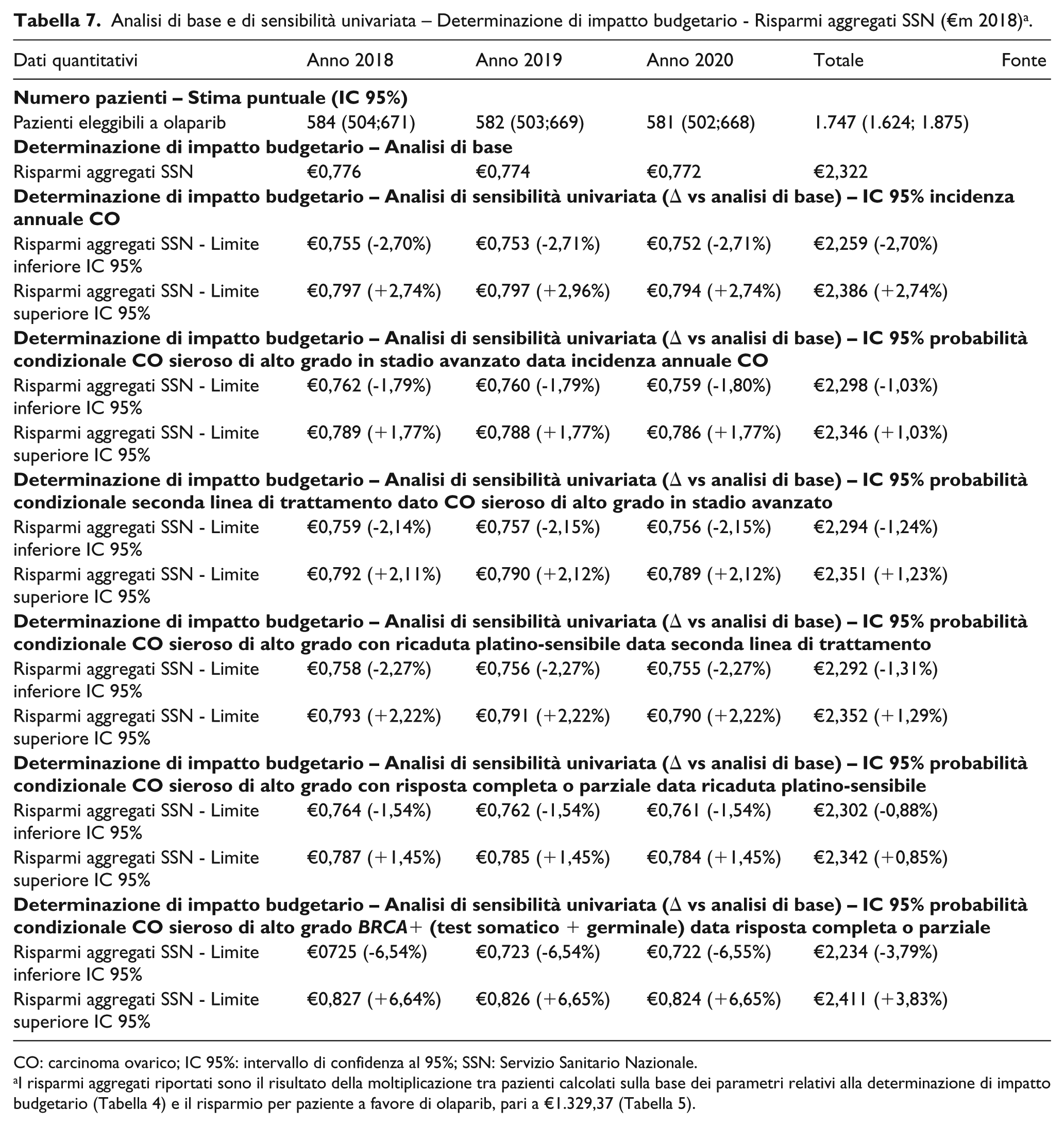
CO: carcinoma ovarico; IC 95%: intervallo di confidenza al 95%; SSN: Servizio Sanitario Nazionale.
In termini percentuali, il numero annuale e complessivo delle pazienti eleggibili a olaparib non eccede l’11,25% del totale dei casi incidenti di CO diagnosticati.
Il risparmio aggregato annuale a favore del SSN, generato dai minori costi per la gestione delle tossicità ematopoietiche totalizzati da olaparib, dato il previsto calo delle pazienti, si riduce contestualmente e si attesta intorno a €0,776m (anno 2018), €0,774m (anno 2019) e €0,772m (anno 2020), mentre il risparmio aggregato triennale raggiunge €2,322m.
Analisi di sensibilità univariata
A seguito della sostituzione degli estremi inferiore e superiore dell’IC 95% della distribuzione Beta relativa alla proporzione delle pazienti incidenti affette da CO sieroso di alto grado in stadio avanzato in seconda linea di trattamento, con ricaduta platino-sensibile, risposta completa o parziale con mutazione BRCA (test somatico + germinale) eleggibili a olaparib, il trattamento con tale principio attivo consentirebbe, nella prima ipotesi, risparmi aggregati per il SSN pari ad €2,234m (-3,79% vs all’analisi di base), mentre, nella seconda ipotesi, risparmi aggregati per il SSN pari ad €2,411m (+3,83% rispetto all’analisi di base) (Tabella 7).
Discussione e conclusioni
Il presente manoscritto ha descritto la metodologia e i risultati di un’analisi di minimizzazione dei costi18,19 condotta secondo la prospettiva del SSN, finalizzata alla comparazione dei costi totalizzati, nel corso di un anno, per la gestione delle tossicità ematopoietiche derivanti dalla terapia con olaparib o niraparib nelle pazienti affette da CO recidivato con mutazione BRCA.
L’intervallo temporale adottato, confortato dai risultati di PFS relativi ai PARPi confrontati,21,22 ha consentito di supportare l’analisi di minimizzazione dei costi mediante un albero decisionale 20 semplice, caratterizzato da due stati di salute (sopravvivenza o decesso), che si aggiungono alla presenza/assenza delle tossicità ematopoietiche oggetto di indagine. È interessante rilevare che la PFS è raccomandata come endpoint primario (ritenuto maggiormente informativo della sopravvivenza totale a partire dalla terza linea di trattamento) negli studi clinici aventi per oggetto l’efficacia dei PARPi nel CO, poiché questi includono pazienti che, pretrattate con diversi regimi chemioterapici, rappresentano, di fatto, una popolazione eterogenea. 56
Pur con le note cautele che debbono caratterizzare il confronto con studi di carattere economico sanitario condotti all’estero, 57 a motivo, ad esempio, delle differenze nelle modalità di valorizzazione delle risorse sanitarie, i costi unitari di gestione delle medesime tossicità ematopoietiche rilevati nei due studi statunitensi precedentemente citati,12,14 espressi in US$ a valori 2017, risultano costantemente superiori a quelli determinati nella presente esperienza di ricerca (anemia: US$7.533-US$7.680, pari ad €6.634,67-€6.764,14; neutropenia: US$13.248-US$13.633, pari ad €11.668,13-US$12.007,22; trombocitopenia: US$5.737-US$10.607, pari ad €5.051,08-€9.342,08) (tasso di cambio €/US$=1,1354, non aggiustato per il tasso d’inflazione USA 2017-2018). 15
Dai risultati descritti ai paragrafi precedenti emergono alcune indicazioni che si reputano interessanti per il decisore. In merito alla gestione delle tossicità ematopoietiche esaminate, nell’analisi di base e per la totalità delle ipotesi considerate nelle analisi di sensibilità univariata e di scenario, olaparib genera risparmi a favore del SSN. Pare opportuno sottolineare che i suddetti risparmi sono spiegati unicamente dalle differenti probabilità di manifestazione delle tossicità ematopoietiche oggetto di indagine, poiché le risorse sanitarie necessarie alla loro gestione sono state identificate, quantificate e valorizzate in maniera analoga per olaparib e niraparib.
Vi è inoltre da considerare che, secondo alcuni Autori, 10 in questa indicazione terapeutica, l’incidenza della neutropenia di grado severo, febbrile e non febbrile, risulta più elevata (0,432) negli RCTs che prevedono la combinazione di olaparib e chemioterapia verso chemioterapia, 21 rispetto ad analoghe esperienze di ricerca volte a sperimentare olaparib in monoterapia verso placebo, che riportano valori di incidenza compresi tra lo 0,037 e lo 0,10.58,59 Pertanto, per quanto concerne l’incidenza della neutropenia di grado severo per olaparib, il modello di valutazione economico-sanitaria ha adottato un’ipotesi di ricerca sfavorevole a tale principio attivo.
In termini più generali, l’impiego dei PARPi in monoterapia o in combinazione con chemioterapia (e, in questo caso, con quali farmaci) nelle pazienti con CO ricorrente pretrattato, richiede la raccolta di ulteriori evidenze empiriche non solo relativamente all’efficacia e alla tossicità di tali opzioni terapeutiche, 56 ma anche ai costi che esse generano a carico del terzo pagante.
Di pari rilevanza si reputa la disponibilità di risultati aggiornati sulla sopravvivenza totale delle pazienti trattate con PARPi e sulla qualità di vita connessa al loro stato di salute (o utilità),18,19,56,60 rispetto alla quale la tollerabilità degli eventi avversi esercita un effetto non trascurabile. In particolare, il tema dell’utilità (e di riduzione delle disutilità causate dalle tossicità da PARPi, sia di pertinenza ematologica ma, riteniamo, anche di differente tipologia) assume particolare rilievo per quelle pazienti per le quali, a motivo di prognosi fortemente infausta, lo spazio terapeutico risulti fatalmente limitato. 56
La valutazione economica realizzata si inserisce in un filone di ricerca di recente attivazione in Italia, 55 dedicato all’indagine degli aspetti economici delle tossicità in ambito oncologico o comprensive di tale obiettivo di ricerca. 30 A tale proposito, confrontando i costi unitari per la gestione delle tossicità ematopoietiche di grado severo affrontate nel presente manoscritto con quanto riportato dalle due recenti pubblicazioni relative al nostro Paese citate con riferimento all’analisi di sensibilità di scenario,30,55 emergono, come precedentemente evidenziato, differenze degne di nota. Riteniamo che tali differenze dipendano solo marginalmente dalle fonti utilizzate per la monetizzazione delle risorse sanitarie secondo la prospettiva del SSN, che appartengono a un novero limitato soprattutto per la valorizzazione dei fattori produttivi diversi dai farmaci, ma essenzialmente dall’opinione qualificata dei clinici, variabile per patologia oncologica ed esperienza relativa al riscontro di determinati eventi avversi.
Inoltre, si osserva che, sebbene i costi unitari comparati si riferiscano a diverse neoplasie, le linee-guida nazionali consultate, 13 dalle quali sono state ottenute parte delle risorse sanitarie finalizzate alla gestione delle tossicità ematopoietiche oggetto di indagine, si concentrano sulla gravità dell’evento avverso anziché sulla tipologia della malattia oncologica sottostante; quest’ultima non pare, pertanto, spiegare le differenze riscontate.
Con riferimento alla determinazione di impatto budgetario secondo incidenza, si evidenzia come il risparmio aggregato a favore di olaparib rimanga positivo, ancorché variabile in termini assoluti, per ciascuna delle variazioni delle ipotesi di base indotte nell’analisi di sensibilità univariata.
Qualora, mantenendo la prospettiva del SSN e confermando la totalità delle ipotesi a supporto della determinazione di impatto budgetario, si sommasse il costo per la gestione delle tossicità ematopoietiche al costo annuale della terapia con olaparib e niraparib, determinato, al netto degli sconti di legge, in €5.302,34 e €8.430,72 mensili,47,48 rispettivamente, nell’analisi di base il risparmio aggregato annuale per il SSN raggiungerebbe €22,64m (anno 2018), €22,59m (anno 2019) ed €22,54m (anno 2020), pari a €67,78m nel triennio 2018-2020. L’indifferenza economica tra olarib e niraparib si otterrebbe solo assumendo uno sconto che si attestasse intorno al 40% del costo mensile di quest’ultimo.
Quali sono i principali limiti relativi alla valutazione economica effettuata?
Un primo limite attiene alla modalità di comparazione indiretta dell’incidenza delle diverse tossicità ematopoietiche indagate nella presente esperienza di ricerca.
Peraltro, la scelta dell’incidenza, che ha informato sia l’analisi di minimizzazione dei costi, sia la determinazione di impatto budgetario (supportando, per quest’ultima, la reiterazione triennale dei risultati di costo ricavati dall’albero decisionale caratterizzato da un unico ciclo, ancorché su una popolazione femminile in lieve diminuzione) è stata essenzialmente dettata dalla disponibilità, secondo tale dimensione epidemiologica, dei dati ricavati dalla meta-analisi ripetutamente citata. 6
Un secondo limite attiene alla natura modellistica dello studio che, per definizione, include dati provenienti da diverse fonti, 61 nonché alcune stime conseguenti a ipotesi di ricerca. Tale ultimo aspetto si riflette, fatalmente, anche sulla quantificazione delle risorse sanitarie dedicate al trattamento delle tossicità ematopoietiche indagate.
Un terzo limite, peraltro riscontrato anche in altri Paesi,62,63 concerne la trasferibilità alla normale pratica clinica, per vincoli istituzionali, organizzativi ed economici, di quanto suggerito dalle linee-guida e dalla letteratura a proposito della gestione delle tossicità ematopoietiche, con possibili riflessi sui contesti di erogazione delle prestazioni sanitarie diverse dai farmaci e, in ultima analisi, sui rispettivi costi unitari.
Un quarto e ultimo limite concerne l’imperfetta comparabilità dei costi di gestione delle tossicità ematopoietiche sopra commentate, poste le differenti modalità seguite per la raccolta dei dati relativi alla quantificazione delle risorse sanitarie. Infatti, mentre nella presente ricerca si è privilegiata l’integrazione tra fonti di letteratura e opinione qualificata di clinico, negli studi italiani precedentemente citati sono state impiegate, rispettivamente, un sondaggio 30 e la metodologia Delphi. 55
Per la totalità dei limiti sopra evidenziati, si profila pertanto la necessità di corroborare i risultati ottenuti con successive esperienze di ricerca empiriche, e possibilmente comparative, tra olaparib e niraparib in tale indicazione terapeutica, realizzate su dati desunti dalle cartelle delle pazienti o da database di carattere amministrativo. 55
In conclusione, fatti salvi i limiti precedentemente dettagliati, si ritiene che, per quanto attiene alla gestione delle tossicità ematopoietiche indagate con riferimento alla terapia del CO BRCA+ pretrattato recidivato, olaparib rappresenti, per il SSN, un programma sanitario economicamente più efficiente di niraparib.
Supplemental Material
Supplemental_Material – Supplemental material for Severe haematological toxicities in relapsed ovarian cancer treated with olaparib or niraparib: an Italian cost-minimization analysis
Supplemental material, Supplemental_Material for Severe haematological toxicities in relapsed ovarian cancer treated with olaparib or niraparib: an Italian cost-minimization analysis by Carlo Lazzaro, Nicola Amedeo Mazzanti and Fabio Parazzini in Global & Regional Health Technology Assessment
Footnotes
Declaration of Conflicting Interest
CL is a consultant for AstraZeneca S.p.A. NAM is an employee of AstraZeneca S.p.A. FP declares no conflicting interest.
Funding
This study was funded by AstraZeneca S.p.A.
Supplemental material
Supplemental material for this article is available online.
References
Supplementary Material
Please find the following supplemental material available below.
For Open Access articles published under a Creative Commons License, all supplemental material carries the same license as the article it is associated with.
For non-Open Access articles published, all supplemental material carries a non-exclusive license, and permission requests for re-use of supplemental material or any part of supplemental material shall be sent directly to the copyright owner as specified in the copyright notice associated with the article.
