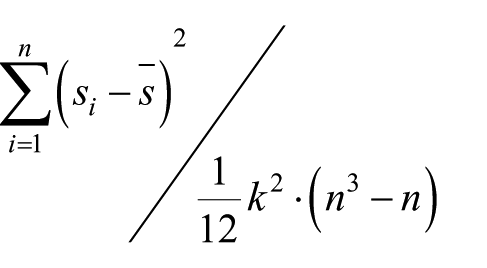Abstract
Introduction:
This paper aims at investigating the role of Patients’ Associations in drugs assessment and appraisal in Italy.
Methods:
Information were gathered through a mostly structured (forced ranking) questionnaire. The questionnaire, once validated, was administered to two national HTA organisations (AIFA and ISS) and Therapeutic Committees / Departments of five regions (Lombardy, Veneto, Emilia Romagna, Latium, Sicily). The average rank and the Kendall rank correlation coefficient were calculated where respondents were forced ranking.
Results:
The interactions with Patients’ Associations are very different across HTA organisations, with only three respondents declaring a systematic relationship with these Associations and a focus on therapeutic targets more affected by new drugs launches. Patients’ Associations are perceived more expert on the organisation of the Italian health care system and drugs reimbursement process than on technical issues (e.g. PROs – Patient Reported Outcomes). Respondents declared that fragmentation of relationships, with many associations involved, is the most important barrier to a systematic interaction with Patients’ Associations and advocated for a stronger integration among them.
Discussion:
The interaction between HTA organisations and Patients’ Associations is expected to increase in the future. To make this interaction more useful, Patients’ Associations should improve their knowledge on drugs assessment techniques - mainly PRO - and enhance their awareness on budget issues for payers: the former could create a virtuous cycle that may drive HTA organisations paying more attention to PROs; the latter may help Patients’ Associations and payers agreeing on actions aimed at making drugs more sustainable.
Introduzione
L’Health Technology Assessment (HTA) è il processo multidisciplinare che utilizza la migliore evidenza disponibile per valutare le implicazioni cliniche, economiche, organizzative, sociali ed etiche delle tecnologie sanitarie, per produrre evidenze per i policy maker (1). Nella pratica reale dell’HTA non sempre però si valutano tutte queste dimensioni di impatto. In particolare, un aspetto poco approfondito, ma non per questo poco importante, è quello relativo all’impatto della tecnologia sul paziente, che nell’HTA Core Model di EUnetHTA (European network for Health Technology Assessment) rientra nel dominio “Patients and Social Aspects” (2).
Il tema del coinvolgimento dei pazienti nelle diverse fasi dell’HTA è stato ed è tuttora oggetto di riflessione e dibattito nel contesto internazionale. I principali motivi alla base del coinvolgimento dei pazienti nel processo di HTA sono riconducibili principalmente a due macro-aspetti. In prima istanza, la loro partecipazione è legata alla necessità di incrementare la trasparenza, la legittimità e l’equità dei processi decisionali correlati all’introduzione delle tecnologie sanitarie (3). Dall’altro lato, i pazienti sono considerati i principali esperti della patologia di cui sono affetti (4).
In generale, il modo in cui i portatori di interesse ed i pazienti in particolare sono coinvolti nell’HTA dipende, tra gli altri aspetti, dal contesto politico e culturale (5).
In linea teorica, i pazienti possono essere coinvolti durante tutte le fasi di un processo di HTA. Menon et al. hanno individuato alcuni esempi di coinvolgimento dei pazienti nei diversi step del percorso di valutazione di una tecnologia sanitaria dall’identificazione delle tecnologie sanitarie, alla selezione delle tecnologie da valutare (priority setting), alla valutazione delle tecnologie (assessment), alla elaborazione delle raccomandazioni (appraisal), fino alla disseminazione delle decisioni finali (6).
I pazienti possono intervenire nei processi di HTA come singoli pazienti o come rappresentanti delle Associazioni dei Pazienti (d’ora in poi AP). Un paziente e/o il suo caregiver possono portare una ricca conoscenza basata sull’esperienza della malattia e dei percorsi diagnostici e terapeutici sperimentati. Nel caso di un AP, invece, la conoscenza è meno specifica, ma è riferita a più pazienti.
Da un’analisi della letteratura emerge un quadro a livello europeo (e, più in generale, internazionale) molto variegato in merito al coinvolgimento dei pazienti nel processo di HTA, coerente con i diversi assetti istituzionali in cui operano i soggetti pubblici (5). In linea generale, però, si assiste ad una convergenza nell’attribuzione di un crescente peso dei pazienti nei processi di valutazione delle tecnologie sanitarie.
A titolo esemplificativo, in Inghilterra il coinvolgimento dei pazienti da parte del NICE (National Institute for Health and Care Excellence) avviene dal 1999, anno della sua stessa costituzione (7). All’interno del NICE è stato creato un gruppo (Public Involvement Programme - PIP), che supporta i pazienti e le AP nel processo di partecipazione ai diversi programmi sviluppati dal NICE (8). Nelle diverse fasi del processo di HTA possono essere coinvolti sia Associazioni dei Pazienti che singoli pazienti, esperti o non. Il PIP identifica le AP più rilevanti a livello nazionale mediante l’utilizzo di database interni, di internet e dei registri delle organizzazioni non profit forniti dalla Charity Commission. Queste organizzazioni vengono coinvolte in un primo momento nella fase di scoping, commentando una bozza del documento preparato dal Ministero della Salute e partecipando ad un workshop. In particolare, le AP contribuiscono, in questa fase, a definire gli outcome di importanza per i pazienti, le criticità correlate alla qualità della vita che non possono essere catturate mediante le misurazioni convenzionali e il profilo di tollerabilità e accettabilità del nuovo trattamento rispetto alle terapie disponibili (9). Nella fase di assessment i pazienti possono essere coinvolti sia come associazioni che come singoli individui, ma attraverso modalità differenti. Le AP sono invitate a sottomettere, mediante un template, le loro considerazioni in merito alle condizioni di vita con la patologia potenzialmente trattabile dalla tecnologia oggetto di valutazione, ai trattamenti disponibili nella corrente pratica clinica, alla prevalenza della patologia e al potenziale grado di innovazione della tecnologia sanitaria (10). Inoltre, il NICE individua due esperti (una persona affetta dalla patologia trattabile con la tecnologia da valutare e una persona che lavora per un’AP) che possono sottomettere una loro opinione scritta (sempre attraverso un template) e partecipare alla prima riunione consultiva del NICE fornendo la prospettiva dei pazienti (cfr. supra) (11). Nella successiva fase di appraisal, le AP e i pazienti esperti sono coinvolti in modo meno rilevante (ad esempio, presentazione di ricorsi in merito ad una raccomandazione finale). Infine ogni 2-4 anni le informazioni cliniche e di costo-efficacia vengono revisionate dal NICE, che consulta anche in quest’ultimo step le AP (12).
Tra i paesi continentali europei, la Germania ha strutturato negli anni la partecipazione dei pazienti al processo di HTA. L’organismo che è responsabile della valutazione delle tecnologie sanitarie in Germania è il Federal Joint Committee (Gemeinsamer Bundesausschuss – G-BA). In genere, il G-BA commissiona l’elaborazione del report di assessment all’Institute for Quality and Efficiency in Healthcare (Insitut für Qualität und Wirtschaftlichkeit im Gesundheitswesen – IQWiG), mentre gestisce direttamente la fase di appraisal (13). Il coinvolgimento nel processo di HTA riguarda soltanto le AP più rilevanti a livello nazionale che sono state individuate dal Ministro della Salute sulla base dei criteri riportati nel Patient Involvement Act (German disability Council, National Association of Patient Advisory Centre, German Association of Self-Help Groups e Federation of German Consumer Organisations). Ognuna delle quattro organizzazioni deve a sua volta identificare dei rappresentanti dei pazienti che hanno il compito di presiedere alle diverse fasi del processo di valutazione delle tecnologie sanitarie (14). Il primo step che vede il coinvolgimento dei pazienti è la fase di proposta del topic da sottoporre all’attenzione del G-BA. Qualunque AP può proporre una domanda di ricerca alle AP definite rilevanti, che valutano a loro volta il valore della proposta e decidono se procedere alla sottomissione dell’istanza al G-BA. A differenza del Regno Unito, non esiste un template, ma le AP sono supportate da un gruppo specializzato nel coinvolgimento dei pazienti del G-BA. Inoltre, i rappresentanti designati dalle AP vengono coinvolti, attraverso la partecipazione alle riunioni della commissione del G-BA, nel processo di prioritizzazione delle tecnologie sanitarie da valutare, mediante la raccolta di informazioni dettagliate sul topic individuato e la valutazione della rilevanza del topic per i pazienti (ad esempio sulla base del burden della patologia, delle alternative terapeutiche disponibili e del beneficio atteso). Nella fase di assessment, spesso (ma non necessariamente) commissionata dal G-BA all’IQWiG, i pazienti sono coinvolti attraverso la somministrazione di un questionario (e più raramente interviste) per identificare gli outcome, i criteri di inclusione ed esclusione delle informazioni da includere nella valutazione e la metodologia per valutare tali informazioni. Successivamente, il protocollo elaborato (report plan) viene pubblicato sul sito web dell’IQWiG che avvia una consultazione pubblica, dando l’opportunità a chiunque di sottomettere i propri commenti (hearing). Le informazioni ottenute attraverso il coinvolgimento dei pazienti, assieme alla valutazione scientifica condotta dall’IQWiG, sono presentate all’interno di un report preliminare, pubblicato anch’esso sul sito web dell’IQWiG e oggetto di una consultazione pubblica. Il report finale viene, infine, sottoposto alla valutazione del G-BA che elabora la decisione finale (15). Anche la fase di appraisal prevede la partecipazione dei rappresentanti delle AP alle riunioni della commissione del G-BA.
In Francia e Spagna il coinvolgimento dei pazienti non è ancora un processo strutturato, anche se sono state implementate alcune iniziative per formalizzarne la partecipazione (16). Anche l’Italia non sembra avere ancora fatto passi importanti nella direzione di un coinvolgimento fattivo dei pazienti nei processi di valutazione delle tecnologie sanitarie ed in particolare dei farmaci. Sono però carenti le evidenze sia oggettive che di natura percettiva. Una recente survey su rappresentanti di AP di diversi paesi, selezionati sulla base della loro partecipazione a network internazionali su HTA (network afferenti a HTAi - HTAi Patient and Citizen Involvement Patient Panel, HTAi Patient and Citizen Involvement in HTA Interest Group; Cochrane Collaboration Consumer Network) riporta che i responder italiani (insieme a quelli di Israele e Giappone) dichiarano di non essere coinvolti da organizzazioni di HTA, a differenza dei rappresentanti di AP in altri paesi (Canada, Inghilterra, Scozia e Galles, Paesi Bassi, Australia, Taiwan) (17).
A livello extra-europeo è interessante il caso australiano dove la valutazione dei farmaci viene effettuata da una commissione di HTA del Governo australiano (Pharmaceutical Benefits Advisory Committee - PBAC). La partecipazione dei pazienti al processo di HTA in Australia è meno strutturata, rispetto a Inghilterra e Germania, ed è limitata alla fase di appraisal. All’interno della commissione del PBAC è presente almeno un rappresentante dei pazienti, nominato dal Consumers Health Forum (CHF), che fornisce la prospettiva dei pazienti nel processo di valutazione del farmaco da rimborsare (18). Il PBAC pubblica l’agenda della riunione della commissione sei mesi prima della stessa e i pazienti possono sottomettere i loro commenti attraverso un modulo online, in merito ai dati clinici ed economici forniti dall’azienda farmaceutica che ha richiesto la valutazione del rimborso di un farmaco. I commenti ricevuti attraverso questa consultazione pubblica vengono valutati e presentati dai rappresentanti dei pazienti alla riunione della commissione. Il PBAC non fornisce feedback ai pazienti in merito all’utilità dei commenti da loro sottomessi, ma si limita a ringraziare nel documento finale per l’apporto dato dai pazienti senza però menzionare i contenuti del contributo dato e come questi abbiano influenzato la decisione finale. Inoltre, recentemente il PBAC ha implementato, per particolari sottomissioni, l’utilizzo delle udienze (hearing) durante le quali i pazienti possono fornire informazioni relative ai benefici, alle reazioni avverse e ai costi della tecnologia sanitaria oggetto di valutazione (19).
Obiettivi e metodi
L’obiettivo della presente ricerca è indagare come i soggetti istituzionali preposti alla valutazione dei farmaci (AIFA – Agenzia Italiana del Farmaco e Regioni) o più in generale alla valutazione delle tecnologie sanitarie (Agenas – Agenzia nazionale per i servizi sanitari regionali, ISS - Istituto Superiore di Sanità e Regioni) (i) si siano relazionati finora con le AP, (ii) come percepiscano il ruolo ed il contributo atteso delle AP (iii) e come intravedano lo sviluppo futuro di tali relazioni. Agenas ha preferito non rispondere al questionario in quanto maggiormente focalizzato sui farmaci. A livello regionale la scelta è ricaduta su cinque tra le regioni italiane più popolose (Lombardia, Veneto, Emilia-Romagna, Lazio e Sicilia), caratterizzate da una diversa collocazione geografica, da un diverso posizionamento circa l’entità dei disavanzi pregressi rispetto al finanziamento erogato per i servizi sanitari e rispetto alla scelta sulle modalità di governo dell’assistenza farmaceutica. Lazio e Sicilia sono interessate da prontuari regionali vincolanti per le aziende sanitarie; Emilia Romagna, oltre ad un prontuario vincolante, ha istituito gruppi di lavoro finalizzati a produrre raccomandazioni sul comportamento prescrittivo; il Veneto ha abbandonato il prontuario regionale vincolante, ma ha attivato numerosi gruppi di lavoro finalizzati a produrre linee di indirizzo prescrittive, di cui due permanenti sui farmaci oncologici e onco ematologici e, comunque, esercita un’azione di orientamento della gestione dei farmaci nelle aziende sanitarie; la Lombardia ha tradizionalmente esercitato una minore azione di governo a livello regionale, non essendo mai stato attivato un prontuario regionale vincolante.
In particolare, sono state indagate:
l’esperienza con le AP a supporto della valutazione dei farmaci (e delle tecnologie sanitarie) ai fini dell’inclusione nei prontuari / della definizione di raccomandazioni alla prescrizione ed all’uso: frequenza dei contatti; aree terapeutiche su cui l’interazione è stata maggiore; livello di preparazione delle AP su argomenti inerenti all’accesso dei farmaci e variabilità di tale livello tra AP;
percezione sul ruolo attuale delle AP: aree su cui le AP possono fornire un contributo utile per il SSN; ambiti relativi alla valutazione di farmaci / tecnologie sanitarie su cui tale contributo è percepito come più utile; ostacoli ad una maggiore interazioni con le AP;
prospettive di sviluppo futuro di tali relazioni: valutazioni prospettiche di intensità delle relazioni; aree terapeutiche su cui l’interazione con le AP sarà maggiore; aspetti sui cui è importante un miglioramento delle conoscenze da parte delle AP; aspetti per i quali le AP dovrebbero impegnarsi maggiormente in futuro nei confronti dei propri associati.
L’attuale assetto delle relazioni con le AP e la valutazione di natura percettiva sono stati indagati attraverso un questionario prevalentemente strutturato (con l’eccezione di alcune domande aperte) (Allegato). Le domande strutturate sono state poste come richiesta di ordinamento di alcune risposte predefinite.
Il questionario è stato validato dai referenti delle AP del pool di “Persone non solo Pazienti” (cfr. infra) e da due potenziali responder e successivamente somministrato attraverso intervista diretta o auto-somministrazione, in funzione delle preferenze dei responder. Eventuali dubbi e perplessità sulle risposte sono stati discussi direttamente con i responder. La richiesta di compilazione del questionario è stata formalizzata alle figure apicali dell’organizzazione (Direzione Generale di AIFA e Presidenza di ISS) e ai referenti di commissioni terapeutiche / servizi farmaceutici regionali. Eventuale delega alla compilazione è stata fornita ad altri referenti nazionali / regionali (ad esempio la Presidenza ISS ha delegato il referente HTA all’interno dell’ISS).
Le sette risposte sono state analizzate con approccio qualitativo (domande aperte) e quantitativo-descrittivo come (i) distribuzione percentuale dei responder tra le diverse opzioni presentate (domande chiuse con diverse opzioni di selezione delle risposte), e (ii) posizione media / grado di concordanza per le domande che richiedevano un ranking delle risposte. Il grado di concordanza è stato valutato sulla base dell’Indice W di Kendall, indice compreso tra 0% (concordanza nulla) e 100% (concordanza assoluta). L’indice W di Kendall è calcolato come:
dove si è la posizione attribuita all’elemento dal responder i, s “barrato” rappresenta il ranking medio attribuito all’elemento “s”, “k” è il numero degli elementi oggetto di ranking, “n” è il numero di responder.
Risultati
Come sopra specificato, tutti i soggetti istituzionali contattati, con l’eccezione di Agenas, hanno risposto al nostro invito a partecipare al survey (AIFA, ISS, Regione Lombardia, Regione Veneto, Regione Emilia-Romagna, Regione Lazio e Regione Sicilia). Sono stati contattati referenti delle Commissioni Terapeutiche Regionali / Servizi Farmaceutici regionali (cfr. “Ringraziamenti”) per un totale di sette responder.
La frequenza nei contatti con le AP è molto variabile: se i rapporti con le AP vengono qualificati come sistematici da AIFA, Regione Veneto e Regione Emilia-Romagna, Lombardia e Lazio hanno dichiarato contatti frequenti mentre in Sicilia (almeno con riferimento alla Commissione del Prontuario Terapeutico Ospedaliero della Regione Sicilia) ed ISS le interazioni sono estemporanee / rare.
Nei casi di coinvolgimento sistematico vengono richiamati:
progetti specifici di interazione: viene ad esempio citata da AIFA la collaborazione con EpaC per la valutazione della prevalenza dell’Epatite C e l’identificazione delle priorità di accesso alle terapie;
la sistematicità dell’interazione: ad esempio, la Regione Veneto ha segnalato la presenza di AP in tutte le commissioni che forniscono raccomandazioni non solo su farmaci, ma anche su dispositivi medici e assistenza protesica; l’Emilia-Romagna ha evidenziato come uno o più rappresentanti delle AP siano presenti nei gruppi di lavoro regionali.
Regione Lombardia ha evidenziato un’interazione più frequente (anche se non finalizzata all’inclusione dei farmaci in prontuario regionale, che non è presente in tale regione) con AP più organizzate. Regione Lazio ha invece, analogamente ad AIFA, richiamato progetti specifici di collaborazione sulle aree dell’Epatite, HIV e Diabete. In alcuni casi sono state segnalate iniziative da parte delle AP stesse in cui sono stati coinvolti i soggetti istituzionali: ad esempio, la Regione Emilia-Romagna ha citato la partecipazione ad incontri promossi dalle AP con patologie reumatiche sul tema dei biosimilari.
Le aree terapeutiche caratterizzate da maggiori relazioni con i pazienti sono quelle in cui si è assistito al lancio più importante di nuovi prodotti sul mercato, prodotti per i quali è risultato essenziale garantire un accesso rapido ma appropriato dei pazienti. Minori sono state le interazioni sulla valutazione di terapie / tecnologie per patologie orfane di trattamento o rare, di farmaci la cui scelta può essere maggiormente condizionata dal paziente (si pensi a farmaci caratterizzati da un profilo sovrapponibile di beneficio / rischio ma con modalità di somministrazione diverse che incidono sull’accettabilità della terapia per i pazienti), e dei farmaci per i quali le evidenze di efficacia sono più deboli o vi è un alto rischio di inappropriato utilizzo. Non esistono però differenze rilevanti nel posizionamento medio nel ranking tra le diverse tipologie di farmaci, segno di un’importante incertezza dei responder, sottolineata anche dal livello di concordanza sul ranking piuttosto basso (Indice W di Kendall pari a 0,24). L’incertezza su quali tipologie di farmaci saranno oggetto di maggiore interazione tra organizzazioni di HTA e AP è ancora più elevata, se si guarda al futuro: in prospettiva sembra assumere più rilevanza il coinvolgimento delle AP sulla valutazione di farmaci per patologie orfane di trattamento e/o rare e sui farmaci per i quali il paziente può avere un ruolo più rilevante nella scelta terapeutica (Figura 1).
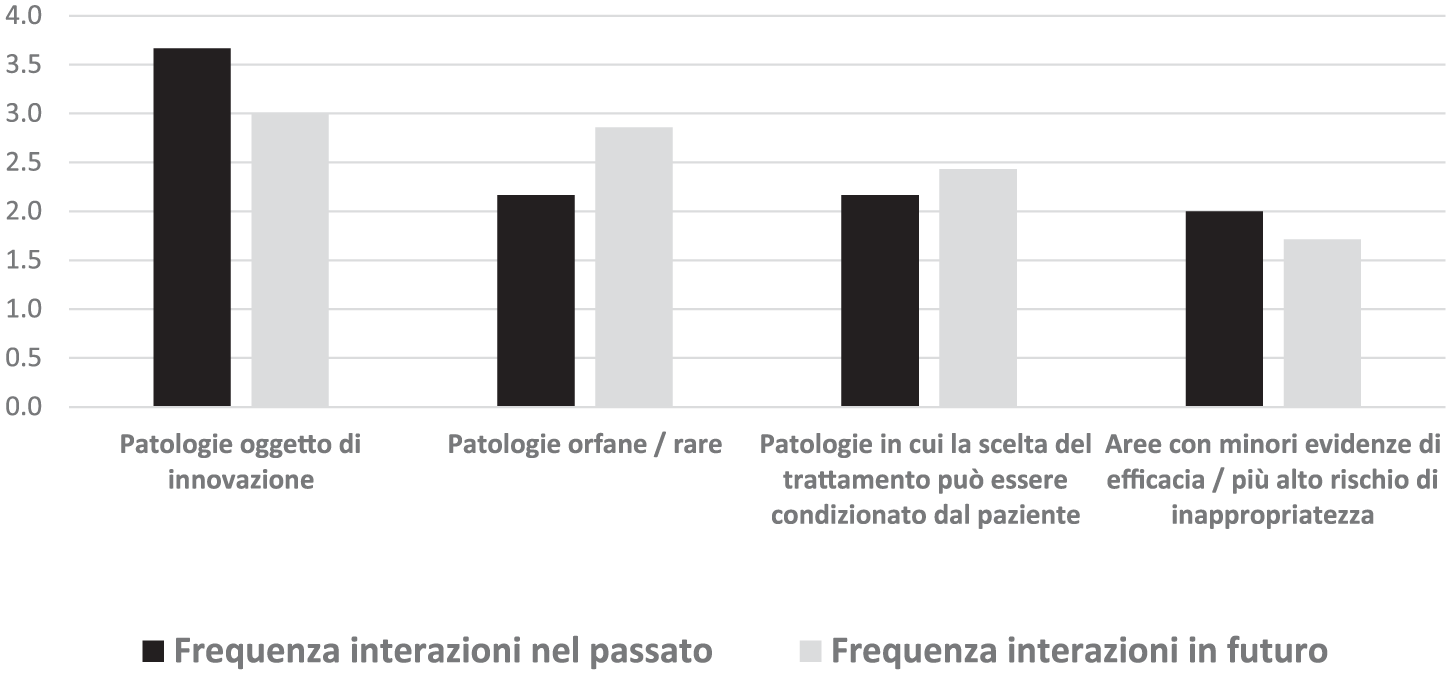
Aree terapeutiche per le quali il responder (nella sua funzione di valutatore dei farmaci / tecnologie) si è maggiormente relazionato e si relazionerà in futuro con i pazienti (valore medio nel ranking tra i responder)*.
Ciò su cui vi è stata un’omogenea indicazione dei responder è il livello di percezione sugli ambiti in cui le AP risultano più preparate (Indice W di Kendall pari a 0,76). Da una parte vi è un riconoscimento di un buon livello di conoscenza del Servizio Sanitario Nazionale (SSN) e degli aspetti di natura regolatoria, in particolare dei vincoli sulla rimborsabilità dei farmaci (Classe di rimborsabilità, Note Aifa, Centri Specialistici autorizzati alla prescrizione / dispensazione dei farmaci, ripetibilità delle ricette, compartecipazioni alla spesa, ecc.). Dall’altra, si stigmatizza il livello di conoscenza piuttosto basso da parte delle AP dei soggetti istituzionali con cui interagiscono, sotto il profilo organizzativo e della gestione economico-finanziaria (Figura 2). Su questi due aspetti è elevata la percezione di variabilità delle conoscenze tra AP (pur in presenza di concordanza molto bassa tra responder, con un Indice W di Kendall pari al 6%). Ancora maggiore è la carenza su aspetti tecnici della valutazione dei farmaci, con riferimento in particolare ai Patient Reported Outcome (PRO), aspetto sul quale i responder hanno evidenziato una variabilità nella conoscenza delle AP leggermente inferiore (ovvero conoscenze tendenzialmente basse in tutte le AP). Speculare, come atteso, è la valutazione delle aree su cui sono maggiori gli spazi di miglioramento delle competenze con i PRO al primo posto e la conoscenza di SSN e sistemi di accesso dei farmaci all’ultimo (ed un indice di concordanza pari a 0,37, minore rispetto all’analisi retrospettiva). Due responder hanno evidenziato, nel campo “Altro”, l’esigenza di una maggiore conoscenza generale (ovvero al di là di esiti misurati dai pazienti) dei sistemi e processi di valutazione critica dei farmaci.
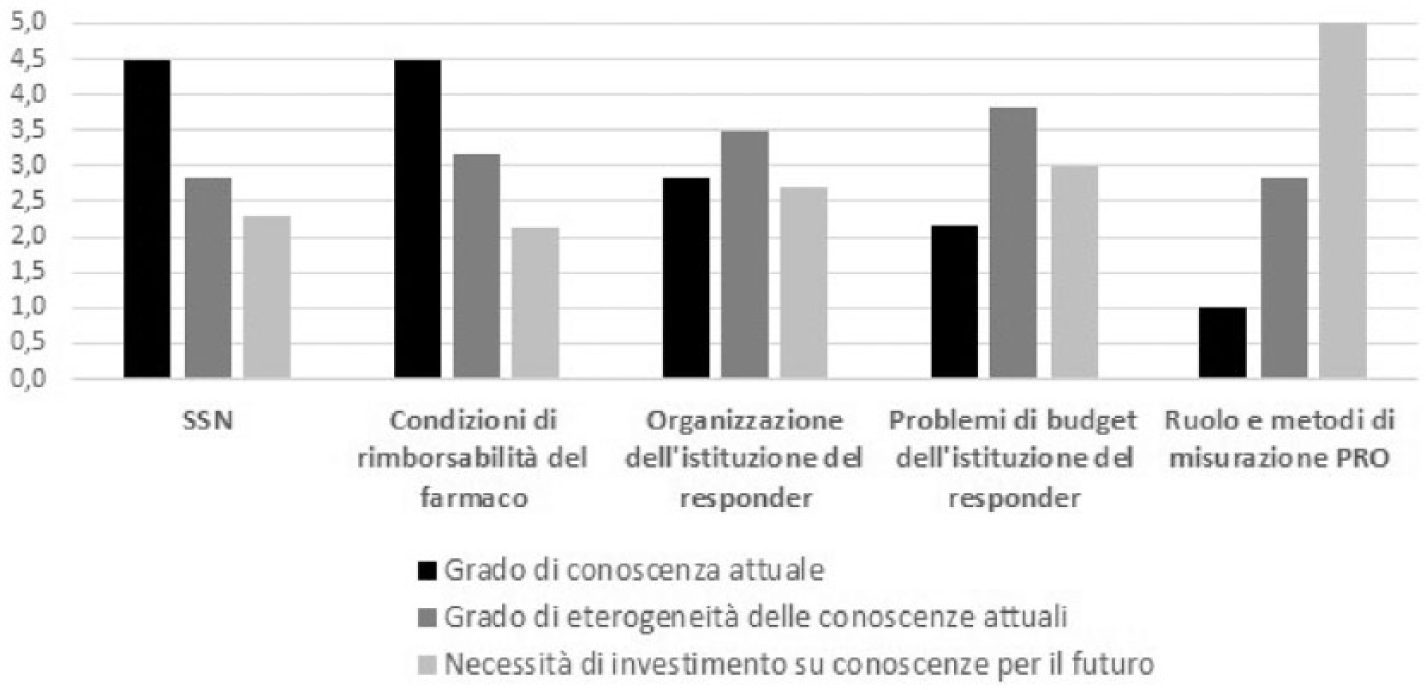
Percezione sul grado e variabilità della conoscenza delle APA su alcune tematiche rilevanti e conseguente necessità di investimento futuro (valore medio nel ranking tra i responder)*.
Molto variabile è la percezione circa gli aspetti per i quali risulta più utile il rapporto con le AP (Indice W di Kendall pari al 15%). Il contributo sulle azioni di governo del percorso terapeutico e, più in generale, del processo assistenziale (PDTA – Percorso Diagnostico Terapeutico Assistenziale), l’erogazione a pazienti di informazioni sui farmaci (ad esempio, azioni finalizzate ad aumentare l’aderenza al trattamento) ed aspetti di tipo amministrativo sull’accesso (ad esempio, esenzioni alla compartecipazione alla spesa) e la segnalazione di problematiche di accesso alle terapie (ritardo nell’inserimento dei farmaci nei prontuari e nella individuazione dei centri autorizzati alla prescrizione / dispensazione dei farmaci) sono in media equamente valutati, ma il livello di accordo sul ranking è molto basso, evidenziando importanti incertezze sulla tematica. È emerso invece un generale consenso sul fatto che non sia particolarmente rilevante il contributo dei pazienti su evidenze / dati di real world (Figura 3).
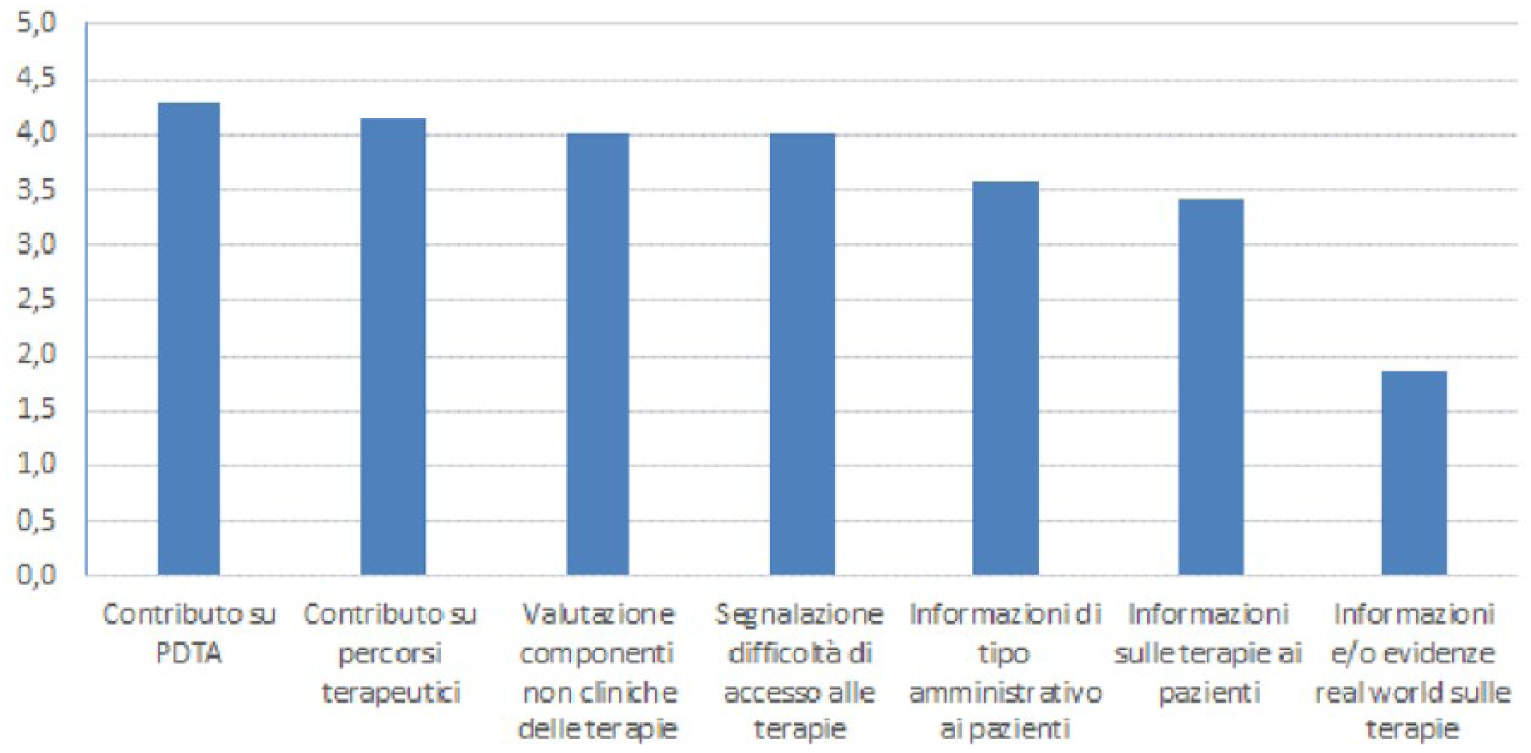
Opinione su aspetti per cui le AP possono fornire un contributo utile al SSN (valore medio nel ranking tra i responder)*.
Con riferimento, in particolare, al contributo fornito dalle AP alla valutazione dei nuovi farmaci, è interessante osservare come il supporto alla valutazione dei benefici (qualità della vita e dimensioni non cliniche, quali formulazioni più accettabili, intervalli liberi da trattamento), sia più rilevante rispetto alla valutazione di impatto sulle dimensioni economiche non sanitarie (costi di trasporto dei pazienti, costi collegati all’assistenza informale dei pazienti, costi collegati alla perdita di produttività) (Indice W di Kendall pari a 0,22) (Figura 4).
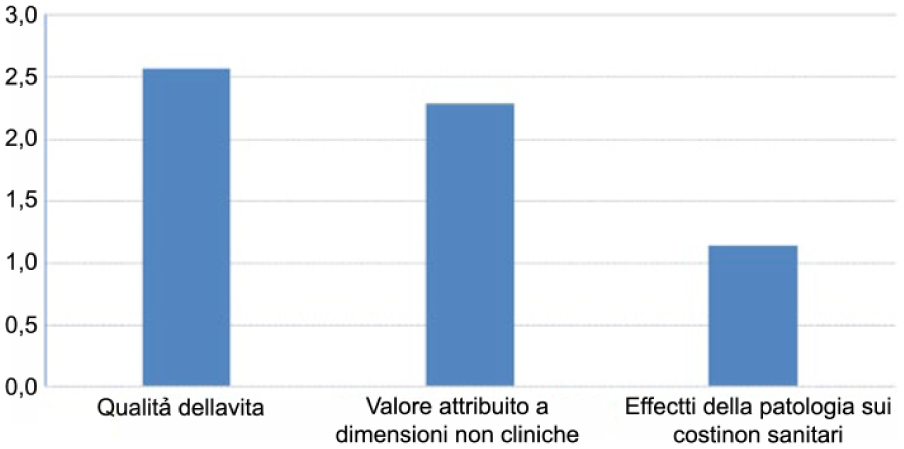
Percezione su utilità delle AP nel supporto alla valutazione di componenti di impatto di un farmaco / tecnologia sanitaria (valore medio nel ranking tra i responder)*.
I maggiori ostacoli all’interazione con le AP sono riferiti ad aspetti organizzativi più che a competenze. In particolare, il loro alto numero e la difficoltà di fare interagire le AP su tematiche comuni, nonché la difficoltà generata dalla presenza di un unico interlocutore per le AP di minori dimensioni, sono state evocate come i principali ostacoli all’interazione (Figura 5). È interessante osservare come i responder non considerino, come ostacolo, l’eventuale approccio rivendicativo (più che collaborativo) delle AP: questa posizione può derivare o dalla circostanza che le AP di fatto collaborino più che rivendicare o che è proprio una maggiore collaborazione a generare approcci meno rivendicativi.
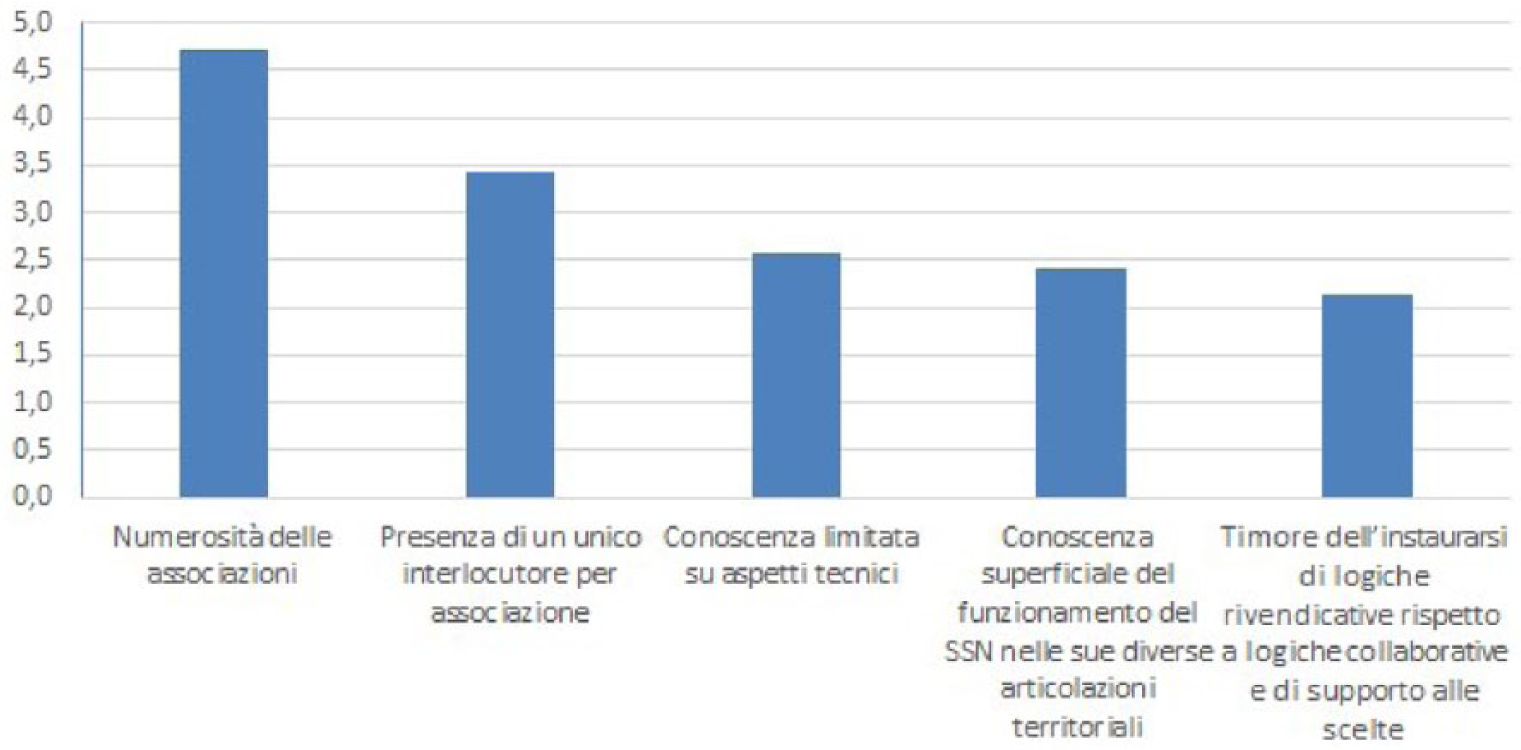
Principali ostacoli ad un’interazione più strutturata con le AP (valore medio nel ranking tra i responder)*.
La percezione dei responder è che il ruolo delle AP sia destinato ad aumentare in futuro. In particolare, ISS ha segnalato l’attivazione di contatti con AP per avviare un programma di coinvolgimento sistematico sul processo di valutazione delle tecnologie, generazione di evidenza e produzione di linee guida nell’ambito del Sistema Nazionale Linee Guida. AIFA ha ribadito l’utilità di incontri mensili (Open AIFA) come strumento di interazione privilegiato con le AP. In questa prospettiva gli interlocutori istituzionali coinvolti hanno evidenziato come le AP possano attivarsi, in ordine di priorità percepita (i) su progettualità di formazione finalizzate ad aumentare le proprie competenze e contribuire quindi ad una corretta valutazione dei farmaci, ad una gestione appropriata degli stessi e ad una maggiore aderenza al trattamento; (ii) su iniziative di comunicazione ai propri pazienti sulle regole di accesso ai farmaci, per contribuire anche con tali iniziative, ad una gestione appropriata delle terapie; (iii) su progetti di ricerca finalizzati a valutare l’impatto dei farmaci, soprattutto in fase di post marketing.
Discussione
La letteratura sulla valutazione delle nuove tecnologie richiama la necessità di un approccio multidisciplinare ed il coinvolgimento, almeno nelle fasi di prioritizzazione e valutazione, dei diversi portatori di interesse. Il coinvolgimento degli stakeholder, e in particolare dei pazienti, è stato analizzato in diversi contributi, ma ad oggi esistono poche evidenze sulla situazione in Italia e analisi limitate sulla percezione dei soggetti preposti alla valutazione delle tecnologie sanitarie su aspetti positivi, criticità e prospettive future dell’interazione con le AP.
Scopo della presente analisi è stato quello di fornire una prima indicazione su tali aspetti, con riferimento in particolare alla valutazione dei farmaci. Tale analisi, per quanto riferita ai due soggetti nazionali deputati direttamente alla valutazione dei farmaci a fini della negoziazione delle condizioni di accesso e prospetticamente alla valutazione delle tecnologie sanitarie e cinque realtà regionali, mostra già un quadro molto frammentato nell’intensità e modalità di coinvolgimento delle AP. Alla frammentazione del quadro delle interazioni si aggiunge un disallineamento abbastanza marcato sulle valutazioni di natura percettiva, con la sola eccezione degli aspetti per i quali le AP sono risultate, agli occhi dei soggetti pubblici, più preparate.
Un primo interessante aspetto che emerge dall’analisi è la diversa lettura del concetto di relazione “sistematica”: da una parte alcune regioni considerano sistematica la relazione in quanto le AP sono rappresentate / presenti nelle commissioni di riferimento (commissioni terapeutiche regionali, commissioni regionali del farmaco); dall’altra, la natura sistematica dell’interazione è stata ricondotta da AIFA all’attivazione di relazioni ogni qual volta si pongono problematiche importanti da risolvere. Una visione più avanzata del rapporto con le AP dovrebbe includere entrambi gli aspetti, ovvero la presenza permanente in commissioni e l’attivazione sistematica di forme qualificate di interazione quando ci sono problemi specifici di valutazione e/o di accesso.
Un secondo elemento di riflessione riguarda l’oggetto dell’interazione. Le indicazioni fornite dai soggetti istituzionali intervistati fanno chiaramente percepire come le AP abbiano ormai maturato una buona conoscenza del SSN e siano molto sensibili alle condizioni di rimborsabilità dei farmaci, argomento su cui interagiscono maggiormente con le istituzioni. A questo proposito è interessante osservare come Regione Sicilia, caratterizzata rispetto alle altre realtà regionali da una minore intensità di relazioni con le AP, abbia richiamato l’attenzione sul fatto che tali associazioni abbiano spesso interagito indirettamente ed ex post con la Commissione del Prontuario Terapeutico Ospedaliero della Regione Sicilia, supportando le Società Scientifiche nella richiesta di modifica della decisione di non inserire un farmaco nel prontuario regionale.
A fronte di tali conoscenze sul sistema sanitario e sugli aspetti regolatori / di accesso, la percezione dei responder è che sia minore nelle AP la sensibilità sulla valutazione di impatto economico delle terapie e sugli effetti che tali terapie hanno sull’equilibrio economico-finanziario complessivo, sulla conoscenza dell’organizzazione degli istituti pubblici e, soprattutto, sulle componenti di valutazione dei farmaci espresse dai pazienti (PRO). A questo proposito si osserva come l’attenzione per i PRO in Italia sia ancora piuttosto bassa: si pensi solo al fatto che la qualità di vita è stata inclusa come uno degli indicatori di valutazione di un farmaco solo nella recente Determina Aifa sui criteri per la classificazione dei farmaci innovativi e dei farmaci oncologici innovativi (Determina 519/2017). Una maggiore conoscenza dei PRO da parte delle AP ed un loro ruolo proattivo nell’adozione di approcci rigorosi nella valutazione dei PRO, potrebbe produrre un circolo virtuoso positivo che darebbe a tali indicatori di esito un peso maggiore rispetto a quello che hanno attualmente.
L’acquisizione di maggiori competenze (ed il riconoscimento delle stesse) non rappresenta però l’unico aspetto da promuovere per un’interazione più matura con le AP. I soggetti istituzionali hanno chiaramente espresso una richiesta di integrazione tra AP su tematiche comuni o aree terapeutiche omogenee, per evitare una frammentazione non facilmente gestibile.
Due regioni hanno posto come elemento aggiuntivo di riflessione il ruolo che l’industria farmaceutica ha nel finanziamento delle AP e del possibile impatto che tale finanziamento può avere sul conflitto di interessi. Tale riflessione sembra rifarsi più ad un approccio istituzionale alla gestione del conflitto di interessi, tipico, in Europa, dei Paesi Continentali, con sistemi di accreditamento delle AP sulla base anche dell’intensità delle relazioni con l’industria (5). Se esiste una sensibilità regionale sul tema è però bene che questo venga affrontato, promuovendo un approccio più vicino a quello pragmatico anglosassone. Tale approccio prevede che gli esperti non possano partecipare alla valutazione di farmaci e tecnologie su cui hanno specificamente svolto attività di supporto scientifico e consulenza alle imprese, ma che non vi sia l’esclusione a priori di esperti che abbiano sistematici rapporti con il mondo industriale.
Conclusioni
La presente analisi (oggettiva e percettiva; retrospettiva e prospettica) delle relazioni tra alcuni soggetti istituzionali deputati alla valutazione di farmaci (e tecnologie sanitarie) ed AP ha un importante limite nel ridotto numero di responder e non vuole quindi fornire un dato rappresentativo della situazione italiana.
L’obiettivo è stato quello di avviare una riflessione sistematica su tale tema a partire da un pool di responder comunque autorevoli e rappresentativi di situazioni diverse (livello nazionale / regionale; soggetti focalizzati sulla sola valutazione dei farmaci / soggetti preposti alla valutazione di tecnologie sanitarie; diversa collocazione geografica; diverso posizionamento rispetto ai vincoli di bilancio pubblico). Tale riflessione può quindi dare indicazioni interessanti sulla gestione futura della relazione tra AP e soggetti valutatori di farmaci (e tecnologie sanitarie).
Queste indicazioni, esposte nel precedente paragrafo, si collocano in un contesto ancora molto diverso da realtà a realtà, ma caratterizzato da due elementi di grande interesse, desunti dall’analisi percettiva dei responder. Dall’esperienza con le AP non trapela né la presenza di frequenti situazioni conflittuali (generate da approcci rivendicativi) né la riflessione che il rafforzamento della voce dei pazienti possa generare in futuro un aumento della pressione rivendicativa rispetto a quella collaborativa. Viene anzi esplicitato che la maturazione e sistematizzazione di tale relazione possa generare un approccio sempre più collaborativo sia sulla valutazione tecnica sia sulle soluzioni per garantire accesso a terapie ad alto valor aggiunto per il SSN. Il secondo elemento è che il rafforzamento del ruolo dei pazienti nella valutazione genera crescenti aspettative sulle loro conoscenze sui metodi per la valutazione di impatto dei farmaci e delle tecnologie sanitarie sui benefici, con riferimento sia alle dimensioni del valore che sono espresse dai pazienti stessi (PRO) sia su quelle che sono maggiormente considerate dai pagatori (esiti clinici), e sui costi.
Questo approccio mutualmente benefico può garantire che il rafforzamento della voce dei pazienti venga effettivamente percepito come opportunità per il SSN.
Ringraziamenti
Si ringraziano, per avere contribuito alla realizzazione dello studio compilando il questionario e rivedendo il draft dell’articolo, Mario Melazzini (Direttore Generale, AIFA), Marco Marchetti (Centro Nazionale Health Technology Assessment, ISS), Massimo Medaglia e Maurizio Bersani (U.O. Programmazione Polo Ospedaliero, Direzione Generale Welfare, Regione Lombardia), che hanno compilato un unico questionario, Giovanna Scroccaro (Coordinamento Regionale Unico sul Farmaco, Regione Veneto), Anna Maria Marata (Area valutazione del farmaco, Servizio Assistenza Territoriale, Regione Emilia-Romagna), Lorella Lombardozzi (Area Risorse Farmaceutiche, Direzione Regionale Salute e Politiche Sociali), Gianluca Trifirò (Commissione Prontuario Terapeutico Ospedaliero Regione Sicilia).
Si ringraziano le Associazioni aderenti al progetto ‘Persone non solo Pazienti’. ‘Persone non solo Pazienti’ è un progetto di Roche, realizzato nell’ambito delle attività finalizzate all’ascolto dei bisogni istituzionali delle AP e delle persone che loro rappresentano, e vede il coinvolgimento di 16 Gruppi AP, che insieme hanno costruito un percorso con l’obiettivo di parlare con un’unica voce alle Istituzioni. A tali Associazioni è stato chiesto di validare il questionario. Si tratta di: ACTO Onlus – Alleanza contro il tumore ovarico; AISM – Associazione Italiana Sclerosi Multipla; AMA Fuori dal Buio – AMA Associazione Malati Autoimmuni Orfani e Rari; AMICI Onlus – Associazione Nazionale per le Malattie Infiammatorie Croniche dell’Intestino; ANMAR Onlus – Associazione Nazionale Malati Reumatici; APMAR Onlus – Associazione Nazionale Persone con Malattie Reumatologiche e Rare; Europa Donna Italia; Famiglie SMA Onlus – Genitori per la Ricerca sull’Atrofia Muscolare Spinale; FAVO – Federazione italiana delle Associazioni di Volontariato in Oncologia; FedEmo – Federazione delle Associazioni Emofilici; FIMARP – Federazione Italiana Malattie Rare Polmonari; Fondazione Paracelso Onlus; La Lampada di Aladino Onlus – Oltre il Cancro; LIFC Onlus – Lega Italiana Fibrosi Cistica; Salute Donna Onlus; WALCE - Women against Lung Cancer in Europe; Salute Donna Onlus.
Footnotes
Funding
The author(s) declared the following financial support for the research, authorship, and/or publication of this article: Si ringrazia infine Roche SpA per il contributo incondizionato alla ricerca fornito a Cergas SDA Bocconi.