Abstract
Introduction:
Renal cell carcinoma (RCC) is the most common form of kidney cancer with >30% already metastatic at diagnosis. For patients who fail tyrosine kinase inhibitor (TKI) therapy, the Italian Medical Oncology Association recommends (level IA) nivolumab and cabozantinib. The aim of this study was to compare the cost-effectiveness of cabozantinib with nivolumab for treatment of adult patients with mRCC following prior TKI therapy in Italy.
Methods:
A partitioned survival (area under the curve) model was developed for the Italian medical environment. Cost-effectiveness was assessed from the Italian National Healthcare Service (SSN) perspective over a 30-year time horizon (annual discount: 3% rate). In the absence of head-to-head studies, clinical evidence was based on results of network meta-analysis. Health-state-related utilities were informed by EQ-5D data from the METEOR study. Resource use and costs were obtained from published sources.
Results:
Treatment with cabozantinib dominates nivolumab across a 30-years time horizon. In the reference case, treatment with cabozantinib results in an incremental 0.268 quality-adjusted life years (QALY) and an incremental 0.349 life years (LY) gained with a total saving, for the Italian SSN, of €5,605 compared to nivolumab over 30 years. Cabozantinib is associated with gains in quality adjusted life years versus nivolumab, in all analyses. Results were shown to be sensitive to drug prices variation and robust when altering other parameters.
Discussion:
Cabozantinib represents an efficient option in the management of mRCC after initial TKI-therapy in Italy. Drug prices impact final results, and this must be carefully considered, especially considering the confidential discounts and outcome/financial-based agreements currently in place in Italy.
Introduzione
Il tumore del rene è un insieme di tumori localizzati a livello del parenchima renale che rappresentano circa il 2.4% di tutti i tumori a livello globale. 1 Il carcinoma renale o a cellule renali (RCC) rappresenta la forma più comune (75%) di tumore maligno del rene. Nel 2012 in tutto il mondo sono stati diagnosticati circa 330,000 nuovi casi e sono stati registrati 140,000 decessi per RCC.1,2
I casi stimati di tumori del rene in Italia nel 2017 sono circa 11,500. 3 Il trend di incidenza del tumore del rene appare sostanzialmente stabile negli ultimi anni, dopo essere incrementato costantemente per alcuni decenni, come anche stabile è oggi la sua mortalità. Nel 2014 sono stati registrati in Italia 3371 decessi per tumore del rene. 3 Il rischio di sviluppare un tumore del rene è estremamente basso nelle fasce di età più giovani e aumenta progressivamente all’aumentare dell’età. La sopravvivenza media a 5 anni in Italia è pari al 71%, con un forte gradiente per età, oltre che in base allo stadio della malattia alla diagnosi. 3 Dati provenienti da un ampio database americano hanno mostrato, infatti, differenze significative nella sopravvivenza della malattia a tre anni tra i diversi stadi di RCC: dal 97% per la malattia localizzata di stadio I al 93%, 81% e 13% rispettivamente per gli stadi II, III e IV. 4
Il tumore del rene spesso resta clinicamente silente per la maggior parte del suo corso: nel 30% dei casi, infatti, il riscontro è occasionale. Nel 35% circa dei casi il tumore si presenta in fase metastatica già alla diagnosi e, nel 25% circa dei casi, la malattia si ripresenta in fase metastatica dopo una chirurgia con intento curativo. 5
Negli ultimi dieci anni il panorama del trattamento del RCC metastatico si è drammaticamente evoluto, a partire dall’epoca dell’immunoterapia basata sulle citochine (di cui pochi pazienti hanno tratto beneficio, a spese di elevate tossicità) fino all’attuale era dei farmaci target e dei nuovi immunoterapeutici, che hanno migliorato notevolmente la prognosi dei pazienti. 6 Questo fenomeno ha avuto un forte impatto sulla sopravvivenza dei pazienti affetti da carcinoma renale metastatico che, infatti, è in continuo aumento: da 2000 in poi rispetto all’ultimo decennio del secolo scorso, si è registrato un incremento assoluto di 25 e 11 punti percentuali, rispettivamente, negli USA e in Italia, che rappresenta uno dei maggiori risultati ottenuti, in gran parte legato alle terapie target innovative utilizzate negli ultimi 13 anni.7,8
Le principali società scientifiche internazionali si sono espresse con raccomandazioni circa il trattamento del RCC metastatico, sia per la prima che per la seconda linea di terapia. In particolare, le linee guida dell’ European Society for Medical Oncology (ESMO) considerano come trattamenti standard di seconda linea post-TKI (tyrosine kinase inhibitor) nei pazienti con RCC nivolumab (livello di evidenza IA) e cabozantinib (IA). 9 Nella popolazione di pazienti trattati con citochine in prima linea, popolazione ormai del tutto virtuale, vengono raccomandati i TKI, axitinib (IIA), sorafenib (IA) e pazopanib (IIA). 9
Le più recenti linee guida nazionali relative al tumore renale dell’Associazione Italiana di Oncologia Medica (AIOM) raccomandano come trattamento di seconda linea post-TKI nivolumab e cabozantinib (raccomandazione positiva forte), mentre axitinib ha una raccomandazione positiva debole. 10 In particolare, in considerazione della mancanza di studi di confronto diretto fra cabozantinib, nivolumab e axitinib e della disponibilità di metanalisi di confronto indiretto fra everolimus e axitinib, le linee guida italiane indicano che i pazienti in progressione dopo il trattamento con un TKI dovrebbero ricevere preferenzialmente un trattamento con nivolumab o cabozantinib, piuttosto che con axitinib. Le stesse linee guida forniscono una raccomandazione negativa per everolimus e sorafenib. 10
Cabozantinib è un farmaco orale recentemente disponibile in Italia per il trattamento del RCC avanzato negli adulti precedentemente trattati con terapia contro il fattore di crescita dell’endotelio vascolare (VEGF).11,12 A differenza degli altri farmaci disponibili per il trattamento del RCC in seconda linea, con meccanismo TKI anti VEGF (axitinib e sorafenib), cabozantinib inibisce non solo i recettori del VEGF, ma anche i recettori MET e AXL. L’inibizione di MET e AXL sembra essere un meccanismo di azione chiave per cabozantinib, dal momento che questi recettori sono implicati nella resistenza acquisita alla terapia anti-VEGF. 13 Cabozantinib ha dimostrato benefici clinici significativi, rispetto ad un comparatore attivo (everolimus), in pazienti con RCC avanzato o metastatico precedentemente trattati con inibitori VEGF, su tre endpoint chiave: sopravvivenza globale (OS), sopravvivenza libera da progressione (PFS) e tasso di risposte obiettive (ORR).10,12,14
Nel panorama, quindi, delle terapie disponibili per il trattamento di seconda linea post-TKI dei pazienti con RCC metastatico, nivolumab e cabozantinib risultano essere i farmaci con le più forti raccomandazioni internazionali e nazionali all’utilizzo, nonché i farmaci con l’efficacia più robusta.9,10 Appare chiaro quindi che il loro rispettivo ruolo in terapia sia ampiamente dibattuto, alla luce dei differenti meccanismi d’azione, velocità nell’istaurarsi del beneficio clinico e profili di tossicità.
L’obiettivo di questa analisi è stato quindi quantificare e confrontare i costi e i benefici clinici (efficacia e sicurezza) dei farmaci cabozantinib e nivolumab, nel trattamento dei pazienti affetti da RCC avanzato/metastatico precedentemente trattati con inibitori VEGF nel contesto italiano.
Metodi
Descrizione del modello
Il modello utilizzato nella presente analisi è un partitioned survival model sviluppato in Microsoft® Excel, sulla base della struttura di modelli economici precedenti utilizzati per la simulazione dell’evoluzione dell’RCC metastatico.15–17 Nei modelli partitioned survival, come dettagliato successivamente, l’appartenenza a uno stato di salute viene determinata in base alle curve parametriche di sopravvivenza e al tempo medio trascorso in ogni rispettivo stato di salute, determinato in base alla area sotto la curva.
Questo modello, utilizzato anche per la sottomissione al NICE (The National Institute for Health and Care Excellence) di cabozantinib, 18 simula l’evoluzione della malattia attraverso la transizione verso stati successivi, secondo probabilità definite. Il modello considera tre stati di salute: pre-progressione, post-progressione e morte. I pazienti che hanno già sperimentato il fallimento nella prima linea di trattamento per RCC metastatico con un inibitore VEGF passano al trattamento con farmaci indicati in seconda linea, con i quali possono tenere sotto controllo la patologia (pre-progressione), o sviluppare un’ulteriore progressione (post-progressione) per la quale il paziente può essere suscettibile di un ulteriore trattamento attivo o della best supportive care. La morte è uno stato cosiddetto assorbente, da cui non sono possibili ulteriori transizioni. La durata di ogni ciclo è fissata in 4 settimane (28 giorni).
La transizione dei pazienti tra i diversi stati di salute durante ogni ciclo è definita tramite i dati di sopravvivenza (OS) e di PFS (percentuale di pazienti nello stato di pre-progressione). L’efficacia dei trattamenti inclusa nel modello è basata sui dati dello studio di fase III di cabozantinib (METEOR) e su una Network Meta-analisi (NMA) delle curve parametriche di sopravvivenza osservate nello studio METEOR e in altri RCT di fase III.
L’analisi di costo-efficacia è stata applicata al contesto italiano considerando la prospettiva del Servizio Sanitario Nazionale. L’orizzonte temporale considerato nel modello è di 30 anni. Pertanto, costi e benefici clinici sono stati scontati ad un tasso pari al 3% annuo (in linea con le raccomandazioni Italiane del Gruppo di lavoro AIES). 19
Per valutare il parametro di costo-efficacia, è stato utilizzato il rapporto incrementale di costo-efficacia, ICER (Incremental Cost Effectiveness Ratio). L’ICER descrive le risorse aggiuntive che devono essere utilizzate per ottenere il beneficio aggiuntivo e si calcola misurando la differenza di costo (ΔC) divisa per la differenza di efficacia (ΔE) tra due alternative proposte. I farmaci che sono stati confrontati nell’analisi sono cabozantinib e nivolumab.
Parametri clinici
Il modello economico è stato inizialmente sviluppato sulla base dei dati provenienti dallo studio METEOR 14 e aggiornato con i risultati dell’ultimo data cut-off del 2 ottobre 2016, che include ulteriori nove mesi di follow-up e altri 110 eventi. 18 Questi risultati mostrano che, a 30 mesi di follow-up, il 35% dei pazienti trattati con cabozantinib è ancora vivente, rispetto al 25% dei pazienti trattati con everolimus, e che le curve di Kaplan-Meier continuano a separarsi piuttosto che a convergere. 18
Nelle simulazioni fra cabozantinib e nivolumab, non essendo disponibili trial clinici di confronto diretto fra questi farmaci, sono stati utilizzati i risultati provenienti da una NMA, alimentata dai risultati degli studi clinici registrativi. Tale NMA, recentemente pubblicata 20 e impiegata nella sottomissione originale al NICE, 18 è stata utilizzata nell’analisi di base per confrontare, secondo il metodo ampiamente validato ed utilizzato di Ouwens e collaboratori, 21 più distribuzioni parametriche di sopravvivenza (lognormal, loglogistic, Weibull, Gompertz e distribuzioni esponenziali).
È stata condotta, inoltre, un’analisi alternativa per il confronto fra cabozantinib e nivolumab utilizzando una seconda NMA, condotta con il metodo dei fractional polynomials sviluppato da Jansen. 22 Questa analisi alternativa era stata richiesta dal NICE durante il processo di valutazione, per esplorare un diverso metodo di fitting dei dati provenienti dagli studi clinici. Il metodo dei fractional polynomials è particolarmente adatto per i dati non lineari e permette un approccio multidimensionale all’effetto del trattamento. 22 In altre parole, l’effetto del trattamento è rappresentato da più parametri invece che da uno o due parametri utilizzati dal metodo di Ouwens nelle distribuzioni lognormal, loglogistic, Weibull, Gompertz e distribuzioni esponenziali.
I dati provenienti dalle NMA sono stati utilizzati per calcolare la percentuale di pazienti in ciascuno stato di salute, in ogni momento dopo l’inizio del trattamento. I valori di utilità legati agli stati di salute (Health Related Quality Of Life - HRQoL) sono stati ripresi, nell’analisi di base dallo studio METEOR, durante il quale erano stati misurati utilizzando l’EuroQol Health questionnaire instrument (EQ-5D-5L) (Tabella 1). 14
Valori di utilità utilizzati nell’analisi di costo-efficacia. 14
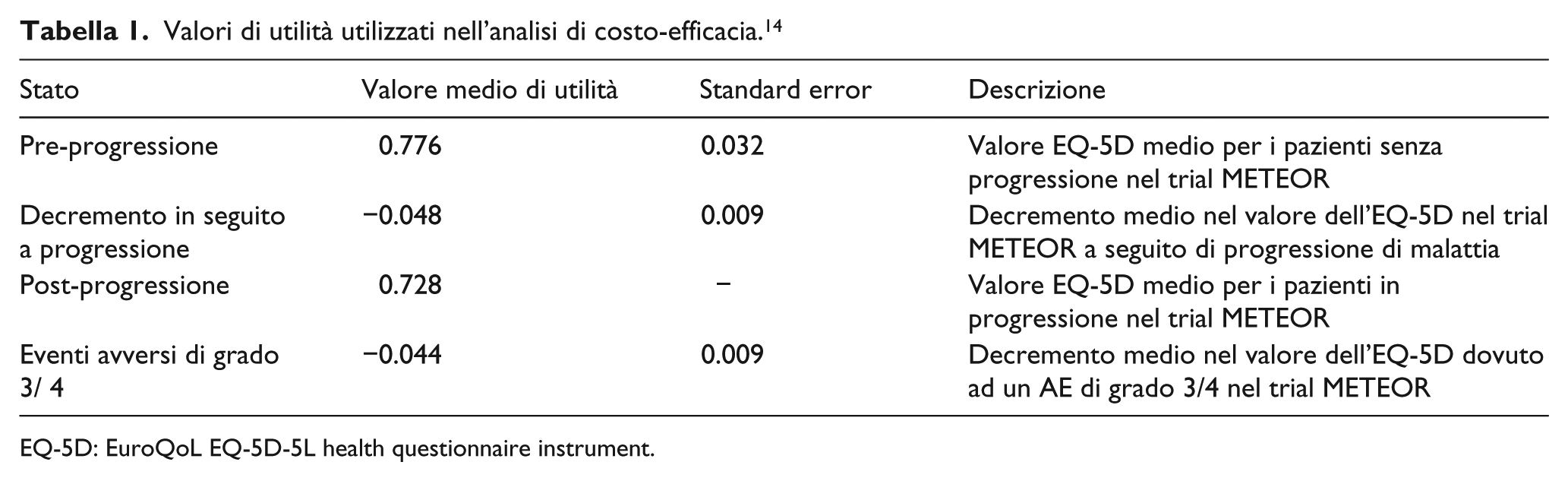
EQ-5D: EuroQoL EQ-5D-5L health questionnaire instrument.
Nel modello sono stati inclusi gli eventi avversi, considerati come eventi temporanei, associati a costi aggiuntivi e disutilità. Sono stati considerati gli eventi avversi di grado 3/4, riscontrati con una frequenza superiore al 5% negli studi registrativi, e giudicati da un panel di clinici come correlati ad un consumo di risorse sanitarie (Tabella 2).14,23
Eventi avversi considerati nel modello (grado 3/4).
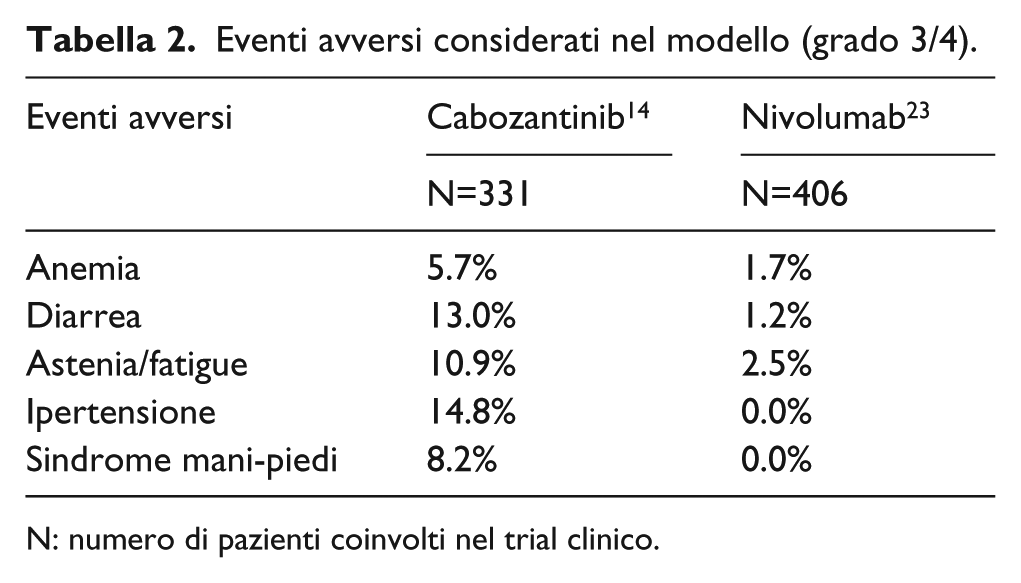
N: numero di pazienti coinvolti nel trial clinico.
Utilizzo di risorse e costi associati
Nell’analisi sono stati considerati i seguenti costi: costi farmacologici, costo degli eventi aversi, costi per la fase di pre-progressione, costi per la fase di post-progressione e costi di fine vita.
Costi farmacologici
Il costo dei farmaci è stato desunto dalla pubblicazione delle relative delibere autorizzative nella Gazzetta Ufficiale e si riferisce al prezzo ex-factory al netto degli sconti obbligatori (Tabella 3).11,24 La posologia delle terapie considerate è stata ripresa dagli specifici RCP di prodotto:12,25 l’intensità di dose applicata agli specifici trattamenti è ripresa dai trial clinici.15,16 Per cabozantinib, l’intensità di dose è stata fissata pari al 100%, considerato che in Italia è stato negoziato un prezzo uguale per i diversi dosaggi del farmaco. 11 Sebbene nivolumab sia un farmaco infusionale, la posologia recentemente approvata di 240 mg ogni 2 settimane permette una somministrazione del farmaco efficiente dal punto di vista ospedaliero, perciò per lo scopo di questa analisi di costo-efficacia non si è considerato alcuno spreco di farmaco.
Costi, confezioni e posologia dei farmaci considerati nell’analisi economica.

Note: * Prezzi ex-factory al netto degli sconti obbligatori -5%/-5%11,24; ** Calcolo basato su posologia di 240 mg ogni 2 settimane. 25
mg: milligrammo; cpr: compressa; conf: confezione.
Per ciò che riguarda il costo di somministrazione dei farmaci, questo è stato considerato pari a zero per i farmaci orali, mentre per nivolumab, che richiede una somministrazione infusionale ogni 14 giorni, si è usato un valore pubblicato pari a €101.7. 26 Questo importo rappresenta una tariffa media regionale per l’accesso ambulatoriale, a copertura dei costi sostenuti dalla struttura che eroga la prestazione di somministrazione infusionale. 26
I trattamenti successivi alla progressione, ovvero i trattamenti di terza linea, considerati nel modello sono stati ottenuti dallo studio clinico METEOR e dagli RCT utilizzati nella NMA per derivarne l’efficacia comparativa. 14 Il costo dei farmaci post-progressione è stato derivato analogamente agli altri farmaci confrontati nell’analisi.
Costo degli eventi avversi
Il costo unitario da attribuire alla gestione degli eventi avversi di grado 3/4 è stato desunto da una pubblicazione italiana 27 che ha esaminato il costo di gestione degli eventi avversi in pazienti affetti da RCC in Italia (Tabella 4). 27
Costi unitari e/o per evento.
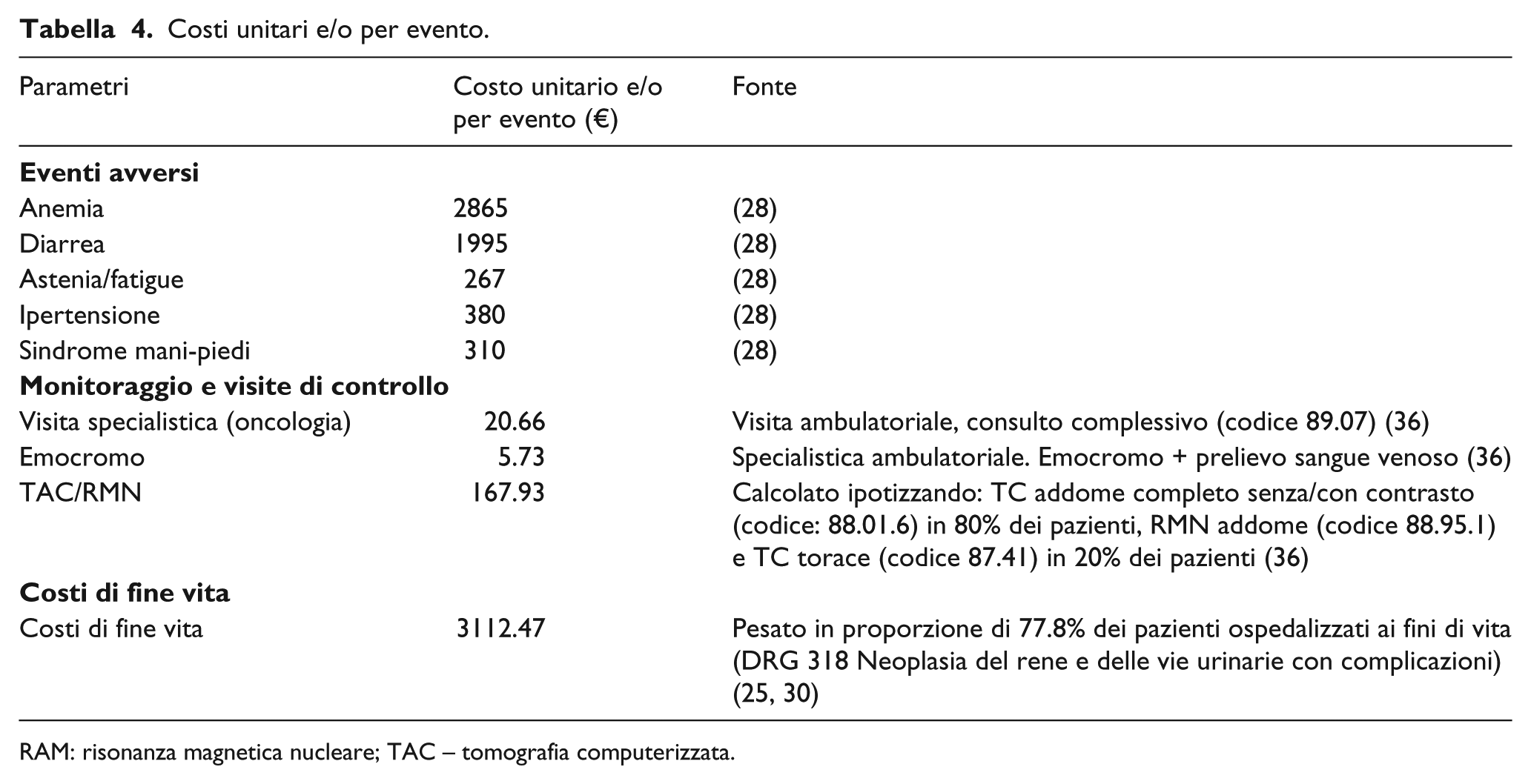
RAM: risonanza magnetica nucleare; TAC – tomografia computerizzata.
Costi della fase di pre-progressione e di post-progressione
Sia per la fase di pre-progressione che per quella di post-progressione, è stato calcolato un costo di follow-up medico corrispondente, nell’arco di un anno, a 12 visite mediche, 4 TAC/RMN e 12 misurazioni del pannello metabolico. Le prestazioni mediche sono state valorizzate in base ai Tariffari Nazionali (Tabella 4). 28
I costi di fine vita sono stati quantificati pari a €3112, sulla base della letteratura italiana disponibile e delle tariffe DRG per il ricovero ospedaliero (Tabella 4). 29
Analisi di sensibilità
Oltre all’analisi di base, condotta utilizzando i dati e le assunzioni sopra descritti, è stata condotta un’analisi di sensibilità deterministica a una via, per identificare i parametri la cui variazione determina il maggior impatto sui risultati. È stata eseguita, in particolare, un’analisi specifica sul prezzo dei farmaci, al fine di valutare l’impatto sui risultati finali di sconti fino al 50%, rispetto ai prezzi ex-factory.
Infine, è stata effettuata un’analisi di sensibilità probabilistica, che ha valutato i risultati del modello sulla base della distribuzione probabilistica di ciascun parametro, considerando media, varianza e forma della distribuzione. I risultati dell’analisi probabilistica hanno consentito di costruire le curve di accettabilità di costo-efficacia di cabozantinib rispetto a nivolumab.
Risultati
Analisi di base
I risultati dell’analisi di base mostrano che cabozantinib ha un profilo farmacoeconomico favorevole rispetto a nivolumab. Nella simulazione, cabozantinib risulta dominante rispetto a nivolumab nel trattamento dei pazienti affetti da RCC avanzato/metastatico precedentemente trattati con inibitori VEGF, producendo allo stesso tempo un incremento della sopravvivenza globale e della sopravvivenza aggiustata per la qualità della vita a fronte di un costo complessivo inferiore rispetto a nivolumab (Tabella 5). Nell’analisi di base, il trattamento con cabozantinib ha prodotto un incremento di sopravvivenza aggiustata per la qualità della vita pari a 0.268 rispetto a nivolumab (quality-adjusted life years (QALY) guadagnati 2.021 e 1.752 per cabozantinib e nivolumab, rispettivamente) lungo l’orizzonte temporale di 30 anni. Il trattamento con cabozantinib si associa ad una sopravvivenza globale maggiore rispetto a nivolumab, sia libera da progressione (PFS) che successiva alla progressione di malattia (PPS), con un incremento di 0.349 LY rispetto a nivolumab.
Risultati dell’analisi di base - cabozantinib versus nivolumab.
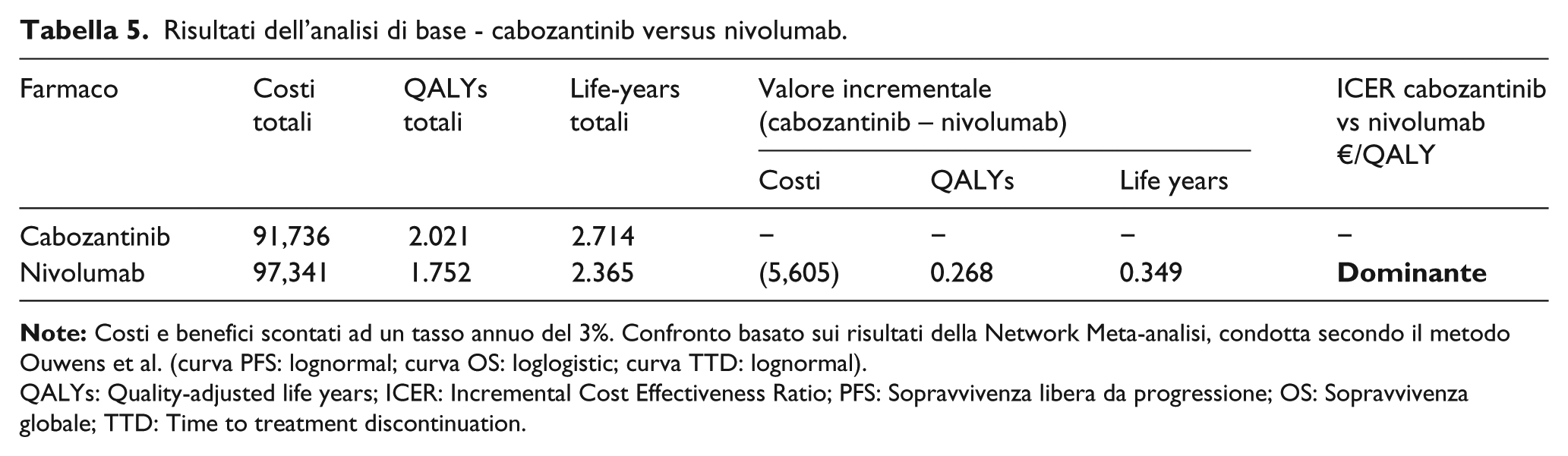
QALYs: Quality-adjusted life years; ICER: Incremental Cost Effectiveness Ratio; PFS: Sopravvivenza libera da progressione; OS: Sopravvivenza globale; TTD: Time to treatment discontinuation.
Il costo di trattamento con cabozantinib, risulta peraltro inferiore rispetto a quello di nivolumab con un risparmio di €5605 su un orizzonte temporale di 30 anni in Italia. I costi complessivi sono guidati in modo preponderante dai costi di acquisizione e somministrazione dei farmaci: i costi farmacologici pesano più dell’80% del totale dei costi, in tutte le simulazioni condotte.
Analisi alternative
I risultati dell’analisi alternativa di cabozantinib verso nivolumab, basata sui risultati della NMA condotta secondo il metodo Jansen, 22 riportano lo stesso trend nel rapporto dei costi ed efficacia dei trattamenti come già evidenziato nell’analisi di base. Sempre con un risparmio nei costi complessivi di trattamento (un risparmio di €2819 rispetto a nivolumab), il trattamento con cabozantinib si associa ad un incremento di 0.128 QALYs e 0.1186 LYs guadagnati rispetto a nivolumab su un orizzonte temporale di 30 anni (Tabella 6).
Risultati dell’analisi alternativa - cabozantinib versus nivolumab.
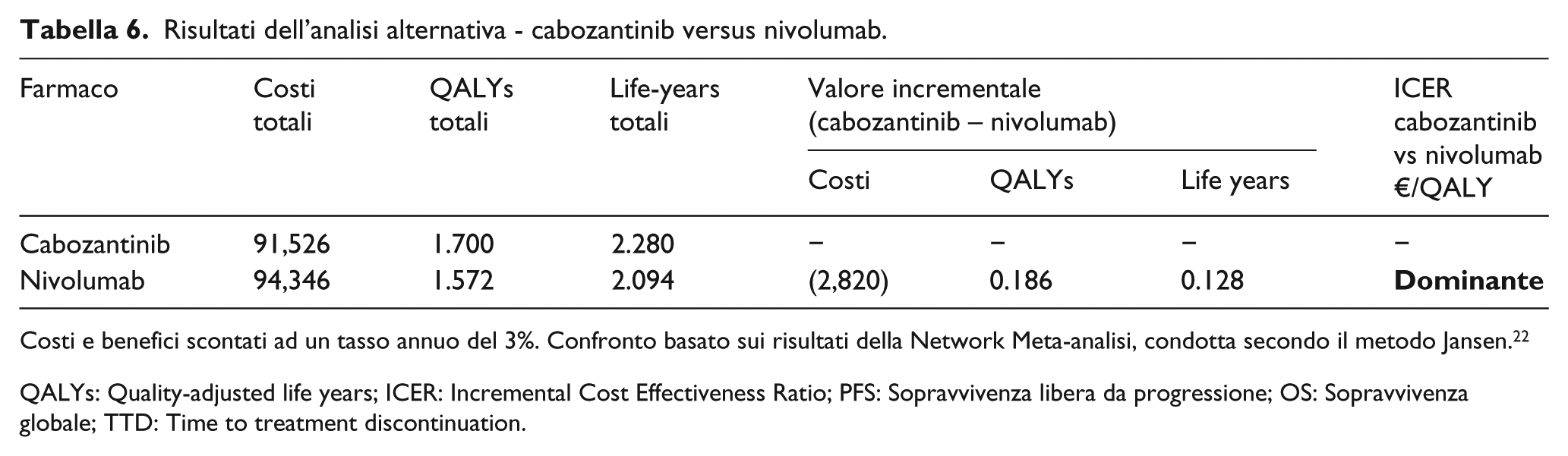
Costi e benefici scontati ad un tasso annuo del 3%. Confronto basato sui risultati della Network Meta-analisi, condotta secondo il metodo Jansen. 22
QALYs: Quality-adjusted life years; ICER: Incremental Cost Effectiveness Ratio; PFS: Sopravvivenza libera da progressione; OS: Sopravvivenza globale; TTD: Time to treatment discontinuation.
Analisi di sensibilità
Nel confronto cabozantinib verso nivolumab, l’analisi di sensibilità deterministica a una via ha evidenziato che i parametri che presentano un maggior impatto sul risultato finale sono: il prezzo dei farmaci, l’esclusione dei costi delle terapie successive alla seconda linea e, in misura minore, i tassi di sconto per costi e benefici e l’orizzonte temporale dell’analisi (Figura 1).
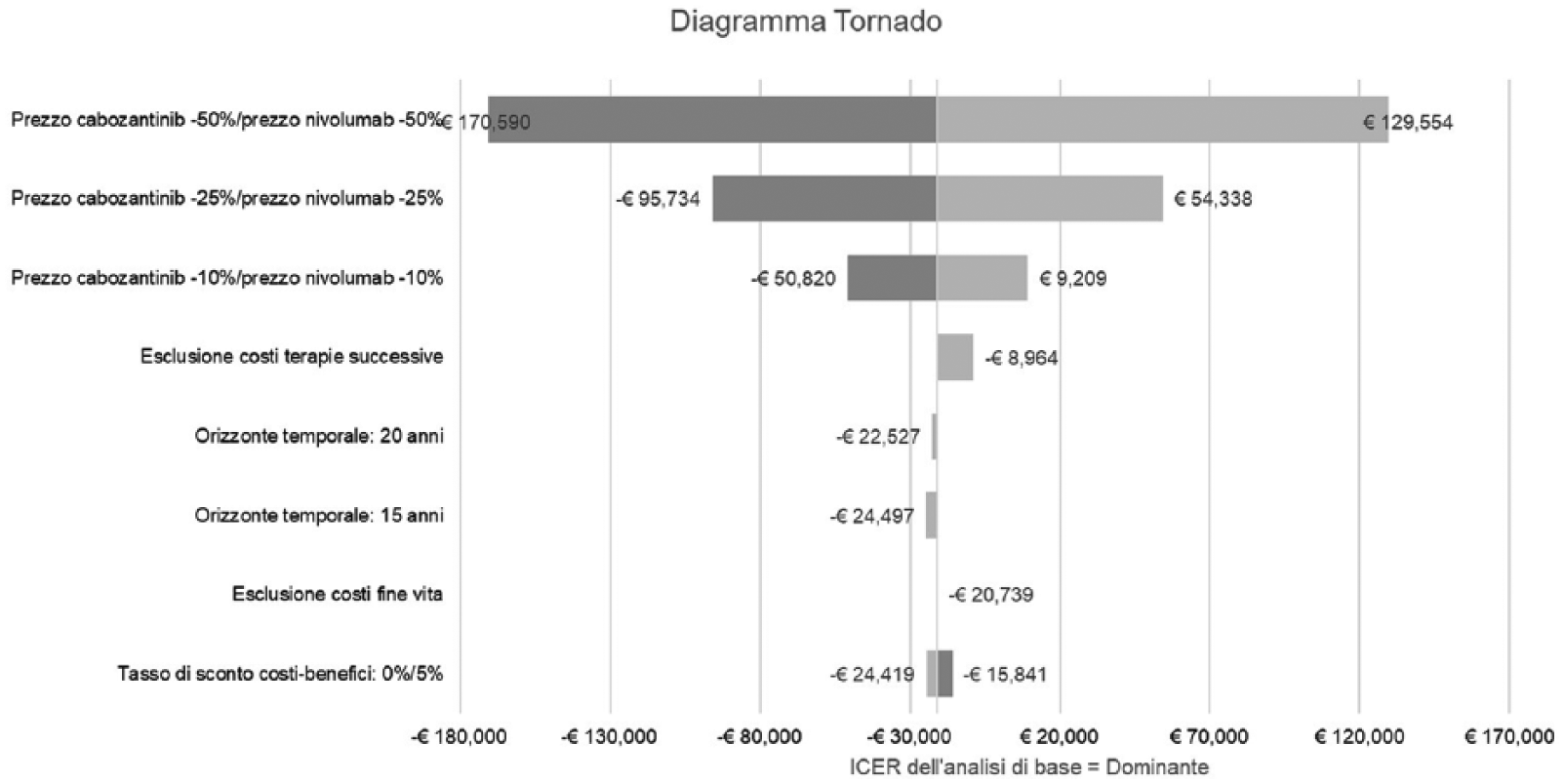
Risultati dell’analisi di sensibilità deterministica a una via - cabozantinib versus nivolumab.
Il prezzo dei farmaci rappresenta la variabile che maggiormente influenza i risultati dell’analisi di costo-efficacia. Nel confronto con nivolumab, i prezzi di entrambi i farmaci si mostrano molto influenti sui risultati finali dell’analisi: in Figura 1 sono riportati alcuni esempi di scontistica applicata all’uno o all’altro farmaco, che mettono in luce l’ampia variabilità dei risultati a seguito della variazione dei prezzi. Ad esempio, uno sconto per nivolumab almeno pari al 10% farebbe sì che, nell’analisi di confronto cabozantinib non risulti strategia dominante, ovvero più efficace e meno costoso, rispetto a nivolumab.
I risultati grafici dell’analisi di sensibilità probabilistica di cabozantinib rispetto a nivolumab, che ha valutato i risultati del modello sulla base della distribuzione probabilistica di ciascun parametro, sono riportati in Figura 2. Gli esiti delle analisi sono rappresentati da un lato nel diagramma scatter plots, all’interno di quattro quadranti in relazione al rapporto di costi e QALYs, dall’altro nella curva di accettabilità per il confronto fra cabozantinib e nivolumab. Nel diagramma scatter plots in ordinata sono riportate le differenze in costi ed in ascissa le differenze in QALYs: i risultati ottenuti mostrano un certo grado di incertezza dei risultati, che comunque si concentrano nel quadrante della costo-efficacia incrementale, in cui più efficace rispetto a nivolumab. Il diagramma della curva di accettabilità riporta in ordinata la probabilità percentuale che il risultato dell’analisi di costo-efficacia sia al di sotto di diverse soglie di accettabilità, riportate in ascissa. Nel grafico vengono evidenziate le soglie comunemente riportate in Italia, ovvero € 25,000 e € 40,000 per QALY guadagnato. Il risultato dell’analisi di costo-efficacia di cabozantinib rispetto a nivolumab ha una probabilità del 81% di collocarsi al di sotto della soglia di € 40,000 per QALY.
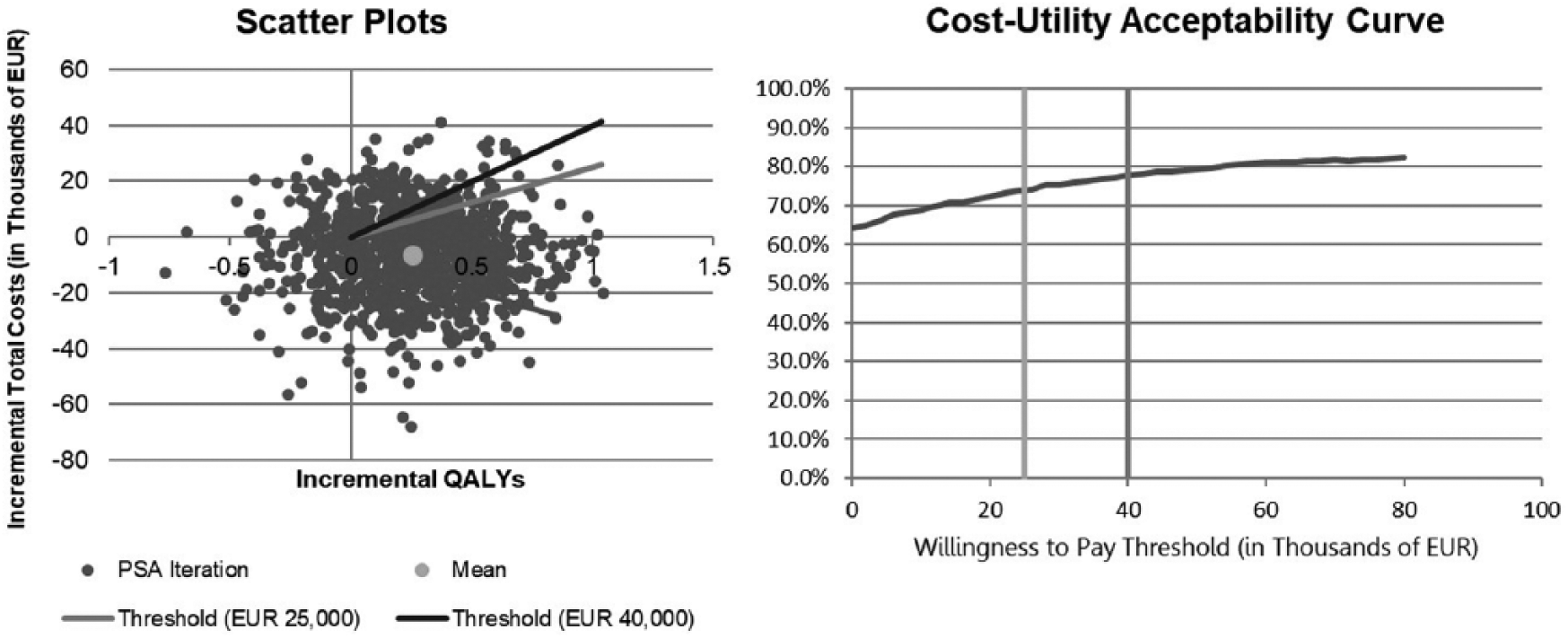
Scatter plot e curva di accettabilità dell’analisi di sensibilità probabilistica cabozantinib versus nivolumab.
Discussione
L’obiettivo di questa analisi economica è stato quello di confrontare il profilo di costo-efficacia di cabozantinib con quello di nivolumab, in quanto principali alternative terapeutiche di seconda linea, utilizzate nel trattamento dei pazienti affetti da RCC avanzato/metastatico precedentemente trattati con inibitori VEGF, nella prospettiva del SSN italiano. In base alle nostre conoscenze, quest’analisi rappresenta la prima valutazione farmacoeconomica, specifica per il contesto italiano, che abbia confrontato i più recenti farmaci introdotti nel trattamento di seconda linea del RCC avanzato/metastatico, nivolumab e cabozantinib.
Dai risultati del modello, cabozantinib emerge come strategia di trattamento dominante rispetto a nivolumab per il SSN italiano. Anche se ad oggi in Italia non esiste una soglia di accettabilità ufficialmente definita, è possibile affermare che i valori di ICER associati a cabozantinib ricadono al di sotto delle soglie individuate in letteratura, e comunemente utilizzate come riferimento (£ 20,000-30,000 da raccomandazioni NICE; 17 €25,000-40,000 da raccomandazioni dell’Associazione Italiana di Economia Sanitaria 19 ).
I risultati dell’analisi sono guidati dalla differenza in termini di benefici clinici, misurati come PFS e OS, tra cabozantinib e nivolumab, così come dalla differenza nei costi di trattamento. Nell’analisi di base cabozantinib risulta più efficace di nivolumab, con un vantaggio in termini di QALY pari a 0.3.
Questa differenza nei benefici clinici è in qualche maniera legata al diverso meccanismo di azione dei due farmaci; cabozantinib, come tutti i TKI, quando funziona tende ad agire precocemente, mentre il tempo di latenza di nivolumab è usualmente maggiore, essendo necessaria l’attivazione e l’espansione delle popolazioni effettrici della risposta immune (e ciò rende tra l’altro ragione dell’iniziale sovrapposizione delle curve di PFS nello studio registrativo di nivolumab). D’altro canto, come tutti i nuovi immunoterapici, nivolumab è in grado di indurre un beneficio di grande durata in una relativamente piccola percentuale di pazienti, caratteristica che, al momento, sembra non condividere con cabozantinib. Appare quindi possibile che queste differenze possano non essere catturate in modo completo ed adeguato da un modello farmacoeconomico come quello qui riportato basato sulla popolazione complessiva dei pazienti affetti con RCC avanzato/metastatico precedentemente trattati con inibitori VEGF.
I risultati dell’analisi di sensibilità a una via hanno dimostrato che i risultati del modello sono più sensibili alle variazioni di costo dei farmaci, orizzonte temporale e tasso di sconto applicato a costi e benefici. Altri input hanno avuto un impatto minimo sui risultati del modello. Il forte impatto dei prezzi dei farmaci sui risultati finali dell’analisi economica deve essere considerato con attenzione, alla luce del fatto che in Italia sono attualmente in vigore sconti confidenziali sui prezzi dei farmaci per il trattamento di numerose neoplasie, tra le quali il RCC avanzato/metastatico, come pure accordi outcome o financial-based.
I risultati emersi dall’analisi di sensibilità probabilistica evidenziano da un lato un’elevata probabilità che cabozantinib sia costo-efficace rispetto a nivolumab, dall’altro la presenza di un certo grado di incertezza associato ai risultati. A causarla concorrono diversi fattori, fra cui l’assenza di uno studio di confronto diretto che permetta di valutare l’efficacia di cabozantinib rispetto a nivolumab e la non disponibilità di dati di efficacia a lungo termine per entrambi i farmaci. Inoltre, l’analisi alternativa basata sul metodo di NMA di Jansen 22 dimostra che i risultanti benefici clinici, sebbene mostrino lo stesso trend complessivo, sono sensibili al diverso metodo NMA impiegato. Come è noto, i modelli di costo-efficacia comportano spesso l’estrapolazione di dati di sopravvivenza globale da end-points surrogati. Il metodo di Jansen offre modelli alternativi per il fitting dei dati provenienti da RCT; tali distribuzioni mostrano una flessibilità maggiore rispetto al metodo di Ouwens et al.21,22 e perciò possono migliorare il fitting statistico, tuttavia il fitting corrisponde alla durata dello studio clinico e non al periodo complessivo di estrapolazione della sopravvivenza globale. È importante sottolineare che in mancanza di dati di real world, l’incertezza nei modelli di costo-efficacia deriva proprio dall’estrapolazione. Oltre al fitting statistico, la scelta del modello per l’analisi di costo-efficacia dipende anche da quanto le stime di sopravvivenza corrispondono ai dati clinici e di real world nella stessa popolazione. 30 Malgrado incertezze innate associate ad ogni estrapolazione di sopravvivenza, la modellistica economica rimane uno degli strumenti indispensabili per prendere decisioni informate. I metodi di Ouwens et al. e Jansen offrono alternative metodologiche nel tentativo di migliorare il fitting statistico e nello stesso tempo rappresentano alternative utili a valutare la rilevanza degli esiti clinici a lungo termine. L’incertezza dei parametri clinici potrà essere parzialmente o completamente superata in futuro quando saranno disponibili ulteriori evidenze da trial clinici o da studi di real world.
I risultati di quest’analisi costituiscono un’ulteriore conferma alle valutazioni precedentemente effettuate dagli istituti di Health Technology Assessment britannici (NICE 18 e il Scottish Medicine Consortium (SMC)) i quali si sono espressi positivamente raccomandando l’utilizzo della tecnologia per il National Healthcare Service (NHS).
Questa analisi è soggetta anche ad altre limitazioni, peraltro comuni a tutti i modelli di simulazione economici, in quanto combina i dati provenienti da diverse e numerose fonti, per ciò implica l’impiego di assunzioni strutturali sui dati inseriti e quindi può essere soggetta a errori. Le prime due limitazioni non possono essere evitate in quanto la motivazione principale per la creazione di qualsiasi modello è la valutazione comparativa delle terapie in assenza di dati completi. Tuttavia, tutte le assunzioni inserite nel modello sono state validate, prima della sottomissione al NICE, per garantire che fossero giustificabili sulla base dei dati esistenti e dell’opinione di un panel di clinici. I dati inseriti nel modello sono stati, inoltre, sottoposti ad analisi di sensibilità. Inoltre, l’utilizzo delle risorse e gli input di costo sono stati popolati utilizzando dati italiani e considerando la pratica medica prevalente di trattamento dell’RCC metastatico.
Nonostante le limitazioni sopraesposte, i modelli di farmacoeconomia svolgono un ruolo importante quando è necessario stabilire indicazioni nello stanziamento delle risorse. Essi, infatti, forniscono ai decisori strumenti utili per scelte più razionali ed efficaci. Raccogliendo i dati appropriati e integrando questi dati all’interno di modelli è possibile ottenere una stima del rapporto costo-efficacia delle diverse strategie di trattamento dei pazienti e fornire elementi significativi da confermare, eventualmente, in valutazioni successive.
I risultati di quest’analisi dimostrano che cabozantinib genera miglioramenti sia in termini di OS che di PFS, che si traducono in un maggior guadagno di anni di vita e di anni di vita aggiustati per la qualità rispetto ad altre terapie di seconda linea considerate. Anche il profilo di costi risulta favorevole rispetto a nivolumab. I risultati dell’analisi di costo-efficacia evidenziano, quindi, che cabozantinib confrontato con nivolumab, l’altro farmaco con le più forti raccomandazioni all’utilizzo in seconda linea di trattamento per RCC, costituisce un’alternativa terapeutica efficace ed efficiente in Italia.
Footnotes
Declaration of Conflicting Interest
The authors declare that there is no conflict of interest.
Funding
This study was supported by an unrestricted grant front IPSEN S.p.A., Milano, Italy.
