Abstract
Background:
Rituximab and trastuzumab were the first monoclonal antibodies (mAbs) approved for the treatment of cancer patients. Both antibodies are administered intravenously (EV), but subcutaneous (SC) formulations have recently been developed. SC formulations proved to be as safe and effective as EV and to offer substantial benefits to the patient.
Objective:
The aim of this study was to provide a multidimensional assessment of the impact of rituximab and trastuzumab SC compared to the EV formulation, providing a particular focus on expected social and economic benefits for the patient.
Methods:
The best established HTA methods were applied to gather and organize evidence concerning the clinical, economic, organizational, social and ethical impact of SC formulations of rituximab and trastuzumab. Social aspects were investigated applying regression methods to data collected with a previous research, while the potential savings associated with the use of SC formulations were estimated by a simple economic model applying the societal perspective.
Results
Patients undergoing subcutaneous formulation are significantly more satisfied with their treatment experience than those treated with intravenous formulation. Subcutaneous formulation reduces patient dosing times, with a positive effect on the care provider’s autonomy and productivity. Potential savings associated with the use of rituximab SC were estimated in € 4,050 per patient per year on average. For trastuzumab SC the estimated potential savings amounted to € 3,400 per patient per year, on average.
Conclusion
Rituximab and trastuzumab are promising treatment options significantly improving patients qol and reducing the treatment burden in terms of societal costs.
Keywords
Background
Rituximab e trastuzumab sono stati tra i primi anticorpi monoclonali (mAb - monoclonal antibodies) approvati per il trattamento dei pazienti oncologici. Entrambi gli anticorpi sono somministrati per via endovenosa (EV), ma recentemente sono state sviluppate formulazioni per la somministrazione sottocutanea (SC). Quest’ultima formulazione di mAb può offrire benefici sostanziali al paziente, rispetto alla somministrazione EV, ma la via SC mostra, per alcuni mAb, anche limitazioni del volume di farmaco introdotto [1].
La ialuronidasi umana ricombinante (rHuPH20) scinde, in modo reversibile, l’acido ialuronico (nei due costituenti fondamentali: acido D-glucuronico e N-acetil-D-glucosamina) permettendo un rilascio SC di volumi di farmaco che non potrebbero altrimenti essere possibili [2,3].
Entrambi i farmaci (trastuzumab e rituximab SC) hanno dimostrato profili di efficacia, sicurezza e farmacocinetica compatibili con le rispettive formulazioni EV. Le reazioni avverse della somministrazione sottocutanea, sebbene siano di base superiori rispetto a quelle verificatesi con la somministrazione endovenosa, si sono dimostrate di lieve o moderata entità [4,5].
Lo studio SABRINA (BO22334) è uno studio di fase III, randomizzato, in aperto, internazionale, multicentrico in pazienti con linfoma follicolare precedentemente non trattati. Lo studio è stato disegnato per valutare la non inferio-rità tra rituximab SC e rituximab EV in termini di: farmacocinetica (Ctrough e AUC) ed efficacia (CR, risposta completa; CRu, risposta completa non confermata; e PR, risposta parziale dopo il completamento della terapia di induzione). I risultati dello studio hanno dimostrato che rituximab SC consente di raggiungere i parametri farmacocinetici di Ctrough e AUC, e risultati di efficacia e sicurezza paragonabili a quelli ottenibili con rituximab EV. In particolare, il valore ottenuto del rapporto tra le medie geometriche di Ctrough SC e Ctrough EV è stato 1,62 [90% CI: 1,36 – 1,94]. Il valore ottenuto dal rapporto tra AUC SC e AUC EV è stato 1,38 (90% CI: 1,241–1,530). [6]
La formulazione sottocutanea mantiene la stessa efficacia clinica in termini di risposta della formulazione endovenosa. Alla fine della fase di induzione il 90,5% dei pazienti nel braccio trattato con rituximab SC ha ottenuto una risposta globale rispetto all’84,4% dei pazienti nel braccio trattato con rituximab EV. La percentuale di pazienti con una risposta completa è risultata pari al 46,0% nel braccio trattato con rituximab SC ed al 29,7% nel braccio trattato con rituximab EV.
Per quanto concerne la sicurezza, l’impiego della formulazione sottocutanea non ha determinato l’insorgenza di nuovi eventi clinicamente rilevanti ed ha presentato un profilo di tollerabilità sovrapponibile alla formulazione endovenosa. L’incidenza delle reazioni correlate alla somministrazione (ARR) è risultata più alta nel gruppo trattato con rituximab SC, ma la maggior parte di tali eventi era di grado lieve-moderato (grado di intensità ≤2) ed era principalmente reazioni cutanee. Allo stesso modo, lo studio di Salar et al. [7] conferma come non siano stati osservati, nel sito di iniezione, danni o eritemi alla cute dovuti alla somministrazione SC. Inoltre, non sono stati riportati eventi avversi di grave intensità in grado di condurre alla morte o a serie complicazioni per la salute. Gli eventi avversi riportati con la formulazione di rituximab SC possono essere correlati con l’equivalente formula-zione endovenosa.
Lo studio HannaH (BO22227) è uno studio di fase III, randomizzato, in aperto, multicentrico, internazionale, condotto nel contesto neoadiuvante/adiuvante in pazienti affetti da EBC HER2 positivo. Si tratta dello studio regi-strativo di fase III per il confronto della farmacocinetica, dell’efficacia e della sicurezza della dose fissa di 600 mg di trastuzumab SC con la farmacocinetica, l’efficacia e la sicurezza della formulazione EV. I risultati dello studio hanno dimostrato che trastuzumab SC ha una farmacocinetica comparabile a quella di trastuzumab EV e un’efficacia non inferiore, raggiungendo entrambi gli endpoint primari. Lo studio ha inoltre dimostrato un profilo di sicurezza comparabile a quello già noto di trastuzumab EV. L’efficacia, valutata mediante l’endpoint primario pCR (pathologic Complete Response), ha confermato la non inferiorità della formulazione sottocutanea rispetto a quella endovenosa (45,4% SC e 40,7% EV), con una differenza nel tasso di risposta del 4,7% (95% IC: 4,0, 13,4) in favore di trastuzumab SC.
Anche il tpCR (ovvero l’assenza di cellule neoplastiche invasive nella mammella e nei linfonodi ascellari) ha confermato la non inferiorità della formulazione sottocutanea rispetto a quella endovenosa (39,2% SC e 34,2% EV), con una differenza nel tasso tpCR di 5,01 (IC al 95%: 3,5 - 13,5) in favore di trastuzumab SC. La risposta globale (ORR) è stata valutata comparabile nei due bracci dello studio: 88,8% (95% IC: 84,4, 92,4) nei pazienti trattati con trastuzumab EV e 87,2% (95% IC: 82,5, 91,0) nei pazienti trattati con trastuzumab SC.
Il profilo di sicurezza di trastuzumab SC è stato com-plessivamente simile al profilo di sicurezza noto della formulazione EV. Quasi tutti i pazienti (94% EV vs 97% SC) hanno avuto esperienza di almeno un evento avverso (AE) nel corso dello studio. L’incidenza degli AE severi (grado ≥ 3) è risultata comparabile in entrambi i bracci di studio. È stata registrata una maggiore incidenza di AE seri (SAEs) nel braccio del SC rispetto al braccio dell’EV (21% SC vs 12% EV), ma non è stata individuata una causa clinica specifica per questo squilibrio. Nel gruppo che ha ricevuto il trattamento sottocutaneo 33 pazienti su 297 (11,1%) hanno manifestato reazioni nella sede di iniezione, con dolore in sede registrato come evento avverso più comune. A parte due eventi di grado 2 tutti gli altri eventi avversi sono stati di grado 1 [8, 9].
Dal punto di vista dei risvolti organizzativi del passaggio alle formulazioni SC, Ponzetti et al. (2016) [10] e Walzer (2016) [11] hanno quantificato il rischio associato alla somministrazione sottocutanea ed endovenosa di rituximab e trastuzumab in un campione di centri italiani. Tale rischio è stato quantificato attraverso l’applicazione della FMEA (Failure Mode and Effect Analysis) al processo “Gestione della terapia farmacologica”. Il modello di analisi FMEA è uno strumento previsionale, interna-zionalmente riconosciuto, che permette di misurare l’Indice di Rischio (IR) con l’utilizzo di dati e tecniche di analisi semi quantitative basate su scale di valore predeterminate. Lo strumento prevede la scomposizione del processo oggetto di studio in attività e l’analisi dei rischi possibili per ognuna di esse. L’introduzione della nuova formulazione comporta una modifica nello svolgimento delle attività di preparazione e somministrazione del farmaco e si correla con un diverso indice di rischio. La nuova formulazione sottocutanea di trastuzumab e rituximab porta all’eliminazione di 12 attività e 23 relativi rischi (eliminazione del 36% delle attività a rischio). In particolare, vi è un effetto sui rischi legati alla somministrazione endovenosa, alla fase di prescrizione (calcolo dosaggio) e alla fase di allestimento delle sacche da infusione e monitoraggio delle pompe infusionali. L’uso della formulazione sottocutanea genera una diminuzione complessiva dell’indice di rischio (IR) del 70%.
Con l’utilizzo della formulazione endovenosa sono presenti 35 aree di rischio: 8 cadono nell’area in alto, 13 nell’area a medio rischio e 14 nell’area a basso rischio. L’uso della formulazione sottocutanea comporta l’eliminazione di 23 attività e rischi correlati, tra cui: il calcolo del dosaggio, la preparazione e gestione delle sacche da infusione, la gestione dell’accesso venoso, la gestione della pompa da infusione ed il monitoraggio dell’infusione. Vengono inoltre a mancare i possibili effetti avversi da infusione (es. stravaso, occlusioni dell’accesso venoso, infezioni, ecc.).
Per le organizzazioni sanitarie, disporre di soluzioni terapeutiche che migliorano la sicurezza del paziente è un obiettivo primario che si riflette sul paziente come fruitore delle prestazioni clinico assistenziali e sulle stesse orga-nizzazioni nel mettere in sicurezza i propri processi. Accrescere la sicurezza dei processi produce un favore-vole impatto nella gestione del rischio clinico, previene i contenziosi e riduce i risarcimenti per sinistri con poten-ziale riduzione dei costi assicurativi. Il tema dei costi assicurativi, nell’ottica di un’evoluzione in atto da coperture assicurative ad auto-assicurazione, con il correlato accantonamento dei fondi sinistri, rappresenta per le Aziende un tema cogente.
Inoltre, diversi studi [7, 12-14] hanno dimostrato che l’utilizzo della formulazione sottocutanea degli anticorpi monoclonali rispetto a quella endovenosa riduce i tempi di somministrazione ed i costi sanitari. Nel caso specifico dei farmaci in oggetto, sono possibili risparmi in termini di materiali di consumo, quantità di farmaco, tempi del personale sanitario, costi di struttura, produttività del paziente e del caregiver. Se ne deduce che la formulazione sottocute possa favorire una più efficiente allocazione delle risorse.
Accanto a robuste evidenze di carattere clinico e organizzativo, numerosi studi sono attualmente in corso a livello nazionale con la finalità di esplorare l’impatto delle nuove formulazioni dei due farmaci sull’esperienza di cura dei pazienti valutata in termini di soddisfazione, qualità della vita e perdita di produttività evitata in relazione ai più brevi tempi di somministrazione.
Tali aspetti assumono importanza cruciale anche sotto il profilo etico. Secondo i criteri valutativi posti dal Core Model® di EuNetHTA, nel caso di farmaci che, utilizzati per un medesimo obiettivo di salute, presentino un rapporto rischi-benefici sovrapponibile, è doveroso somministrare quello che sia in grado di garantire la miglior qualità di vita per i pazienti come pure quello che sia in grado di consentire una più equa allocazione delle risorse. Ne consegue che la formulazione sottocutanea sarebbe da preferirsi a quella endovenosa, qualora garantisse una migliore qualità di vita per i pazienti e/o consentisse dei risparmi.
Sulla base di quanto detto, l’obiettivo del presente la-voro è fornire una valutazione dell’impatto sociale ed economico delle formulazioni sottocutanee di rituximab e trastuzumab nelle rispettive indicazioni.
Materiali e Metodi
L’analisi effettuata in questo studio, viene strutturata in due fasi, distinte ma altamente complementari:
Un’analisi di regressione finalizzata a stimare la relazione tra il tipo di trattamento ricevuto dal paziente, da un lato, e i) la qualità di vita percepita dai pazienti e ii) l’esperienza complessiva avuta in ospedale alla luce del trattamento ricevuto, dall’altro. Più precisamente, si intende valutare la relazione esistente tra l’alternativa terapeutica e la soddisfazione del paziente. L’analisi è volta a confrontare le due alternative terapeutiche, SC e EV.
Un’analisi dei costi legati alla presenza ed alle ca-ratteristiche dei caregiver ossia degli accompagnatori dei pazienti che ricevono il trattamento, confrontando le alternative SC e EV. Le caratteri-stiche prese in considerazione riguardano la regione di provenienza, il fatto di essere o meno occupati e la presenza di accompagnatori “lavoratori”. In questa fase, per ottenere una stima dell’impatto economico delle formulazioni sottocutanea, vengono computati i costi diretti sanitari e le perdite di produttività sia del paziente che del caregiver.
La valutazione dell’impatto economico e sociale delle terapie con somministrazione del farmaco sottocutanea rispetto alla somministrazione tradizionale, per via endovenosa, è stata condotta grazie all’analisi statistica di dati primari già disponibili e raccolti nell’ambito dei progetti «Going Lean» e SCUBA (SubCUtaneous Benefit Analysis), entrambi condotti nel contesto italiano.
Analisi di impatto sociale
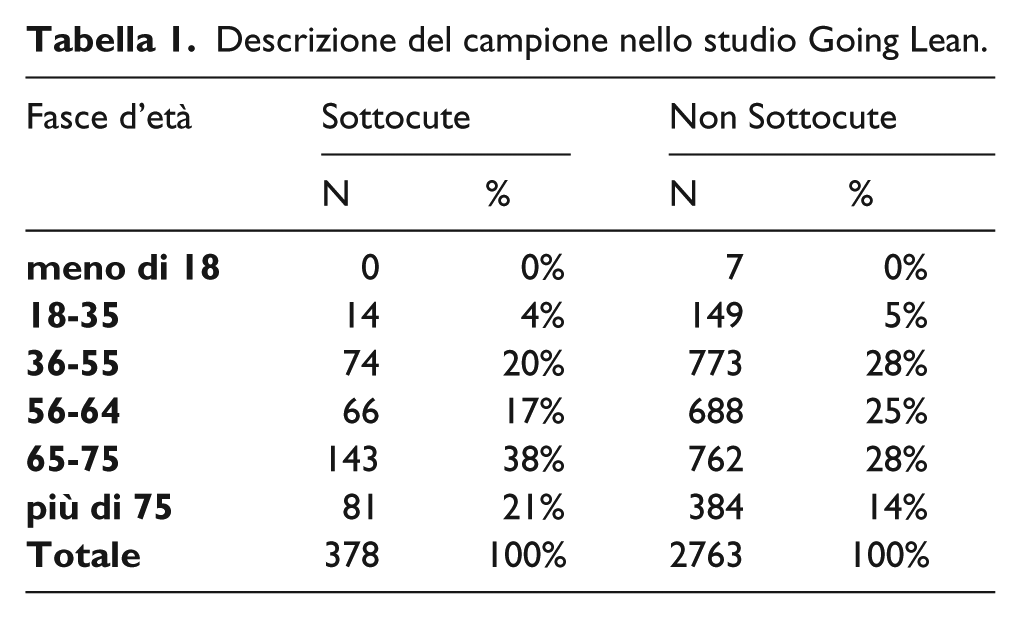
L’analisi di impatto sociale si basa sui dati raccolti nell’ambito dello studio Going Lean. Tale progetto intende fornire un supporto alle Aziende Ospedaliere nel riorga-nizzare il percorso di cura dei pazienti in onco-ematologia e facilitare l’adozione di un modello organizzativo che massimizzi i benefici delle nuove formulazioni sottocutanee. Inoltre, si pone come obiettivo quello di creare dei percorsi di cura omogenei con standard uniformi e di massimo li-vello. Il progetto Going Lean, inoltre, è stato condotto con l’obiettivo di rilevare l’utilità percepita delle due diverse soluzioni terapeutiche, SC e EV, attraverso la sommini-strazione di un questionario a pazienti e professionisti coinvolti nella terapia. Tale questionario è composto principalmente da tre differenti sezioni: la prima sezione viene compilata da un professionista sanitario che indica la data, la struttura, il tempo di trattamento e se il tipo di trattamento prevedesse solo l’utilizzo di formulazioni sottocutanee. La seconda viene compilata dal paziente e include la fascia d’età, la presenza di un accompagnatore e la fascia d’età dell’accompagnatore. La terza ed ultima sezione, si pone come obiettivo quello di valutare l’esperienza com-plessiva e la qualità di vita del paziente sottoposto al trattamento. Il questionario è stato somministrato in 37 centri in diverse regioni italiane (Calabria, Lazio, Lombardia, Campania, Puglia, Sicilia, Abruzzo, Veneto, Toscana, Emilia-Romagna, Sardegna e Basilicata) a infermieri e pazienti dei reparti di oncoematologia. La Tabella 1 riporta la stratificazione dei pazienti rispondenti alla survey per fasce d’età in valori assoluti e percentuali.
Descrizione del campione nello studio Going Lean.
La presente analisi, come detto in precedenza, intende verificare l’impatto del trattamento di tipo “SC” rispetto al trattamento tradizionale “EV” sulla qualità della vita percepita e l’esperienza complessiva in ospedale a fronte del trattamento ricevuto. A tal fine, sono stati stimati due mo-delli di regressioni distinti. In un primo modello la variabile dipendente utilizzata è il giudizio complessivo della propria esperienza in ospedale. Nel secondo modello la variabile dipendente considerata è la valutazione espressa della propria qualità della vita alla luce della durata delle terapie ricevute durante la permanenza in ospedale. Ciascuna delle due variabili assume valori che vanno da 1 a 10 (1=minimo; 10=massimo), in aderenza alle scale di risposta proposte al paziente per i due item.
La variabile indipendente principale riguarda – come già anticipato – il tipo di trattamento ricevuto dal paziente in ospedale, distinguendo SC da EV. A riguardo il que-stionario “Going Lean” prevede un esplicito campo “Solo sottocute?” nella prima Sezione con risposta (compila-zione a cura dell’infermiere) di tipo binario SI/NO. Sulla base di questa informazione è stata ricavata una variabile binaria, denominata “SC” che assume valore 1 quando il campo contrassegnato è SI, e 0 nel caso opposto.
Altre variabili indipendenti che riguardano fattori che possono influenzare le variabili dipendenti, e dunque incluse nel modello, sono le seguenti:
“Fascia di età del paziente”. La fascia di età del paziente sottoposto al trattamento, corrisponde ad una delle seguenti opzioni: “Età, meno di 18” “Età, 18-35” “Età, 36-55” “Età, 56-64” “Età, 65-75” “Età, più di 75”.
“Accompagnatore”. In base alla risposta alla domanda “È venuto da solo o accompagnato?” questa variabile binaria assume valore 1 quando l’opzione contrassegnata è “Accompagnato”, oppure 0 nel caso opposto.
“Supporto”. Il questionario prevede la domanda “Durante la sua permanenza in reparto si è sentito supportato/ben seguito?”, al quale il paziente può rispondere esprimendo valori in un range da 1 a 10 (1=per niente; 10=molto). La variabile “Supporto” assume valori da 1 a 10.”Comfort”. Il questionario prevede la domanda “Ritiene che la somministra-zione della terapia (“iniezione”) avvenga in un ambiente confortevole?”, alla quale il paziente può rispondere esprimendo valori in un range da 1 a 10 (1=per niente; 10=molto). La variabile “Comfort” assume valori da 1 a 10.
La particolare natura delle due variabili dipendenti consi-derate ha reso opportuno utilizzare il metodo della regressione logistica multinomiale al fine di ottenere una stima dei parametri più completa e robusta. Un ulteriore accorgimento utilizzato nella stima dei modelli si ha con l’utilizzo dello standard error clusterizzato per regione [15].
Stima dell’impatto economico
La stima dell’impatto economico della formulazione SC rispetto a quella EV è stata effettuata partendo dai risultati preliminari degli studi “Going Lean” e SCUBA.
In particolare, i principali driver del confronto sono: a) i tempi di somministrazione del farmaco e di attraversamento (la totalità del tempo trascorso dal paziente e dal caregiver all’interno del reparto dove viene effettuata la terapia), b) le risorse sanitarie direttamente impiegate nel processo di cura.
L’analisi di impatto economico è stata condotta comparando i costi associati alla formulazione SC con quelli associati alla formulazione EV, secondo la prospettiva dell’ospedale, del servizio sanitario e della collettività.
Per ciascun accesso in ospedale finalizzato alla sommi-nistrazione del farmaco, sono stati presi in considerazione i differenziali di consumo delle risorse sanitarie (costi di somministrazione, costi del farmaco, costo del personale, costo dei materiali di consumo, costo degli scarti e costi della struttura) così come emersi dai risultati preliminari dello studio SCUBA. Tale progetto, ancora in corso in diversi ospedali italiani, si pone l’obiettivo di quantificare i benefici organizzativi ed economici delle formulazioni sottocutanee. Le analisi preliminari sono state condotte sull’estrapolazione di un campione di 210 pazienti e dimostrano che l’utilizzo delle formulazioni sottocutanee, oltre ad un minor consumo di risorse sanitarie, implica anche una riduzione dei tempi medi di attraversamento, derivante dalla riduzione del tempo di somministrazione del farmaco. Applicando il metodo del capitale umano [16], è stato possibile stimare, per ogni accesso in ospedale, i risparmi espressi in termini di perdite di produttività dei pazienti e dei caregiver, derivanti dalla riduzione dei tempi di attraversamento. In questa fase, si è tenuto conto del tasso di occupazione per fascia di età (ISTAT, 2016) e della proporzione di pazienti che si recano in ospedale accompagnati che emergeva dallo studio Going Lean. La perdita di produttività è stata calcolata, per ciascuna delle due formulazioni dei farmaci, moltiplicando le ore di lavoro perse dal paziente e dal caregiver per il salario lordo orario (ISTAT, 2014). Il costo evitabile con la formulazione sottocutanea rispetto a quella endovenosa è stato ottenuto per differenza.
Per ogni indicazione, il numero di accessi in ospedale per la ricezione del farmaco si basa su quanto riportato sugli RCP (Riassunto delle Caratteristiche del Prodotto) in riferimento ad un paziente medio.
I risultati, ottenuti in due centri ospedalieri per ogni principio attivo, sono stati quindi proiettati a livello na-zionale, tenendo conto dei pazienti trattabili con i due farmaci oggetto di studio nelle diverse indicazioni. L’esercizio è stato replicato tenendo conto della popolazione delle singole regioni.
Il numero di pazienti potenzialmente eleggibili ai trattamenti di linfoma follicolare e DLBCL per quanto riguarda rituximab, e di cancro alla mammella in fase iniziale o metastatico per quanto riguarda trastuzumab, è riportato in Appendice (Tabelle 1A - 4A).
Risultati
Analisi di impatto sociale
I risultati del modello di Regressione Logistica Multinomiale, per quanto riguarda l’esperienza complessiva in ospedale (Tabelle 2 e 3), mostrano che i pazienti sottoposti a terapia SC hanno una probabilità maggiore di giudicare positivamente l’esperienza complessiva in ospedale rispetto ai pazienti in trattamento con terapia EV (0,67 vs 0,55). La probabilità di valutazioni negative o medie invece risulta maggiore nei pazienti sottoposti a terapie EV.
Valutazione dell’esperienza in ospedale: regressione logistica multinomiale.
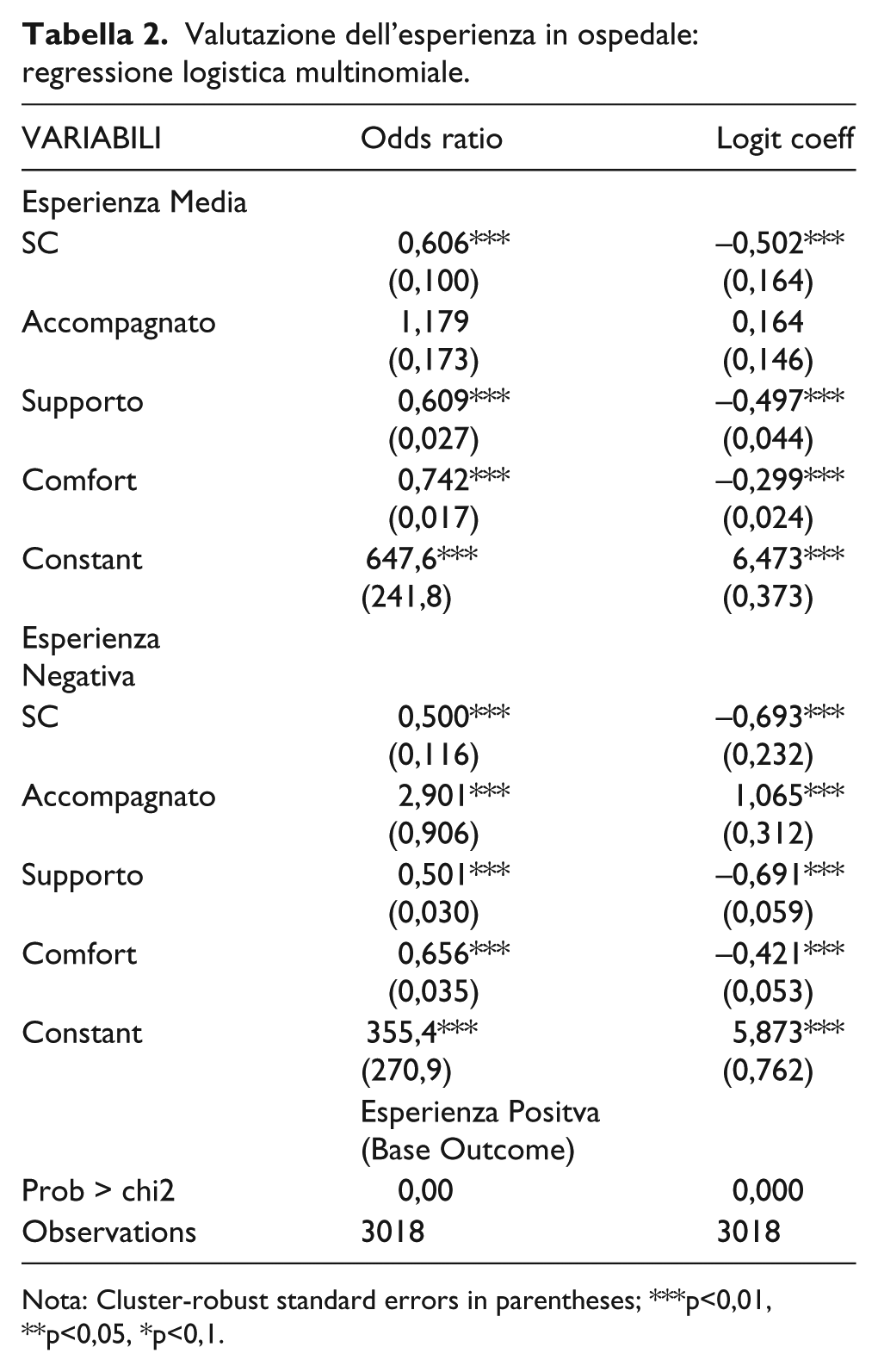
Nota: Cluster-robust standard errors in parentheses; ***p<0,01, **p<0,05, *p<0,1.
Valutazione dell’esperienza in ospedale: probabilità stimate.
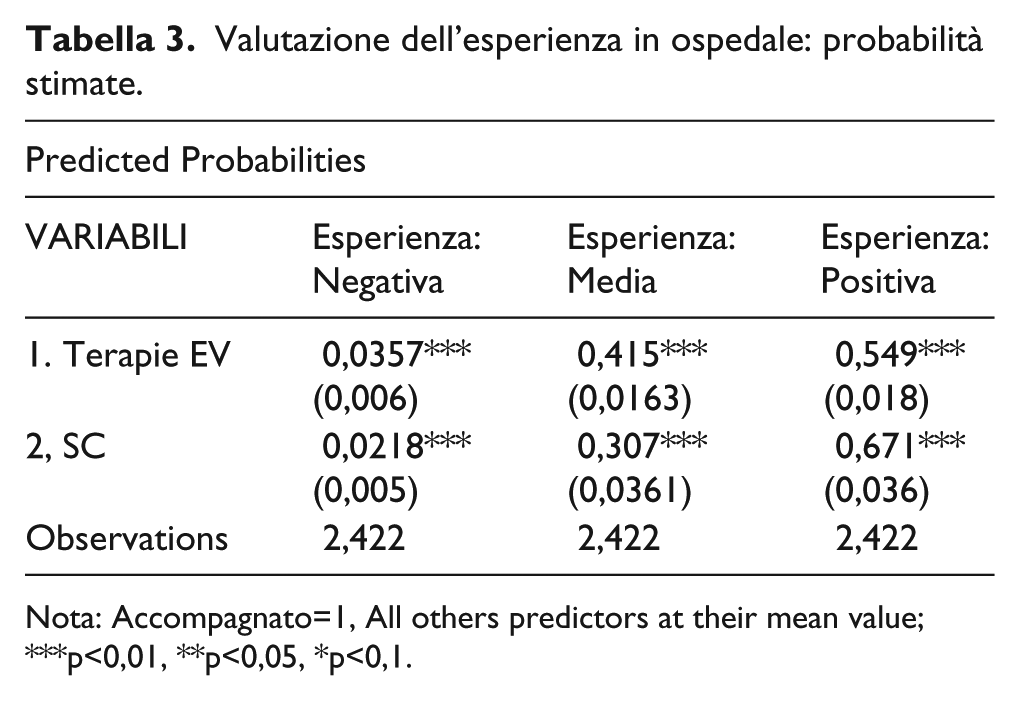
Nota: Accompagnato=1, All others predictors at their mean value; ***p<0,01, **p<0,05, *p<0,1.
I risultati del modello di Regressione Logistica Multinomiale, per quanto riguarda invece la qualità della vita percepita (Tabelle 4 e 5), dimostrano che i pazienti sottoposti a terapia SC hanno una probabilità maggiore di valutare positivamente la propria qualità di vita rispetto ai pazienti in trattamento con terapia EV (0,38 vs 0,26). La probabilità di valutazioni negative o medie invece risulta maggiore nei pazienti sottoposti a terapie EV.
Qualità della vita: regressione logistica multinomiale.

Nota: Cluster-robust standard errors in parentheses; ***p<0,01, **p<0,05, *p<0,1.
Qualità della vita: probabilità stimate.
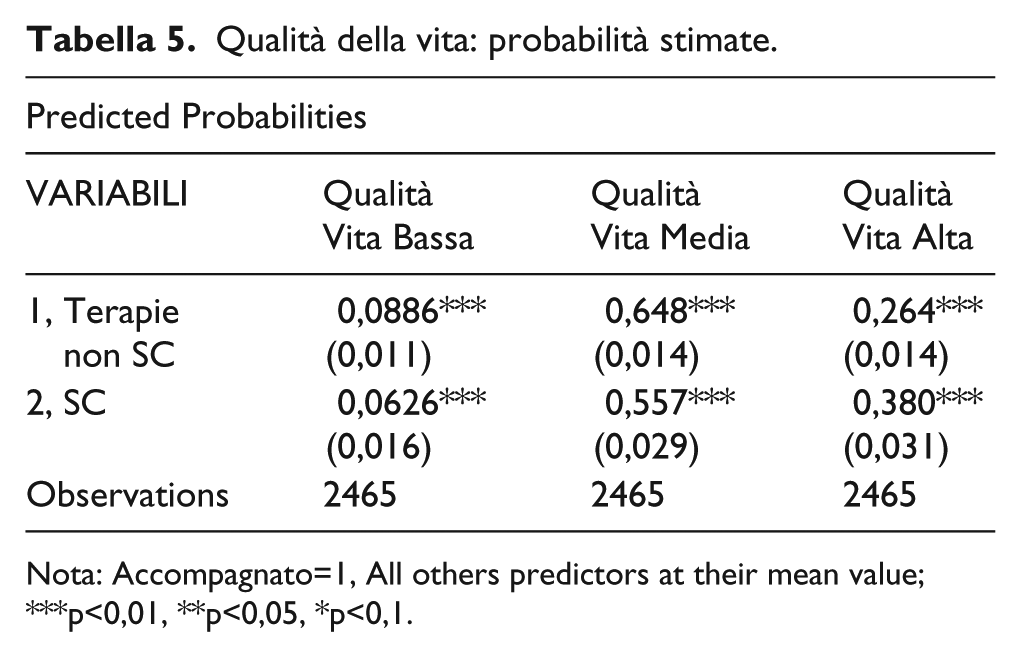
Nota: Accompagnato=1, All others predictors at their mean value; ***p<0,01, **p<0,05, *p<0,1.
Stima dell’impatto economico dell’uso di Rituximab SC
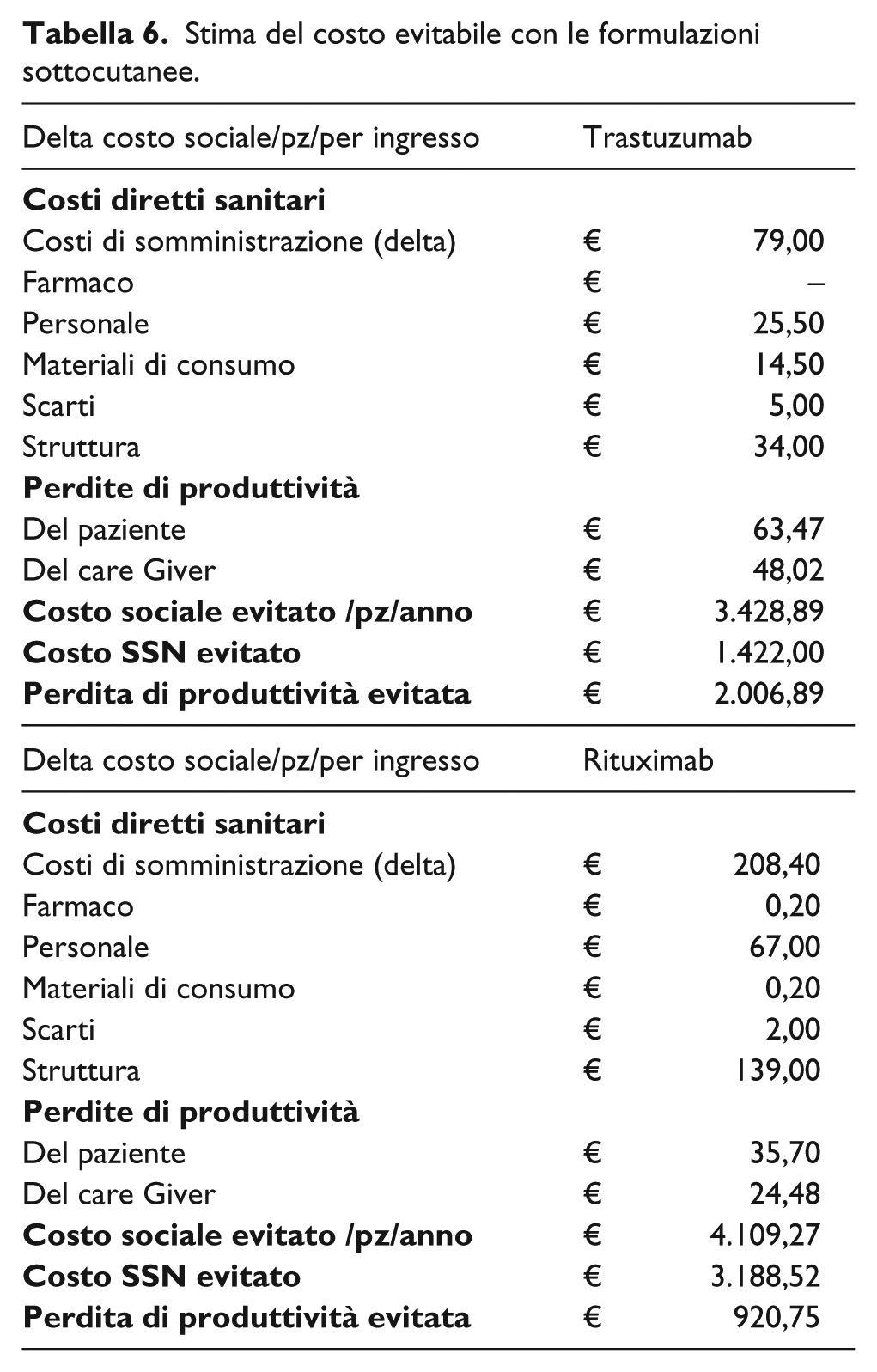
In uno dei due centri è stato stimato un risparmio potenziale per paziente per anno pari a 4.025 €. Tale valore tiene conto dei risparmi ottenibili in termini di costi diretti sanitari (2.876 €) e di perdite di produttività evitate per il paziente e per il caregiver (1.149 €). Nell’altro centro, invece, il risparmio potenziale per paziente per anno ammonta a 4.109 €, di cui 3.188 € sono costi sanitari evitabili e 920 € sono perdite di produttività evitabili tramite la riduzione dei tempi di attraversamento. Queste stime tengono conto del numero di somministrazioni per anno previste da RCP.
Il costo evitabile per paziente per anno, ottenibile optando per la formulazione sottocutanea rispetto a quella endovenosa, è risultato in media di 4.067,58 €. I risparmi potenziali attribuibili dal passaggio da formulazione en-dovenosa a formulazione sottocutanea sono riportati nella Tabella 6. Al fine di ottenere una stima del potenziale ri-sparmio sociale a livello regionale e nazionale, tale importo è stato moltiplicato per il numero di pazienti potenzialmente eleggibili al trattamento. La ripartizione della po-polazione di pazienti tra le regioni è stata costruita sulla base dei residenti in ciascuna regione italiana, ipotizzando quindi che i tassi di incidenza fossero uguali in tutte le regioni italiane. Nel caso dei pazienti con Linfoma Follicolare si stima dunque un costo evitabile annuo di 8.621.752 € per il Servizio Sanitario Nazionale. Tenendo conto anche delle perdite di produttività evitabili per il paziente e per il caregiver, il costo sociale evitabile sarebbe pari a 11.564.755 €. Il costo indiretto rappresenterebbe il 25,45% del costo evitabile totale.
Stima del costo evitabile con le formulazioni sottocutanee.
Analogamente, moltiplicando il risparmio medio per paziente, ottenuto nei due centri, per la popolazione potenziale dei pazienti con DLBCL si ottiene a livello nazionale un costo evitabile annuo di 1.007.788 € per il Servizio Sanitario Nazionale. Tenendo conto anche delle perdite di produttività evitabili per il paziente e per il caregiver, il costo sociale evitabile sarebbe pari a 20.113.779 €.
Le Tabelle 1A e 2A in Appendice riportano la specifica del risparmio potenziale a livello regionale e nazionale per le due indicazioni di rituximab oggetto di analisi.
La Figura 1 riporta i risultati di un’analisi di scenario che simula il costo evitato ipotizzando che la quota di pazienti trattati con formulazione SC sia del 25% e del 50%. Le stesse ipotesi sono state applicate alle due indicazioni terapeutiche.
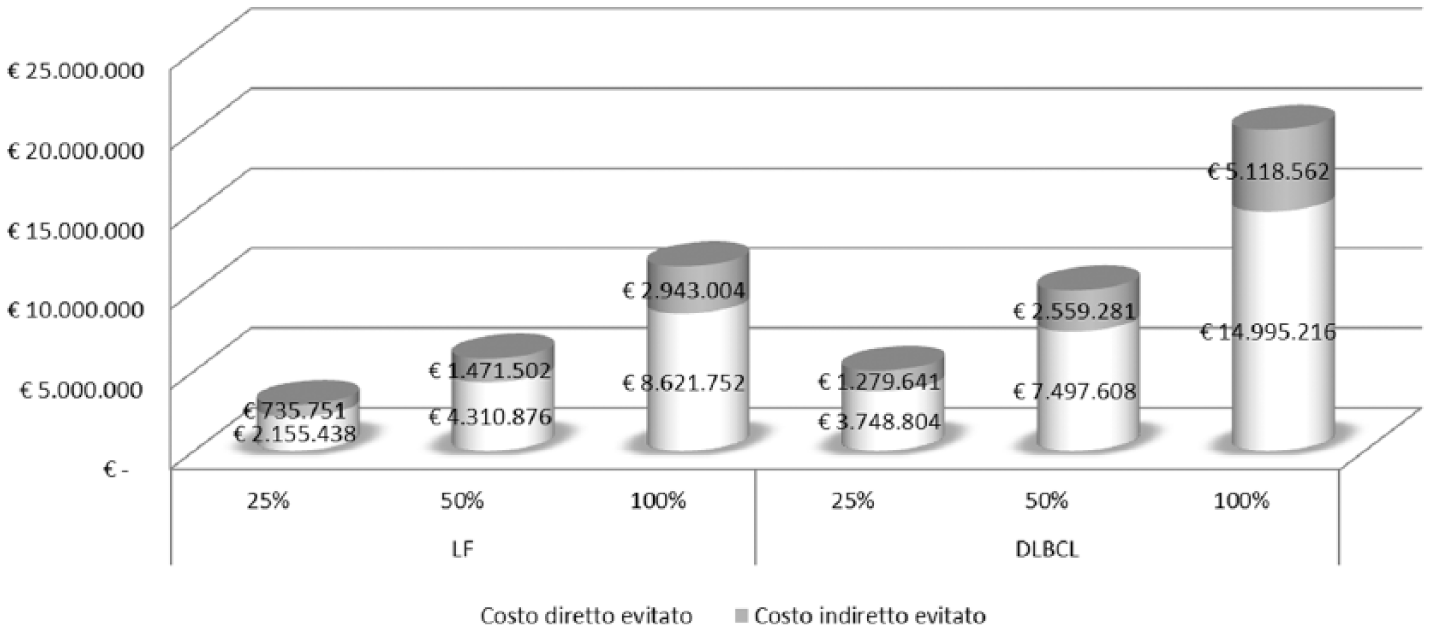
Stima dei risparmi potenziali associati all’uso di rituximab SC: analisi di scenario. LF: Linfoma Follicolare; DLBCL: Linfoma Diffuso a Grandi Cellule B
Stima dell’impatto economico dell’uso di Trastuzumab SC
In un centro, è stato stimato un risparmio potenziale per paziente per anno pari a 3.548,78 €. Tale ammontare tiene conto dei risparmi ottenibili in termini di costi diretti sanitari (1.530 €) e di perdite di produttività evitate per il paziente e per il caregiver (2.018,78 €). Nell’altro centro, invece, il risparmio potenziale per paziente per anno ammonta a 3.309 € di cui 1.314 € sono costi sanitari evitabili e 1.995 € sono perdite di produttività evitabili tramite la riduzione dei tempi di attraversamento. Queste stime tengono conto del numero di somministrazioni per anno previste da RCP. I risparmi potenziali attribuibili dal passaggio da formulazione endovenosa a formulazione sottocutanea sono riportati nella Tabella 6.
Il costo evitabile per paziente per anno, ottenibile optando per la formulazione sottocutanea rispetto a quella endovenosa, è risultato in media di 3.429 €. Nel caso dei pazienti con early breast cancer si stima un costo evitabile annuo di 9.828.864 € per il Servizio Sanitario Nazionale. Tenendo conto anche delle perdite di produttività evitabili per il paziente e per il caregiver, il costo sociale evitabile sarebbe pari a 13.871.636 €. Il costo indiretto rappresenterebbe il 59% del costo evitabile totale.
Analogamente, moltiplicando il risparmio medio per paziente, ottenuto nei due centri, per la popolazione potenziale dei pazienti con mBC si ottiene a livello nazionale un costo evitabile annuo di 2.871.018 € per il Servizio Sanitario Nazionale. Tenendo conto anche delle perdite di produttività evitabili per il paziente e per il caregiver, il costo sociale evitabile sarebbe pari a 6.922.933 €.
Le Tabelle 3A e 4A in Appendice riportano la specifica del risparmio potenziale a livello regionale e nazionale per le due indicazioni di trastuzumab oggetto di analisi.
La Figura 2 riporta i risultati di un’analisi di scenario che simula il costo evitato ipotizzando che la quota di pazienti trattati con trastuzumab SC sia del 25% e del 50%. Le stesse ipotesi sono state applicate alle tre indicazioni terapeutiche.
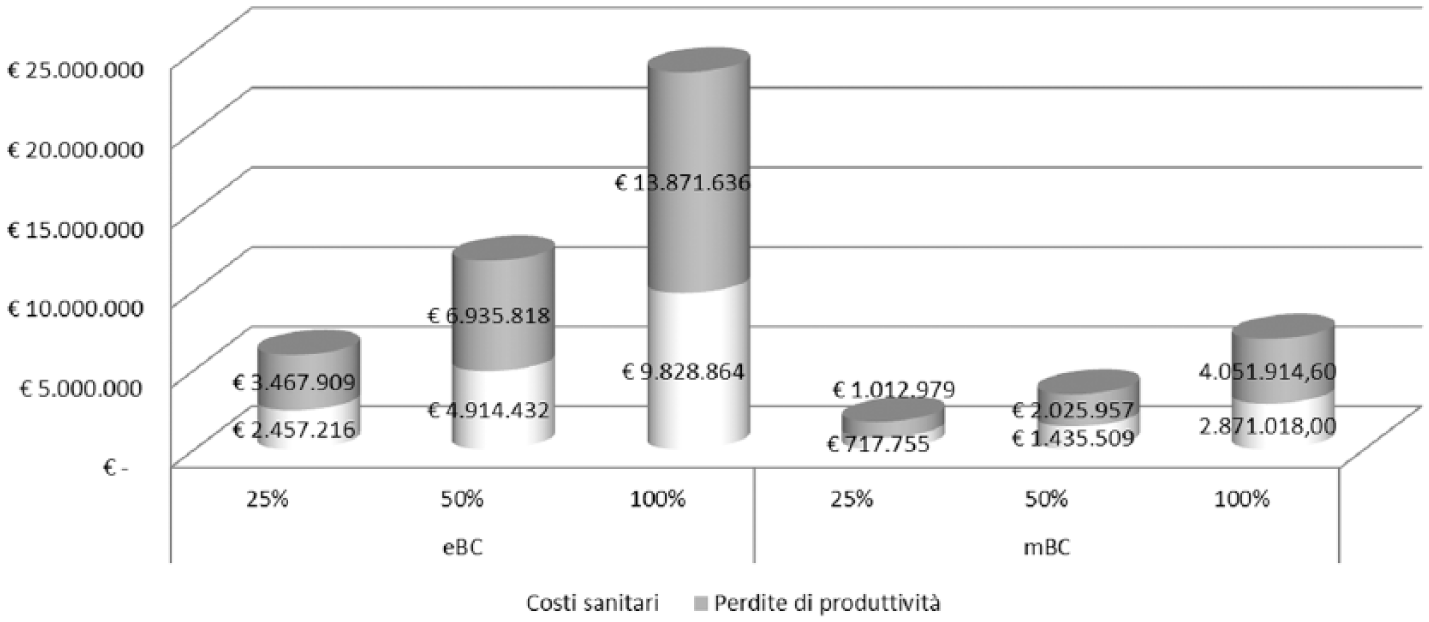
Stima dei risparmi potenziali associati all’uso di trastuzumab SC: analisi di scenario. eBC: early Breast Cancer; mBC: metastatic Breast Cancer.
Discussione
La formulazione sottocutanea di rituximab e trastuzumab offre la possibilità alle diverse Unità Operative onco-ematologiche di beneficiare di un nuovo approccio per la ge-stione della patologia in termini economico-organizzativi.
Come descritto, all’interno del percorso di day hospital la formulazione sottocutanea genera risparmi in termini di tempo dedicato alla preparazione e somministrazione del farmaco, sprechi di prodotto evitati e riduzione del rischio clinico. La riduzione di tale rischio è correlata al risultato dell’analisi FMEA. Tale strumento prevede la scomposizione del processo oggetto di studio in attività e nell’analisi dei rischi possibili per ognuna di esse. La nuova formulazione sottocutanea di trastuzumab e rituximab porta all’eliminazione di 12 attività e 23 relativi rischi (eliminazione del 36% delle attività a rischio). I diversi contesti ospedalieri in cui si muovono i pazienti oncoematologici sono caratterizzati da un certo grado di variabilità nell’organizzazione delle cure in termini di efficienza gestionale. La complessità della dimensione ospedaliera, della patologia e dei trattamenti ad essa associati genera dei fenomeni più o meno virtuosi all’interno delle singole unità operative, le quali spesso trovano difficoltà nel gestire l’afflusso dei pazienti e la somministrazione dei trattamenti: il congestionamento dei reparti è, infatti, uno dei problemi che spesso le direzioni amministrative e sanitarie si trovano ad affrontare.
L’inserimento della formulazione sottocutanea in tali contesti, oltre a garantire la comprovata efficacia clinica di rituximab e trastuzumab, apporterebbe un beneficio orga-nizzativo importante in un’ottica di razionalizzazione delle risorse sanitarie. La riduzione dei tempi tecnici di preparazione e somministrazione del trattamento permette-rebbe di decongestionare le farmacie ospedaliere ed i reparti di day hospital, consentendo al personale sanitario, in particolare a quello infermieristico, di gestire l’afflusso dei pazienti e l’assistenza in modo più efficiente. Per ottenere un risparmio significativo di risorse, perciò, è necessario che tali reparti siano riorganizzati secondo un approccio orientato al “lean thinking” [17].
Il dosaggio fisso delle due formulazioni non necessita della fase di preparazione che, oltre ad impegnare il farmacista ospedaliero, può essere soggetta ad errori nel calcolo della dose e quindi può comportare un rischio per il paziente e generare sprechi di prodotto, anche in quelle unità operative che minimizzano le inefficienze nella ge-stione degli scarti. Inoltre, la formulazione SC garantisce una forte riduzione del rischio clinico legato alla gestione del prodotto ed alla sua somministrazione, generando non solo un beneficio per il paziente, ma anche per l’intera struttura sanitaria.
Attraverso il modello economico e statistico sopra descritto, si evince come il passaggio dalla formulazione endovenosa a quella sottocutanea, può avere un forte impatto sulle risorse impiegate dal SSN liberando risorse che potrebbero essere reinvestite nel miglioramento delle cure per i pazienti ed in innovazione. Tuttavia, la stima dei risparmi potenziali in termini di risorse per il SSN va considerata con cautela essendo stata proiettata a livello regio-nale e nazionale partendo da dati estrapolati da due centri ospedalieri. Un altro limite dello studio potrebbe essere rappresentato dal fatto che non viene considerata la diffe-renza di impatto economico rispetto ad un biosimilare. Tuttavia, al momento della conduzione dello studio, non erano ancora disponibili farmaci biosimilari per le molecole oggetto dell’analisi. Quindi, è auspicabile che l’analisi venga estesa ai biosimilari in un prossimo futuro, una volta che siano stabilmente entrati nella pratica clinica.
Le formulazioni sottocutanee dei mAbs possono contribuire ad accrescere l’efficienza del sistema, senza de-pauperare, anzi migliorando la qualità del servizio offerto ai cittadini, così come dimostrato dalla valutazione riportata dai pazienti trattati con formulazione SC.
Infine, presentando l’impiego delle formulazioni sottocutanee un rapporto rischi-benefici favorevole, e consentendo una migliore qualità della vita e risparmi economici è da un punto di vista etico giustificato e prefe-ribile alla somministrazione endovenosa.
Conclusioni
Le formulazioni SC dei MAbs oggetto di questo studio dimostrano efficacia e sicurezza sovrapponibili a quelle delle formulazioni EV. Dal punto di vista del paziente, la somministrazione sottocutanea riduce la necessità di essere accompagnato nel centro per ricevere il trattamento ed i minori tempi di attraversamento esitano in minori perdite di produttività del paziente e del caregiver.
Se da una parte i vantaggi offerti dalle formulazioni SC sono accolti positivamente dai pazienti che la associano ad una migliore qualità della vita percepita e ad una migliore esperienza di cura, dall’altra l’utilizzo di queste formula-zioni nell’ambito di un contesto organizzativo pronto ad accoglierle potrebbe generare risparmi significativi per il Servizio Sanitario Nazionale.
Supplemental Material
Supplemental material for Assessing social and economic impact of subcutaneous mAbs in oncology
Supplemental material, Supplementary_Material for Assessing social and economic impact of subcutaneous mAbs in oncology by Americo Cicchetti, Silvia Coretti, Daniele Mascia, Nicola Mazzanti, Pietro Refolo, Francesca R. Rolli and Filippo Rumi in Global & Regional Health Technology Assessment
Footnotes
Acknowledgements
Authors are thankful to the Experts Advisory Board of the Project: Alessandra Cassano, Vito Antonio Delvino, Francesco Merli, Alessandro Mugelli, Davide Petruzzelli, Tiziana Sabetta, Mario Scaletti and Maurizio Zega.
Declaration of Conflicting Interest
The authors declare that there is no conflict of interest.
Funding
This project was funded by Roche S.p.A. Publication of results was not contingent on sponsor’s approval. The views expressed here are those of the authors and not necessarily those of the funder.
References
Supplementary Material
Please find the following supplemental material available below.
For Open Access articles published under a Creative Commons License, all supplemental material carries the same license as the article it is associated with.
For non-Open Access articles published, all supplemental material carries a non-exclusive license, and permission requests for re-use of supplemental material or any part of supplemental material shall be sent directly to the copyright owner as specified in the copyright notice associated with the article.
