Abstract
Budget impact analysis in the maintenance raltegravir-containing regimen in virologically suppressed HIV infected patients
Background
A one-year cost analysis was conducted to estimate the impact from the perspective of the Italian National Health Service (NHS) of nevirapine or etravirine or rilpivirine plus raltegravir administration as maintenance antiretroviral therapy in virologically suppressed HIV-1 infected patients.
Methods
Patient data were retrieved from the electronic medical record system in use (year 2016) in a reference HIV centre in South Italy. The analysis considered patients with long-term (more than 1 year) virological suppression (HIV-1 RNA <50 copies/mL) on Highly Active Antiretroviral Therapy (HAART) and no prior exposure to integrase inhibitors (INIs). To estimate the total HAART expenditure, we calculated the annual treatment cost for each enrolled patient. Subsequently, to estimate the dual therapy hypothetical expenditure, we assumed to treat the same patients with nevirapine or rilpivirine or etravirine and raltegravir. We took into account only drug costs (ex-factory prices, included all discounts and VAT) from the perspective of the Italian NHS.
Results
In 2016, the total expenditure for the 116 enrolled HIV-1 infected patients treated with HAART was €869,889. The mean treatment cost per patient was €7,499. If all patients were treated with the dual therapy (nevirapine/raltegravir), the total expenditure would be €641,016 (-26.3%) with a mean treatment cost per patient of €5,526 and a potential total saving of €228,873. On the contrary, the dual regimen based on etravirine or rilpivirine associated with raltegravir would engender respectively a 35.5% and 8.7% expenditure increase.
Conclusions
From the Italian NHS perspective, nevirapine/raltegravir represent a cost-saving option as maintenance antiretroviral therapy in virologically suppressed HIV-1 infected patients.
Introduzione
La terapia antiretrovirale di combinazione (cART) ha modificato la storia naturale dell'infezione da HIV (Human Immunodeficiency Virus), influenzando sia lo stato di salute del soggetto con HIV sia la trasmissibilità dell'infezione stessa (1).
Riguardo la valenza epidemiologica della terapia, lo studio randomizzato e controllato HTPN052 ha evidenziato una riduzione a 10 anni del 93% della trasmissione dell'HIV (2), mentre lo studio PARTNER, condotto su coppie HIV+ discordanti, ha fornito ampie dimostrazioni sull'assenza di trasmissione sessuale dell'infezione quando il soggetto con HIV sia in terapia con una viremia anche solo inferiore a 200 copie/ml (3).
Sono molteplici le evidenze scientifiche disponibili in letteratura che riportano il benefico clinico della cART nel trattamento di pazienti con linfociti T CD4 <500 cellule/μL (1). Due recenti studi randomizzati (INSIGHT START e TEMPRANO ANRS) (4, 5) hanno però evidenziato la presenza di un beneficio clinico in termini di progressione della malattia (AIDS o decesso) anche per i pazienti con linfociti T CD4 >500 cellule/μl. Sulla scia di questi risultati, le Linee Guida italiane del 2016 inerenti l'utilizzo dei farmaci antiretrovirali ribadiscono, rispetto al passato, l'importanza di somministrare fin da subito la cART a tutti i soggetti con infezione da HIV, indipendentemente dal quadro immuno-virologico (1). Alla terapia intrapresa precocemente (Early Treatment) viene infatti associato un rapido controllo della replicazione dell'HIV, che permette di raggiungere un adeguato consolidamento della risposta immunitaria (4, 5). In virtù di una soppressione virologica plasmatica (non rilevabilità di HIV-RNA), la terapia antiretrovirale di combinazione riduce rapidamente morbosità e mortalità correlate all'infezione (1).
La terapia farmacologica somministrata per il trattamento dell'HIV nel paziente naïve è di norma una terapia di combinazione, cioè un'associazione di farmaci antiretrovirali (1). Le più recenti Linee Guida italiane consigliano l'associazione di due NRTI (inibitori nucleosidici della trascrittasi inversa) con un terzo farmaco INI (inibitore dell'integrasi) o un NNRTI (inibitore non-nucleosidico della trascrittasi inversa) o in alternativa un PI (inibitore della proteasi) potenziato con ritonavir o cobicistat quale standard di trattamento per i pazienti HIV-infetti (1). Queste combinazioni, che contengono almeno tre farmaci antiretrovirali, costituiscono i cosiddetti regimi complessi o HAART (Highly Active Antiretroviral Therapy).
Nonostante i notevoli risultati raggiunti dalla ricerca clinica, la terapia “perfetta” rimane ancora un'utopia, particolarmente se si considerano le problematiche legate alla tossicità e alla tollerabilità, spesso associate ai regimi complessi, nel breve e, soprattutto, nel lungo termine (6, 7).
Negli ultimi anni la disponibilità di farmaci innovativi che potessero garantire alcuni vantaggi nei pazienti a elevato rischio cardiovascolare, metabolico e con alterazione della funzionalità renale, ha reso possibile la combinazione e somministrazione di regimi NRTI– e PI-sparing in specifici gruppi di pazienti con infezione da HIV, caratterizzati da resistenze o intolleranze a queste due classi di farmaci.
Questi nuovi regimi, definiti di semplificazione, si caratterizzano per il ridotto numero dei farmaci somministrati (uno o due invece di tre) e sono stati oggetto di numerosi studi clinici. Fra gli altri meritano particolare attenzione i regimi caratterizzati dalla combinazione di un NNRTI più un INI utilizzati nel trattamento di mantenimento in pazienti HIV in soppressione virologica.
Alcuni studi in particolare hanno valutato la combinazione di raltegravir, il primo inibitore dell'integrasi (in uso ormai da diversi anni), con un NNRTI. Fra gli studi clinici effettuati in ambito europeo (8–11) una prima analisi, condotta in Francia, riporta i risultati del regime nevirapina/ raltegravir nel trattamento di mantenimento in pazienti in soppressione virologica (8). Trentasei pazienti con HIV-RNA plasmatico <50 copie/ml da più di 6 mesi, in trattamento con un regime a base di nevirapina (NVP) e senza una precedente esposizione agli INI, sono stati avviati a un regime semplificato nevirapina (400 mg/die) e raltegravir [400 mg due volte al giorno (BID)] (8). Al follow-up a 96 settimane tutti i pazienti avevano mantenuto una carica virale <50 copie/ml, mentre non è stato registrato alcun evento avverso di grado 3 o 4 (8).
Un secondo studio spagnolo ha analizzato 25 pazienti in soppressione virologica in trattamento con HAART (in media da 15,6 anni) avviati a un regime semplificato con etravirina/raltegravir (9) a causa di tossicità (n = 19) o interazioni (n = 9). Nessun paziente presentava un precedente fallimento o resistenza a etravirina e/o raltegravir. Dopo un follow-up mediano di 722 giorni non sono stati registrati casi di fallimento virologico. Soltanto un paziente ha interrotto il trattamento a causa di un evento avverso (rash di grado 2). A 48 settimane il mantenimento della soppressione virologica è stato registrato nel 96% dei pazienti arruolati. Non ci sono stati casi di tossicità epatica di grado 3-4, il livello di colesterolo totale e dei trigliceridi si è ridotto significativamente (colesterolo: -17 mg/dl; p = 0,01; trigliceridi: -42 mg/dl; p = 0,01).
Un terzo studio osservazionale e retrospettivo, condotto in sei Centri clinici italiani (10), ha valutato pazienti in trattamento con il regime combinato nevirapina/raltegravir. Sono stati esclusi dall'analisi i pazienti con un precedente fallimento terapeutico a NNRTI o raltegravir, che assumessero terapie concomitanti con potenziali interazioni con il regime semplificato e quelli con una diagnosi di epatite B. In totale sono stati valutati 77 soggetti (età media 52 anni; 76,6% maschi). Dopo un tempio mediano di 32 mesi, l’89,6% dei pazienti è risultato in soppressione virologica, mentre il 6,5% ha presentato fallimento virologico e il 3,9% ha interrotto il trattamento per eventi avversi (rash cutaneo o tossicità epatica) (10). Anche in questo caso è stata rilevata una riduzione significativa dei livelli di trigliceridi e un miglioramento della funzionalità renale.
In un altro studio clinico prospettico sono stati osservati 38 pazienti afferenti a un Ospedale del Centro Italia con diagnosi di HIV e in soppressione virologica, provenienti da un regime HAART caratterizzato da due NRTI e PI/r avviati a un regime semplificato con raltegravir/etravirina (11). La motivazione che aveva determinato il passaggio al regime semplificato era stata in 29 casi la tossicità e nei rimanenti nove casi la resistenza a NRTI (11). Nessun paziente presentava un precedente fallimento a raltegravir o mutazioni di resistenza a etravirina. A 48 settimane dal cambio di terapia, la percentuale di pazienti con HIV-RNA <20 copie/ml è stata dell’81,6%. Il passaggio al regime semplificato ha determinato una significativa riduzione dei livelli dei trigliceridi (-81,2 mg/dl), del colesterolo (-44,3 mg/dl), della prevalenza della proteinuria (-30,2%), un significativo aumento della fosforemia (+0,52 mg/dL) e della densità minerale ossea (circa +5,6%) (11). Due pazienti hanno manifestato un fallimento terapeutico a causa di scarsa aderenza, cinque hanno interrotto il trattamento a causa di eventi avversi (11).
I risultati di queste esperienze mostrano come, in un ben definito setting di pazienti, il passaggio a una duplice terapia con nevirapina/raltegravir o etravirina/raltegravir permetta di mantenere nel lungo periodo un'adeguata soppressione virologica.
Per quanto riguarda il terzo NNRTI, rilpivirina, e il possibile regime di combinazione raltegravir/rilpivirina, escludendo alcuni casi aneddotici (<1% delle Dual Therapy arruolate nella corte ICONA) (12), allo stato attuale non esistono, a nostra conoscenza, studi spontanei o trial registrativi basati su quest'ultima combinazione.
Oltre che per la rilevanza clinica, la semplificazione dei regimi cART è stata valutata anche come potenziale fonte di risparmio economico dovuto alla diminuzione del numero di molecole somministrate o all'eventuale utilizzo, ove possibile, di farmaci generici o bio-equivalenti. A tale proposito una recente analisi finanziaria condotta presso l'Unità Operativa di Malattie Infettive dell'Ospedale “G.B. Rossi” di Verona ha dimostrato che l'utilizzo del regime semplificato nevirapina/raltegravir è in grado di determinare una riduzione potenziale fino al 29,6% della spesa complessiva per farmaci antiretrovirali a carico del Centro (13).
Obiettivo
La presente analisi è stata condotta con l'obiettivo di stimare, a parità di livello di efficacia di cura erogata, il potenziale impatto finanziario conseguente al passaggio da regimi HAART a un regime semplificato composto da raltegravir in combinazione rispettivamente con nevirapina, etravirina o rilpivirina nel trattamento di mantenimento dei pazienti HIV-1 infetti in soppressione virologica da almeno 1 anno e con una tossicità correlabile al regime HAART ricevuto.
Metodi
Disegno dello studio e definizione del campione
L'analisi, osservazionale retrospettiva non interventistica, è stata condotta presso l'Unità Operativa Complessa di Malattie Infettive dell'Azienda Ospedaliera di Rilievo Nazionale e di Alta Specializzazione Garibaldi di Catania (d'ora in poi identificata nel testo come “Centro”). È stata presa in considerazione la coorte di pazienti HIV-infetti che al primo dicembre 2015 afferivano al Centro. All'interno di questa coorte sono stati identificati i pazienti in trattamento con un regime HAART (2 NRTI + PI/r, 2 NRTI + NNRTI) in soppressione virologica da almeno 12 mesi (mantenimento nel corso dell'anno di una carica virale <50 copie/ml) e senza una precedente esposizione a un inibitore dell'integrasi (INI). Tra questi, quale giustificazione clinica del cambio di terapia, sono stati infine considerati soltanto i pazienti che all'inizio del periodo di osservazione presentavano una tossicità [es. dislipidemia, ipercolesterolemia, eGFR <60 ml/min stimato con il CKD-EPI, osteopenia e/o osteoporosi (misurata all'esame DEXA o alla QUS)] correlabile al regime HAART ricevuto.
Tutti i pazienti che alla data di arruolamento soddisfacevano i criteri di selezione sono stati seguiti per i 12 mesi successivi (fino a novembre 2016) con l'obiettivo di calcolare l'effettiva spesa per la terapia antiretrovirale a carico del Centro. Successivamente, è stata ricostruita la spesa per la terapia antiretrovirale potenziale, riconducibile al passaggio ai regimi di semplificazione costituiti dalla combinazione nevirapina 400 mg/die o etravirina 200 mg BID o rilpivirina 25 mg/die in associazione con raltegravir 400 mg BID.
Costo di trattamento
Con lo scopo di calcolare l'effettiva spesa per la terapia antiretrovirale a carico del Centro, per ogni paziente considerato, in riferimento all'arco temporale dicembre 2015-novembre 2016, è stato rilevato il rispettivo costo annuo generato dalla terapia antiretrovirale ricevuta. Tale costo è stato calcolato sulla base del prezzo di acquisto dei farmaci al netto di tutti gli sconti (obbligatori e no) e comprensivo di IVA (10%) effettivamente sostenuto dalla Farmacia Ospedaliera del Centro durante i 12 mesi di osservazione.
Analisi dei costi
Sulla base di quanto proposto in analisi comparabili (13), sono stati confrontati due scenari: quello “reale”, dove la spesa per gli antiretrovirali è composta dai costi reali generati dai regimi HAART, e quello “potenziale”, dove tale spesa è composta dai costi potenziali associati ai regimi semplificati NNRTI/raltegravir. In quest'ultimo caso la spesa per i farmaci antiretrovirali è stata costruita considerando un costo medio annuo di €5.526 nel caso di un paziente trattato con il regime nevirapina/raltegravir, di €10.158 nel caso del regime etravirina/raltegravir e di €8.148 nel caso del regime raltegravir/rilpivirina (8, 10, 13). Il costo giornaliero di raltegravir, etravirina e rilpivirina è stato valorizzato considerando un costo di acquisto pari rispettivamente a €14,63, €13,20 ed €7,69, mentre per nevirapina, essendo presente sul mercato la specialità generica, ma in assenza di uno specifico dato fornito dalla Farmacia Ospedaliera del Centro, è stato considerato come proxy il prezzo di cessione applicato in Regione Veneto, pari a €0,36 per una compressa da 200 mg (costo/die €0,72) (14). Infine il costo giornaliero è stato prima estrapolato al mese (moltiplicandolo per 30 giornate) e successivamente all'anno (moltiplicandolo per 12 mesi).
Analisi dei dati
Le variabili quantitative sono state descritte come valore medio (±deviazione standard), mentre quelle categoriche come valore numerico (percentuale). La significatività delle differenze tra i dati rilevati/elaborati è stata verificata applicando il test t di Student (a due code). L'analisi è stata supportata dai programmi Microsoft® Excel® per Windows® (Microsoft Corporation, Seattle, WA, USA) e SPSS® versione 13.0 per Windows® (SPSS Inc., Chicago, IL, USA).
Risultati
Caratteristiche del campione
A dicembre 2015 afferivano al Centro 550 pazienti con diagnosi di HIV. Di questi, 116 (21,1%) soggetti [81 maschi (69,8%), età media 51,3 (±11,7) anni] sono stati inclusi nella presente analisi. Il tempo medio dalla diagnosi di HIV era di 4,3 (±2,3) anni. La Figura 1 riporta invece la stratificazione del campione in base alla classificazione del Centers for Disease Control (CDC) di Atlanta (USA) dell'infezione da HIV e dell'AIDS; circa il 60% dei pazienti è stato classificato come CDC A.
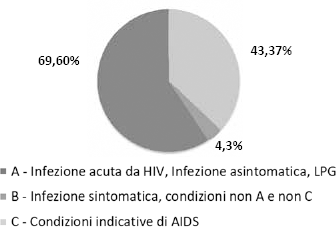
Distribuzione dei pazienti in base alla classificazione del Centers for Disease Control (CDC) dell'infezione da HIV e dell'AIDS. LPG = linfoadenopatia persistente generalizzata.
La Tabella I riporta le principali caratteristiche cliniche dei pazienti all'arruolamento (dicembre 2015). Durante i 12 mesi di osservazione tutti i pazienti hanno mantenuto una carica virale inferiore alle 50 copie/ml. In nessun caso sono state riscontrate mutazioni di resistenza associate a NNRTI o INI.
Principali caratteristiche cliniche del campione
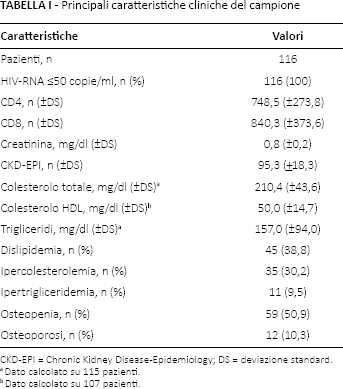
CKD-EPI = Chronic Kidney Disease-Epidemiology; DS = deviazione standard.
Dato calcolato su 115 pazienti.
Dato calcolato su 107 pazienti.
Nei 12 mesi di osservazione, 74 (63,8%) soggetti sono stati trattati con un regime HAART costituito da 2 NRTI + 1 NNRTI; ai restanti 42 (36,2%) pazienti è stato somministrato un regime complesso costituito da 2 NRTI + 1 PI/r.
Costo di trattamento
Per trattare i 116 soggetti con regime HAART il Centro ha speso mediamente nell'anno €7.499 (± 1.751) (Tab. II). Alla combinazione 2 NRTI + 1 PI è associato il costo medio annuo maggiore (€8.857 ± 1.893). La differenza di costo (€2.128) rispetto alla combinazione 2 NRTI + 1 NNRTI (€6.728 ± 1.074) è risultata statisticamente significativa (p<0,0001).
Costo medio annuo per paziente trattato e HAART ricevuta
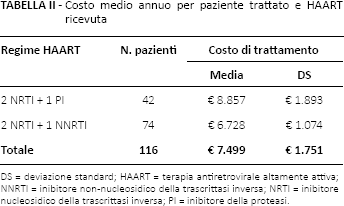
DS = deviazione standard; HAART = terapia antiretrovirale altamente attiva; NNRTI = inibitore non-nucleosidico della trascrittasi inversa; NRTI = inibitore nucleosidico della trascrittasi inversa; PI = inibitore della proteasi.
Analisi dei costi
Il costo totale sostenuto dal Centro per trattare i 116 pazienti con regime HAART è risultato pari a €869.889, di cui circa il 57% generato dai pazienti in trattamento con 2 NRTI + 1 NNRTI (€497.907) (Tab. III). Nell'ipotesi del passaggio da un regime complicato al regime semplificato nevirapina/raltegravir, la spesa a carico del Centro diminuirebbe di €228.873 (-26,3%). Nonostante la minore numerosità di pazienti (n = 42), ma in virtù di una maggiore differenza tra i costi medi annui di trattamento (€2.128), lo switch al regime semplificato nevirapina/raltegravir dei pazienti attualmente in trattamento con 2 NRTI + 1 PI/r (-37,6%; -€139.891) determinerebbe la principale componente di riduzione della spesa a carico del Centro. Più contenuto risulterebbe invece il risparmio rispetto al regime 2 NRTI + 1NNRTI (-17,9%; -€88.893).
Analisi dei costi: HAART vs NNRTI/RAL
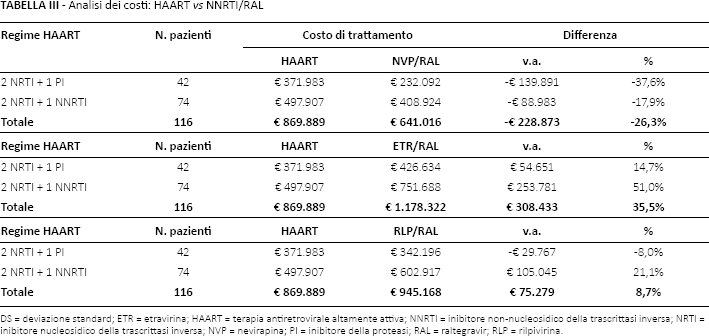
DS = deviazione standard; ETR = etravirina; HAART = terapia antiretrovirale altamente attiva; NNRTI = inibitore non-nucleosidico della trascrittasi inversa; NRTI = inibitore nucleosidico della trascrittasi inversa; NVP = nevirapina; PI = inibitore della proteasi; RAL = raltegravir; RLP = rilpivirina.
Considerando gli altri due regimi semplificati, raltegravir/etravirina e raltegravir/rilpivirina, si registrerebbe invece un incremento della spesa del 35,5% e dell’8,7%, rispettivamente (Tab. III). Solo il confronto tra i regimi raltegravir/rilpivirina e 2 NRTI + 1 PI/r determinerebbe una riduzione della spesa a carico del Centro (-8,0%, pari a -€29.767), non sufficiente tuttavia a controbilanciare l'aumento di spesa determinato rispetto ai regimi 2 NRTI + 1 NNRTI (+17,9%, pari a +€105.045) (Tab. III).
Discussione
Alcuni regimi antiretrovirali semplificati, quando somministrati a particolari coorti di pazienti con HIV, sembrano in grado – a parità di soppressione virologica – di determinare il raggiungimento di una più efficiente allocazione delle risorse disponibili. Infatti, qualora fosse possibile realizzare uno switch al regime nevirapina/raltegravir per tutti i 116 pazienti qui considerati, la spesa annuale sostenuta dal Centro di Catania per la terapia cART si ridurrebbe di circa €230.000, rispetto ai circa €870.000 realmente sostenuti per trattare gli stessi pazienti con i regimi di triplice terapia.
Questo risultato conferma quanto rilevato in un'analoga esperienza condotta presso l'Unità Operativa di Malattie Infettive dell'Ospedale “G.B. Rossi” di Verona (13). Le caratteristiche demografiche (età media, sesso ecc.), cliniche (conta dei CD4) e la numerosità dei pazienti afferenti ai due Centri (Verona e Catania) appaiono sovrapponibili. Nell'anno di osservazione (2014) al Centro di Verona afferivano 667 pazienti in terapia antiretrovirale, di cui 103 (15,4%) eleggibili allo switch. A fine 2015 erano 550 i pazienti in terapia antiretrovirale che afferivano al Centro di Catania, di cui 116 (21,1%) eleggibili a una terapia semplificata (switch). Nello studio di Verona il maggior numero di pazienti veniva trattato con 2 NRTI + 1 PI (51%), mentre in quello di Catania è il regime 2 NRTI + 1 NNRTI a essere maggiormente utilizzato (64%). Ciò potrebbe riflettere una possibile differenza nell'approccio al trattamento. La differenza di €409 tra il costo medio annuo per paziente trattato del Centro di Verona (€7.908) rispetto a quello di Catania (€7.499) non è risultata statisticamente significativa (p = 0,11). In entrambi i casi i pazienti trattati con 2 NRTI + 1 PI/r determinano il maggior costo medio annuo di trattamento (Verona: €9.439; Catania: €8.857; p = 0,11) rispetto a quelli trattati con 2 NRTI + 1 NNRTI (Verona: €6.432; Catania: €6.728; p = 0,16). Il cambio di terapia verso il regime semplificato nevirapina/raltegravir determinerebbe in tutti e due i Centri una riduzione potenziale di circa un terzo della spesa sostenuta per i farmaci antiretrovirali.
Differentemente da quanto realizzato nello studio condotto a Verona, al fine di completare lo scenario proposto, nella presente analisi è stato valutato anche il potenziale impatto finanziario a carico del Centro derivante dall'impiego dei regimi semplificati etravirina/raltegravir (costo medio annuo per paziente trattato: €10.158) e raltegravir/rilpivirina (costo medio annuo per paziente trattato: €8.148), meno convenienti rispetto al regime nevirapina/raltegravir (costo medio annuo per paziente trattato: €5.526).
L'utilizzo del regime etravirina/raltegravir, caratterizzato da un costo medio annuo per paziente trattato (€10.158) sensibilmente superiore a quello dei regimi 2 NRTI + 1 PI (€8.857) e 2NRTI + 1 NNRTI (€6.728), determinerebbe un aumento del 35,5% della spesa per la terapia antiretrovirale del Centro. A livello di singolo paziente in trattamento con regime HAART, soltanto in 5 casi su 116 si evidenzierebbe un costo medio annuo per paziente trattato superiore a quello associato al regime etravirina/raltegravir.
Il costo medio per paziente trattato associato al regime raltegravir/rilpivirina (€8.148) risulterebbe invece vantaggioso rispetto ai regimi con 2 NRTI + 1 PI (€8.857), ma non conveniente rispetto a quelli con 2 NRTI + 1 NNRTI (€6.728). A causa della maggiore numerosità dei pazienti trattati con questi ultimi regimi, l'impatto finanziario conseguente l'utilizzo del regime raltegravir/rilpivirina determinerebbe un aumento dell’8,7% della spesa a carico del Centro. Oltre alla mancanza di dati in letteratura sul mantenimento della soppressione virologica, nonostante il regime raltegravir/rilpivirina sia potenzialmente caratterizzato da un minore rischio di interazioni farmacologiche, la bassa barriera genetica e l'asimmetria posologica costituiscono le principali limitazioni a un suo utilizzo.
Da questa prima analisi i regimi semplificati etravirina/raltegravir e rilpivirina/raltegravir non sembrerebbero essere economicamente vantaggiosi. In realtà, i risultati presentati in questa sede sono riconducibili alla sola variazione della spesa per gli antiretrovirali determinata dallo switch nel breve periodo (12 mesi). Non sono stati, ad esempio, valorizzati altri aspetti conseguenti al cambio di terapia, quale la riduzione dei costi per le terapie di supporto (dislipidemia, osteopenia, comorbidità cardiovascolari ecc.) e per gli esami clinici necessari per monitorare gli eventuali eventi avversi (semplificazione proattiva) generati dalla terapia HAART (15–19). Una corretta valutazione della sostenibilità dello switch dovrebbe in realtà coprire un più ampio orizzonte temporale (medio-lungo periodo) idoneo a includere nell'analisi anche il consumo di altre risorse sanitarie (farmaci concomitanti, prestazioni specialistiche, ricoveri, accessi in day-hospital ecc.) erogate per il trattamento di questi pazienti. L'inclusione di questi elementi potrebbe rendere più vantaggioso l'utilizzo dei regimi etravirina/raltegravir e rilpivirina/ raltegravir.
È necessario infine leggere i presenti risultati alla luce di alcune osservazioni. Prima fra tutte l'impossibilità di condurre uno studio caso-controllo e di conseguenza la necessità di ipotizzare che, malgrado la somministrazione di un regime semplificato, venga mantenuta la soppressione virologica (8, 10). Un secondo punto di riflessione è costituito dal costo medio associato al paziente in trattamento con i tre regimi a base di raltegravir. Tale costo si basa su un calcolo teorico effettuato sui dosaggi indicati in letteratura (8, 10, 13), ipotizzando un'aderenza del 100% nell'anno. Tale scelta, in realtà, potrebbe avere sottostimato i risultati qui trovati, escludendo di fatto la possibile presenza di casi di under-consumption, pur mantenendo la risposta virologica.
Conclusioni
La presente valutazione economica, condotta con l'obiettivo di verificare i risultati elaborati in un'analoga analisi condotta in un Centro del Nord Italia, ha confermato che la somministrazione del regime semplificato nevirapina/raltegravir, nel trattamento di specifiche coorti di pazienti con HIV – a parità di mantenimento della soppressione virologica – è in grado di determinare una più efficiente allocazione delle risorse disponibili, riducendo di circa un terzo gli attuali costi per i farmaci antiretrovirali a carico della Farmacia Ospedaliera.
Footnotes
Financial support: No financial support was received for this submission.
Conflict of interest: BMC was member of board and received travel grants and speaker's honoraria from BMS, MSD, Abbvie, Janssen, ViiV and Gilead. The other authors have no conflict of interest.
