Abstract
Intravitreal corticosteroids for the treatment of macular edema: review and assessment of quality of the evidence
Introduction
Treatment options for macular edema include intravitreal corticosteroids. Traditionally, an injectable suspension of triamcinolone acetonide (TA) had been employed off-label; in recent years, authorities have approved sustained-release drug delivery systems (DDSs) for corticosteroids. This review aims to compare the quality of the evidence on efficacy and safety of three different formulations of intravitreal corticosteroids: the dexamethasone (DEX) implant, the fluocinolone acetonide (FA) implant, and the preservative-free injectable suspensions of TA, in the management of two retinal pathologies: diabetic macular edema (DME) and macular edema secondary to retinal vein occlusion (RVO).
Methods
A search of clinical trials on MEDLINE from 01/01/2000 to 12/16/2015 was performed. Studies were included in the analysis if they met the following criteria: i) related to at least one of the preparations of interest in patients with DME or macular edema secondary to RVO; ii) included a control group treated with placebo, observation, sham procedures or conventional treatments; and iii) included visual acuity, retinal thickness and/or safety parameters as outcomes. Results were summarized in a narrative manner.
Results
Twenty-five publications from 19 RCTs were included. We observed increased attention of researchers towards TA compared to DEX and FA; however, studies for TA are less robust. Scientific publications related to DEX and FA implants are of higher quality, especially in terms of randomization and masking procedures.
Discussion
Although trials on TA are numerous, evidence on DEX and FA implants is more robust. Since their introduction, these relatively new DDSs have been included in the main guidelines for the management of macular edema.
Keywords
Introduzione
L'edema maculare si verifica quando si accumulano liquidi e proteine nello spazio extracellulare della retina neurosensoriale, e si caratterizza da un ispessimento della macula. Tale patologia si manifesta, principalmente, come complicanza di disturbi infiammatori, di retinopatie vascolari (tra le quali la retinopatia diabetica e l'occlusione venosa retinale) e della neovascolarizzazione coroideale (1).
La disabilità visiva associata all'edema maculare ha un grande impatto sulla qualità della vita dei pazienti nonché sulla sanità pubblica. Tale impatto giustifica il notevole interesse dei ricercatori nei confronti dei trattamenti utilizzati per questa patologia.
Nel presente documento si terrà conto di due condizioni in particolare, per le quali sono indicati i corticosteroidi intravitreali:
Edema maculare diabetico (DME): la retinopatia diabetica costituisce una complicanza microvascolare del diabete, ed è prevalente nel 34,6% dei diabetici (2). Quando in questa condizione si presenta la rottura della barriera emato-retinica (BER), si verifica il DME, prevalente nel 6,81% degli individui con diabete (2). Il DME è la principale causa di perdita della vista in questi pazienti.
Edema maculare secondario all'occlusione di una branca della vena centrale della retina (BRVO) o all'occlusione della vena centrale della retina (CRVO): l'occlusione venosa retinica (RVO) è un'ostruzione del sistema venoso della retina dovuta alla formazione di trombi. La causa più comune è la compressione da arterie retiniche aterosclerotiche adiacenti. Altri possibili fattori eziologici sono la compressione esterna o la presenza di malattie della parete venosa quali la vasculite. La RVO può coinvolgere la vena centrale della retina (CRVO) o una sua branca (BRVO) (3). Le due complicanze principali della RVO sono l'edema maculare e l'ischemia retinica, la quale porta alla neovascolarizzazione dell'iride e della retina. L'edema maculare è la causa più comune della disabilità visiva nei pazienti con RVO, seguita dall'ischemia foveale (3).
I farmaci intravitreali consentono di somministrare una quantità efficace di farmaco nella camera vitrea garantendone un'azione mirata e la riduzione della dose circolante, limitando il rischio di eventi avversi sistemici (4). Per quanto riguarda i corticosteroidi somministrati per via intravitreale, storicamente è stata utilizzata la sospensione iniettabile di triamcinolone acetonide; negli ultimi anni, per prolungarne gli effetti e per limitare il numero di somministrazioni, sono stati autorizzati dalle autorità competenti (FDA, EMA e AIFA) impianti intravitreali a rilascio prolungato controllato: Iluvien® (fluocinolone acetonide) e Ozurdex® (desametasone). Questi tre farmaci costituiscono l'oggetto della presente revisione; nella Tabella I si presentano in maniera sintetica le loro caratteristiche.
Farmaci oggetto dello studio
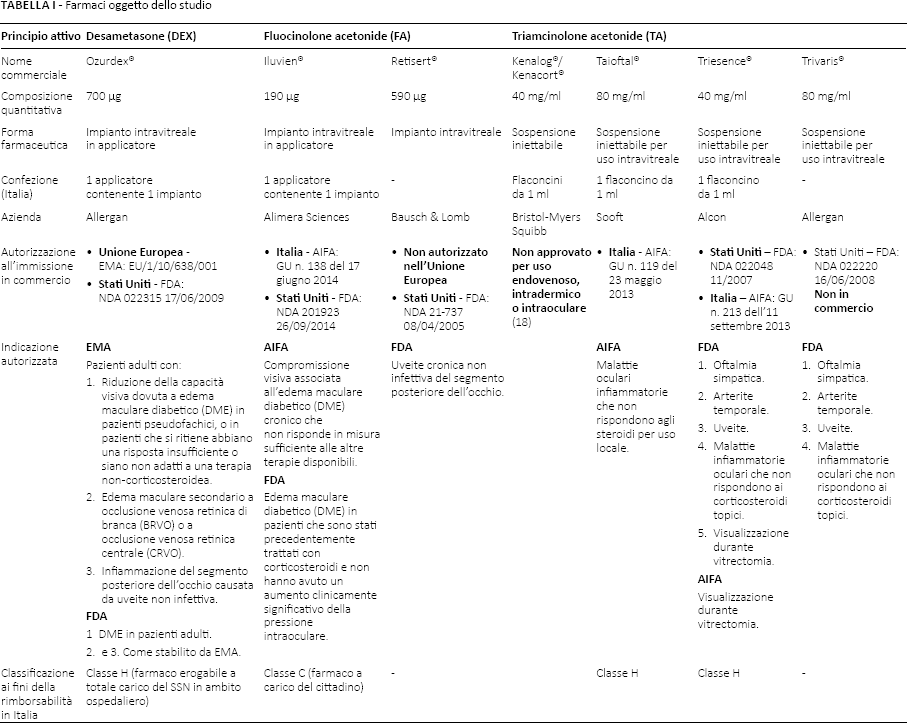
Considerando l'ipotesi che i farmaci esaminati vengano utilizzati sulla base di evidenze ampiamente variabili in termini di qualità metodologica e di robustezza, lo scopo della presente analisi è stato appunto verificare se le evidenze presenti in letteratura fossero comparabili tra loro in termini qualitativi. Una migliore analisi della qualità delle evidenze a corredo dei farmaci potrebbe infatti influenzare i processi approvativi e le raccomandazioni di utilizzo.
Nel primo decennio degli anni 2000, triamcinolone acetonide (TA) è stato ampiamente utilizzato off-label, per via intravitreale o perioculare, nel trattamento di diversi disturbi del vitreo e della retina (5–11), compresi l'infiammazione intraoculare e l'edema maculare, così come per la visualizzazione intraoperatoria durante vitrectomia.
Tra le formulazioni di TA presenti in commercio, quella usata più comunemente contiene alcool benzilico come conservante nel veicolo (Kenalog®-40/Kenacort®, Bristol-Myers Squibb) (12, 13). È stato suggerito che questo conservante sia responsabile di potenziali effetti tossici sulla retina (14–16) e di eventi avversi come l'endoftalmite (17), a tale punto che l'Agenzia Italiana del Farmaco (AIFA) avverte che si deve evitare la somministrazione di Kenacort® per via intravitreale (18), la quale costituisce un utilizzo off-label. Pertanto, gli studi riguardanti le specialità Kenacort®/Kenalog-40® e Triamhexal® (Hexal AG), sospensioni di TA contenenti conservanti, sono stati esclusi dalla presente revisione.
Tuttavia, non è confermato che l'alcool benzilico sia l'unica causa degli eventi avversi (17); inoltre, non è chiaro se il TA senza conservanti (preservative-free TA, PFTA) abbia effettivamente una minore probabilità di causare una risposta infiammatoria, in confronto al TA con conservanti (17, 19, 20).
Gli eventi avversi più comuni associati alla somministrazione intravitreale di TA sono l'aumento della pressione intraoculare (21) e la progressione della cataratta (22). Un evento avverso meno frequente è l'endoftalmite. Questa condizione è stata descritta in tre forme: endoftalmite infettiva, endoftalmite non infettiva o sterile e pseudoendoftalmite (17). L'incidenza di endoftalmite associata alla somministrazione intravitreale di TA è molto variabile; ricavare conclusioni dai dati pubblicati richiede un'attenta valutazione poiché la maggior parte degli studi sono retrospettivi e utilizzano protocolli e agenti terapeutici diversi (23).
Una percentuale tra lo 0,87% e il 7,3% (24, 25) dei pazienti sviluppa l'endoftalmite non infettiva o sterile poco dopo l'iniezione intravitreale di TA o PFTA. Questa condizione è una reazione infiammatoria acuta nella quale, di solito, l'acuità visiva diminuisce in modo significativo, ma i pazienti raramente esperimentano dolore o disagio. Il miglioramento è veloce con una buona prognosi visiva.
I pazienti con endoftalmite infettiva acuta presentano diminuzione della vista e dolore durante un periodo mediano di 7,5 giorni dopo l'iniezione; questa complicanza di solito ha un tempo di recupero prolungato ed è associata a risultati meno positivi in termini di acuità visiva (26). L'endoftalmite infettiva ha un'incidenza stimata tra lo 0,43% e lo 0,87% (26, 27).
D'altra parte, la pseudoendoftalmite è causata dalla migrazione di cristalli di TA nella camera anteriore, e non dall'infezione. I pazienti non presentano dolore; i sintomi della vista sono minimi e si risolvono senza trattamento nel giro di pochi giorni (28, 29). L'incidenza di pseudoendoftalmite è tra lo 0,1% e il 6,7% (30–32).
I rapporti compilati nella banca dati europea delle segnalazioni di sospette reazioni avverse ai farmaci EudraVigilance (33) per il triamcinolone, concernenti i disturbi oculari, sono (aggiornati a marzo 2016) riferiti a: ipertensione oculare (22 casi), cataratta (59 casi), endoftalmite non infettiva (8 casi) e pseudoendoftalmite (7 casi).
A causa delle potenziali reazioni avverse correlate all'alcool benzilico, l’American Academy of Ophthalmology ha richiesto lo sviluppo di una formulazione di Kenalog®-40 (Kenacort®) senza conservanti (34). Le preparazioni galeniche di PFTA (formulazioni con conservanti che vengono “purificate”) sono successivamente divenute disponibili, ma sono state sostituite in gran parte dal PFTA commercializzato con approvazione della FDA per uso intraoculare (Triesence®, Alcon Laboratories). Un secondo PFTA ha ricevuto l'approvazione negli Stati Uniti per l'uso intraoculare (Trivaris®, Allergan Inc), ma non è stato commercializzato. In Italia, l'immissione in commercio del PFTA Taioftal® (Sooft) è stata autorizzata nel 2013.
Tuttavia, le differenze tra le formulazioni commerciali di PFTA e la sospensione di TA con conservanti che viene “purificata” (e che, quindi, non contiene conservanti) non sono ben specificate, anche se i produttori dei primi commercializzano il prodotto come “specifico per l'occhio” (35).
Inoltre, in assenza di studi clinici di confronto diretto, la sovrapponibilità tra le diverse formulazioni di PFTA non è nota. Zacharias et al (13) hanno suggerito che il fatto che esse contengano cristalli di triamcinolone di diverse dimensioni in sospensione potrebbe comportare diversità dei profili farmacocinetici (es. eliminazione dall'occhio) e farmacodinamici (durata dell'efficacia e comparsa di eventi avversi) tra le formulazioni.
La ricerca di un sistema di erogazione o via di somministrazione dei corticosteroidi che permetta di erogarli direttamente nel segmento posteriore dell'occhio e di ridurre al minimo l'assorbimento sistemico (pertanto, provocando minore tossicità), oltre a ridurre la necessità d'iniezioni intraoculari frequenti e i tassi di complicanze oculari, ha portato allo sviluppo d'impianti intravitreali di corticosteroidi a rilascio prolungato.
Seguendo l'anno di pubblicazione delle linee guida (3, 40–46) per il trattamento delle malattie d'interesse (Tab. II), si nota come si sia assistito nel tempo a un'evoluzione delle indicazioni sui diversi corticosteroidi consigliati. Le linee guida più datate riflettono la disponibilità del solo triamcinolone come corticosteroide, mentre a partire dal 2014 la disponibilità dei nuovi prodotti ha permesso di sostituirlo con questi agenti di più recente introduzione.
Linee guida
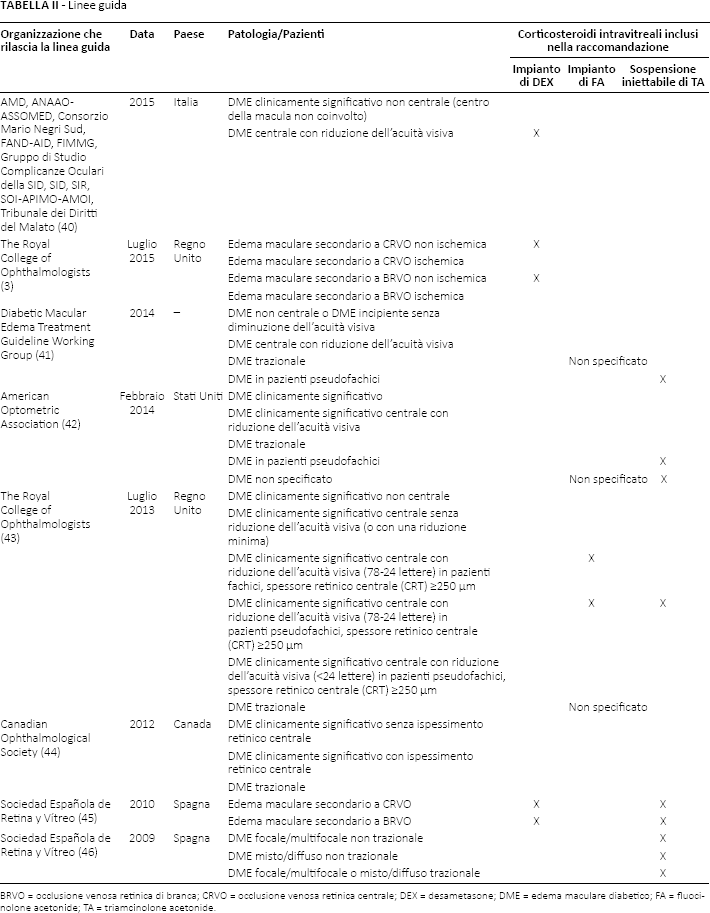
BRVO = occlusione venosa retinica di branca; CRVO = occlusione venosa retinica centrale; DEX = desametasone; DME = edema maculare diabetico; FA = fluocinolone acetonide; TA = triamcinolone acetonide.
Obiettivo
Comparare la qualità dell'evidenza sull'efficacia e la sicurezza di tre diverse formulazioni di corticosteroidi (impianto di desametasone, impianto di fluocinolone acetonide e sospensione iniettabile di triamcinolone acetonide senza conservanti) comprese nelle principali linee guida e approvate all'immissione in commercio in Europa e/o negli Stati Uniti per il trattamento di tre diverse patologie dell'occhio [edema maculare diabetico (DME); edema maculare secondario a occlusione venosa retinica di branca (BRVO) o a occlusione venosa retinica centrale (CRVO)].
Metodologia
La presente revisione e valutazione della qualità dell'evidenza deriva da un'analisi descrittiva della distribuzione nel tempo delle pubblicazioni che esaminano ognuna delle tre formulazioni di corticosteroidi per via intravitreale sotto studio, le quali sono state classificate inoltre secondo i livelli di evidenza.
Inizialmente, al fine di individuare le terapie indicate per il trattamento dell'edema maculare sulle quali basare la ricerca in letteratura, è stata eseguita una ricerca delle linee guida esistenti che offrono raccomandazioni per il trattamento di questa malattia, pubblicate in lingua inglese o italiana dal 2006. Questa ricerca è stata effettuata con l'unico termine di ricerca “macular edema” su: banca dati MEDLINE attraverso il motore di ricerca PubMed, Centre for Reviews and Dissemination (CRD), e National Guidance Clearinghouse dell'AHRQ (www.guideline.gov); e con i termini di ricerca “macular edema” AND “guideline” su Google Scholar. I risultati della ricerca sono presentati nell'Introduzione della presente revisione per illustrare la descrizione dell'intervento oggetto di studio.
La strategia di ricerca principale è stata finalizzata a identificare gli studi pubblicati da gennaio 2000 al momento della ricerca (16/12/2015) sulla banca dati MEDLINE attraverso il motore di ricerca PubMed. La stringa di ricerca è riportata di seguito: ((((((((Retinal disorders) OR “Retinal Diseases”[Mesh]) OR retinal disease) OR (((“Macular Edema”[Mesh]) OR diabetic macular edema) OR DME)))))) AND ((((((“Triamcinolone acetonide”[Mesh]) OR triamcinolone acetonide)) OR ((“Dexamethasone”[Mesh]) OR dexamethasone)) OR ((“Fluocinolone acetonide”[Mesh]) OR fluocinolone acetonide)) OR intravitreal corticosteroids). Nella ricerca sono stati applicati i seguenti limiti: (i) Tipologia di studio: Case Reports, Clinical Trial, Controlled Clinical Trial, Observational Study, Randomized Controlled Trial; (ii) Disponibilità: Abstract; (iii) Periodo di pubblicazione: (dal 01/01/2000 al 16/12/2015); (iv) Lingua: (Inglese, Italiano); (v) Campo di ricerca: (Title); (vi) Genere: (Umani). Non sono state eseguite ricerche addizionali.
Per la presente valutazione sono stati considerati unicamente gli studi clinici d'accordo con la struttura PICO riportata nella Tabella III. Gli studi sono stati scelti in modo sequenziale, in base alla lettura dei titoli e degli abstract. I testi completi sono stati ulteriormente analizzati. I dati sulla struttura degli studi selezionati sono stati estratti e compilati in una tabella; successivamente, è stato utilizzato lo strumento della Cochrane Collaboration (47) per la valutazione del rischio di bias degli studi (Tab. IV). I risultati della revisione e della valutazione sono stati riportati e sintetizzati in modo narrativo.
Struttura PICO del quesito di ricerca
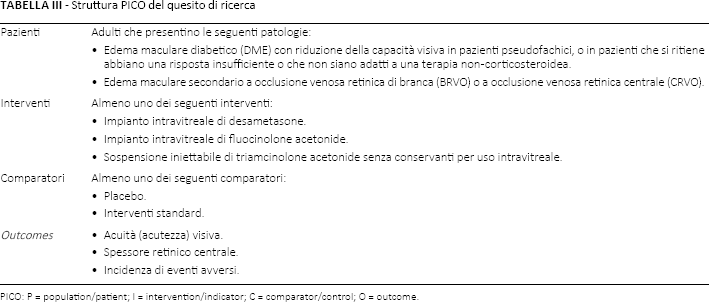
PICO: P = population/patient; I = intervention/indicator; C = comparator/control; O = outcome.
Schema per la valutazione del rischio di bias (47)

Risultati
Sono state identificate 25 pubblicazioni che si riferiscono a 19 studi, le cui caratteristiche sono sintetizzate nella Tabella V.
Studi inclusi nell'analisi
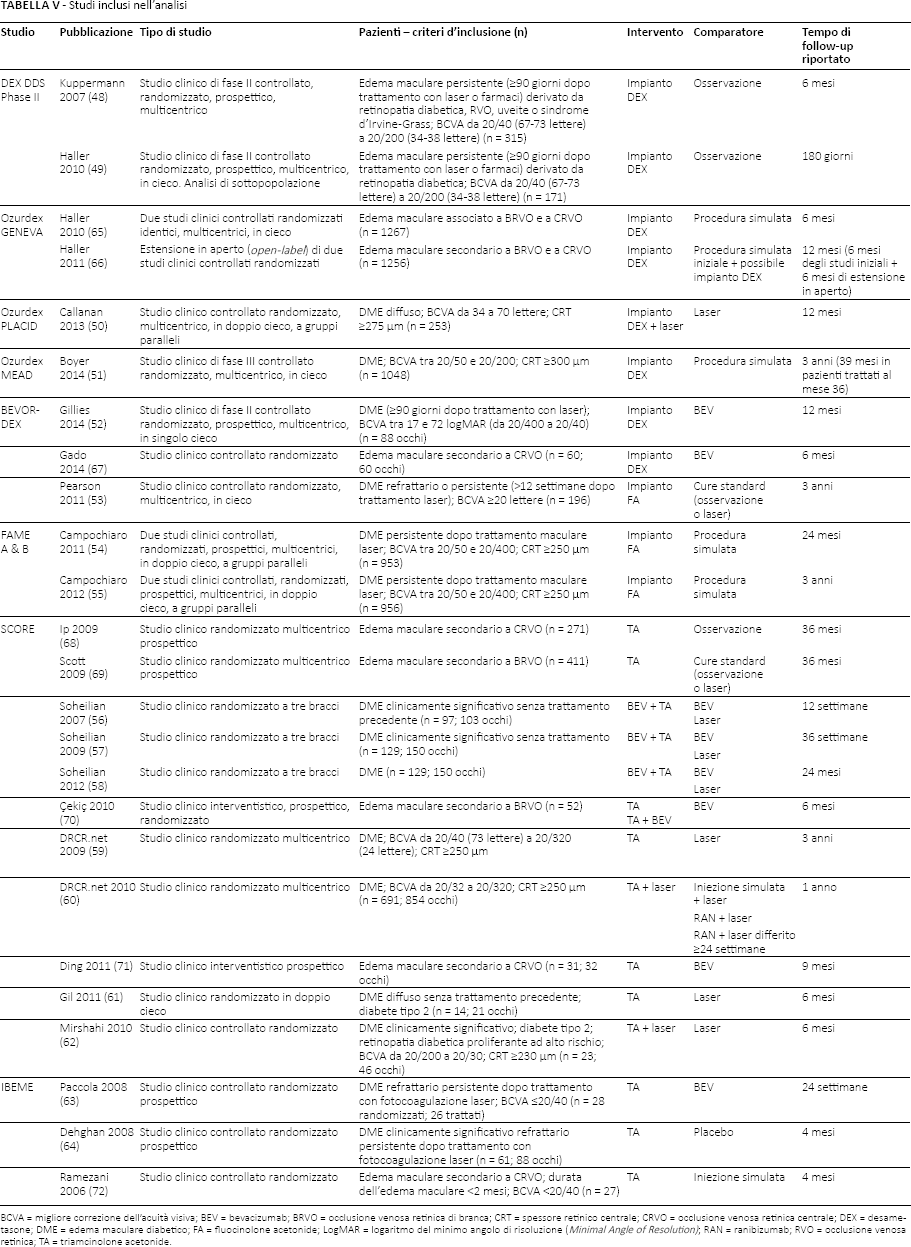
BCVA = migliore correzione dell'acuità visiva; BEV = bevacizumab; BRVO = occlusione venosa retinica di branca; CRT = spessore retinico centrale; CRVO = occlusione venosa retinica centrale; DEX = desametasone; DME = edema maculare diabetico; FA = fluocinolone acetonide; LogMAR = logaritmo del minimo angolo di risoluzione (Minimal Angle of Resolution); RAN = ranibizumab; RVO = occlusione venosa retinica; TA = triamcinolone acetonide.
Tutti gli studi analizzati corrispondono a trials clinici randomizzati e controllati. I dettagli sulle procedure di randomizzazione e il tipo di mascheramento vengono analizzati più avanti in questa sezione. I periodi di follow-up variavano tra i 6 e i 36 mesi. Il numero di pazienti arruolati in ogni studio variava da 14 a 1267 (21-1267 occhi).
Tredici studi hanno incluso pazienti con DME (DEX DDS Phase II (48, 49); PLACID (50); MEAD (51); BEVORDEX (52); Pearson et al (53); FAME (54, 55); Soheilian et al (56–58); DRCR.net, 2009 (59); DRCR.net, 2010 (60); Gil et al (61); Mirshahi et al (62); IBEME (63); Dehghan et al (64)); mentre i pazienti con edema maculare secondario a RVO sono stati analizzati in sette studi (DEX DDS Phase II (48, 49); GENEVA (65, 66); Gado et al (67); SCORE (68, 69); Çekiç et al (70); Ding et al (71); Ramezani et al (72)). Uno studio ha incluso un campione contenente pazienti con entrambe le diagnosi (DEX DDS Phase II). I criteri per l'inclusione dei partecipanti variano da studio a studio (Tab. V). Non è stato identificato alcuno studio che analizzasse l'impianto di FA in pazienti con edema maculare secondario a RVO.
Gli studi DEX DDS Phase II (48, 49), GENEVA (65, 66) e MEAD (51) analizzano l'impianto di DEX e hanno effettuato sperimentazioni con due dosaggi diversi del farmaco: 0,35 mg e 0,7 mg. Lo studio di Gado et al (67) e gli studi PLACID (50) e BEVORDEX (52), tra i più recenti per questa preparazione farmaceutica, hanno applicato come trattamento sperimentale unicamente la dose di 0,7 mg, che corrisponde alla dose approvata dagli organismi regolatori per il medicinale Ozurdex®.
Lo studio di Pearson et al (53) analizza un impianto di FA contenente una dose di 0,59 mg, che corrisponde al medicinale Retisert®, approvato negli Stati Uniti dalla FDA. D'altra parte, gli studi FAME A e B (54, 55), realizzati per l'approvazione del medicinale Iluvien®, sperimentano con due impianti che si differenziano tra di loro nella quantità di farmaco che rilasciano in forma controllata dentro il vitreo: 0,2 µg/die e 0,5 µg/die. Iluvien® rilascia inizialmente 0,25 µg di FA/die.
Gli studi SCORE (68, 69), DRCR.net (2009) (59) e DRCR.net (2010) (60) hanno sperimentato con una sospensione di PFTA approvata negli Stati Uniti, Trivaris®; lo studio IBEME (63) e quello di Ding et al (71) hanno utilizzato PFTA preparato dal laboratorio Ophthalmos (Sao Paulo, Brasile) e da Pharm Co (Kunming, China), mentre che per lo studio di Gil et al (61) è stata utilizzata una preparazione di PFTA non specificata. Gli altri studi (56–58, 62, 64, 70, 72) hanno applicato una sospensione di TA non specificata dagli articoli. Non sono stati reperiti studi che avessero utilizzato i medicinali Taioftal® o Triesence®, entrambi sospensioni di PFTA in commercio.
Inoltre, alcuni studi hanno esplorato le terapie combinate TA + fotocoagulazione laser (60, 62) o TA + anti-VEGF (56–58, 70).
Gli interventi scelti come controllo dai ricercatori includono la sola osservazione (48, 49, 53, 68, 69) o impianti o iniezioni simulati (65, 66, 51, 54, 55, 64, 72) e/o gli interventi convenzionali indicati per l'edema maculare, quali il trattamento di fotocoagulazione laser (50, 53, 56–62, 68, 69), o i farmaci anti-VEGF (52, 56–58, 60, 63, 67, 70, 71).
La maggior parte degli studi ha esplorato tutti gli outcomes d'interesse per la presente revisione: acuità visiva, spessore della retina e sicurezza (incidenza di eventi avversi). Le misure dell’outcome variano da studio a studio.
La qualità metodologica degli studi inclusi è stata valutata secondo il rischio di distorsione (bias) utilizzando lo strumento della Cochrane Collaboration. I risultati della valutazione sono presentati nella Tabella VI ed esaminati di seguito:
Valutazione del rischio di bias degli studi inclusi applicando la Cochrane check-list
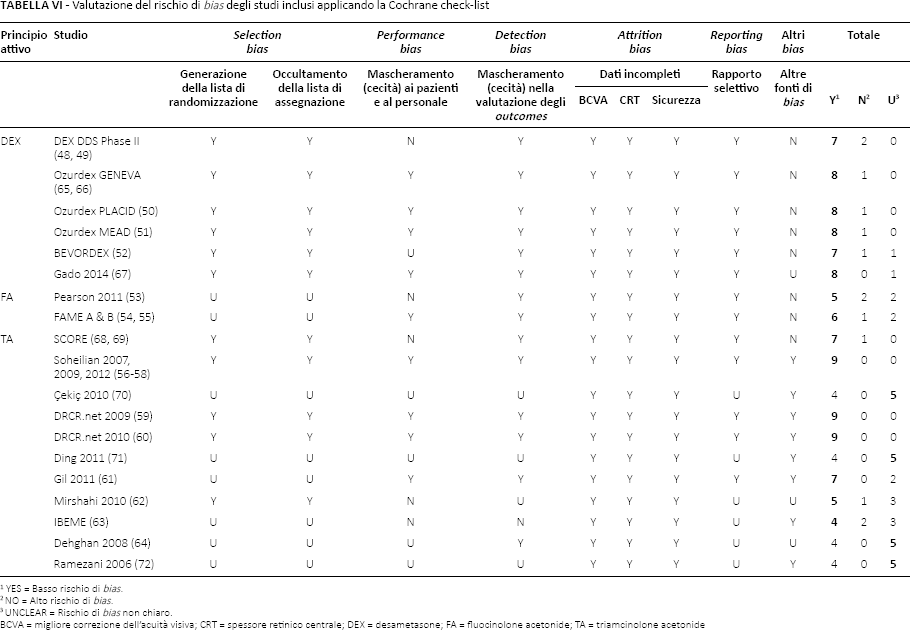
BCVA = migliore correzione dell'acuità visiva; CRT = spessore retinico centrale; DEX = desametasone; FA = fluocinolone acetonide; TA = triamcinolone acetonide
YES = Basso rischio di bias.
NO = Alto rischio di bias.
UNCLEAR = Rischio di bias non chiaro.
il numero di studi sull'impianto di DEX che presentano un basso rischio di bias in otto dei nove elementi della check-list Cochrane sono quattro (67%); gli altri due (33%) studi presentano un rischio basso in sette elementi della check-list;
gli studi sull'impianto di FA presentano risultati positivi in cinque (1 studio) e sei (1 studio) dei nove elementi della check-list;
tre studi sul TA intravitreale (27%) presentano un basso rischio di bias assoluto. Altri tre studi sul TA presentano un basso rischio di bias in otto (1 studio; 9%), sette (1 studio) e cinque (1 studio) dei nove elementi della check-list;
cinque degli studi sul TA (45%) presentano risultati negativi nell'analisi del rischio di bias.
È stato riscontrato che non tutti gli RCT inclusi nell'analisi presentano metodi chiari per l'allocazione di pazienti nei gruppi di studio.
In particolare, nel caso dell'impianto di FA, non sono chiari i metodi per l'allocazione di pazienti in nessuno dei due studi riportati; mentre nel caso della sospensione di TA, il rischio di bias è basso in cinque studi su undici (45%) e non chiaro nei restanti sei (55%). Tutti gli studi che analizzano l'impianto di DEX hanno compiuto procedure appropriate.
Il mascheramento è stato adeguato in quattro studi su sei (67%) relativi all'impianto di DEX, in uno studio su due (50%) relativi all'impianto di FA e in quattro studi su undici (36%) relativi al TA. Gli studi che hanno omesso informazioni sulle pratiche di mascheramento sono stati tre su undici (27%) relativi al TA; un altro studio sul TA (9%) ha avuto metodi non efficienti.
Per il 45% (n = 5) degli studi sul TA non sono stati ritrovati i protocolli che permettessero l'analisi dei metodi per l'individuazione del rischio di reporting bias.
Per la valutazione del rischio di altri bias, si è tenuta in conto la sponsorizzazione da parte dell'industria per l'esecuzione degli studi. Gli studi che hanno avuto questo tipo di sponsorizzazione sono stati classificati con alto rischio di bias, I risultati osservati si spiegano con il fatto che durante il periodo d'interesse, gli impianti intravitreali di corticosteroidi rappresentavano tecnologie per le quali l'industria aveva l'interesse di investire nella ricerca. Dall'altra parte, il TA è stato studiato dagli anni 1990, e durante il periodo 2000-2015 ha avuto un solo studio sponsorizzato.
Complessivamente, quindi, la qualità degli studi sull'impianto di DEX appare superiore. In questi studi l'unico elemento a rischio di bias è la sponsorizzazione dell'azienda produttrice degli impianti. Peraltro, trattandosi di una criticità comune negli studi registrativi di qualsiasi entità terapeutica, tale elemento non appare così rilevante da abbassare il livello complessivo di qualità delle evidenze. È inoltre da rimarcare il fatto che tale criticità, per altro verso, fornisce migliori garanzie nel senso dell'esecuzione degli studi in aderenza ai criteri di good clinical practice (GCP).
Discussione
Lo sviluppo di forme farmaceutiche che permettono un rilascio controllato e prolungato di corticosteroidi a livello intravitreale ha incrementato la disponibilità di studi recenti sugli impianti contenenti desametasone (DEX) e fluocinolone acetonide (FA) nel trattamento dell'edema maculare. Triamcinolone acetonide (TA) è stato ampiamente impiegato come trattamento dell'edema maculare fin dagli anni ‘90, ma la formulazione senza conservanti è presente e studiata dalla letteratura solo a partire dal 2007.
Alla disponibilità e pubblicazione dei risultati degli studi sulle nuove formulazioni farmaceutiche, è collegata la loro inclusione nelle linee guida più recenti così come la rispettiva autorizzazione all'immissione in commercio. Nel 2013, le linee guida del RCO (Regno Unito) hanno raccomandato l'utilizzo dell'impianto di FA nei pazienti fachici e pseudofachici con DME centrale clinicamente significativo con riduzione dell'acuità visiva (78-24 lettere) e con spessore retinico centrale (CRT) ≥250 µm. Le linee guida pubblicate a partire dal 2015 raccomandano l'utilizzo dell'impianto di DEX per il trattamento del DME centrale con riduzione dell'acuità visiva (40) e dell'edema maculare secondario a RVO non ischemica (3).
La presente revisione ha come obiettivo la valutazione della qualità complessiva degli studi pubblicati sull'utilizzo di corticosteroidi intravitreali nel trattamento dell'edema maculare. L'analisi eseguita ha portato all'identificazione della letteratura che esplora l'uso delle tre formulazioni (TA, impianto di FA e impianto di DEX) come monoterapia o in combinazione con i trattamenti standard. Gli studi considerati nella nostra revisione hanno analizzato tali terapie confrontandole con procedure simulate o con la sola osservazione o rispetto ai trattamenti standard come il laser o i farmaci anti-VEGF. Relativamente al follow-up, il periodo di osservazione è andato da un minimo di 6 mesi sino a 3 anni.
La valutazione qualitativa di tali studi ha portato a una serie di considerazioni illustrate di seguito in maniera sintetica.
Per quanto riguarda triamcinolone acetonide, sono stati reperiti studi eterogenei in termini di popolazione studiata, tipologia d'intervento sperimentale (formulazioni, dosaggi e intervalli di ritrattamento variabili), tipo d'intervento di controllo e misure degli outcomes di efficacia e sicurezza. Non è scopo di questa revisione esaminare i risultati di efficacia e di sicurezza a cui sono giunti i singoli studi, quanto la loro qualità metodologica. Da questo punto di vista appare più difficile esprimere giudizi in merito a triamcinolone acetonide, poiché questo fa riferimento a formulazioni diverse, i cui risultati non possono essere considerati sovrapponibili, sia perché fanno riferimento a prodotti non omogenei sia perché questi sono stati utilizzati con posologie diverse o addirittura non specificate. Si segnala inoltre che attualmente in Italia è in commercio anche una formulazione di TA per uso terapeutico per la quale questa revisione di letteratura non ha identificato alcuno studio. Un altro limite è correlato all'inclusione di studi che utilizzano tutte le diverse formulazioni di PFTA, giacché potrebbe non essere possibile assumere una proprietà transitiva tra di esse, d'accordo con i risultati di sperimentazioni in vivo (13) che indicano differenze in termini di farmacocinetica e farmacodinamica.
A prescindere dall'eterogeneità, tuttavia, l'insieme delle evidenze sull'impianto di DEX e di fluocinolone si osserva metodologicamente più robusto, specialmente in termini di procedure di randomizzazione e mascheramento, entrambe fondamentali per l'ottenimento di risultati di elevata validità interna ed esterna nell'ambito degli studi clinici randomizzati, oltre che per la chiara identificazione della posologia. I dati sull'impianto di fluocinolone fanno però riferimento al solo utilizzo per DME.
Nonostante tutte e tre le formulazioni di corticosteroidi incluse siano approvate all'immissione in commercio e comprese nelle linee guida per il trattamento dell'edema maculare, è da sottolinearsi la necessità di riesaminare i requisiti per l'approvazione dei farmaci e il loro inserimento nelle raccomandazioni cliniche, così come l'importanza del monitoraggio post-marketing per la generazione di nuove evidenze che arricchiscano l'insieme delle prove.
I potenziali bias della presente revisione sono legati ai limiti definiti per l'inclusione dei dati, i quali appartengono solo a pubblicazioni su riviste indicizzate nella banca dati MEDLINE. Inoltre un limite potenziale è rappresentato dal fatto che questo lavoro non ha confrontato, perché non rientrante tra i suoi obiettivi, l'efficacia e la sicurezza dei diversi farmaci, ma solo la qualità dell'evidenza prodotta per ognuno di essi.
I dati delle pubblicazioni incluse presentano eterogeneità e non permettono di essere ulteriormente analizzati tramite metanalisi. È importante che ulteriori studi clinici siano in futuro disegnati in modo che possano essere comparabili ai trials esistenti. Le future ricerche cliniche dovrebbero confrontare in modo diretto le diverse formulazioni farmaceutiche di corticosteroidi intravitreali nel trattamento del DME e dell'edema maculare secondario a RVO.
Inoltre, l'esecuzione di ricerca primaria che esplori la differenza in termini di efficacia e di reazioni avverse tra le diverse formulazioni disponibili di PFTA, suggerita da alcuni autori, potrà essere di aiuto per la comprensione degli effetti di questi farmaci in particolare. È da tenere in considerazione che, poiché la somministrazione di questi farmaci prevede pratiche invasive, non devono essere trascurati gli effetti indesiderati associati e le possibili complicanze (endoftalmite settica e/o asettica, ipertensione oculare, emorragia sottocongiuntivale e/o endovitreale, insorgenza/progressione di cataratta, distacco della retina, dolore, arrossamento oculare e sensazione di corpo estraneo, transitoria comparsa di corpi mobili). Solo sulla base di studi di efficacia con casistica numericamente qualificata potranno essere messe in evidenza con chiarezza le reali indicazioni e applicazioni nella pratica clinica.
Footnotes
Acknowledgement
We greatly appreciate the critical review of the manuscript and valuable comments provided by Silvia Adami (Sezione Attuazione Programmazione Sanitaria, Settore Farmaceutico Regionale, Regione Veneto), Stefano Bianchi (UOC Farmacia, Azienda Ospedaliera Ospedali Riuniti Marche Nord), Adele De Francesco (UO SC Farmacia. Azienda Ospedaliera Universitaria “Mater Domini”, Catanzaro), and Massimo Medaglia (Dipartimento Farmaceutico e UO Farmacia, Ospedale Luigi Sacco, Milano). We also thank Francesca Rolli, Paola Codella and Federica Romano for building the PubMed search query and participating in the selection of the articles.
Financial support: The project received unconditioned financial support by Allergan Italia S.p.A.
Conflict of interest: M. Marchetti, P. Navarra and M. Oradei have received consulting fees from Allergan; L.I. Urbina and M. Ruggeri have no competing financial interests to declare.
Meeting presentation: An extended version of the present manuscript was presented at the Experts Meeting on Retinal Diseases, April 7, 2016, Rome, Italy. The event was organized by Allergan Italia S.p.A.
