Abstract
Ants, as eusocial insects essential to terrestrial ecosystems, are found across a wide range of habitats around the world. In Durango, Mexico, the convergence of Nearctic and Neotropical regions promotes high species diversity. This study analyzed ant diversity patterns across five vegetation types in the state. From August 2016 to September 2017, we collected 1,590 specimens representing 5 subfamilies, 14 tribes, 23 genera, and 36 species. Myrmicinae was the most diverse subfamily (19 species), followed by Formicinae (10 species), Dolichoderinae (5 species), with Ponerinae and Dorylinae each represented by a single species. We assessed alpha diversity using Hill numbers (°D, 'D, 2D) and spatial beta diversity through Jaccard (incidence) and Bray-Curtis (abundance) indices. Results showed that the Xerophytic Shrubland (MX) exhibited the highest species richness (D) and diversity ('D, 2D). Abundance-based beta diversity ranged from 0.52% to 0.95%, indicating significant differences in species composition among habitats. This study highlights the remarkable ant diversity in Durango, influenced by distinct vegetation types, with Xerophytic Shrubland showing the highest diversity. These findings underscore the importance of environmental factors in shaping ant community distribution and richness, providing valuable information for biodiversity conservation.
Introducción
Las hormigas son insectos eusociales ampliamente distribuidos alrededor del mundo, en un gran número de hábitats terrestres excepto en zonas altas de las montañas y en los polos (Fernández, 2003; Hölldobler & Wilson, 1990; Tuma et al., 2020; Vásquez-Bolaños, 2015). La biomasa total de las hormigas se estima en un 15% del total mundial siendo un componente clave en los ecosistemas terrestres (Eggleton, 2020). Su importancia radica en las múltiples interacciones que establecen con otros organismos (Chomicki & Renner, 2017). Estas interacciones pueden generar un cambio espacio-temporal de su rol trófico donde tienen un papel clave dentro de la cadena trófica actuando como presa de aves, anfibios, reptiles, mamíferos, artrópodos entre otros, así como, depredadoras que se alimentan de grandes cantidades de insectos plaga y con ello pueden ayudar en la prevención y control de plagas oportunistas y dentro de la cadena de detritos.
Además, por su abundancia tienen efectos positivos en los ecosistemas (Eggleton, 2020). Las hormigas ayudan a mejorar la calidad del suelo, creando macroporos y aumentando los nutrientes en este. En regiones tropicales, diversos estudios han demostrado que las hormigas son los principales organismos responsables de excavar el suelo y remover nutrientes. Se ha registrado que son responsables del 61% de todo el alimento extraído por invertebrados en el suelo de la selva tropical (Agosti et al., 2000; Arenas & Armbrecht, 2018; Choate & Drummond, 2011; Fayle et al., 2011; Griffiths et al., 2018; Mooney & Tillberg, 2005; Tan & Corlett, 2012; Wilson, 2000).
La riqueza específica es un parámetro destacable de las hormigas para estudios de biodiversidad (Kaspari et al., 2000), siendo más conocido que en otros artrópodos. Así mismo, debido a su abundancia y riqueza la importancia en el funcionamiento de los ecosistemas y su relativa facilidad para ser muestreadas se ha demostrado que las hormigas son un indicador eficiente para definir cambios ecológicos (Soto-Cárdenas et al., 2019). A su vez estos atributos han sido utilizados para observar la rehabilitación de terrenos mineros junto con la composición de grupos funcionales (Andersen, 1997, 1999; Andersen et al., 2003; Greenslade & Greenslade 1984; Lapolla et al., 2007; Rosenberg et al., 1986). En la actualidad se han descrito 14.191 especies de hormigas dentro de 16 familias (Bolton, 2024). En México hay 911 especies válidas y particularly para Durango 70 especies (AntWeb, 2024; Soto-Cárdenas et al., 2019).
México es un país con una gran diversidad que contiene dos regiones biogeográficas: Neártica y Neotropical. Debido a su posición geográfica, en el estado de Durango dichas regiones convergen, así como la zona de Transición Mexicana, trayendo consigo una amplia diversidad de especies entre ellas las hormigas (Dáttilo et al., 2020; Ríos-Casanova et al., 2004). De igual manera en Durango se encuentran presentes cinco tipos de vegetación: Bosque de coníferas y encinos, Bosque tropical caducifolio, Matorral xerófilo, Paztizal y Zonas antropizadas.
Bosque de coníferas y encinos: este tipo de vegetación tiene una gran variación altitudinal, sin embargo, el referente puede darse entre los 1500 m s.n.m. con una temperatura media anual de 10 °C a 26 °C y precipitación media anual que va de 600 mm a 1200 mm (CONABIO, 2008; Rzedowski, 2006).
Bosque tropical caducifolio: se desarrolla entre 0 y 1,900 m s.n.m. y tiene una temperatura media anual que oscila de los 20 °C a 29 °C además, presenta dos estaciones bien definidas la lluviosa y la seca (5 a 8 meses secos), mientras que la precipitación está en el orden de los 300 mm a 1800 mm (CONABIO, 2008; Rzedowski, 2006).
Matorral xerófilo: en este tipo de vegetación se pueden encontrar temperaturas medias de 12 °C a 26°C con una precipitación media anual entre 100 mm a 400 mm (CONABIO, 2008; Rzedowski, 2006).
Pastizal: este tipo de vegetación se encuentra en México en altitudes entre 1,100 a 1,800 m.s.n.m. con temperatura media anual de 12 °C a 20 °C. Por su parte, la precipitación media anual está entre 300 mm a 600 mm con 6 a 9 meses secos (CONABIO, 2008; Rzedowski, 2006).
Zonas antropizadas: son sitios donde las actividades humanas generan procesos de cambio en el medio ambiente desde una población hasta el paisaje completo. Ejemplo de ello es el cambio de uso de suelo, producto de actividades humanas, que genera que más del 58 % de los ecosistemas terrestres presenten empobrecimiento en su biodiversidad, además, esta pérdida de biodiversidad está estrechamente asociada a la disminución de los servicios ecosistémicos (Álvarez, et al., 2019; CONABIO, 2008; Newbold et al., 2016; Rzedowski, 2006).
Entre los trabajos que se han realizado acerca de la diversidad de hormigas en diferentes tipos de vegetación en México se encuentra el realizado por Gómez-Otamendi et al. (2018), quienes compararon la riqueza, abundancia, diversidad y composición de especies epigeas de hormigas entre zonas de matorral xerófilo dominado por Opuntia spp.; además detectaron posibles especies indicadoras en cada tipo de vegetación y evaluaron la influencia de algunas variables del hábitat en la riqueza, abundancia y diversidad de las comunidades de hormigas. Otro ejemplo es el realizado por Hernández-Ruiz y Castaño-Meneses (2006), quienes caracterizaron las comunidades de hormigas en cultivos con dos sistemas de riego y sus variaciones espaciales y estacionales para encontrar especies que puedan ser utilizadas como bioindicadoras y así evaluar los niveles de perturbación por riego en los ecosistemas agrícolas del Valle del Mezquital. Finalmente, Ríos-Casanova et al. (2006), analizaron la comunidad de hormigas presente a lo largo de un abanico aluvial ubicado en el Valle de Tehuacán, una zona semiárida del centro de México. Por su parte este trabajo tiene por objetivo analizar los patrones de diversidad y su relación con los tipos de vegetación presentes en el estado de Durango, México.
Materiales y métodos
El presente estudio se realizó en el estado de Durango, ubicado al norte de México (22°40′ y 26°50′N; 102°25′55″ у 107°08′50″O), siendo el cuarto más grande del país por extensión territorial con 123,364 Km2. Altitudinalmente presenta una variación de 200 a 3,328 metros sobre el nivel del mar (INEGI, 2017).
Muestreo de campo
Se realizaron recolectas manuales en cinco localidades, tomando en cuenta los tipos de vegetación presentes en el estado de Durango: Bosque de Coníferas y Encinos (BCE), Bosque Tropical Caducifolio (BTC), Matorral Xerófilo (MX), Pastizal (P) y Zonas Antropizadas (ZA) (Figura 1). Entre el 15 de agosto de 2016 y el 15 de septiembre de 2017 se realizaron recolectas quincenales en 57 localidades. En cada visita y sitio se estableció un transecto lineal de 100 m, que se recorrió completamente durante un esfuerzo estandarizado de 3 h por sitio. La recolección se efectuó mediante búsqueda activa utilizando hisopos de algodón estériles, pinceles finos y pinzas entomológicas. Se capturaron individuos observados forrajeando en el suelo, en nidos visibles y sobre árboles y arbustos hasta 1,75 m de altura, así como bajo piedras, en la hojarasca y en troncos caídos. Los ejemplares fueron identificados mediante claves taxonómicas (Del Toro et al., 2009, Demarco & Cognato, 2015; Mackay & Mackay, 1989, 2002, 2004), cuantificados y preservados en alcohol al 96%. Los ejemplares se encuentran depositados en la Colección Entomológica del Centro de Estudios en Zoología de la Universidad de Guadalajara, México y La Colección Entomológica CIIDIR Durango.
Estructura de la comunidad de Formicidae
Para evaluar la estructura de cada una de las localidades muestreadas se utilizó la diversidad alfa mediante el número de especies efectivas, representado por los números de Hill, y se emplearon medidas de diversidad verdadera para tres niveles de q, según Jost (2006, 2007).
La influencia de las especies comunes o poco comunes en la medida de la diversidad se determina según la sensibilidad de estas medidas a la abundancia de las especies. Esto está vinculado al valor asignado al exponente q. Cuando q es igual a 0, la diversidad es igual a la riqueza de especies, lo que implica solo considerar su presencia o ausencia. Cuando q es igual a 1, todas las especies se tienen en cuenta con un peso proporcional a su abundancia, equivalente al exponencial del índice de Shannon-Weiner (eH’). Por último, cuando q es igual a 2, se refiere al inverso del índice de dominancia de Simpson, donde se priorizan las especies más comunes o dominantes (Jost, 2006, 2007).
Para verificar posibles diferencias significativas entre las localidades y corregir cualquier sesgo en el esfuerzo de recolección (Cumming et al., 2007), se llevaron a cabo curvas de rarefacción. Estas curvas se construyeron utilizando la diversidad alfa verdadera de orden q = 0, 1 y 2, con intervalos de confianza (Bootstrap) del 95% (Cultid-Medina & Escobar, 2019), mediante el paquete iNEXT (Hsieh et al., 2020). Se estimó el número de especies no recolectadas en los tres órdenes de q utilizando los estimadores no paramétricos Chao 1 (abundancia) y Chao 2 (incidencia) (Budka et al., 2019; Chao et al., 2014; Hsieh et al., 2020).
Se determinó la diversidad beta espacial a través de los índices relativizados de Jaccard para la incidencia de especies (Baselga, 2010, 2012) y Bray-Curtis para la abundancia (Baselga, 2013). La disimilitud en la composición de especies entre localidades, medida a través de datos de incidencia, fue calculada utilizando el índice de Jaccard relativizado (JAC) propuesto por Baselga (2010, 2012). Los resultados de este índice se presentan en un intervalo de 0 (0%) a 1 (100%). Cuando los valores son iguales a 0, los sitios tienen la misma composición de especies; mientras que un valor de 1 indica que no hay especies compartidas entre pares de sitios.
Para evaluar en qué medida los cambios espaciales en la composición de especies pueden atribuirse al recambio de especies y/o anidamiento, se empleó el marco teórico propuesto por Baselga (2012). Se realizaron dos análisis basados en el índice de Jaccard (Baselga, 2012).
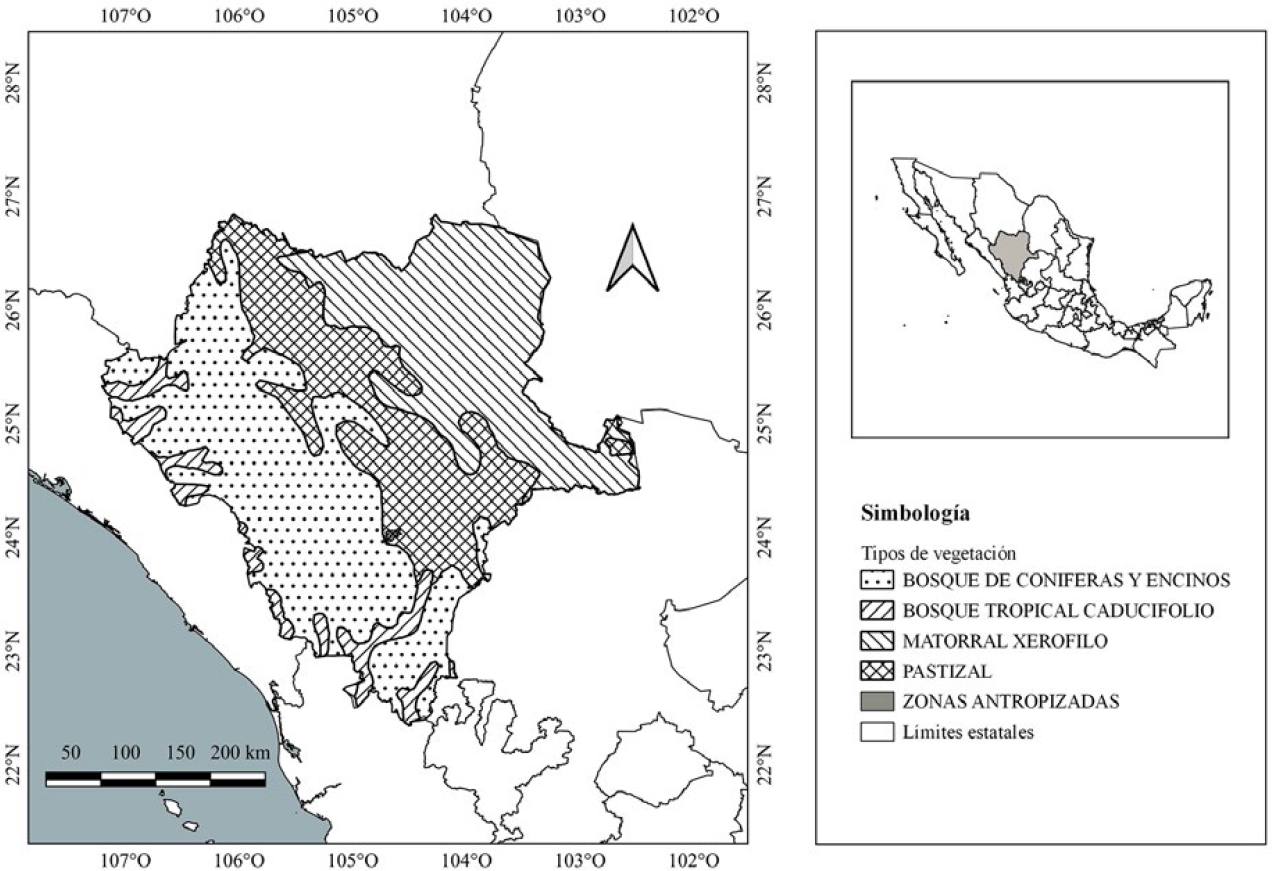
Área de estudio caracterizada por tipos de vegetación.
Mientras tanto, el índice relativo de Bray-Curtis (Bray), se calculó siguiendo el marco teórico propuesto por Baselga (2013) que utiliza la disimilitud basada en abundancia y separado en dos componentes: 1) el componente de variación equilibrada (Bray.bal) donde los individuos de algunas especies en un sitio son sustituidos por el mismo número de individuos de diferentes especies en otro sitio y 2) el componente de gradiente de abundancia (Bray.gra) donde algunos individuos se pierden de un sitio a otro. Todos los procedimientos mencionados se realizaron mediante el paquete beta.part (Baselga et al., 2023) en el entorno R (R Core Team, 2020).
Resultados
Se registraron 1,590 individuos distribuidos en cinco subfamilias, 14 tribus, 23 géneros y 36 especies. La subfamilia con mayor número de especies registradas fue Myrmicinae con 19, seguido de Formicinae con 10, Dolichoderinae con cinco y Ponerinae y Dorylinae ambas con una especie. Las tribus más ricas fueron Attini con cinco especies, Crematogastrini, Plagiolepidini y Pogonomyrmecini con cuatro especies y Camponotini, Dolichoderini y Solenopsidini con tres especies, las siete tribus restantes contienen entre una y dos especies. Los géneros con el mayor número de especies fueron
La cobertura de muestra obtuvo porcentajes de completitud de muestreo entre 96% - 100% con respecto a la diversidad estimada (Tabla 2). La comparación de la diversidad °D entre tipos de vegetación mostró que la riqueza del Matorral Xerófilo (MX) es mayor. Sin embargo, esta diferencia disminuye cuando se usan los valores correspondientes al esfuerzo de recolección extrapolado, ya que los intervalos de confianza del MX y de Zonas Antropizadas (ZA) se traslapan. Por su parte, la diversidad 1D y 2D colocaron al MX como el tipo de vegetación más diverso, sin embargo, los intervalos de confianza se superponen con los de las ZA y el Bosque de Coníferas y Encinos (BCE), lo que sugiere que no existen diferencias significativas (Figura 2).
Especies de hormigas (Formicidae Latreille, 1809) en vegetaciones de Durango, México.
*Tipos de vegetación: Bosque de Coníferas y Encinos (BCE), Bosque Tropical Caducifolio (BTC), Matorral Xerófilo (MX), Pastizal (P) y Zonas Antropizadas (ZA).
Diversidad observada (Obs), diversidad estimada (Est) y porcentaje de completitud de muestreo de siete localidades en Durango.
*Entre paréntesis el porcentaje de diversidad verdadera observada respecto al valor estimado. Tipos de vegetación: Bosque de Coníferas y Encinos (BCE), Bosque Tropical Caducifolio (BTC), Matorral Xerófilo (MX), Pastizal (P) y Zonas Antropizadas (ZA).
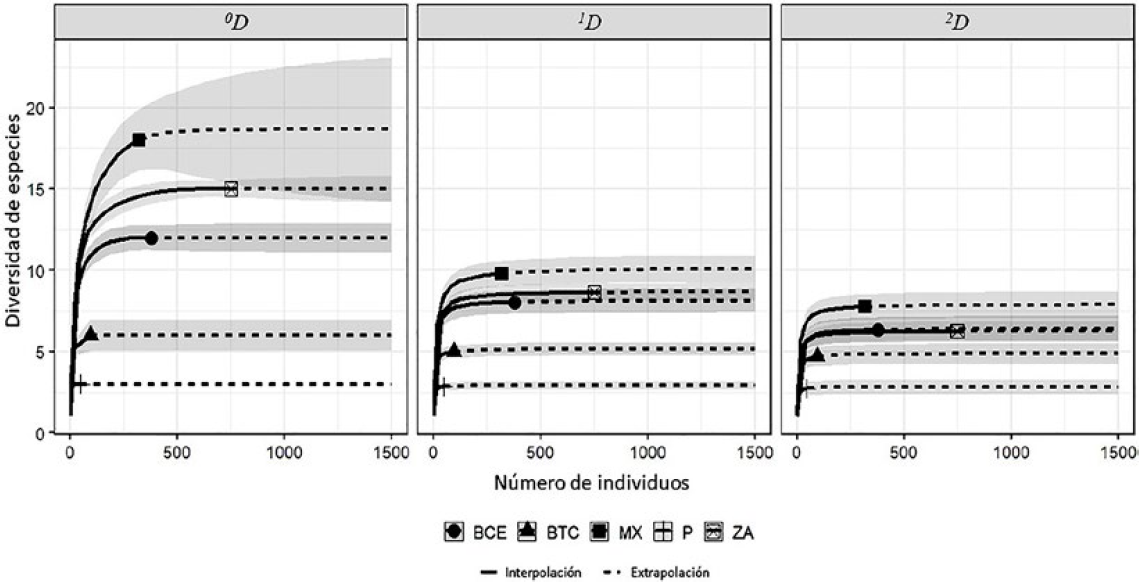
Curvas de rarefacción de las siete localidades, D= Riqueza de especies; Chao2, 1D = Exponencial del índice de Shannon; Chao1 y 2D = Inverso del índice de Simpson; Chao1. BCE: Bosque de coníferas y encinos: BTC: Bosque Tropical Caducifolio; MX: Matorral Xerófilo; P: Pastizal; ZA: Zonas antropizadas.
La diversidad beta basada en incidencia (JAC) varió entre 1% - 0,71%, siendo el BCE-ВТС у ВСЕ-P los que presentaron una mayor disimilitud entre sí. Los pares de sitios que resultaron más similares fueron BTC-P. Los pares de sitios en los que la diversidad beta fue representada mayormente por el componente de recambio (JTU) fueron BCE-BTC, BCE-MX, BCE-P, BCE-ZA, BTC-P, BTC-ZA, MX-ZA y P-ZA. Los pares de sitios en los que la diversidad beta fue representada mayormente por el componente de anidamiento (JNE) fueron BTC-MX y MX-P (Tabla 3).
La diversidad beta basada en la abundancia (Bray) varió entre 0,95 % - 0,52 %, siendo BCE y MX los que presentaron una mayor disimilitud entre sí. Los pares de sitios que resultaron más similares fueron BTC-P. Los pares de sitios en los que la diversidad beta fue representada mayormente por variación equilibrada en abundancia (Bray.bal) fueron ВСЕ-ВТС, ВСЕ-МХ, ВСЕ-P, BCE-ZA, BTC-P, MX-ZA y P-ZA. Los pares de sitios en los que la diversidad beta fue representada mayormente por el componente de gradiente de abundancia (Bray.gra) fueron BTC-MX, BTC-ZA y MX-P (Tabla 4).
Valores del componente de recambio (JTU), del componente de anidamiento (JNE) y de la diversidad beta general basada en incidencia entre pares de sitios (JAC) entre cinco tipos de vegetación en Durango.
Discusión
Los resultados muestran una comunidad de hormigas en Durango, México, compuesta por 1,590 individuos distribuidos en 36 especies, donde la subfamilia Myrmicinae (19 spp.) y los géneros
Estudios como por ejemplo el presentado por Gómez-Otamendi et al. (2018) encontraron 23 especies en un Matorral Xerófilo e indican que su inventario fue del 100%. En este trabajo se encontraron porcentajes de completitud de muestreo entre 96% y 100%. Mientras que Hernández-Ruiz y Castaño-Meneses (2006) señalan que en una zona con vegetación predominante por matorral xerófilo y pastizal describen valores de H' de 1,55 – 2,14. Por otro lado, Ríos-Casanova et al. (2006) indican que en una zona de Matorral Xerófilo del Centro de México encontraron 26 especies de hormigas y valores de Shannon-Wiener (H') entre 1,29 y 2,27, por su parte, en este trabajo este valor para este tipo de vegetación fue de 9,79. Así mismo, Hernández-Ruiz y Castaño-Meneses (2006) reportan 21 especies de hormigas y sugieren que la riqueza en este tipo de hábitats puede deberse a la diversidad microambiental, además de que la vegetación natural y su cercanía con parcelas de riego permiten una vegetación más diversa y permanente, que proporciona refugio y hábitat para varias especies de hormigas. En este trabajo se encontraron 11 especies de hormigas dentro de Matorral Xerófilo sin embargo, estos números pueden verse afectados por el tipo de muestreo realizado. En este estudio, el muestreo realizado fue exhaustivo, garantizando así que las listas de especies proporcionen una completitud de muestreo alta en estos entornos (Tabla 2). El tipo de vegetación que resultó más diverso fue el Matorral Xerófilo (MX). Esta observación sugiere una relación específica entre la composición de especies de hormigas y las características del hábitat, así como la disponibilidad de recursos, la estructura de la vegetación y la variabilidad del microclima (Quiroz-Robledo & Valenzuela-González, 1995).
Se ha demostrado que la diversidad de Formicidae suele ser mayor en las etapas sucesionales y en los matorrales, en comparación con los bosques, especialmente los de coníferas, que tienden a albergar una menor abundancia y diversidad de hormigas (Jiménez & Tinaut, 1992). Es crucial investigar qué factores ambientales están impulsando la diversidad en el Matorral xerófilo y cómo estas especies interactúan con el ecosistema circundante o sucesional.
Si bien el Matorral Xerófilo (MX) muestra la mayor diversidad de especies en términos absolutos, es importante considerar la completitud del muestreo y la extrapolación de la diversidad para evitar sesgos en la comparación entre hábitats. La superposición de intervalos de confianza entre el Matorral Xerófilo (MX), Zonas Antropizadas (ZA) y Bosque de Coníferas y Encinos (BCE) sugiere una posible homogeneidad en la diversidad de hormigas entre estos hábitats una vez que se ha alcanzado el esfuerzo máximo de muestreo en cada sitio (Figura 2).
Los análisis de diversidad beta revelan patrones en la estructura de la comunidad de hormigas entre los diferentes sitios de muestreo. Por ejemplo, la mayor disimilitud entre el BCE y el MX sugiere diferencias significativas en la composición de especies entre estos hábitats. La notable disparidad en la diversidad beta general, medida por incidencia, entre los pares de sitios comparados, fue principalmente atribuible al componente de recambio de especies (JTU), el cual, a su vez, refleja la presencia de especies exclusivas en cada ubicación. En contraste, el componente de anidamiento (JNE) tuvo una influencia considerablemente menor (Calderón-Patrón et al., 2016). El recambio de especies (JTU), en términos generales, indica la adquisición o pérdida de especies como resultado de diferencias en las condiciones ambientales, las interacciones competitivas entre especies y los eventos históricos específicos de cada localidad de estudio (Leprieur et al., 2011). Además, la presencia de componentes de recambio y anidamiento (JTU y JNE) en la diversidad beta indica la importancia de los procesos de especiación y extinción, así como la heterogeneidad ambiental en la configuración de la estructura de la comunidad de hormigas (He & Hu, 2005) (Tabla 3).
El análisis de la diversidad beta basada en la abundancia revela una variabilidad significativa entre los sitios estudiados, lo que refleja diferentes patrones de distribución y composición de especies en el área de estudio. Los valores de diversidad beta fluctuaron entre el 0,52 % y el 0,95 %, lo que indica una considerable heterogeneidad en la estructura de las comunidades de especies (Tabla 3).
Es fundamental observar la distribución de los componentes de diversidad beta en los diferentes pares de sitios. Se observa que, en varios pares, como BCE-BTC, BCE-MX, BCE-P, BCE-ZA, BTC-P, MX-ZA y P-ZA, la diversidad beta se ve principalmente influenciada por una variación equilibrada en la diversidad de especies (Bray. Bal) (Tabla 4). Esto sugiere una distribución uniforme de las especies entre los sitios, lo que podría estar relacionado con la presencia de condiciones ambientales similares o la ausencia de factores que promuevan la dominancia de ciertas especies sobre otras (Baselga 2013, 2017; Baselga & Rodríguez, 2019; Castro-Insua et al., 2018). Por otro lado, en los pares de sitios BTC-MX, BTC-ZA y MX-P, la diversidad beta está principalmente representada por el componente de gradiente de abundancia (Bray, Gra). Esto sugiere que la diferencia en la abundancia de especies entre estos sitios es el principal factor que contribuye a la diversidad beta, lo que podría estar relacionado con gradientes ambientales o la influencia de factores que promueven la dominancia de ciertas especies en ciertos sitios (Almeida-Neto et al., 2011; Baselga 2013, 2017; Castro-Insua et al., 2016; Harrison et al., 1992; Philpott & Armbrecht, 2006).
Valores del componente de variación equilibrada en abundancia (Bray.bal), del componente de gradientes de abundancia (Bray.gra) y de la diversidad beta general basada en la abundancia entre pares de sitios (Bray) entre cinco tipos de vegetación en Durango.
Conclusiones
Este estudio resalta que la diversidad de hormigas varía significativamente entre los diferentes tipos de vegetación y destaca al Matorral Xerófilo (MX) como el tipo de vegetación con mayor riqueza específica; sin embargo, no se presentan diferencias estadísticamente significativas con ZA y BCE. Los géneros
Origen y financiamiento
El presente trabajo derivó de la línea de investigación con hormigas que se desarrolla en la academia de entomología del Centro Interdisciplinario de Investigación para el Desarrollo Integral Regional, fue parte del trabajo de Tesis de Doctorado del primer autor y estancia posdoctoral del autor de correspondencia.
Contribución de los autores
La primera autora planteó los objetivos de la investigación, contribuyó en el análisis de los datos, el trabajo en campo у en la escritura del artículo.
El segundo autor desarrolló el análisis de los datos y la escritura del artículo conjuntamente al primer autor.
El tercer autor contribuyó en el trabajo de campo y la identificación de los ejemplares, así como su adjunción en el acervo entomológico donde se encuentran depositados, además a la revisión del artículo.
El cuarto autor consiguió la financiación del proyecto, contribuyó al trabajo en campo, la cuantificación e identificación de los ejemplares y la revisión del artículo.
El quinto autor contribuyó al planteamiento de los objetivos, el modelo experimental, el trabajo en campo, la identificación de ejemplares, contribuyó en el análisis de datos y la escritura del manuscrito.
Conflicto de intereses
Todos los autores están de acuerdo y expresan que no hay conflictos de intereses en este estudio.
